Слайд 2ГОСТ ИСО/МЭК 17025
п. 5.4.5 Оценка пригодности методик
5.4.5.1 Оценка пригодности
— это подтверждение путем исследования и предоставления объективных доказательств того,
что конкретные требования к специфическому целевому использованию выполняются.
5.4.5.2 Лаборатория должна оценивать пригодность нестандартных методик, методик, созданных/разработанных лабораторией, стандартных методик, используемых за пределами целевой области распространения ее деятельности, а также расширений и модификаций стандартных методик для подтверждения того, что они подходят для целевого использования.
Полнота этой оценки зависит от необходимости соответствовать потребностям данного применения или области применения.
Лаборатория должна регистрировать полученные результаты, процедуру, использованную для оценки пригодности, и решение о том, подходит ли метод для целевого использования.
Слайд 3ГОСТ ИСО/МЭК 17025
Примечание 1 - Оценка пригодности может включать в
себя процедуры отбора образцов, обращения и транспортирования.
Примечание 2 -
Эффективность метода определяют одним из следующих способов или их сочетанием:
- калибровкой с использованием исходных эталонов и стандартных образцов;
- сравнением результатов, полученных с помощью других методов;
- межлабораторными сравнительными испытаниями;
- систематическим оцениванием факторов, оказывающих влияние на результат;
- оцениванием неопределенности результатов на основе научного осмысления теоретических принципов метода и практического опыта.
Примечание 3 - Если в оцененные на пригодность нестандартные методы/методики внесены изменения, то влияние этих изменений следует задокументировать и, если уместно, провести новую оценку.
Слайд 4ГОСТ ИСО/МЭК 17025
5.4.5.3 Диапазон и точность оценок (таких как неопределенность
результатов, предел обнаружения, избирательность метода, линейность, предел повторяемости и/или воспроизводимости,
устойчивость к внешним воздействиям и/или чувствительность к влиянию матрицы пробы/объекта испытаний), получаемых методиками, пригодность которых подтверждена, как соответствующих назначению, должны удовлетворять потребностям заказчиков.
Примечание 1 - Оценка пригодности включает в себя спецификацию требований, определение характеристик методик, проверку соответствия требованиям с помощью используемого метода и подтверждение пригодности.
Примечание 2 - По мере разработки методики следует проводить регулярный анализ с целью проверки того, что потребности заказчика все еще удовлетворяются. Любое изменение в требованиях, требующее внесения изменений в план разработки, должно быть одобрено и утверждено.
Примечание 3 - Оценка пригодности — это всегда компромисс между затратами, риском и техническими возможностями. Известно много случаев, когда диапазон определения и неопределенность значений (например, точности, предела обнаружения, избирательности, линейности, повторяемости, воспроизводимости, устойчивости, чувствительности к влияниям) были даны только в упрощенном виде из-за недостатка информации.

Слайд 5КРИТЕРИИ АККРЕДИТАЦИИ
23.14. Наличие правил выбора и использования методик исследований (испытаний)
и измерений, соответствующих области деятельности лаборатории, предусматривающих:
а) правила документирования
сведений об используемых методиках исследований (испытаний) и измерений, а также обеспечения методиками исследований (испытаний) и измерений работников лаборатории;
б) правила документирования сведений о зафиксированных отклонениях при проведении исследований (испытаний), измерений от требований, установленных в методиках исследований (испытаний) и измерений, в том числе правила технического обоснования указанных отклонений, их одобрения со стороны заказчика исследований (испытаний) и измерений;
23.15. Наличие правил разработки, оценки пригодности и использования лабораторией нестандартных методик; методик, разработанных лабораторией; стандартных методик, используемых за пределами целевой области их применения; расширений и модификаций стандартных методик (если указанные методики используются или их планируется использовать);
Слайд 6Общие положения
На пригодность оцениваются все методики, используемые в лаборатории, до
их первого рабочего применения.
При оценке пригодности методики рекомендуется составлять
план ее проведения.
Процедура оценки пригодности методики включает:
- установление области применения,
- определение характеристик методики (диапазон возможных значений результата, неопределенность или степень достоверности),
- проверку прослеживаемости методики,
- проверку того, что требования могут быть удовлетворены с помощью используемого метода.
Оценка пригодности методик производится одним из следующих перечисленных приемов или их сочетаниями:
- использованием образцов сравнения, СО и сравнительных коллекций;
- сравнением с результатами, достигнутыми с помощью других методов;
- межлабораторным сравнением результатов;
- систематическим оцениванием факторов, влияющих на результат;
- иными способами.
По результатам оценки составляется итоговый документ, например акт внедрения. Методике должен быть присвоен регистрационный номер, и она должна быть зарегистрирована в документах лаборатории.
Слайд 7
ОЦЕНКА ПРИГОДНОСТИ – ВАЛИДАЦИЯ (EURACHEM Guide)
Валидацию метода можно интерпретировать
как процесс определения аналитических требований и подтверждения того, что возможности
рассматриваемого метода соответствуют целям его использования.
5. Когда необходима валидация методов?
5.1 Метод должен быть утвержден, если необходимо убедиться в том, что его рабочие характеристики соответствуют использованию в целях решения конкретной аналитической задачи.
Например:
• новый метод, разработанный под решение конкретной задачи;
• общепризнанный метод, пересмотренный и усовершенствованный, либо расширенный в целях охвата новой задачи;
• если контроль качества свидетельствует об изменениях общепризнанного метода с течением времени;
• общепризнанный метод, используемый в другой лаборатории, другими аналитиками или с использованием другой аппаратуры;
• для демонстрации эквивалентности двух методов, например, нового и стандартного.
5.2 Степень требуемой валидации или ревалидации будет зависеть от характера изменений, внесенных в метод, который предполагается использовать в других лабораториях, где будут отличаться приборы, операторы и условия использования метода. Определенная степень валидации целесообразна всегда, даже если речь идет о применении хорошо известных, стандартных или опубликованных методов

Слайд 8В идеале, столкнувшись с определенной аналитической задачей, лаборатория должна прежде
всего согласовать с клиентом аналитические требования, определяющие требования к рабочим
характеристикам, которыми должен обладать метод, чтобы быть пригодным для решения данной аналитической задачи.
После этого лаборатория оценивает пригодность уже существующих методов, и, при необходимости, разрабатывает новый.
Такой итеративный процесс разработки и оценки продолжается до тех пор, пока не будет найден метод, соответствующий поставленному требованию; дальнейшая разработка не требуется, и аналитическая работа может быть продолжена.
Слайд 9
ГОСТ Р 52960-2008
Аккредитация судебно-экспертных лабораторий. Руководство по применению ГОСТ Р
ИСО/МЭК 17025
При оценке пригодности методик испытаний может возникнуть необходимость проверки
влияния дополнительных факторов:
- матричных эффектов;
- интерференционных эффектов;
- степени однородности (гомогенность) образца;
- диапазонов концентраций;
- специфики объекта исследований;
- стабильности определяемых компонентов;
- линейности градуировочной характеристики;
- прецизионности результатов измерений в регламентированных методикой анализа условиях проведения эксперимента;
неопределенности результата измерения (анализа).
Оценка пригодности метода может проводиться в процессе его аттестации (как в случае со стандартными методами) или самой судебно-экспертной лабораторией, если метод был разработан внутри лаборатории или если в ранее оцененный на пригодность (или аттестованный) метод были внесены значительные изменения.
Слайд 10EURACHEM Guide «ПРИГОДНОСТЬ К ИСПОЛЬЗОВАНИЮ АНАЛИТИЧЕСКИХ МЕТОДОВ. Руководство для лабораторий
по валидации методов и сопутствующим вопросам»
Шесть принципов аналитической практики :
1
Аналитические измерения должны удовлетворять установленным требованиям (т.е. определенным целям);
2 Аналитические измерения должны проводиться с использованием проверенных методов и оборудования, пригодного для этих целей;
3 Сотрудники, производящие аналитические измерения, должны обладать соответствующей квалификацией и быть достаточно компетентными для выполнения этой задачи (а также продемонстрировать, что они могут выполнить анализ должным образом);
4 Необходима регулярная независимая оценка технических характеристик лаборатории;
5 Аналитические измерения, выполненные в одной лаборатории, должны быть сопоставимы с измерениями, выполненными в других лабораториях;
6 Организации, производящие аналитические измерения, должны иметь четко определенные процедуры контроля и гарантии качества.
Слайд 11Набор исследуемых валидационных характеристик за-
висит от назначения аналитической методики.
Типичные
валидационные характеристики:
- Правильность (Accuracy)
- Прецизионность (Precision)
- Сходимость (Repeatability)
- Внутрилабораторная прецизионность
(Intermediate Precision)
- Специфичность (Specificity)
- Предел обнаружения (Detection Limit)
- Предел количественного определения (Quantitation Limit)
- Линейность (Linearity)
- Диапазон применения (Range)
Слайд 12ГОСТ ИСО/МЭК 17025
5.4.1 Общие положения
Лаборатория в своей деятельности должна
использовать методы и процедуры, соответствующие области ее деятельности. Они включают
отбор образцов, обращение с ними, транспортирование, хранение и подготовку объектов, подлежащих испытаниям и/или калибровке, и, если уместно, оценку неопределенностей измерений, а также статистические методы анализа данных испытаний и/или калибровки.
Отклонения от методик испытаний и калибровки допускаются только при условии их документального оформления, технического обоснования, одобрения и согласия заказчика.
Примечание - Международные, региональные, национальные стандарты или общепринятые технические условия, содержащие достаточную и краткую информацию о том, как проводить испытания и/или калибровку, не нуждаются в дополнениях или переоформлении в качестве внутренних процедур, если эти стандарты написаны так, что они могут быть использованы в опубликованном виде сотрудниками лаборатории. При необходимость разрабатывают дополнительную документацию на случай альтернативных вариантов методики или дополнительных подробностей.

Слайд 13ГОСТ ИСО/МЭК 17025
5.4.2 Выбор методик
Лаборатория должна использовать методики испытаний
и/или калибровки, включая методы отбора образцов, которые отвечают потребностям заказчиков
и пригодны для предпринимаемых испытаний и/или калибровки. Преимущественно следует использовать методики, приведенные в международных, региональных (межгосударственных) или национальных стандартах. Лаборатория должна гарантировать, что она использует последнее действующее издание стандарта, кроме случаев, когда оно не подходит или это невозможно сделать. При необходимости к стандарту можно приложить дополнительные подробности с тем, чтобы обеспечить согласованное применение.
Если заказчик не указал метод, который следует использовать, то лаборатория должна выбрать соответствующие методы, которые приведены в международных, региональных или национальных стандартах, рекомендованы авторитетными техническими организациями, описаны в соответствующих научных статьях или журналах или были рекомендованы изготовителем оборудования. Разработанные или принятые лабораторией методики также могут быть использованы, если они пригодны и оценены. О выбранном методе следует уведомить заказчика.
Лаборатория должна подтвердить, что она может правильно использовать стандартные методики, прежде чем приступить к испытаниям или калибровке. Если стандартная методика меняется, то подтверждение следует повторить.
Лаборатория должна известить заказчика в случае, если предложенная им методика представляется непригодной или устаревшей.

Слайд 14Рекомендации по метрологии
Р 50.2.060-2008
Внедрение стандартизованных методик
количественного химического анализа в
лаборатории
Подтверждение соответствия установленным требованиям
Слайд 15Алгоритм процедуры внедрения МИ
Приказ (распоряжение) о назначении руководителя работ по
внедрению методики и комиссии по оценке показателей качества результатов испытаний
(измерений);
Руководитель работ разрабатывает программу (план и т.п.) внедрения и представляет ее на утверждение руководителю организации (лаборатории);
Оформление акта внедрения МИ по окончании работ и выпуск приказа (распоряжения) о внедрении МИ с ознакомлением персонала
Слайд 16Руководитель процесса
Специалисты, осуществляющие анализ рабочих проб
Комиссия
Слайд 17 Распространяется на процедуры внедрения в лаборатории методик, разработанных и аттестованных
в соответствии с ГОСТ Р 8.563
Процедура подтверждения – элемент системы
менеджмента качества лаборатории (п. 5.4.2 ГОСТ ИСО/МЭК 17025) – подтверждение возможности правильно использовать методику в лаборатории – демонстрация адекватности (подтверждение соответствия) реализуемой МКХА требованиям НД на МИ
УТВЕРЖДАЮ
___________________
«___»____________ 20 г.
ПРОГРАММА ВНЕДРЕНИЯ
(полное наименование НД на МИ в соответствии со свидетельством об аттестации )
1 Цель внедрения НД на МИ в деятельность (наименование юр. лица и лаборатории):
- обеспечение производственного экологического контроля;
- социально-гигиенический мониторинг;
- выполнение испытаний для целей сертификации продукции;
- ветеринарный контроль и т.п.
Слайд 19
2 Внедрение методики осуществляется в соответствии с требованиями Р 50.2.060-2008
специалистами лаборатории (наименование лаборатории) под руководством (должность, ФИО) по видам
работ, представленным в таблице.
Слайд 212 Этап. Подтверждение соответствия реализуемой в лаборатории методики требованиям НД
Обеспечение
и контроль необходимых условий для проведения анализа
Проверка соответствия операций и
правил, осуществляемых при реализации МИ, требованиям НД
Экспериментальная проверка правильности
использования МИ в лаборатории
Слайд 25ПРОЦЕДУРА ПОДТВЕРЖДЕНИЯ
Внедрение методики
Рабочие измерения
(при внесении изменений в НД на МИ)
Слайд 26Показатели качества методики
Показатель точности
U
Показатель воспроизводимости
σ R
S R
Показатель повторяемости
σ r
S r
Слайд 27Процедура подтверждения, порядок регистрации полученных результатов, требования к заключению о
соответствии реализованной методики требованиям НД устанавливаются в Руководстве по качеству
лаборатории (допускается разработка отдельного документа в ранге СТО, регламента, процедуры, инструкции и т.п.)
Положительные результаты процедуры – основание для использования методики в лаборатории и проведения внутреннего контроля качества результатов испытаний (анализа, исследований), получаемых с ее использованием
Слайд 28В результате конкретизации (уточнения) отдельных этапов процедуры анализа во взаимодействии
с разработчиком методики разрабатываются соответствующие лабораторные процедуры в дополнение к
установленным в НД. Такие дополнения должны быть оформлены официальным согласующим письмом разработчика, либо официальным внесением разработчиком изменения в НД на МИ (по ГОСТ 8.563)
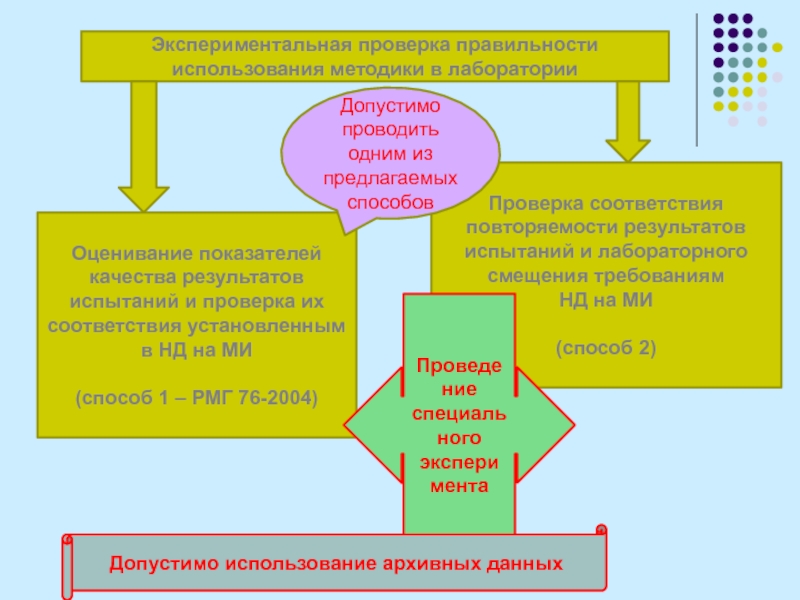
Слайд 29Экспериментальная проверка правильности использования методики в лаборатории
Оценивание показателей качества результатов
испытаний и проверка их соответствия установленным в НД на МИ
(способ
1 – РМГ 76-2004)
Проверка соответствия повторяемости результатов испытаний и лабораторного смещения требованиям
НД на МИ
(способ 2)
Допустимо проводить одним из предлагаемых способов
Проведе
ние специального экспери
мента
Допустимо использование архивных данных
Слайд 30Способ 1
Организация специального эксперимента и алгоритмы оценивания – приложение Б,
В РМГ 76-2004
Оценка выполнения условий:
σ rЛ ≤ σ r, σ RЛ ≤ σ R , ΔЛ ≤ Δ
Вывод о соответствии процедуры анализа при реализации в лаборатории требованиям НД на МИ
Оформление фактически обеспечиваемых показателей качества результатов анализа протоколом (приложение Б к Р 50.2.060-2008)
Установление нормативов ВЛК применительно к реализуемым схемам контроля
Слайд 31Способ 2
Организация специального эксперимента для проверки соответствия повторяемости требованиям МИ:
- с использованием одной рабочей пробы;
- с использованием нескольких рабочих проб
Условие для принятия решения:
S rЛ ≤ K r
Организация специального эксперимента для проверки соответствия лабораторного смещения требованиям МИ:
- с использованием ОК;
- с использованием метода добавок;
- с использованием другой (контрольной) методики анализа
Условие для принятия решения:
|θ Л | ≤ 2S Δ
Слайд 32Выводы:
Процедура анализа (измерений, испытаний) при реализации в лаборатории соответствует требованиям
НД на методику испытаний
За значение показателя точности результатов анализа допустимо
принять значение показателя точности МИ (Δ), за значение показателя внутрилабораторной прецизион-ности результатов анализа – значение показателя воспроизводимости МИ (σR )
Нормативы ВЛК допустимо устанавливать с использованием показателей качества МИ (0,84 Δ; 0,84 σR)
Слайд 33Условия проведения специальных экспериментов
Экспериментальную проверку проводят для рабочего диапазона измерений
при применении методики в лаборатории
Экспериментальную проверку проводят для поддиапазонов измерений
с постоянными значениями показателей качества методики. Поддиапазоны выбирают по п. 6.1.11 РМГ 76-2004
Используемые ОК должны быть адекватны по составу анализируемым пробам
Слайд 34Акт внедрения
цель внедрения
список исполнителей
сроки выполнения работ (допустимы ссылки
на программу внедрения – приложение к акту);
перечень контролируемых объектов
и показателей;
детальные сведения о результатах выполненных работ (в соответствии с программой), либо ссылки на документы (отчеты, справки, служебные записки, журналы, графическая информация (хроматограммы, спектры, калибровочные кривые) и др. формы записей – приложения к акту), в которых содержатся такие сведения;
детальные условия проведения экспериментов, включая процедуры отбора и подготовки проб к испытаниям, в том числе учет мешающих влияний, записи о выполненных работах (акты отбора проб, копии рабочих журналов исполнителей и пр. – приложения к акту);
процедуры вычислений и статистической обработки результатов, результаты контрольных процедур, МСИ, протоколы результатов испытаний – приложения к акту;
резюме и заключения (выводы);
протокол установленных значений показателей качества результатов испытаний – приложение к акту.
Слайд 35Оценка показателей качества результатов анализа при реализации методик в лаборатории
Организация
специального эксперимента с использованием ОК.
Пример 1
Исходные данные:
- методика
КХА проб питьевых вод для определения массовой концентрации ионов кобальта фотометрическим методом;
- диапазон измерений - от 0,4 до 0,8 мг/дм3;
- значениям показателей точности, правильности, прецизионности установлены при аттестации методики и приведены в свидетельстве об аттестации методики и НД на МИ;
- в соответствии с прописью аттестованной методики результат анализа массовой концентрации ионов кобальта в рабочих пробах питьевых вод представляет собой среднее арифметическое двух результатов единичного анализа (параллельных определений).
Задача - оценка показателей качества результатов анализа при реализации методики в конкретной лаборатории.
Слайд 36Оценка показателей качества результатов анализа при реализации методик в лаборатории
Метод
оценки показателей точности, правильности и прецизионности – с применением образца
для оценивания (ОО) в виде аттестованного раствора при получении экспериментальных данных в условиях внутрилабораторной прецизион-ности.
Образец для оценивания - аттестованный раствор, приготовленный на основе государственного стандартного образца состава раствора ионов кобальта - ГСО 7258-96.
Аттестованная характеристика ГСО 7268 - 96 – аттестованное значение массовой концентрации ионов кобальта 1 мг/см3, относительная погрешность аттестованного значения – 1 %.
Метрологические характеристики аттестованного раствора: аттестованное значение - массовая концентрация ионов кобальта - 0,50 мг/дм3; погрешность аттестованного значения - 0,01 мг/дм3 при Р=0,95.
Основные допущения в рамках выбранного метода оценки:
- распределение случайной и систематической погрешности результатов испытаний принимают нормальным;
- распределение погрешности аттестации СО принимают равномерным;
- влияющие факторы пробы не оказывают значимого влияния на погрешность результата испытания.

Слайд 37
Таблица 1 Значения показателей точности, правильности, прецизионности методики анализа (приведены
в свидетельстве об аттестации методики)
Слайд 38Выбор количества серий результатов единичного анализа, которое должно быть получено
в каждой лаборатории, проводилось в соответствии с п. …ГОСТ Р
ИСО 5725-2 (РМГ 76-2004 (Приложение Ж))
Для числа параллельных определений, приведенных в прописи методики (n=2), учитывая, что значения неопределенности оценок должны быть не более 0,33, рассчитываем
Устанавливаем
При n=2 и
= 2,2, L=20 (для оценки погрешности),
L = 15 (для оценки внутрилабораторной
прецизионности)
Слайд 39Условия проведения эксперимента
Экспериментальные данные были получены в лаборатории при вариации
всех факторов, формирующих внутрилабораторную прецизионность - серии результатов единичного анализа
получали:
- в разное время (указать период или сослаться на пункт программы внедрения);
- разные операторы (перечислить ФИО);
- используя разные наборы мерной посуды;
- применяя разные партии реактивов одного типа (конкретизировать).
Результаты единичного анализа внутри каждой серии были получены в одинаковых условиях и практически одновременно.
Время проведения эксперимента составило период, охватывающий следующие изменения:
- градуировку средств измерений (КФК-3) (как альтернатива – проверка стабильности градуировки КФК-3);
- смену реактивов одного типа (конкретизировать);
- изменение условий окружающей среды (конкретизировать);
- и т. п.
Слайд 40Оценка показателей качества результатов испытаний
Экспериментальные данные оформляют в виде сводных
таблиц (формы записей разрабатываются лабораторией!).
Оценка показателя повторяемости результатов испытаний
По результатам
экспериментальных данных, полученных внутри каждой серии, рассчитывают среднее арифметическое и выборочную дисперсию S2l результатов единичного анализа аттестованного раствора, полученных в условиях повторяемости (параллельных определений).
l=1…..L (для результатов L=20 , N=2)
n = 1….N
и выборочную дисперсию
результатов испытаний
Слайд 41На основе полученных значений двадцати выборочных дисперсий проверяют гипотезу о
равенстве генеральных дисперсий, используя критерий Кохрена (РМГ 61).
Для этого выбирают
максимальную дисперсию
и рассчитывают сумму всех дисперсий, включая максимальную.
Расчетное значение критерия Кохрена рассчитывают по формуле:
и сравнивают его с табличным
где
соответствующее числу суммируемых дисперсий, и принятой вероятности
Слайд 42Таким образом,
>
=0,389 – дисперсии не однородны.
из дальнейших расчетов
исключают.
Затем находят сумму оставшихся 19 дисперсий и максимальную дисперсию.
Рассчитывают значение
критерия Кохрена для максимальной дисперсии (из оставшейся выборки).
Сравнивают его с табличным значением для L=19.
Таким образом,
<
= 0,403 – т.е. дисперсии однородны.
(количество дисперсий, оставшихся после проверки дисперсий на однородность, L*=19).
Не исключенные из расчетов дисперсии считают однородными и по ним оценивают Srл - СКО, характеризующее повторяемость результатов единичного анализа (параллельных определений) СО.
Слайд 43В качестве показателя повторяемости
принимают: σrл ~ Srл =0,02 мг/дм3.
.
Рассчитывают предел повторяемости:
Оценка
показателя внутрилабораторной прецизионности результатов испытаний
Рассчитывают общее среднее (
) результатов испытаний, полученных в
- средних по серии) относительно общего среднего значения (
условиях внутрилабораторной прецизионности, и среднее квадратическое отклонение, характеризующее разброс средних арифметических (
)
Показатель внутрилабораторной прецизионности результатов анализа в виде среднего квадратического отклонения – σRл устанавливаем, принимая его равным SRл.
σRл = SRл = 0,04 ;
Рассчитывают предел внутрилабораторной прецизионности:
= 2,77 . 0,04 = 0,11 мг/дм3.
Слайд 44Оценка показателя правильности результатов испытаний
(систематической погрешности лаборатории при реализации методики)
Рассчитывают
оценку математического ожидания систематической погрешности лаборатории как разность между общим
средним арифметическим значением результатов испытаний (
) и аттестованным значением в
СО – (С):
Рассчитываем значение квантиля t распределения Стьюдента:
где
– погрешность аттестованного значения аттестованного раствора.
Полученное значение t сравнивают с табличным значением критерия Стьюдента (РМГ 61) tтабл при числе степеней свободы f=L’-1=19-1=18, для доверительной вероятности Р=0,95, tтабл=2,10.
незначима на фоне случайного разброса и принимаем ее равной нулю.
Показатель
правильности результатов анализа (верхнюю (
) и нижнюю (
границы, в которых неисключенная систематическая погрешность лаборатории находится с принятой вероятностью р=0,95 рассчитываем по формуле:
мг/дм3
Оценка показателя точности результатов испытаний
Показатель точности результатов испытаний [верхнюю (
) и нижнюю (
)
границы, в которых погрешность любого из совокупности результатов испытаний, полученных в лаборатории при реализации методики находится с принятой вероятностью Р=0,95, рассчитывают по формуле:
мг/дм3.
Слайд 46Результаты расчета показателей точности, правильности, повторяемости и внутрилабораторной прецизионности оформляются
в виде таблице
Таблица – Значения показателей точности, правильности, повторяемости,
внутрилабораторной
прецизионности результатов анализа.
Установленные в лаборатории значения показателей точности, правильности, повторяемости, внутрилабораторной прецизионности результатов анализа не превосходят значений показателей точности, правильности, повторяемости и воспроизводимости методики анализа. Результаты оценки показателей качества результатов анализа оформляют протоколом.
Слайд 47Рекомендуемые способы установления расчетных значений показателей точности (характеристик погрешности), показателей
правильности (характеристик систематической погрешности), показателей прецизионности: повторяемости и воспроизводимости (характеристик
случайной погрешности: в условиях повторяемости, в условиях воспроизводимости) методик анализа