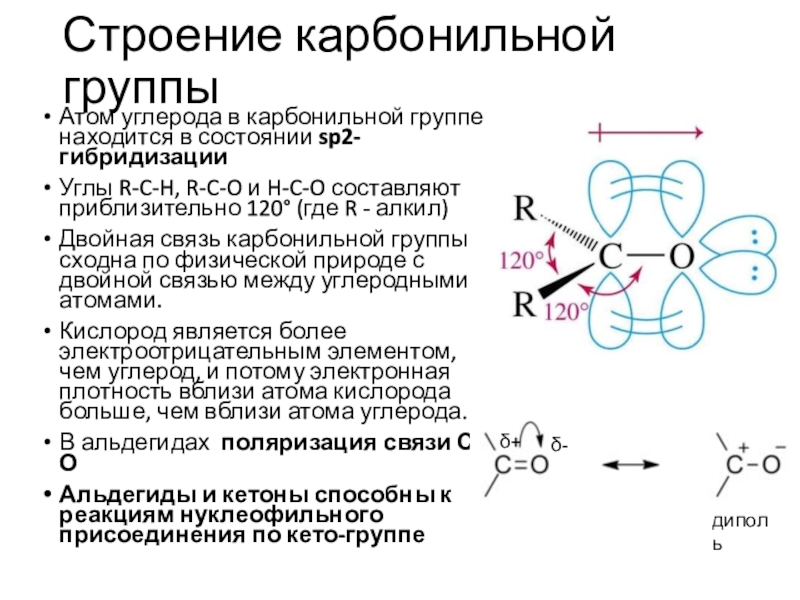
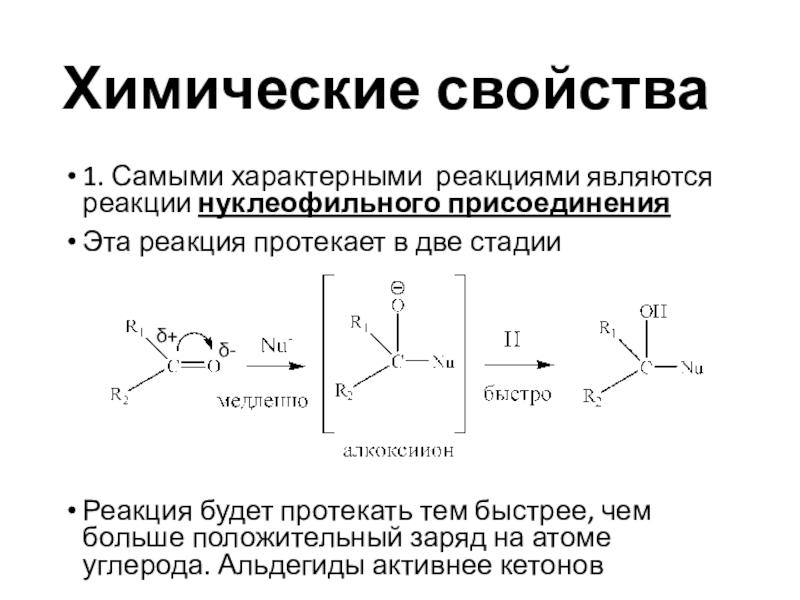
карбонильной группой
Она придает данным соединениям специфические свойства, которые разительно
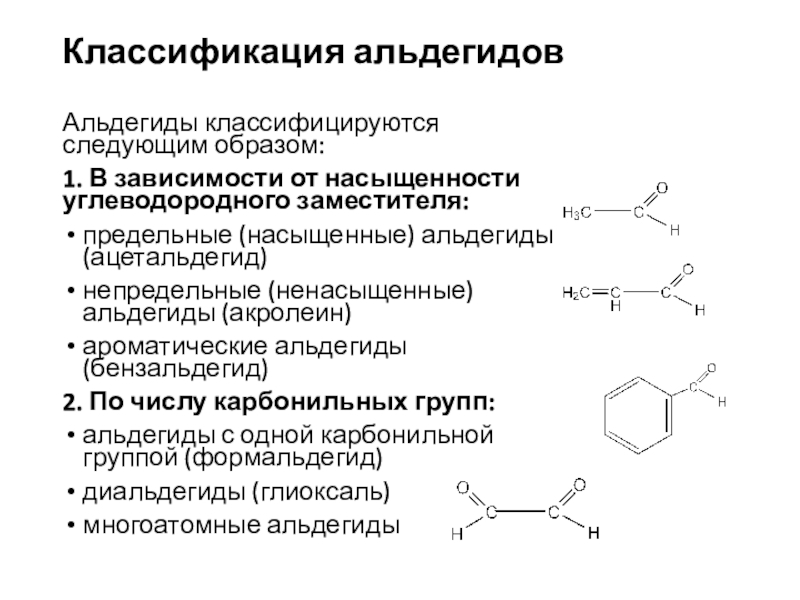
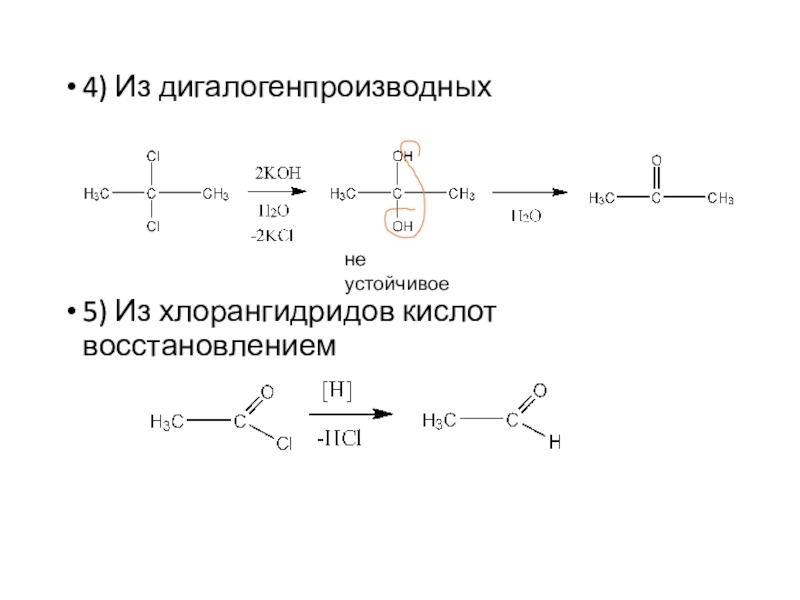
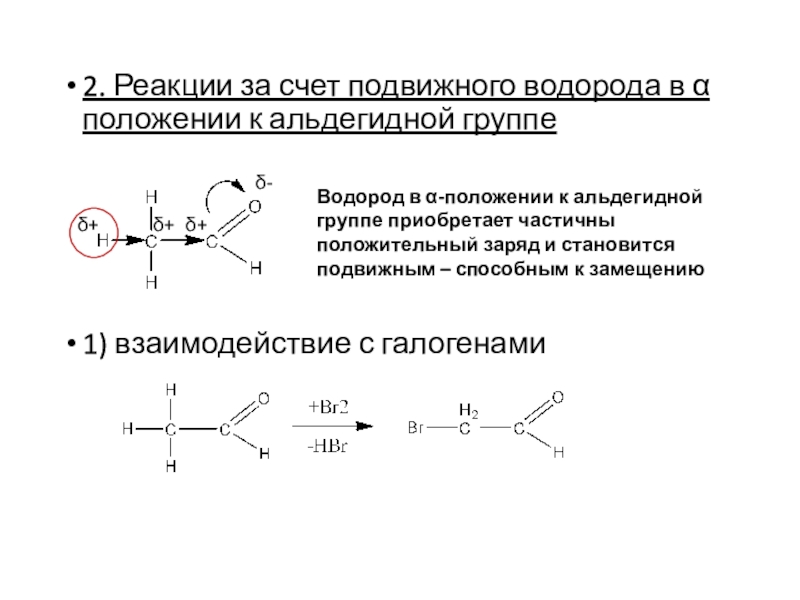
отличают их от соединений других классовЕсли карбонильный атом связан с одним атомом углерода и водородом, т.е. расположен в начале цепи, то соединение принадлежит к классу альдегидов
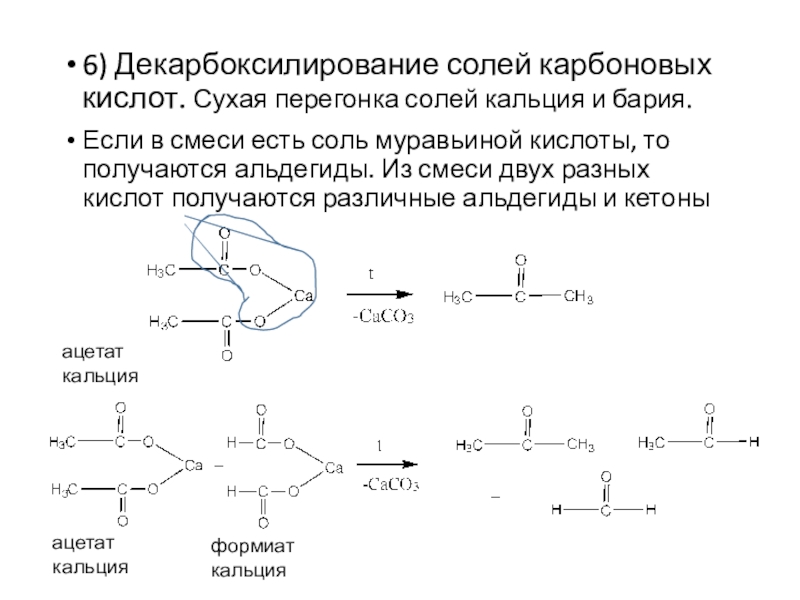
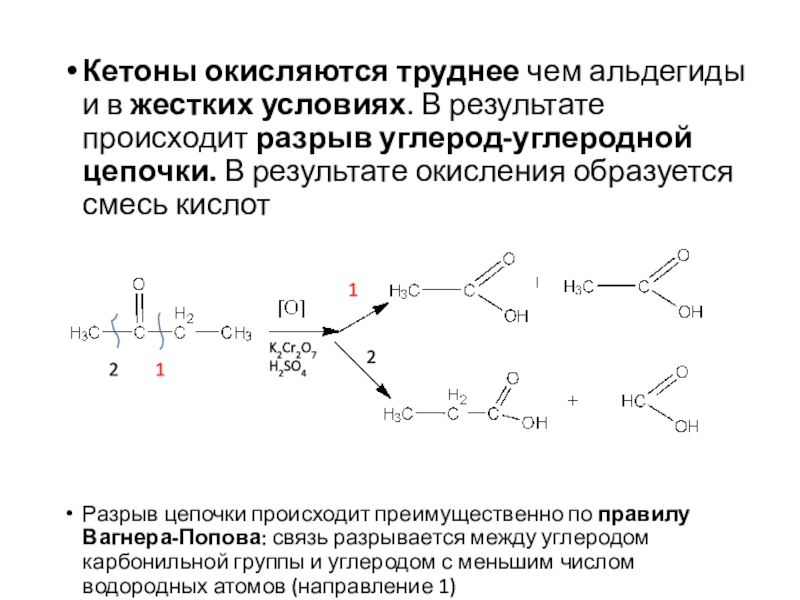
Если карбонильная группа связана с двумя углеродными атомами, и находится внутри цепи – это класс кетонов
альдегид
кетон