ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ
КАФЕДРА ХИМИИЛекция
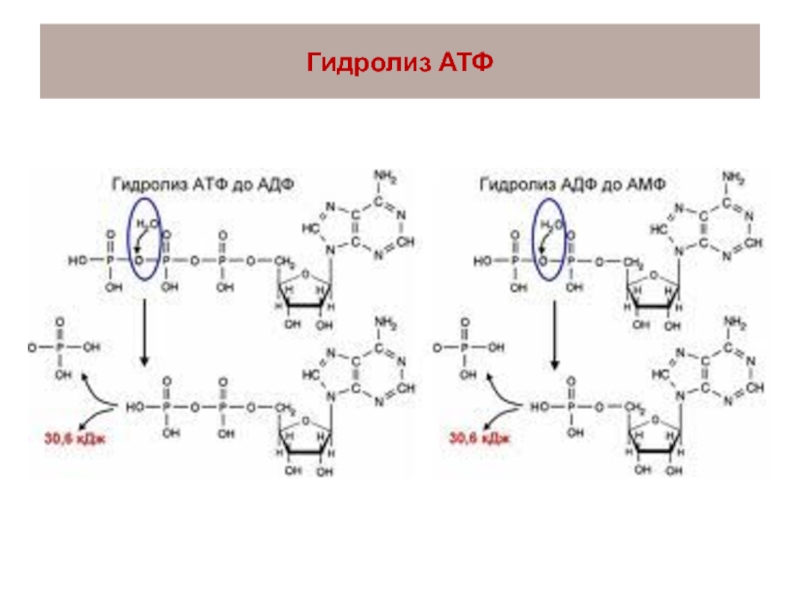
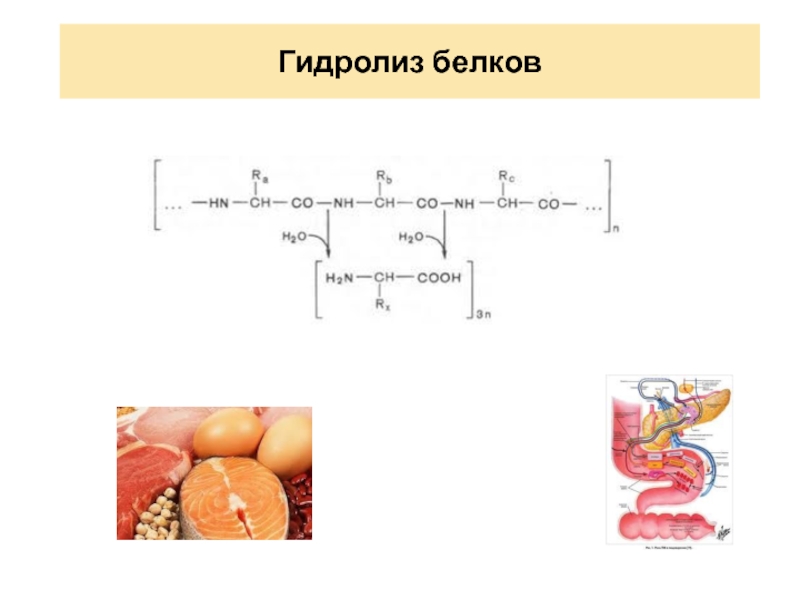
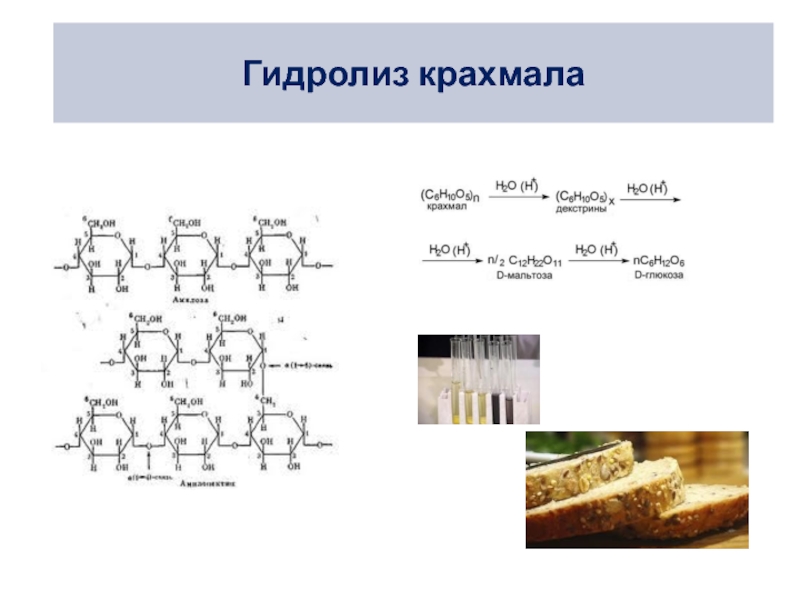
Процессы гидролиза. Количественные характеристики гидролиза
и его биологическая роль
Определение гидролиза.
Виды гидролиза солей.
Протолитические равновесия процесса гидролиза.
Количественные характеристики процесса гидролиза.
Лектор: Ирина Викторовна Ганзина
кандидат биологических наук
доцент кафедры химии














![ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ
КАФЕДРА ХИМИИ
Лекция
Процессы Умножим обе части уравнения на [H2O]:Обозначим произведение двух констант – константа Умножим обе части уравнения на [H2O]:Обозначим произведение двух констант – константа гидролиза :Тогда:Кравн. . [H2O] =Кравн.](/img/thumbs/ad0d76d5ec5480d8712b4068618c5c9a-800x.jpg)
![ОМСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ
КАФЕДРА ХИМИИ
Лекция
Процессы Кгидр. =[H+] .[OH-] = Кв = 10-14=, аКгидр. =, тогда: Кгидр. =[H+] .[OH-] = Кв = 10-14=, аКгидр. =, тогда: 1Kдисс. (NH4OH)](/img/thumbs/4135f27b95d1ff8004558e024ce90bbf-800x.jpg)