Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Опыты Резерфорда. Ядерная модель атома
Содержание
- 1. Опыты Резерфорда. Ядерная модель атома
- 2. Атомная и ядерная физика раздел физики, изучающий
- 3. Явления, подтверждающие сложное строение атома Явление электролиза
- 4. Демокрит существует предел деления атома АристотельДелимость вещества
- 5. Первая модель атома— модель Томсона (1903 г.).
- 6. Недостатки модели атома Томсона Она не могла
- 7. Томсон, пытаясь согласовать эту модель с данными
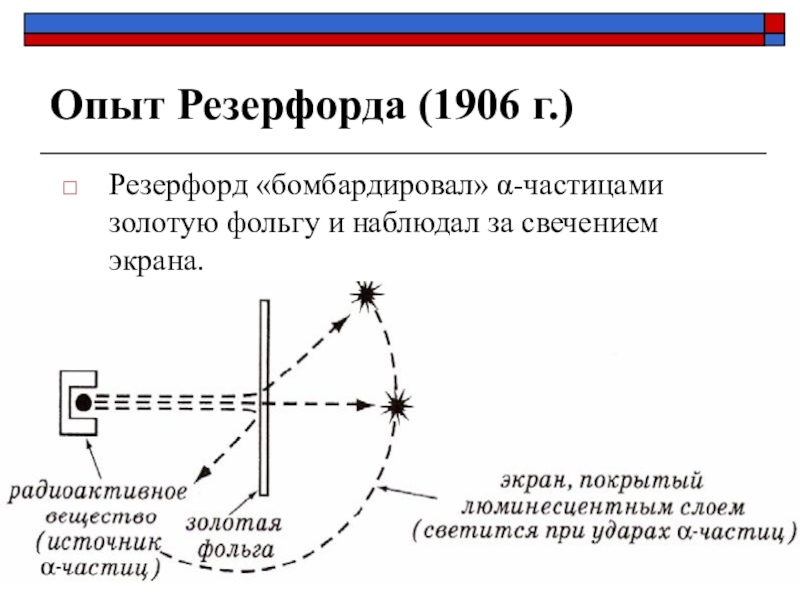
- 8. Опыт Резерфорда (1906 г.) Резерфорд «бомбардировал» α-частицами золотую фольгу и наблюдал за свечением экрана.
- 9. При попадании α-частицы на экран возникает свечение люминесцентного слоя.
- 10. Наблюдения из опыта большинство α -частиц пролетает
- 11. Слайд 11
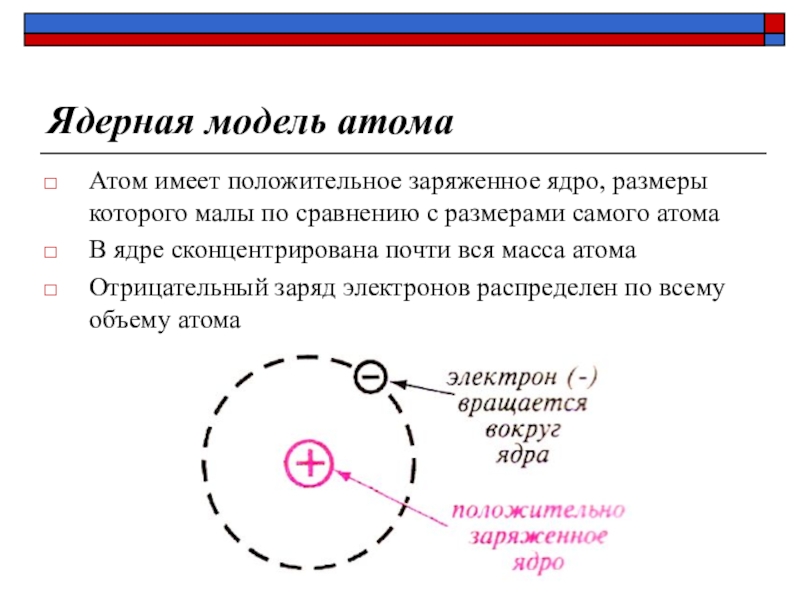
- 12. Ядерная модель атома Атом имеет положительное заряженное
- 13. Выводы Резерфорда (модель атома):
- 14. Отличие атомных систем от планетных Планеты притягиваются
- 15. Противоречия планетарной модели атома и классической физики Но: атом устойчив!!!1)
- 16. 2) Вследствие непрерывной потери Е электрона, атом
- 17. ВыводЭти противоречия объясняются невозможностью применения к электронам в атомах законов классической физики.
- 18. Это интересноЕсли бы все электроны тела человека
- 19. Это интересноРезерфорд был первым человеком, которому открылась
- 20. Скачать презентанцию
Атомная и ядерная физика раздел физики, изучающий строение атома и атомного ядра и процессы, связанные с ними
Слайды и текст этой презентации
Слайд 2Атомная и ядерная физика
раздел физики, изучающий строение атома и атомного
ядра и процессы, связанные с ними
Слайд 3Явления, подтверждающие сложное строение атома
Явление электролиза (Фарадей, 1833г)
Электромагнитная теория
света (Максвелл)
Рентгеновские лучи (1895)
Явление радиоактивности (Беккерель, 1896г)
Катодные лучи – электроны
(Дж. Томсон, 1897г)Линейчатые спектры
Фотоэффект
Опыты Резерфорда по зондированию вещества
Слайд 4Демокрит
существует предел деления атома
Аристотель
Делимость вещества бесконечна
1626г, Париж
Учение об атоме запрещено по страхом смерти
Слайд 5Первая модель атома
— модель Томсона (1903 г.). Положительно заряженный шар,
внутри которого находятся электроны («пудинг с изюмом»).
Суммарный положительный заряд =
суммарному отрицательному заряду (атом в целом нейтрален).Слайд 6Недостатки модели атома Томсона
Она не могла объяснить излучения большого
числа спектральных линий
Не давала возможность понять, чем определяются размеры
атомов. Оказалась в полном противоречии с опытами Резерфорда
Слайд 7Томсон, пытаясь согласовать эту модель с данными спектроскопии и периодическим
законом Менделеева, распределял электроны по концентрическим кольцам, приписав каждому из
электронов собственную частоту колебаний, совпадающую с одной из частот спектра излучения атомаСлайд 8Опыт Резерфорда (1906 г.)
Резерфорд «бомбардировал» α-частицами золотую фольгу и наблюдал
за свечением экрана.
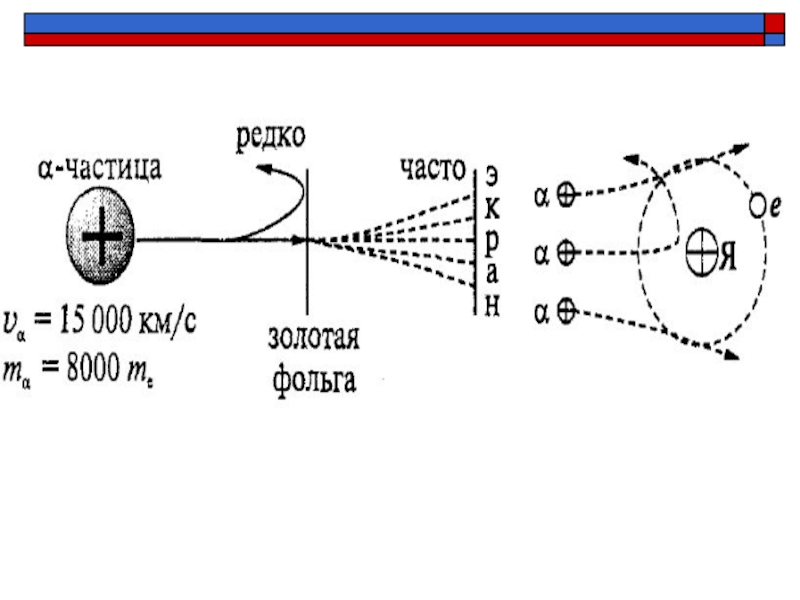
Слайд 10Наблюдения из опыта
большинство α -частиц пролетает сквозь фольгу не отклоняясь
небольшое
количество α -частиц отклоняется на небольшие углы
есть α-частицы, отклоняющиеся на
углы более 90°Слайд 12Ядерная модель атома
Атом имеет положительное заряженное ядро, размеры которого
малы по сравнению с размерами самого атома
В ядре сконцентрирована
почти вся масса атома Отрицательный заряд электронов распределен по всему объему атома
Слайд 14Отличие атомных систем от планетных
Планеты притягиваются к Солнцу силами
всемирного тяготения.
Электроны притягиваются к ядру кулоновскими силами.
Силы гравитационного
притяжения между электронами и ядром ничтожно малы по сравнению с электромагнитными Слайд 162) Вследствие непрерывной потери Е электрона, атом должен излучать непрерывный
спектр, но атом излучает линейчатый спектр.
3) Атом излучает свет
не все время, а лишь при определенных условиях (прохождение тока в газах, нагревание до высокой температуры),т.е. при сообщении ему энергии. Противоречия планетарной модели атома и классической физики