Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Оренбургская государственный медицинский университет Кафедра нормальной
Содержание
- 1. Оренбургская государственный медицинский университет Кафедра нормальной
- 2. Слайд 2
- 3. Новая иммунология – иммунология
- 4. Чарльз Джаневей (1943—2003)Чарльз Дженуэй (1943-2003) и Руслан Меджитов
- 5. 1988 г. – C. Hashimoto, K. L. Hudson, K. V. Anderson
- 6. Определение понятия иммунной системы и иммунитетаИммунная система
- 7. Виды иммунитета и главные функцииВрожденный иммунитетАдаптивный иммунитетЗащита
- 8. Виды веществ, несущих признаки генетически чужеродной информации
- 9. Определение понятия антиген, свойства антигеновАнтиген – молекула,
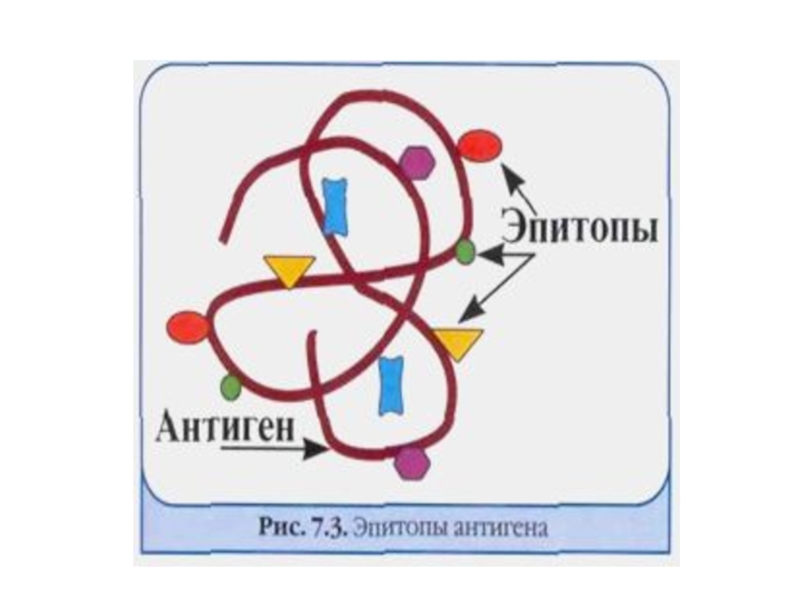
- 10. ЭПИТОПЫ АНТИГЕНА
- 11. Виды антигеновПо физико-химическим свойствам:
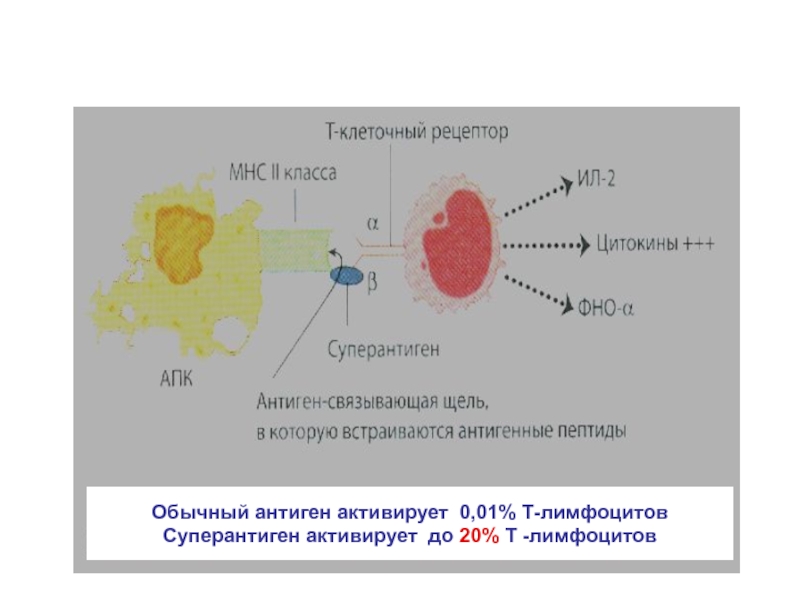
- 12. Обычный антиген активирует 0,01% Т-лимфоцитовСуперантиген активирует до 20% Т -лимфоцитовПОСЛЕДСТВИЯ СТИМУЛЯЦИИ Т-ЛИМФОЦИТОВ СУПЕРАНТИГЕНОМ
- 13. АнтителаАнтитела – специфические гаммаглобулины (гликопротеиновые молекулы из
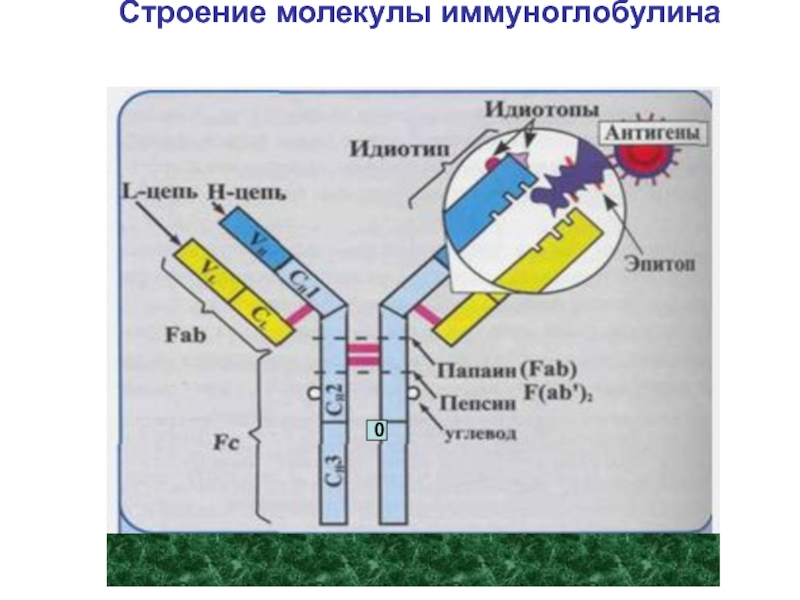
- 14. Строение молекулы иммуноглобулина G0
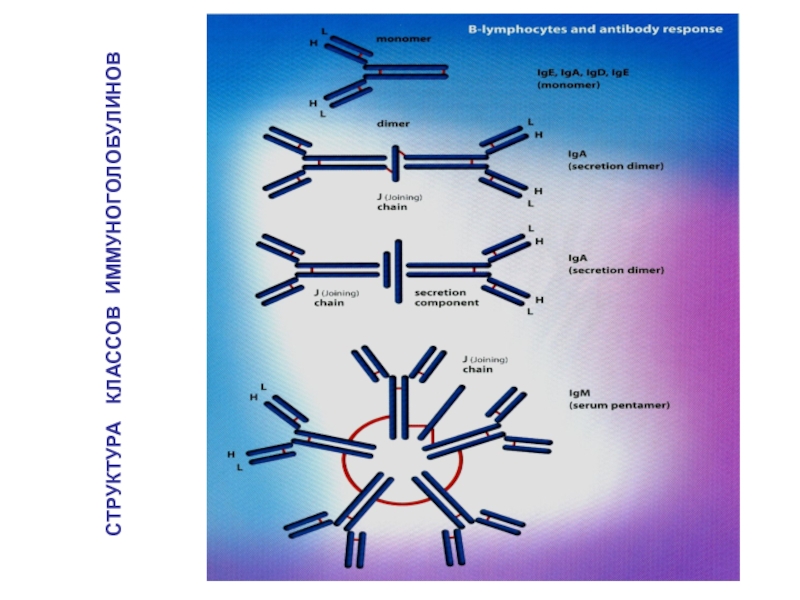
- 15. СТРУКТУРА КЛАССОВ ИММУНОГОЛОБУЛИНОВ
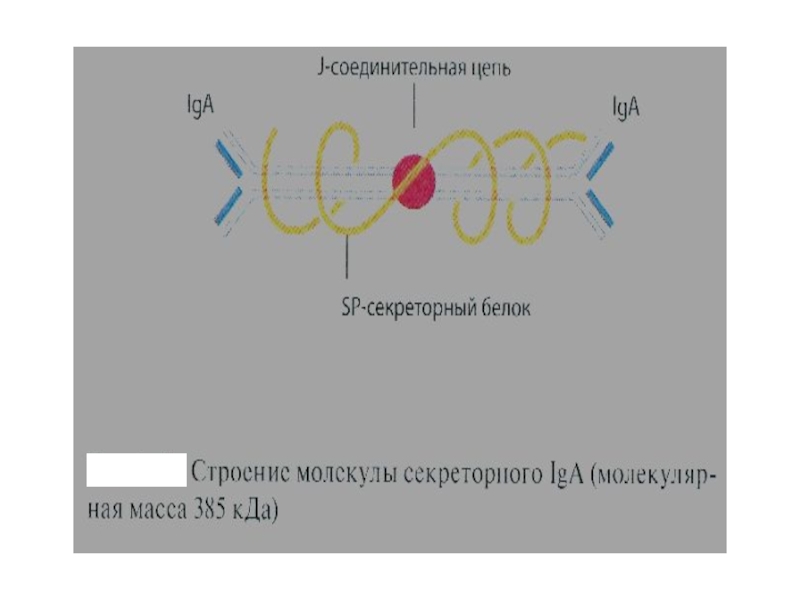
- 16. Слайд 16
- 17. Функции антителСпецифическое связывание АГ Fab-фрагментом АТ, образование
- 18. Слайд 18
- 19. Структура иммунной системыЦентральные органы (красный костный
- 20. Центральные и периферические органы иммунной системы
- 21. СТРУКТУРА И КЛЕТОЧНЫЙ СОСТАВ ТИМУСА (СХЕМА) КораМедуллаТельца ГассаляКортико-медулл.сочленениеСубкасуляр-ная зонаТрабекулаКапсулаКортикальныеТЭКМедуллярныеТЭКТимоцитыДендритныеклеткиМакрофаги
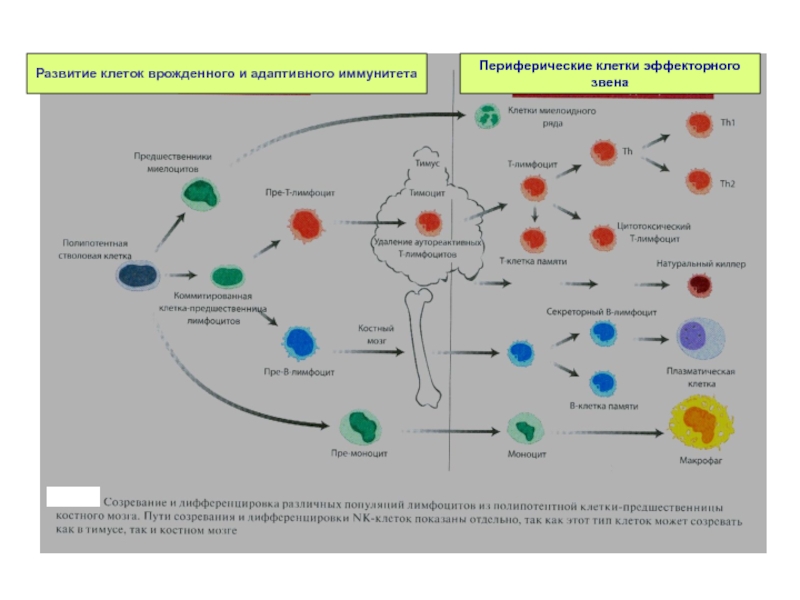
- 22. Развитие клеток врожденного и адаптивного иммунитетаПериферические клетки эффекторногозвена
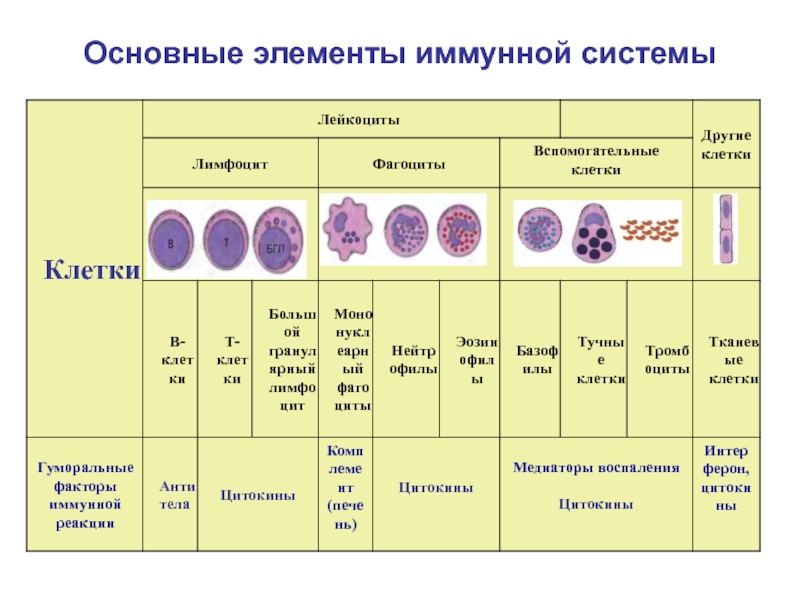
- 23. Основные элементы иммунной системы
- 24. Нейтрофилы фагоцитоз
- 25. Слайд 25
- 26. Слайд 26
- 27. Свойства иммунной системыВысокая специфичность (лимфоциты с помощью
- 28. Основные понятия и термины, используемые при изучении
- 29. Регуляторные Т - клетки CD4+ CD25+Foxp3+ возникают
- 30. Интервалы распределения фенотипов лимфоцитов условно здоровых доноров
- 31. Основные понятия и термины, используемые при изучении
- 32. Основные понятия и термины, используемые при изучении
- 33. Основные понятия и термины, используемые при изучении
- 34. Основные понятия и термины, используемые при изучении
- 35. Основные понятия и термины, используемые при изучении
- 36. Взаимосвязь врожденного и адаптивного иммунитета I. Врожденный
- 37. Понятие врожденного иммунитета Врожденный иммунитет
- 38. Отличительтные свойства врожденного иммунитетаЯвляется главной системой (сенсором)
- 39. Механизмы распознавания «своего» и «чужого» на
- 40. Эффекторы врожденного иммунитета (клетки, гуморальные факторы)Фагоцитирующие клетки
- 41. Эффекторные молекулы врожденного иммунитетаПептиды: Дефенсины беспозвоночныхβ-дефенсиныα-дефенсины-дефенсиныкателицидины (LL-37,
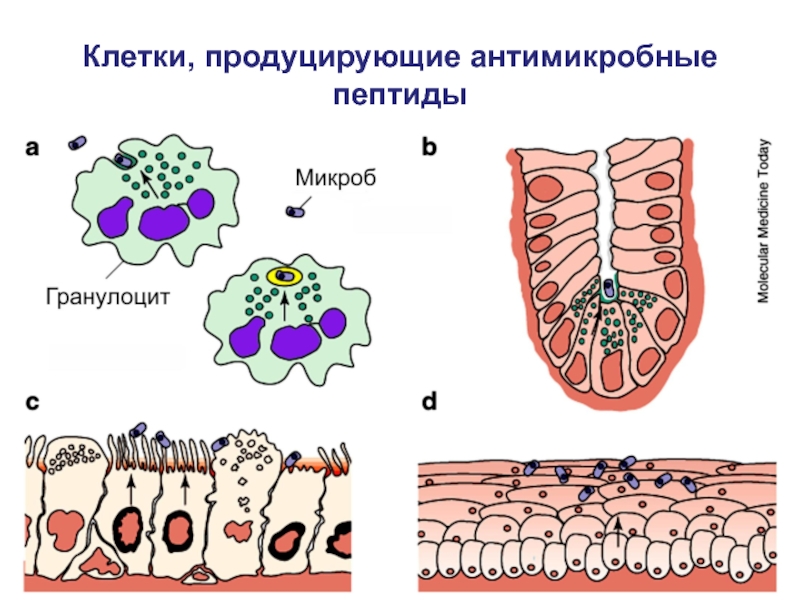
- 42. Клетки, продуцирующие антимикробные пептиды
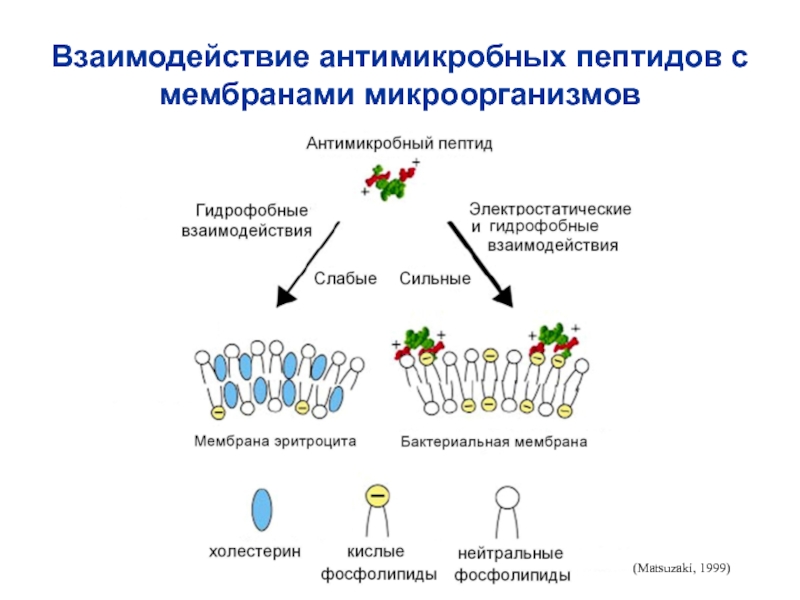
- 43. Взаимодействие антимикробных пептидов с мембранами микроорганизмов(Matsuzaki, 1999)
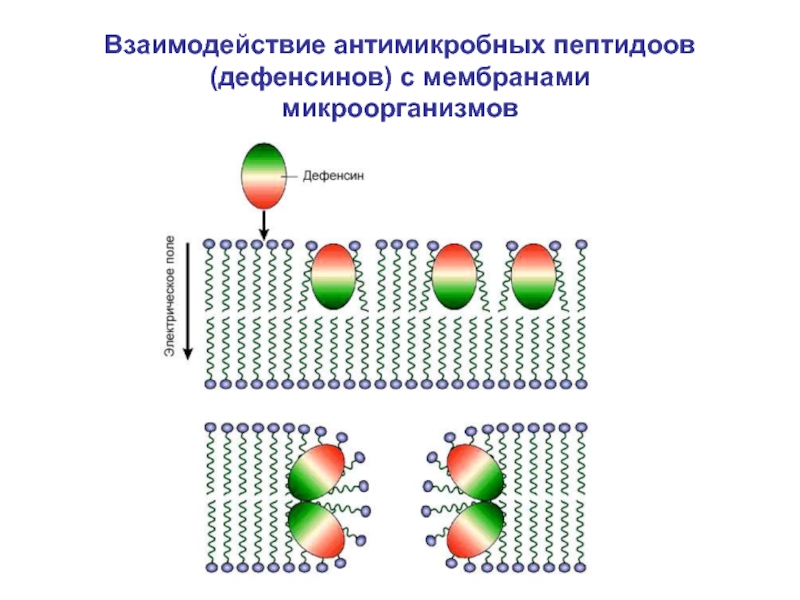
- 44. Взаимодействие антимикробных пептидоов (дефенсинов) с мембранами микроорганизмов
- 45. Слайд 45
- 46. Слайд 46
- 47. Слайд 47
- 48. Провоспалительные цитокиныПровоспалительные цитокиныИнфекционноевоспалениеСтерильноевоспалениеБелки теплового шока, коисталлы уратов, кристаллы пирофофата кальция, амилоид В, холестерин
- 49. Патоген (ПГ, ЛПС) - рецепторы (Toll-like, NOD-like,
- 50. Цитокины – эндогенные полипептидные медиаторы межклеточного взаимодействияCистема
- 51. Транскрипциягенов цитокиновПролиферация,секреция биологически активных молекул,цитотоксичность
- 52. Классификация цитокинов по биологическим эффектам 1. Факторы
- 53. Классификация цитокинов по влиянию на воспалениепровоспалительныеИЛ-1, ИЛ-6,
- 54. Слайд 54
- 55. Типы цитокиновой регуляции клеток - мишеней
- 56. Схема передачи цитокинового сигналаЦитокин - Рецептор– транскрипционный фактор – активация генов –синтез и секреция цитокина
- 57. СВОЙСТВА ЦИТОКИНОВПринадлежность к пептидамСетевой принцип работыИндуцибельностьСинтез de novoИзбыточностьПлейотропность действияСпецифичностьСинергизмАнтагонизмКаскадность
- 58. Особенности взаимодействия цитокинов
- 59. Слайд 59
- 60. ЦИТОКИНОВЫЙ ШТОРМThe term “cytokine storm” calls up
- 61. Блокировка ФНО: лекарства* *Примерная стоимость курса лечения в Европе – 15 тыс Евро в год
- 62. Гранулемы образуются вокруг клеток, зараженных бактериями, инкапсулируя
- 63. Адаптивный иммунитетЭволюционно более поздний. Эффекторы адаптивного иммунитета:
- 64. Механизмы распознавания «своего» и «чужого» адаптивным иммунитетом
- 65. Слайд 65
- 66. Строение молекул МНС I и МНСII классовщель Бьоркмана
- 67. РАСПОЗНАВАНИЕ АНТИГЕНА МЕХАНИЗМАМИ АДАПТИВНОГО ИММУНИТЕТА
- 68. Слайд 68
- 69. Слайд 69
- 70. Иммунный ответ Иммунный ответ – специфическая
- 71. Типы иммунного ответаКлеточный (клеточно-воспалительный; клеточно-цитотоксический)Гуморальный
- 72. Cхема развития гуморального иммунного ответаСинтез АТ (IgM, IgG, IgA
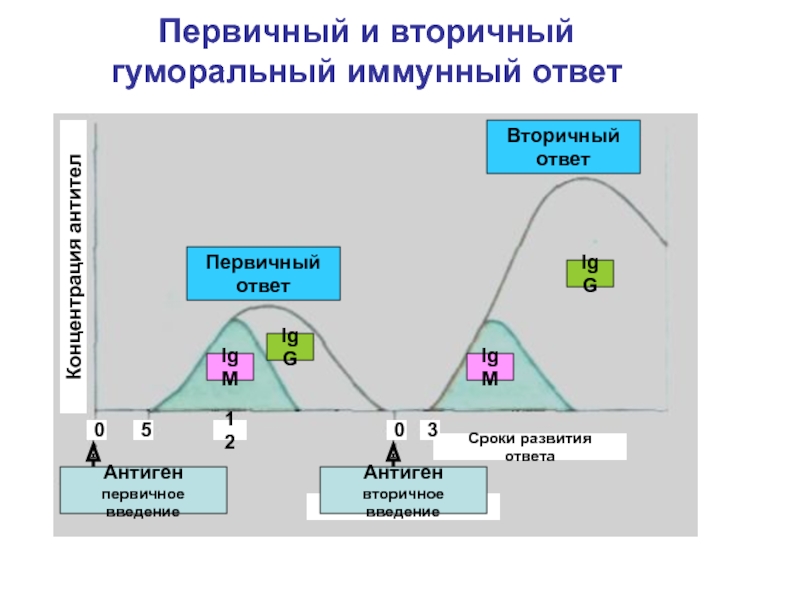
- 73. Первичный и вторичный гуморальный иммунный ответПервичныйответВторичныйответАнтигенпервичное введениеКонцентрация антителIg MIg GIgGIg MСроки развития ответа012503Антигенвторичное введение
- 74. Слайд 74
- 75. Слайд 75
- 76. Слайд 76
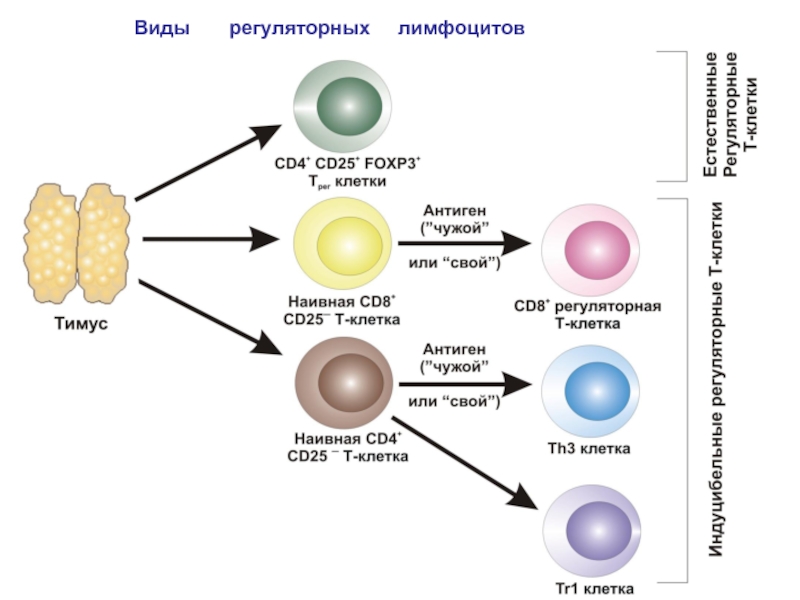
- 77. Виды регуляторных лимфоцитов
- 78. Основные характеристики ТрегПостоянные маркерыСD25+ (альфа цепь рецептора
- 79. В презентации доклада использованы материалы лекции :
- 80. Благодарю за внимание !
- 81. Типы иммунного ответаФакторы, определяющие тип ИО природа
- 82. Слайд 82
- 83. Иммунный синапс - структурированная (упорядоченная ) зона
- 84. Характеристика регуляторных Т-клеток В 1995 г. С.
- 85. Неоднородность CD4+Th клетокПосле активации, индуцированной антиген-представляющими клетками,
- 86. Слайд 86
- 87. ЭТАПЫ ПРЕДСТАВЛЕНИЯ АГ Т-КЛЕТКАМФерментативная переработка экзогенных и
- 88. Ц И Т О К И Н
- 89. Основные понятия и термины, используемые при изучении
- 90. Лекарственные препараты на основе генно-инженерных гуманизированных моноклональных
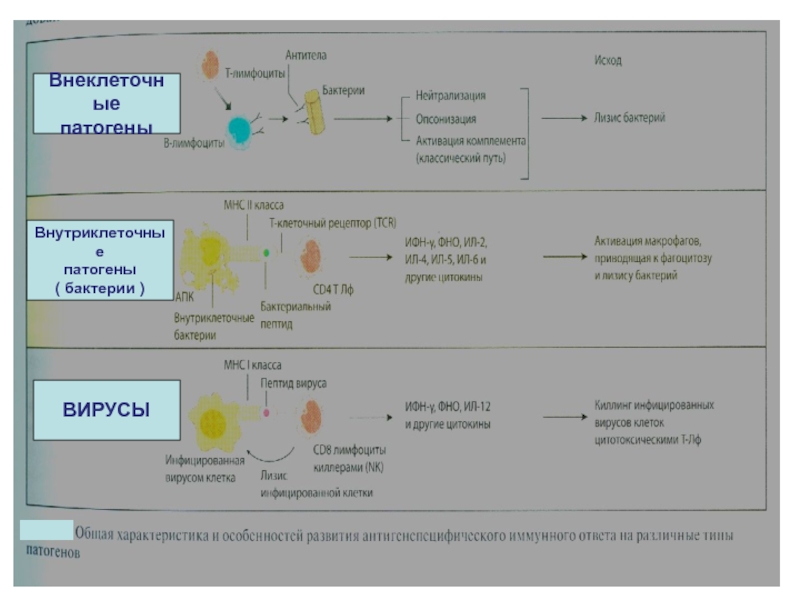
- 91. ВнеклеточныепатогеныВнутриклеточныепатогены ( бактерии )ВИРУСЫ
- 92. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Оренбургская государственный медицинский университет
Кафедра нормальной физиологии
Физиология иммунной системы
проф. Чайникова И.Н.
Слайд 3 Новая иммунология – иммунология
образраспознающих
рецепторов
( К.А.Лебедев, И.Д.Понякина,2006 )
Слайд 6Определение понятия иммунной системы и иммунитета
Иммунная система – совокупность органов
и тканей, обеспечивающих иммунитет
(клетки, которые осуществляют иммунную защиту организма,
коллективно создают иммунную систему, но они не составляют систему в смысле анатомически связанных органов, подобно желудочно-кишечному тракту или сердечно сосудистой системе) Иммунитет – способность организма защищать генетическую однородность, биологическую индивидуальность
Основная цель иммунитета – распознать чужеродное и уничтожить (удалить, элиминировать)
Слайд 7Виды иммунитета и главные функции
Врожденный иммунитет
Адаптивный иммунитет
Защита организма от агрессии
биологического происхождения:чужеродных и опасных агентов - инфекций и опухолей (АГ)
Защита
от внедрения в ДНК генетически чужеродного материала из инфекционных агентов (т.е. от «генетической грязи») Слайд 8Виды веществ, несущих признаки генетически чужеродной информации
микроорганизмы (внутри- и
внеклеточные): бактерии, вирусы, грибы, простейшие
чужеродные вещества немикробного происхождения (продукты
питания - аллергены)чужеродные клетки, ткани, мутантные клетки (опухолевые)
Слайд 9Определение понятия антиген, свойства антигенов
Антиген – молекула, которую могут специфически
распознавать элементы иммунной системы (антитела и иммунные клетки)
Свойства антигена: чужеродность,
специфичность, антигенность, иммуногенностьАнтигенная детерминанта (эпитоп)-участок молекулы АГ, определяющий его специфичность и связывающийся с антителами и АГ-распознающими рецепторами Т- лимфоцитов (ТКР) и В-лимфоцитов (ВКР).
Слайд 11Виды антигенов
По физико-химическим свойствам:
растворимые (бактериальные
токсины); корпускулярные (частицы вирусов, бактериальные клетки, пыльца растений, эритроциты)
По способности
вовлекать в иммунный ответ Т-лимфоциты:
тимусзависимые (большинство природных антигенов)
тимуснезависимые (липополисахарид - ЛПС грамотрицательных бактерий, флагеллин бактерий)
Суперантигены (бактериальные продукты- стафилококковые энтеротоксины, скарлатинозный токсин) - вызывают избыточную активацию лимфоцитов,
взаимодействуя неспецифически (вне
антигенсвязывающего центра) с АГ- распознающими
рецепторами лимфоцитов
Слайд 12Обычный антиген активирует 0,01% Т-лимфоцитов
Суперантиген активирует до 20% Т -лимфоцитов
ПОСЛЕДСТВИЯ
СТИМУЛЯЦИИ Т-ЛИМФОЦИТОВ СУПЕРАНТИГЕНОМ
Слайд 13Антитела
Антитела – специфические гаммаглобулины (гликопротеиновые молекулы из семейства иммуноглобулинов -
Ig), образующиеся под действием антигена и вступающие во взаимодействие с
этим антигеномПаратоп - участок молекулы антитела, комплементарный эпитопу антигена и способный специфически с ним связываться
Слайд 17Функции антител
Специфическое связывание АГ Fab-фрагментом АТ, образование иммунного комплекса (АГ+АТ)
Связывание
комплекса АГ-АТ с макрофагами и нейтрофилами,
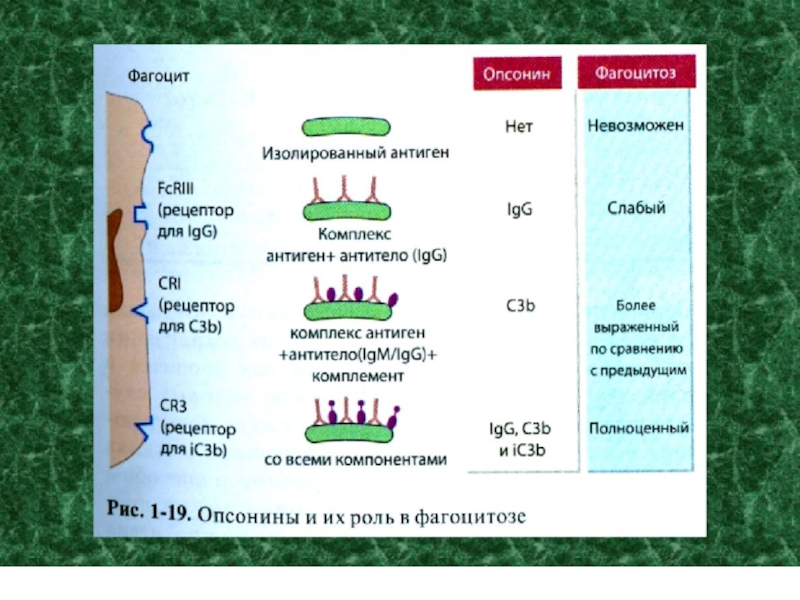
экспрессирующими на поверхности Fc-рецепторы, и последующая активация фагоцитоза (опсонизация)
Активация системы комплемента (по классическому пути) и
комплемент - опосредованный лизис бактериальной клетки
Нейтрализация токсинов
Антителозависимая клеточная цитотоксичность, опосредуемая через
Fc-рецепторы на натуральных киллерах (NK-клетки) и запускающая
перфорин-гранзимовый механизм цитотоксичности, с уничтожением клетки-
мишени
Связывание комплекса АГ (аллерген) - АТ (IgE) с тучными клетками и базофилами, экспрессирующими на поверхности Fc-рецепторы, последующая дегрануляция этих клеток и высвобождение медиаторов воспаления (гистамин, лейкотриены, простагландины, цитокины)
Нейтрализация вирусов
Слайд 19Структура иммунной системы
Центральные органы (красный костный мозг, тимус).
В них происходят процессы антигеннезависимой дифференцировки (созревания) лимфоцитов (иммунопоэз).
В красном костном мозге из гемопоэтические стволовые клетки формируются все клетки иммунной системы кроме Т- лимфоцитов В тимусе из мигрирующих из красного мозга предшественников лимфоцитов проходят дальнейшие этапы их дифференцировки и образуются Т-лимфоциты
Периферические органы иммунной системы (лимфатические узлы, селезенка, миндалины, пейеровы бляшки, лимфоидная ткань, ассоциированная с кожей и слизистыми оболочками и т.д.).
В них происходит антигензависимая дифференцировка лимфоцитов - иммунный ответ (иммуногенез).
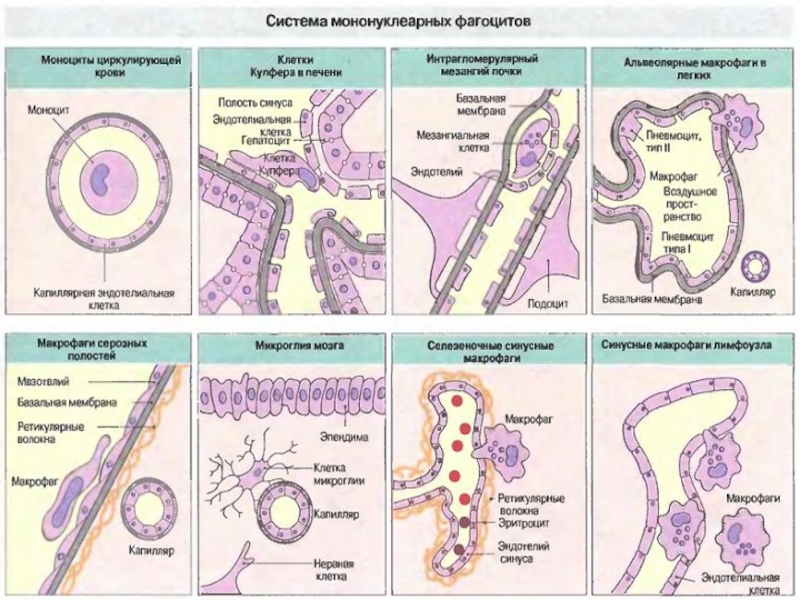
Отдельные рассеянные по организму клетки иммунной системы (макрофаги, дендритные клетки, лимфоциты)
Кровь и лимфа объединяют отдельные разобщенные компоненты иммунной системы в единое целое, обеспечивают рециркуляцию лимфоцитов и миграцию клеток из центральных органов в периферические по мере их созревания.
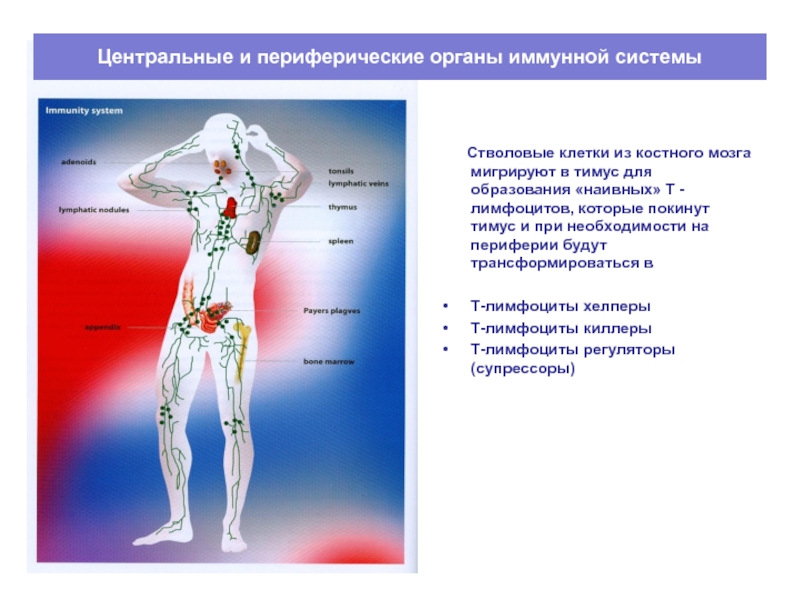
Слайд 20Центральные и периферические органы иммунной системы
Стволовые клетки
из костного мозга мигрируют в тимус для образования «наивных» Т
- лимфоцитов, которые покинут тимус и при необходимости на периферии будут трансформироваться вТ-лимфоциты хелперы
Т-лимфоциты киллеры
Т-лимфоциты регуляторы (супрессоры)
Слайд 21
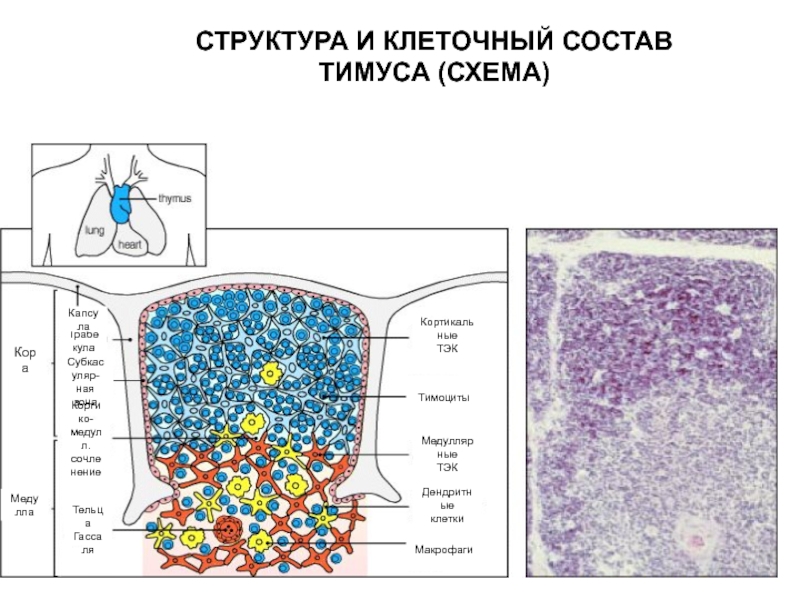
СТРУКТУРА И КЛЕТОЧНЫЙ СОСТАВ ТИМУСА (СХЕМА)
Кора
Медулла
Тельца
Гассаля
Кортико-
медулл.
сочленение
Субкасуляр-
ная зона
Трабекула
Капсула
Кортикальные
ТЭК
Медуллярные
ТЭК
Тимоциты
Дендритные
клетки
Макрофаги
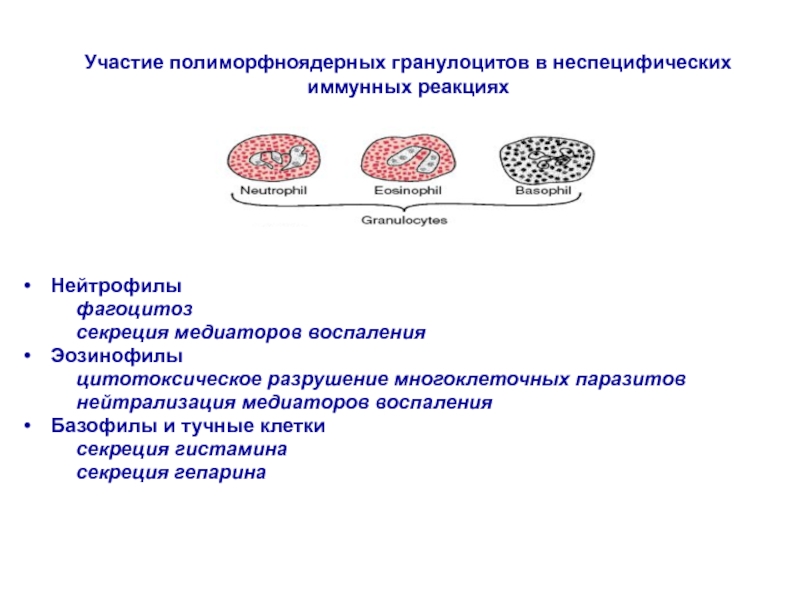
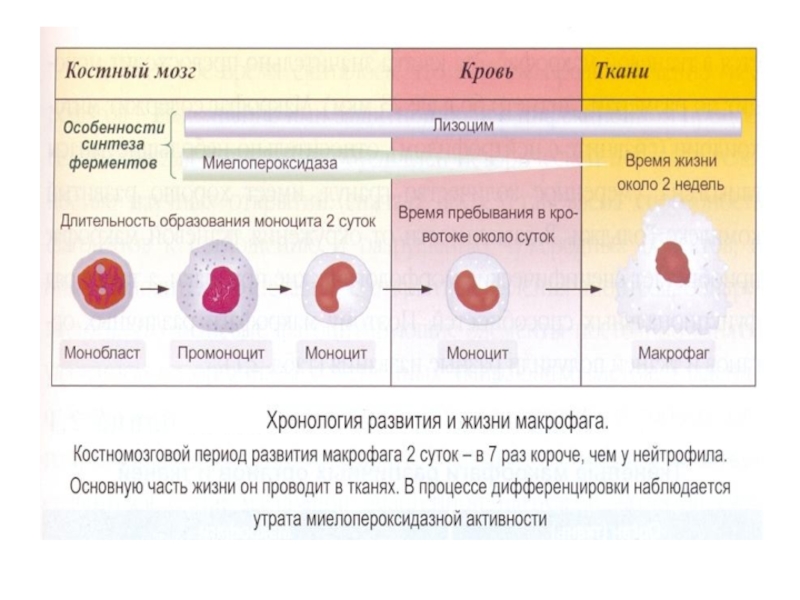
Слайд 24Нейтрофилы
фагоцитоз
секреция медиаторов воспаления
Эозинофилы
цитотоксическое разрушение
многоклеточных паразитовнейтрализация медиаторов воспаления
Базофилы и тучные клетки
секреция гистамина
секреция гепарина
Участие полиморфноядерных гранулоцитов в неспецифических иммунных реакциях
Слайд 27Свойства иммунной системы
Высокая специфичность (лимфоциты с помощью антигенспецифических рецепторов распознают
антигенные молекулы, различающиеся по 1-2 аминокислотным остаткам и удаляют их
из организма).Высокая чувствительность (лимфоциты распознают АГ на уровне отдельных молекул. Взаимодействие АГ-АТ- одна из наиболее высокочувствительных биологических реакций).
Иммунологическая индивидуальность (для каждого организма характерен свой генетически контролируемый тип иммунного ответа. Основной постулат иммуногенетики- конкретность иммунного ответа).
Клональный принцип организации лимфоцитов (способность всех клеток в пределах отдельного клона отвечать только на один АГ- (антигенную детерминанту). Согласно клонально-селекционной теории Ф. Бернета, в иммунной системе формируются клоны лимфоцитов, способные распознавать огромное количество вариантов атигенных молекул, составляющих так называемый антигенный репертуар.
Иммунная система наряду с нервной и эндокринной системой является важнейшей регуляторной системой организма. Иммунная система, подобно ЦНС, формирует морфо-функциональную доминанту, ядром которой являются АГ-специфические клоны Т-иВ-лимфоцитов. Важную роль во взаимодействии всех трех систем играет цитокиновая сеть, наличие рецепторов на лимфоцитах к гормонам, нейромедиаторам.
Слайд 28Основные понятия и термины, используемые при изучении физиологии иммунной системы
СD
(от англ. Cluster Differentiation) – единая система номенклатуры антигенных маркеров
(мембранных белков) клеток иммунной системыСD3- на всех Т-лимфоцитах
СD19-на всех В-лимфоцитах
Субпопуляции лимфоцитов
СD4 - Т-хелперы СD8-цитотоксические лимфоциты (ЦТЛ) В1-, В2- лимфоциты
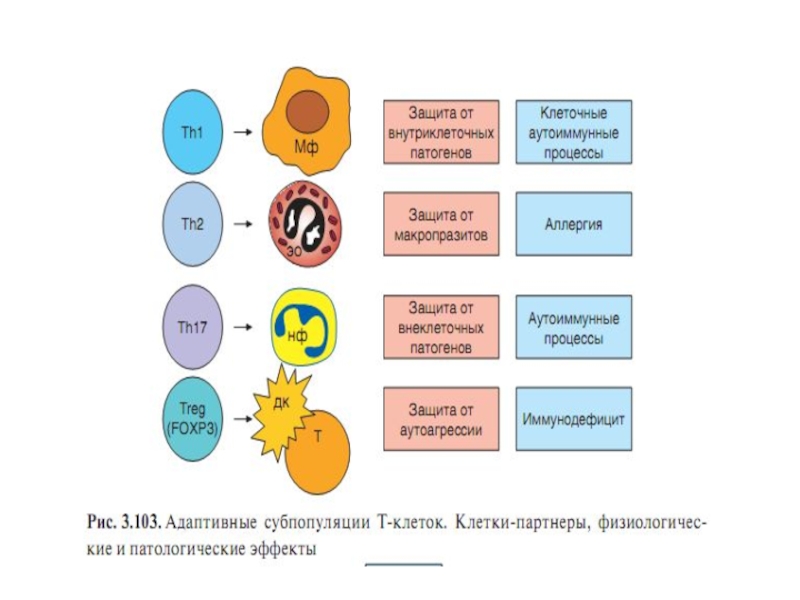
Разновидности Т-хелперов : Th1(СD4+), Th2(СD4+), Т-регуляторный лимфоцит с
супрессорной функцией (Т-reg) - СD4+CD25+Foxp3, Th17 (СD4+)
Функциональные различия Т-хелперов :
Th1 – регулируют клеточный иммунитет (цитотоксические реакции с участием
макрофагов, цитотоксических лимфоцитов, усиливают фагоцитоз), секретируя цитокины
(ИНФγ).
Th2 – регулируют гуморальный иммунитет (повышают активность В-лимфоцитов,
продукцию иммуноглобулинов плазматическими клетками), секретируя ИЛ-4, ИЛ-5.
Th17 – усиливают приток нейтрофилов в очаг воспаления, секретируя ИЛ-17.
Т-reg –супрессируют активность всех лимфоцитов, макрофагов, ограничивая
избыточность иммунных реакций, воспаления, секретируя ИЛ-10 и трансформирующий
фактор роста – ТФРβ.
Популяции лимфоцитов
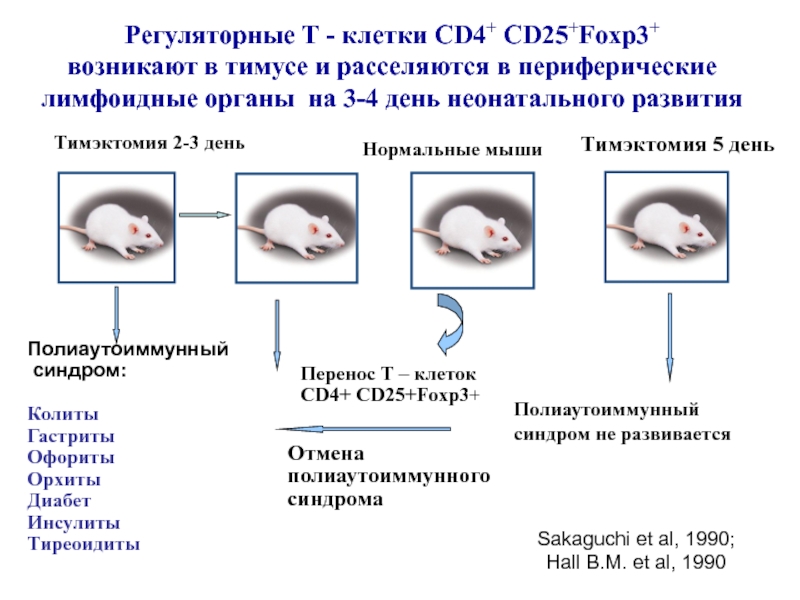
Слайд 29Регуляторные Т - клетки CD4+ CD25+Foxp3+ возникают в тимусе и расселяются
в периферические
лимфоидные органы на 3-4 день неонатального развития
Sakaguchi et al,
1990;Hall B.M. et al, 1990
Тимэктомия 2-3 день
Полиаутоиммунный
синдром:
Колиты
Гастриты
Офориты
Орхиты
Диабет
Инсулиты
Тиреоидиты
Нормальные мыши
Перенос Т – клеток
CD4+ CD25+Foxp3+
Отмена
полиаутоиммунного
синдрома
Тимэктомия 5 день
Полиаутоиммунный синдром не развивается
Слайд 30Интервалы распределения фенотипов лимфоцитов условно здоровых доноров (n = 362)
Тип
клеток % ПК
Абс.к-во кл/лЛимфоциты (CD45bright) 28 - 36 1,363-2,808 х 109
В-клетки (CD3-CD19+HLA-DR+) 7 - 17 0,111-0,376 х 109
В-1 клетки (CD19+CD5+) 0,5 - 2,1 0,022-0,115 х 109
В-2 клетки (CD19+CD5-) 6,5 - 14,9 0,081-0,323 х 109
В клетки памяти (CD19+CD5-CD27+) 1,8 - 6,8 0,012-0,040 х 109
NK (LGL) (CD3-CD16+CD56+) 8 - 17 0,123-0,369 х 109
NK цитолитические (от общих NK-клеток) 93,7 - 97,5 0,081-0,323 х 109
NK цитокин-продуцирующие (от общих NK-клеток) 2,5 - 6,2 0,003-0,022 х 109
Т-клетки (CD3+CD19-) 61 - 85 0,946-2,079 х 109
Т хелперы (CD3+CD4+) 35 - 55 0,576-1,336 х 109
Т цитотоксические (CD3+CD8+) 19 - 35 0,372-0,974 х 109
Т хелперы активированные/
памяти (CD4+CD45R0+) 5 - 25 0,068-0,702 х 109
Т хелперы наивные (CD4+CD45RА+) 20 - 40 0,272-1,123 х 109
-Т клетки (CD3+-ТсR+-ТcR-) 60,8 - 80,2 0,924-1,964 х 109
-Т клетки (CD3+-ТcR+-ТсR- ) 1,8 - 7,4 0,022-0,115 х 109
Т-NK клетки (CD16+CD56+CD3+) 0,5 - 6 0,007-0,165 х 109
Т клетки актив. (HLA-DR+CD25+) 0,5 - 6 0,007-0,165 х 109
Регуляторные Т-клетки (CD4+CD25brightCD127neg) 0,6 - 3,19 0,009-0,078 х 109
Индекс соотношения (Тх/Тц) 1,5 - 2,6
Слайд 31Основные понятия и термины, используемые при изучении физиологии иммунной системы
TCR
–T-клеточный рецептор (высокоспецифичный АГ-распознающий рецептор
Т – лимфоцитов)
ВCR –В - клеточный
рецептор (высокоспецифичный АГ-распознающий рецептор В – лимфоцитовСлайд 32Основные понятия и термины, используемые при изучении физиологии иммунной системы
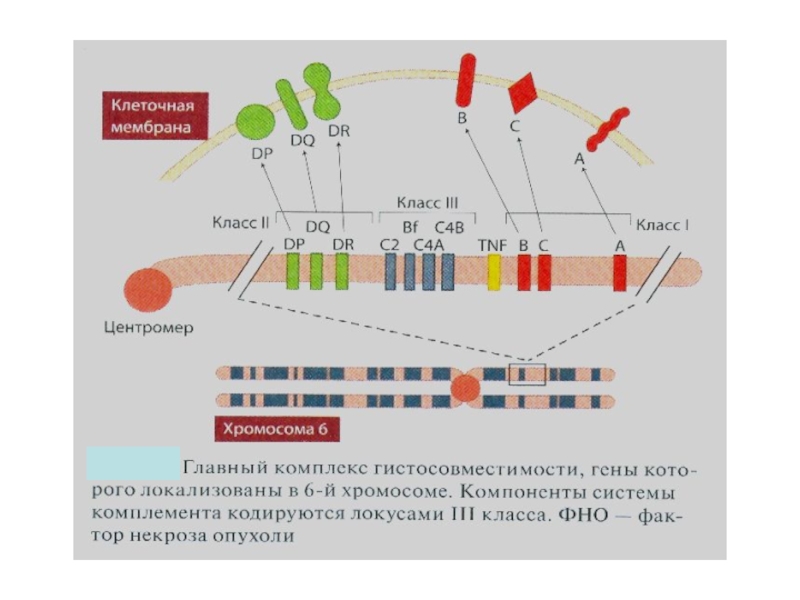
МНС
– главный комплекс гистосовместимости; у человека обозначается как HLA
Комплекс
тесно сцепленных генетических локусов и кодируемых имимолекул, ответственных за развитие и регулирование иммунного ответа и
тканевую совместимость
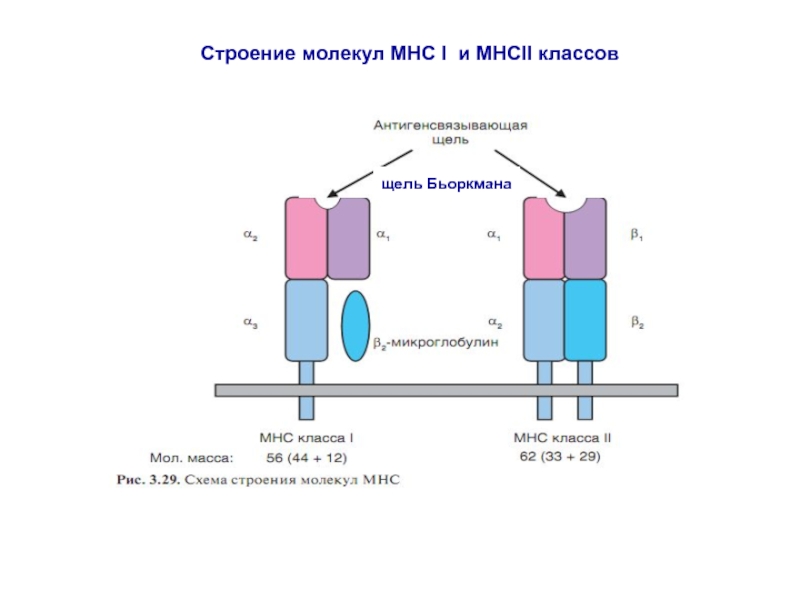
Свойства молекул МНС I класса
МНС I класса присутствуют на поверхности всех ядросодержащих клеток и синтезируются постоянно.
Определяют индивидуальный паспорт человека.
МНС I класса связывают пептид (антиген) и представляют его CD-8 цитотоксическим лимфоцитам (ЦТЛ, Т- киллеры).
Свойства молекул МНС II класса
MHC II класса располагаются на мембране профессиональных АПК: дендритных клетках (ДК), макрофагах, В-лимфоцитах, активированных Т –лимфоцитах, фибробластах, эндотелиальных клетках.
MHC II класса связывают пептид (антиген) и представляют его для распознавания Т-хелперам (CD- 4 лимфоциты).
Экспрессия МНС II класса усиливается при развитии иммунного ответа
Свойства молекул МНС III класса
Кодируют компоненты системы комплемента
Общие свойства молекул МНС
Определяют индивидуальность иммунного ответа (уровень экспрессии молекул МНС), гены иммунного ответа (Ir ) сцеплены с HLA
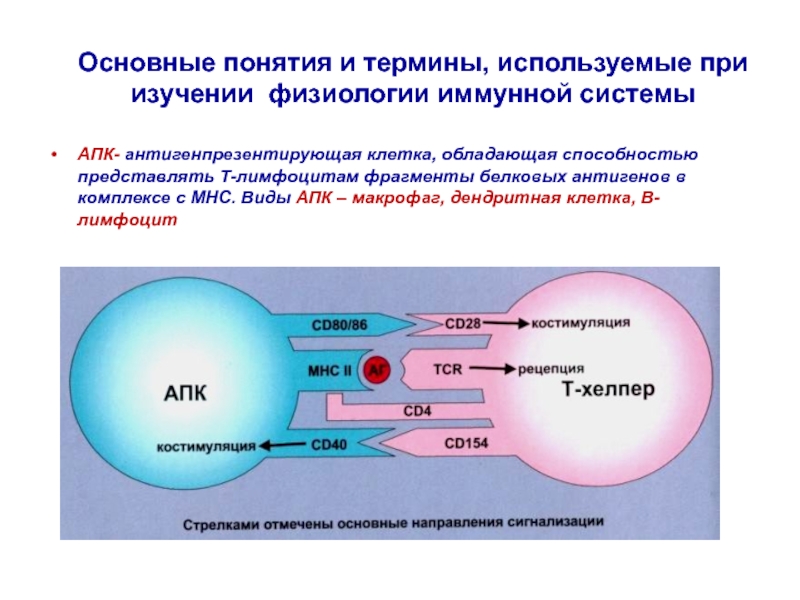
Слайд 33Основные понятия и термины, используемые при изучении физиологии иммунной системы
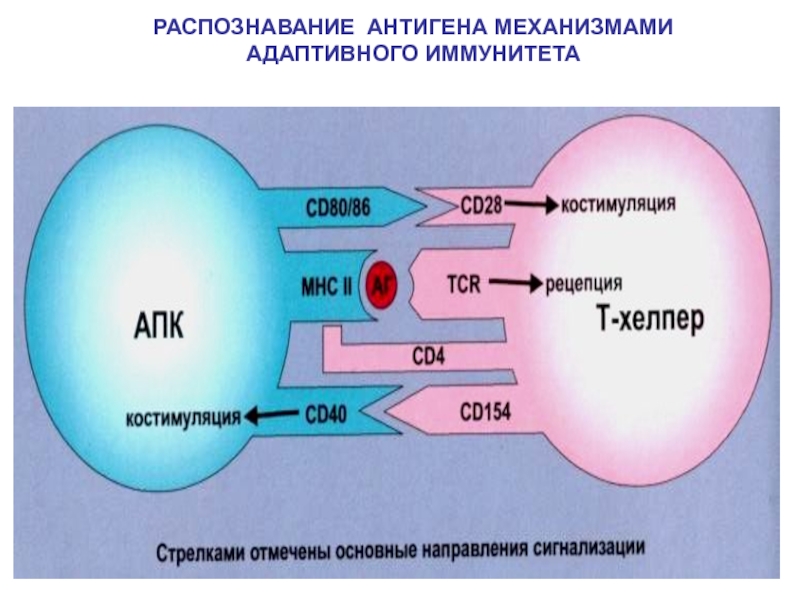
АПК-
антигенпрезентирующая клетка, обладающая способностью представлять Т-лимфоцитам фрагменты белковых антигенов в
комплексе с МНС. Виды АПК – макрофаг, дендритная клетка, В-лимфоцитСлайд 34Основные понятия и термины, используемые при изучении физиологии иммунной системы
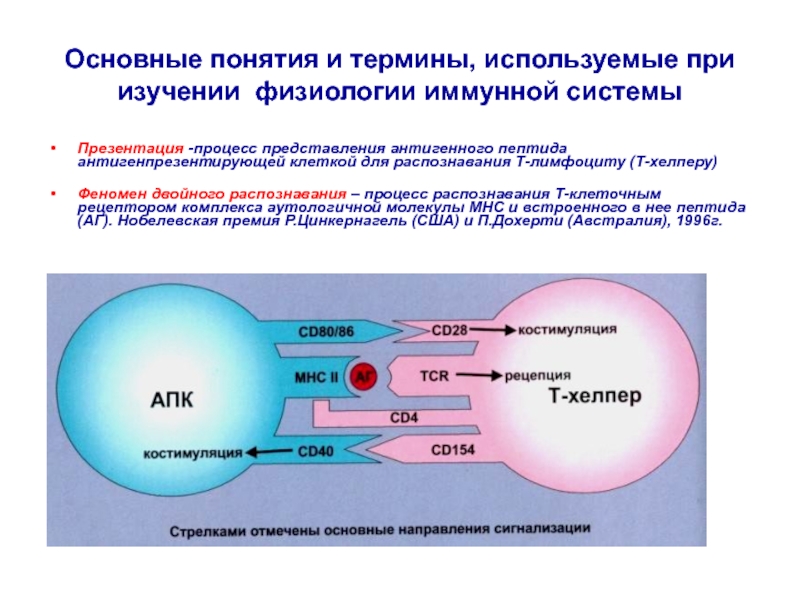
Презентация
-процесс представления антигенного пептида антигенпрезентирующей клеткой для распознавания Т-лимфоциту (Т-хелперу)
Феномен
двойного распознавания – процесс распознавания Т-клеточным рецептором комплекса аутологичной молекулы МНС и встроенного в нее пептида (АГ). Нобелевская премия Р.Цинкернагель (США) и П.Дохерти (Австралия), 1996г.Слайд 35Основные понятия и термины, используемые при изучении физиологии иммунной системы
Реаранжировка
генов – процесс перестройки генов Т- и В- клеточного рецептора
Клон
лимфоцитов- потомство одного лимфоцита, имеющее АГ-распознающий рецептор одинаковой антигенной специфичностиСелекция - процесс выбраковки созревающих лимфоцитов:отбираются лимфоциты, способные распознать чужеродные АГ и толерантные (терпимые) к антигенам клеток своего организма
Экспансия клона клеток - активация и пролиферация специфичных АГ Т- и В-лимфоцитов
.
.
.
.
.
.
.
.
.
.
.
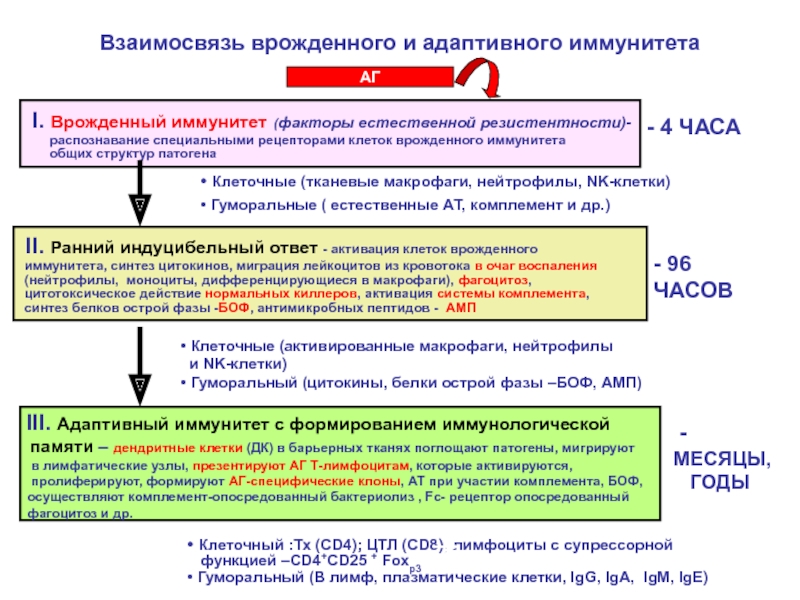
Слайд 36Взаимосвязь врожденного и адаптивного иммунитета
I. Врожденный иммунитет (факторы естественной
резистентности)-
распознавание специальными рецепторами клеток врожденного
иммунитетаобщих структур патогена
II. Ранний индуцибельный ответ - активация клеток врожденного
иммунитета, синтез цитокинов, миграция лейкоцитов из кровотока в очаг воспаления
(нейтрофилы, моноциты, дифференцирующиеся в макрофаги), фагоцитоз,
цитотоксическое действие нормальных киллеров, активация системы комплемента,
синтез белков острой фазы -БОФ, антимикробных пептидов - АМП
III. Адаптивный иммунитет с формированием иммунологической
памяти – дендритные клетки (ДК) в барьерных тканях поглощают патогены, мигрируют
в лимфатические узлы, презентируют АГ Т-лимфоцитам, которые активируются,
пролиферируют, формируют АГ-специфические клоны, АТ при участии комплемента, БОФ,
осуществляют комплемент-опосредованный бактериолиз , Fc- рецептор опосредованный
фагоцитоз и др.
- 4 ЧАСА
- 96 ЧАСОВ
- МЕСЯЦЫ,
ГОДЫ
• Клеточные (тканевые макрофаги, нейтрофилы, NK-клетки))
• Гуморальные ( естественные АТ, комплемент и др.)
• Клеточные (активированные макрофаги, нейтрофилы
и NK-клетки)
• Гуморальный (цитокины, белки острой фазы –БОФ, АМП)
• Клеточный :Тх (СD4); ЦТЛ (СD8); лимфоциты с супрессорной
функцией –CD4+CD25 + Foxp3
• Гуморальный (В лимф, плазматические клетки, IgG, IgА, IgМ, IgЕ)
АГ
Слайд 37Понятие врожденного иммунитета
Врожденный иммунитет ( от англ.innate
or natural immunity)- наследственно закрепленная система защиты многоклеточных организмов от
любых патогенных микробов и эндогенных продуктов тканевой деструкцииСлайд 38Отличительтные свойства врожденного иммунитета
Является главной системой (сенсором) распознавания «чужого» (например,
заражения патогенами) и первой линией защиты, развивающейся в течении нескольких
минут и часов после проникновения патогена.Все компоненты врожденного иммунитета (клеточные, гуморальные) передаются по наследству, кодируются относительно небольшим количеством генов зародышевой линии и не меняются в течении жизни.
Из-за ограниченности числа генов рецепторы (сенсоры) врожденного иммунитета( Toll-подобные рецепторы TLR и др.) распознают не индивидуальный патоген, а целые классы патогенов (все грамположительные, имеющие пептидогликан, все грамотрицательные, имеющие липополисахсрид - ЛПС идр.).
Клетки врожденного иммунитета не образуют клонов, клеток-памяти
Активация врожденного иммунитета служит обязательным условием развития адаптивного иммунного ответа
Защищает все виды живых существ, в то время как адаптивный иммунитет есть только у высших позвоночных
Слайд 39Механизмы распознавания «своего» и «чужого» на
начальных этапах врожденного иммунитета
Цель
распознавания – раннее установление различий между патогенами и непатогенами
Кто распознает
? – клетки миеломоноцитарного ряда (макрофаги, дендритные клетки-ДК, нейтрофилы, тучные клетки, эозинофилы, базофилы, а теакже естественные киллеры-NK-клетки) и др.Что распознается ? – консервативные, общие для многих видов патогенных микроорганизмов структуры (или образцы -«паттерны») - РАМР (ЛПС, пептидогликаны, белок флагеллин и т.д.).
Чем распознают ? – паттернраспознающими рецепторами (PRR) – молекулярные структуры распознавания различных типов микроорганизмов (Toll-подобные рецепторы (TLR), NOD-1, NOD-2, RIG и др.)
Слайд 40Эффекторы врожденного иммунитета (клетки, гуморальные факторы)
Фагоцитирующие клетки ( нейтрофилы, моноциты,
макрофаги )
Презентирующие антиген клетки (дендритные клетки, макрофаги)
Клетки, выделяющие медиаторы воспаления
(базофилы, тучные клетки, эозинофилы )Натуральные киллеры (NK-клетки ) осуществляют цитотоксические реакции
Гуморальные факторы или молекулы: естественные антитела, белки комплемента, белки острой фазы, цитокины, катионные противомикробные пептиды, лизоцим и др.
Слайд 41Эффекторные молекулы врожденного иммунитета
Пептиды:
Дефенсины беспозвоночных
β-дефенсины
α-дефенсины
-дефенсины
кателицидины (LL-37, протегрины, профенины)
Белки:
лизоцим
Фосфолипаза А2
Сериновые
протеиназы (эластаза, катепсин G)
Бактерицидный проницаемость-увеличивающий белок
Лактоферрин
Пероксидазы (миелопероксидаза, эозинофильная пероксидаза, лактопероксидаза)
Активные
формы кислорода и азотаO2-,, H2O2, OH., OCl-, NO.
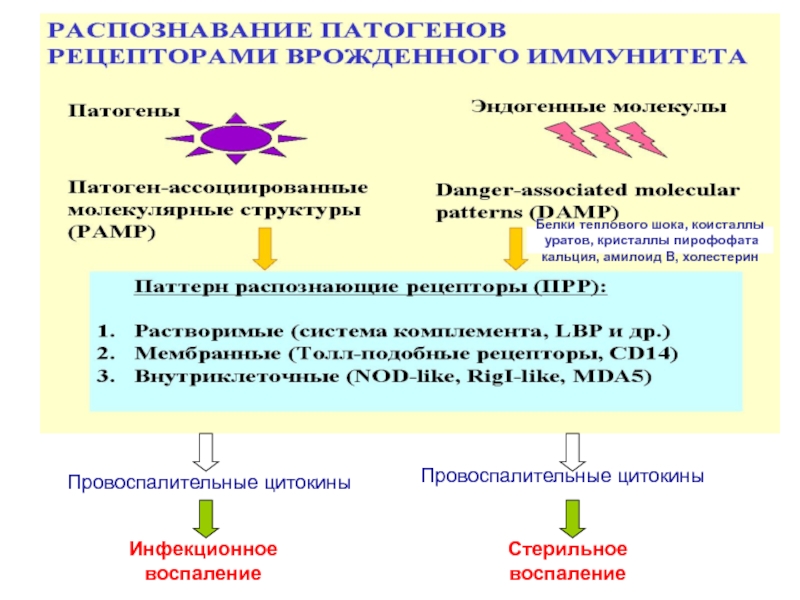
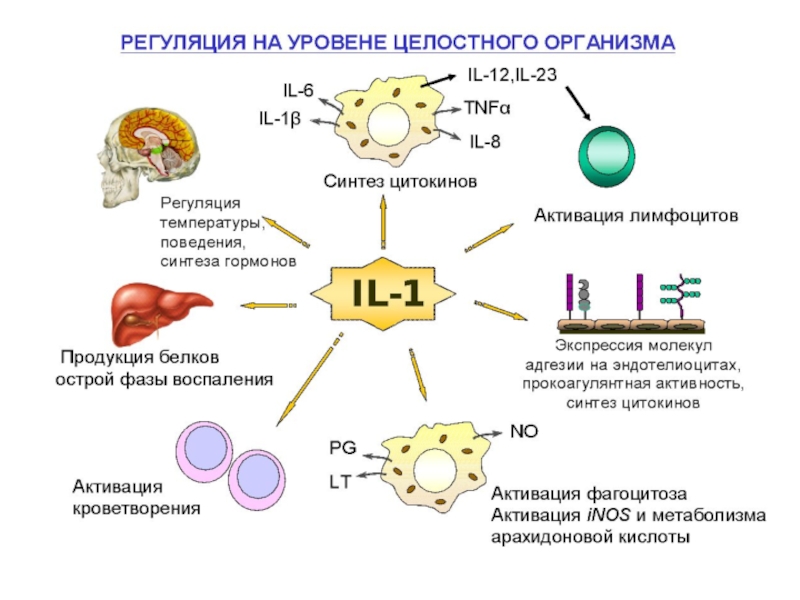
Слайд 48Провоспалительные цитокины
Провоспалительные цитокины
Инфекционное
воспаление
Стерильное
воспаление
Белки теплового шока, коисталлы
уратов, кристаллы пирофофата
кальция,
амилоид В, холестерин
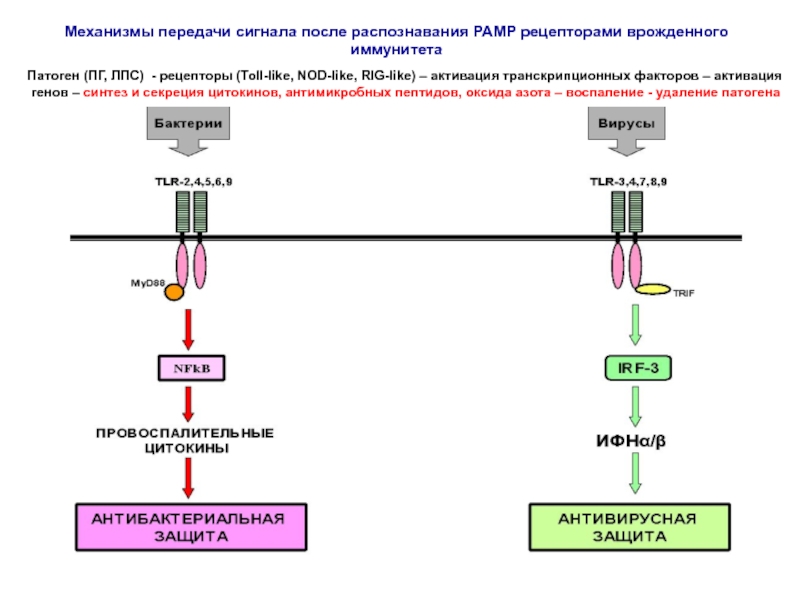
Слайд 49Патоген (ПГ, ЛПС) - рецепторы (Toll-like, NOD-like, RIG-like) – активация
транскрипционных факторов – активация
генов – синтез и секреция цитокинов,
антимикробных пептидов, оксида азота – воспаление - удаление патогенаМеханизмы передачи сигнала после распознавания PAMP рецепторами врожденного иммунитета
Слайд 50
Цитокины – эндогенные полипептидные
медиаторы межклеточного взаимодействия
Cистема цитокинов объединяет:
клетки-продуценты;
растворимые цитокины и их антагонисты;
клетки-мишени, экспрессирующие рецепторы цитокинов
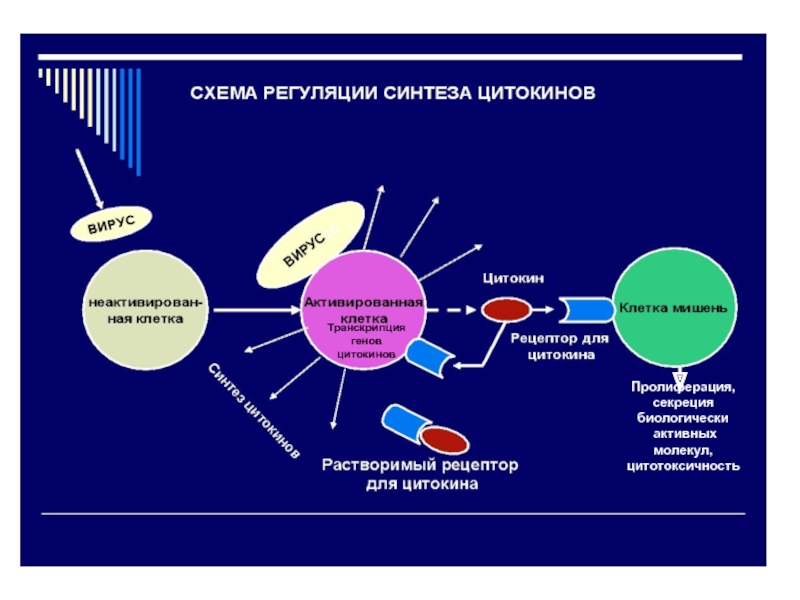
Слайд 51Транскрипция
генов цитокинов
Пролиферация,
секреция биологически
активных молекул,
цитотоксичность
Слайд 52Классификация цитокинов по биологическим эффектам
1. Факторы роста и дифференцировки
кроветворных клеток
2. Интерфероны
3. Интерлейкины (1-37)
4. Хемокины
5. Семейство фактора некроза
опухолей6. Ростовые факторы
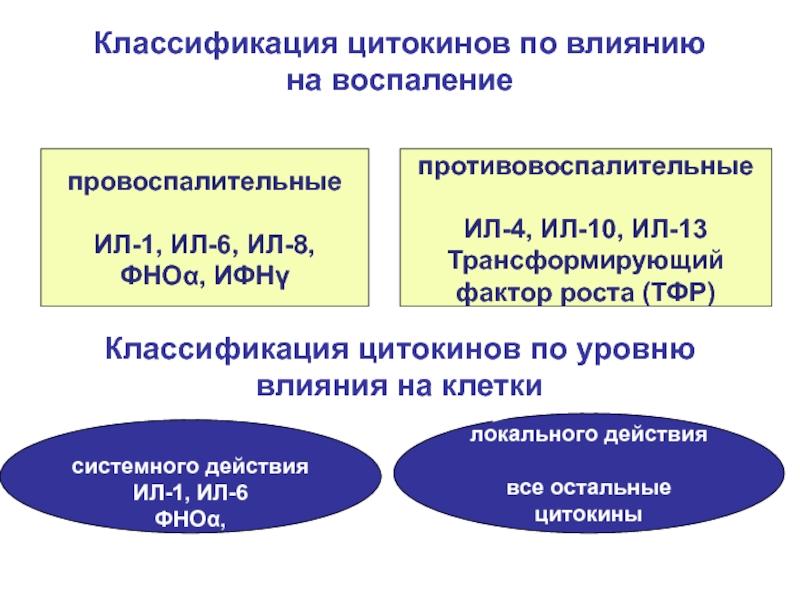
Слайд 53Классификация цитокинов по влиянию
на воспаление
провоспалительные
ИЛ-1, ИЛ-6, ИЛ-8,
ФНОα, ИФНγ
противовоспалительные
ИЛ-4,
ИЛ-10, ИЛ-13
Трансформирующий
фактор роста (ТФР)
локального действия
все остальные цитокины
Классификация цитокинов по
уровню влияния на клетки
системного действия
ИЛ-1, ИЛ-6
ФНОα,
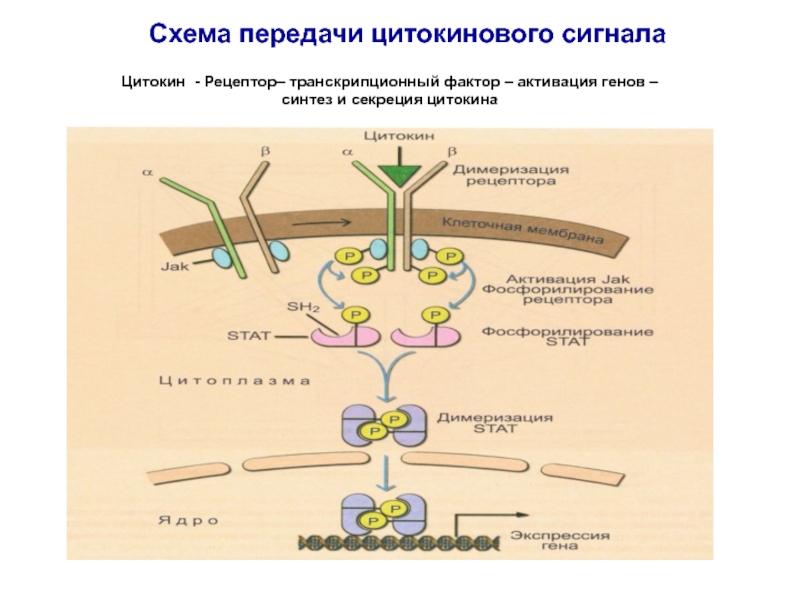
Слайд 56Схема передачи цитокинового сигнала
Цитокин - Рецептор– транскрипционный фактор – активация
генов –
синтез и секреция цитокина
Слайд 57СВОЙСТВА ЦИТОКИНОВ
Принадлежность к пептидам
Сетевой принцип работы
Индуцибельность
Синтез de novo
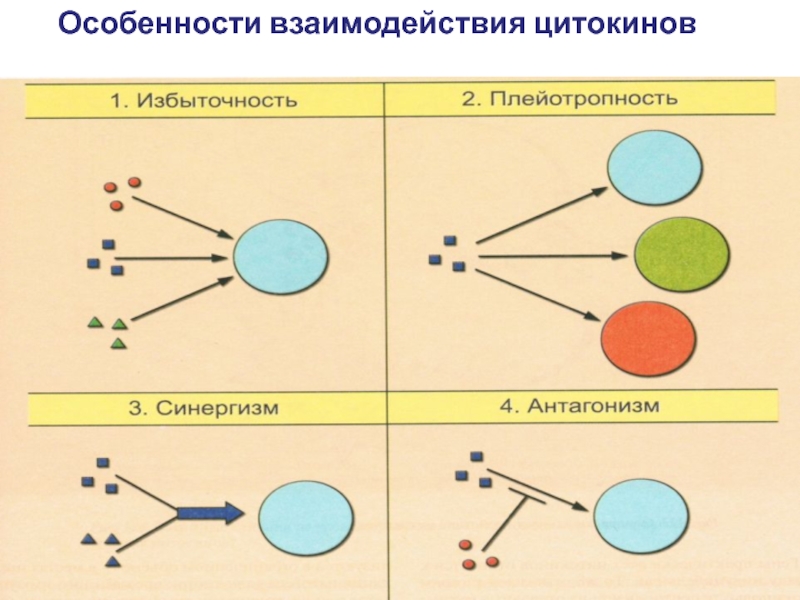
Избыточность
Плейотропность действия
Специфичность
Синергизм
Антагонизм
Каскадность
Слайд 60ЦИТОКИНОВЫЙ ШТОРМ
The term “cytokine storm” calls up vivid images of
an immune system gone awry and an inflammatory response flaring
out of controlТермин «цитокиновый шторм» вызывает яркий образ иммунной системы, которая пошла наперекосяк и воспалительная реакция сожгла контроль
J. R. Tisoncik et al., 2012
Слайд 62
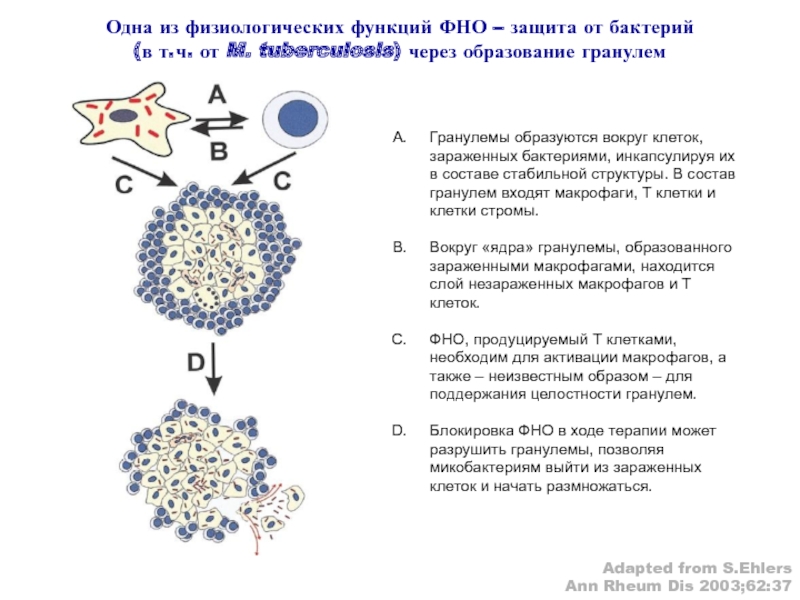
Гранулемы образуются вокруг клеток, зараженных бактериями, инкапсулируя их в составе
стабильной структуры. В состав гранулем входят макрофаги, Т клетки и
клетки стромы.Вокруг «ядра» гранулемы, образованного зараженными макрофагами, находится слой незараженных макрофагов и T клеток.
ФНО, продуцируемый Т клетками, необходим для активации макрофагов, а также – неизвестным образом – для поддержания целостности гранулем.
Блокировка ФНО в ходе терапии может разрушить гранулемы, позволяя микобактериям выйти из зараженных клеток и начать размножаться.
Adapted from S.Ehlers
Ann Rheum Dis 2003;62:37
Одна из физиологических функций ФНО – защита от бактерий
(в т.ч. от M. tuberculosis) через образование гранулем
Слайд 63Адаптивный иммунитет
Эволюционно более поздний.
Эффекторы адаптивного иммунитета:
Т- и В-лимфоциты с их антигенраспознающими рецепторами
(TCR и BCR)Антитела (иммуноглобулины – IgM,IgG,IgA,IgE)
TCR и BCR рецепторы образуются в результате рекомбинации генов зародышевой линии. Теоретически TCR и BCR готовы к распознаванию любого АГ, благодаря генетической рекомбинации, проходящей в формирующихся Т- и В-лимфоцитах.
Опасности процесса рекомбинации - образование аутореактивных клонов, способных реагировать на антигены собственного организма. Отбраковка (селекция) таких клонов идет в тимусе и красном костном мозге).
Слайд 64Механизмы распознавания «своего» и «чужого» адаптивным иммунитетом иммунитета
Кто распознает ?
– Т- и В-лимфоциты
Что распознается ? – В-лимфоцит распознает «чужое»
(эпитоп ), Т – лимфоцит – измененное «свое» ( антиген в составе молекул гистосовместимости )Чем распознают ? –Т- и В- клеточными рецепторами
Слайд 70Иммунный ответ
Иммунный ответ – специфическая реакция лимфоцитов на
антиген, направленная на его элиминацию
Фазы иммунного ответа
1.индуктивная
(реализуется в течение 5 -7 суток после попадания АГ) 2. эффекторная (длится около 2-х недель)
индуктивная
переработка и презентация АГ на АПК
распознавание АГ Т-лимфоцитом,
активация и пролиферация специфического клона лимфоцитов,
дифференцировка лимфоцитов, направленная на формирование эффекторных клеток и клеток памяти
эффекторная
реализуется клеточная и гуморальная защита для элиминации (удаления) АГ, вызвавшего реакцию, и формируется иммунологическая память (Т- В-клетки памяти)
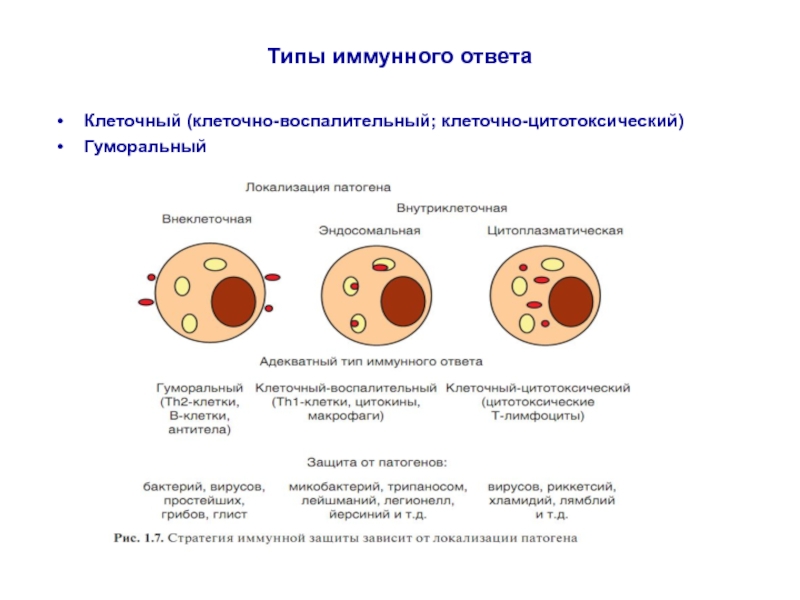
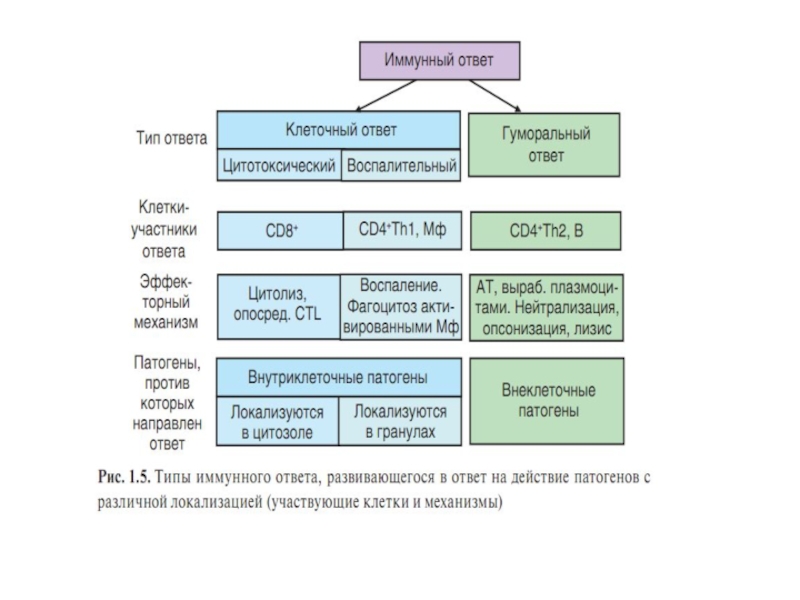
Слайд 71Типы иммунного ответа
Клеточный (клеточно-воспалительный; клеточно-цитотоксический)
Гуморальный
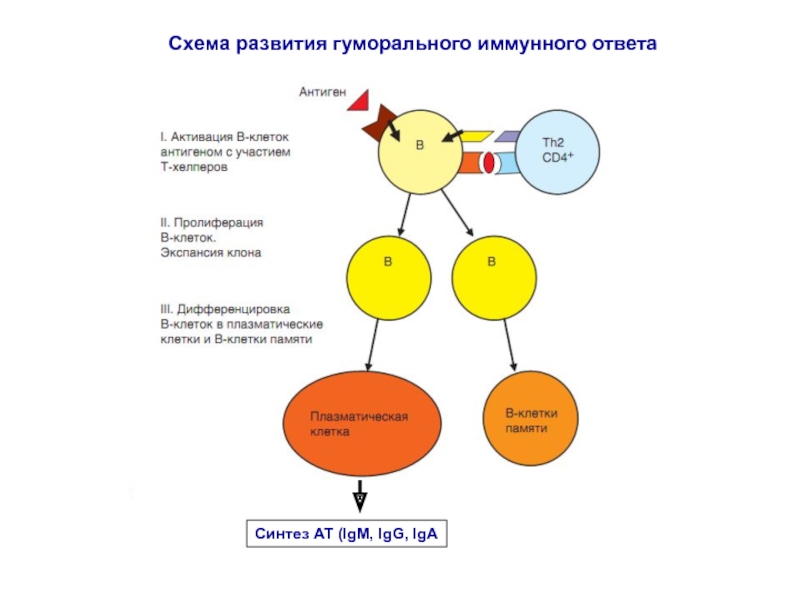
Слайд 73Первичный и вторичный гуморальный иммунный ответ
Первичный
ответ
Вторичный
ответ
Антиген
первичное введение
Концентрация антител
Ig M
Ig G
IgG
Ig
M
Сроки развития ответа
0
12
5
0
3
Антиген
вторичное введение
Слайд 78Основные характеристики Трег
Постоянные маркеры
СD25+ (альфа цепь рецептора ИЛ-2)
Foxp3 (ядерный фактор
транскрипции, связанный с Х-
хромосомой)Непостоянные маркеры:
маркёры активации CD69 (gp28/34); CD62L (L selectin)
поздние маркёры СD45RO (клетки памяти)
маркёры дифференцировки GITR
(глюкокортикортикоид- индуцированный рецептор ФНО)
Цитокины:
ИЛ-10, ИЛ-35
TGFβ (трансформирующий фактор роста β)
CTLA (ассоциированный с Т-лимфоцитами антиген-4)
CD4+
CD25+
Периферическая кровь
2-6%
Слайд 79В презентации доклада использованы материалы лекции :
С.А.Недоспасова (Институт
Молекулярной Биологии им. В.А. Энгельгардта РАН Институт Физико-химической биологии им.А.Н.
Белозерского МГУ )В.Н.Кокрякова ( ГУ НИИ Экспериментальной Медицины РАМН,Санкт-Петербург)
Слайд 81Типы иммунного ответа
Факторы, определяющие тип ИО
природа АГ
локализация АГ
по отношению к клетке
способ поступления АГ и его концентрация
направление дифференцировки
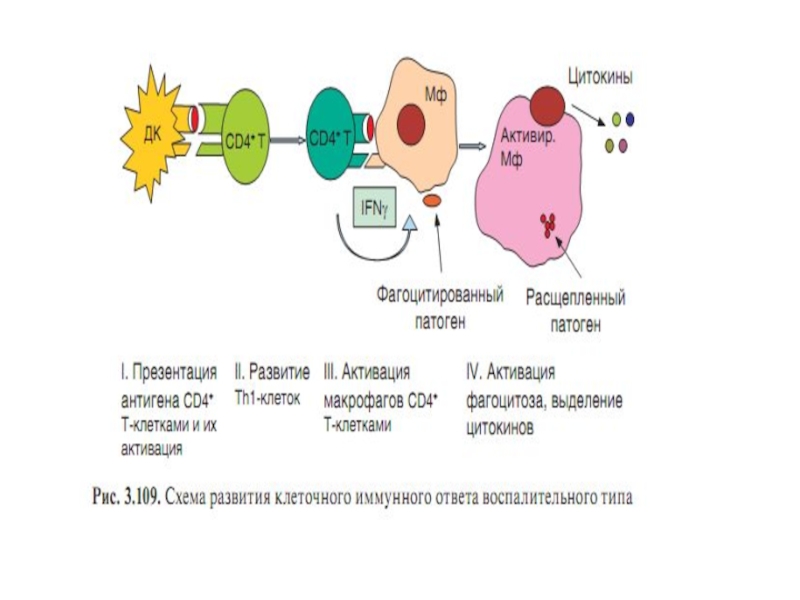
Т-хелперовклеточный иммунный ответ формируется преимущественно на
вирусные, опухолевые, трансплантационные антигены,
внутриклеточные патогены (вирусы, бактерии)
гуморальный иммунный ответ формируется на аллергены, антигены
микроорганизмов (внеклеточные бактерии, их токсины, вирусы), простейшие
гельминты
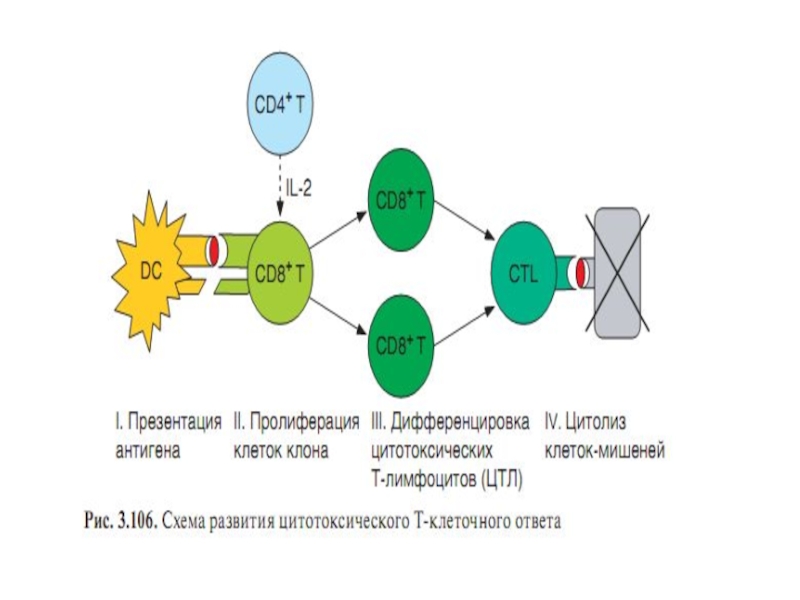
АГ располагается внутриклеточно в цитозоле – (вирусы, риккетсии, хламидии, лямблии) включается клеточно-опосредованный цитотоксический ответ (эффекторы- цитотоксические Т-лимфоциты). Удаление патогена происходит путем уничтожения инфицированной клетки.
АГ располагается внутриклеточно в гранулах, эндосомах- (микобактерии, легионеллы, лейшмании, ийерсинии) формируется Тх1-индуцированное воспаление с участием макрофагов. Бактерицидными факторами макрофагов (активные формы кислорода, азота, лизосомальные ферменты, провоспалительные цитокины) уничтожается патоген, возможна и деструкция тканей.
Внеклеточные патогены и их токсины активируют гуморальный ИО (АГ распознается В-лимфоцитом, презентируется Тх2-клеткам, происходит экспансия В-лимфоцитов, дифференцировка в плазматические клетки и В-клетки памяти, секретируются антитела, АГ удаляется эффекторными функциями АТ-нейтрализация, опсонизация, стимулирующая фагоцитоз, комллементзависимый лизис.
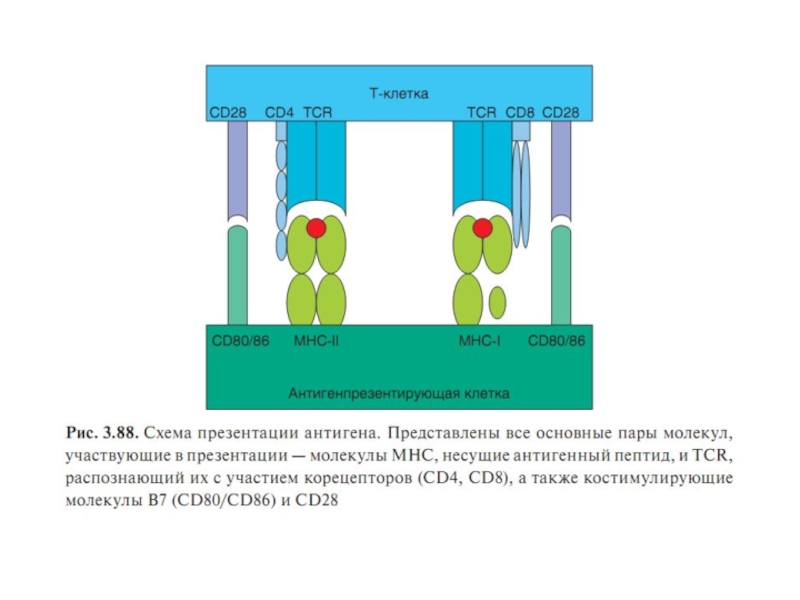
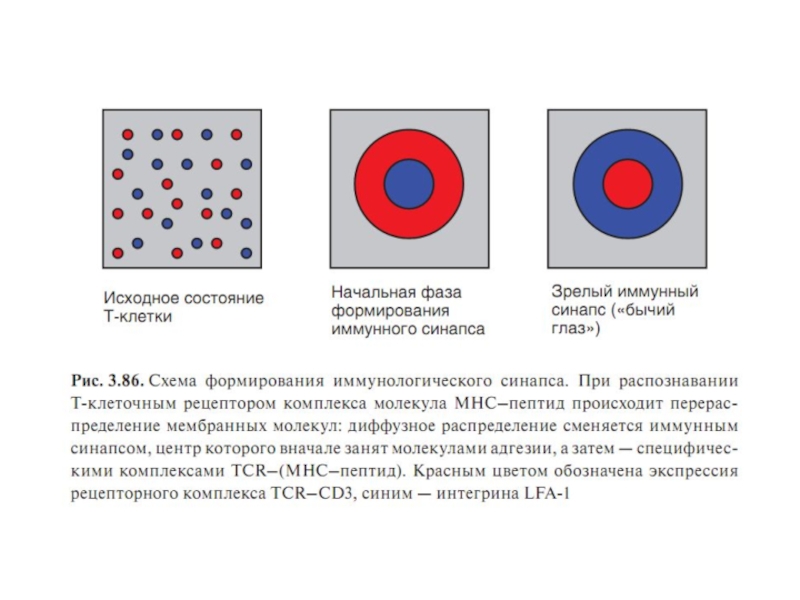
Слайд 83Иммунный синапс - структурированная (упорядоченная ) зона контакта между клетками,
участвующими в реализации той или иной формы иммунологического распознавания и
связанной с ним передаче сигнала.Иммунный синапс формируется с участием зрелой дендритной клетки , CD4+ Т-лимфоцита и костимулирующих молекул
Слайд 84Характеристика регуляторных Т-клеток
В 1995 г. С. Сакагучи (S. Sakaguchi)
и соавт. описали естественные регуляторные
Т- клетки (Тreg).Супрессорная активность CD4+ регуляторных T-клеток связана с транскрипционным фактором FОХР3 (скурфин).
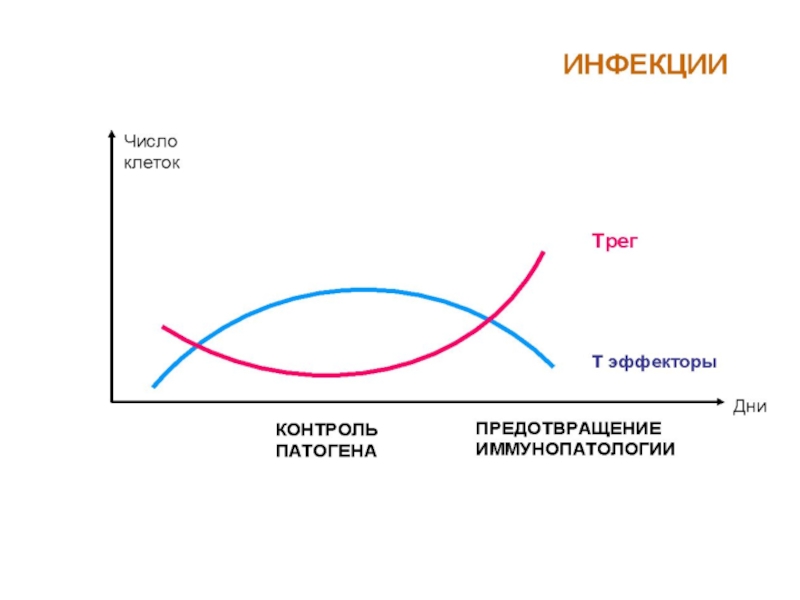
Главная задача Тreg— предотвращение развития аутоиммунных процессов
Супрессия иммунного ответа осуществляется секрецией Тreg супрессорных цитокинов: IL-10, трансформирующего фактора роста β (ТФР- β)
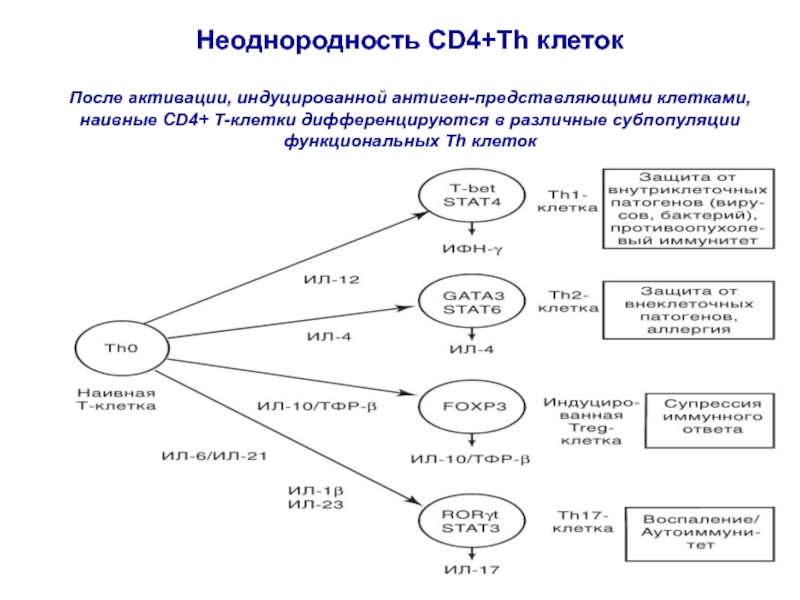
Слайд 85Неоднородность CD4+Th клеток
После активации, индуцированной антиген-представляющими клетками, наивные CD4+ Т-клетки
дифференцируются в различные субпопуляции функциональных Th клеток
Слайд 87ЭТАПЫ ПРЕДСТАВЛЕНИЯ АГ Т-КЛЕТКАМ
Ферментативная переработка экзогенных и эндогенных АГ до
коротких пептидов
Синтез молекул HLA в эндоплазматическом ретикулуме
Образование (сборка ) комплекса
“антигенный пептид-молекула HLA” ( процессинг антигена ); эндогенные пептидыобразуют комплекс с молекулой HLA-I, экзогенные- HLA-II
Транспорт образовавшегося комплекса на клеточную
мембрану
Презентация антигенного пептида Т-лимфоцитам
Слайд 88Ц И Т О К И Н Ы (от греч.CYTO
– КЛЕТКА,KINOS-ДВИЖЕНИЕ)-
низкомолекулярные белковые вещества, продуцируемые активированными клетками иммунной системы (реже
другими клетками ), осуществляющие регуляцию межклеточных взаимодействий и иммунорегуляциюЦитокины как биорегуляторные (иммунорегуляторные) молекулы, контролируют разнообразные этапы жизненного цикла клеток, включая процессы пролиферации, дифференцировки, функциональной активации и апоптоза.
Цитокины обеспечивают взаимосвязь врожденного и адаптивного иммунитета (известно около 200 цитокинов).
Синтез цитокинов начинается с транскрипции генов. Вырабатываются как правило на активирующий стимул, но могут синтезироваться и констутитивно.
Клетки вырабатывают цитокины в низких концентрациях (пикограммы).
Цитокины действуют кратковременно и короткодистантно на клетки мишени.
Цитокины формируют цитокиновую сеть. В сети цитокины могут действовать синергидно (согласованно) (ФНО-ḁ, ИЛ-6 и ИЛ-1), каскадно (одни цитокины индуцируют синтез других, антагонистично)
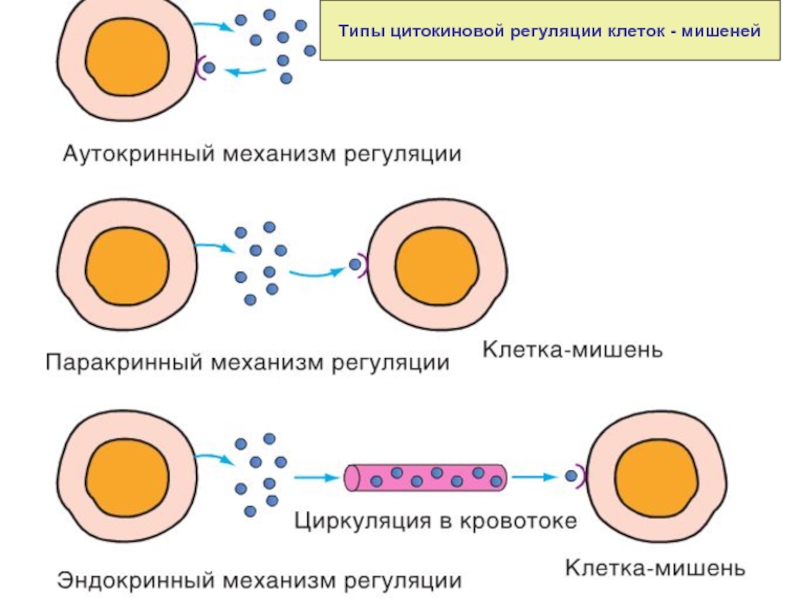
Цитокины действуют на клетки аутокринно, паракринно, эндокринно.
Выделяют:
Интерлейкины (провоспалительные цитокины, ростовые факторы лимфоцитов, регуляторные
цитокины - противовоспалительные),
Факторы некроза опухоли – цитокины с цитотоксическим и регуляторным действием: ФНО-ḁ и лимфотоксины (ЛТ),
Интерфероны
Факторы роста гемопоэтических клеток
Хемокины
Слайд 89Основные понятия и термины, используемые при изучении физиологии иммунной системы
СD
(от англ. Cluster Differentiation) – единая система номенклатуры антигенных маркеров
(мембранных белков) клеток иммунной системыTCR –T-клеточный рецептор (высокоспецифичный АГ-распознающий рецептор Т – лимфоцитов)
ВCR –В - клеточный рецептор (высокоспецифичный АГ-распознающий рецептор В – лимфоцитов)
МНС – главный комплекс гистосовместимости; у человека обозначается как HLA
АПК- антигенпрезентирующая клетка, обладающая способностью представлять Т-лимфоцитам фрагменты белковых антигенов в комплексе с МНС
Презентация -процесс представления антигенного пептида антигенпрезентирующей клеткой для распознавания Т-лимфоциту (Т-хелперу)
Феномен двойного распознавания – процесс распознавания Т-клеточным рецептором комплекса аутологичной молекулы МНС и встроенного в нее пептида (АГ)
Реаранжировка генов – процесс перестройки генов Т- и В- клеточного рецептора
Клон лимфоцитов- потомство одного лимфоцита, имеющее АГ-распознающий рецептор одинаковой антигенной специфичности
Селекция - процесс выбраковки созревающих лимфоцитов:отбираются лимфоциты, способные распознать чужеродные АГ и толерантные (терпимые) к антигенам клеток своего организма
Экспансия клона клеток - активация и пролиферация специфичных АГ Т- и В-лимфоцитов
Слайд 90Лекарственные препараты на основе генно-инженерных гуманизированных моноклональных антител
МАТ против IgE
человека – лечение тяжелых форм бронхиальной астмы и ряда других
проявлений аллергии.МАТ против ФНО, ИЛ-6, ИЛ-17 человека – лечение аутоиммунных заболеваний, псориаза и др.
МАТ против вирусных и бактериальных патогенов
4. Иммуносорбенты на основе гуманизированных генно-инженерных моноклональных антител