Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Органическая химия
Содержание
- 1. Органическая химия
- 2. Органическая химияТема. Карбоновые кислоты. Гомологический ряд предельных одноосновных карбоновых кислот. Получение.
- 3. Карбоновые кислотыКарбоновые кислоты часто называют просто органическими
- 4. Карбоновые кислоты -класс органических соединений, молекулы которых
- 5. Номенклатура карбоновых кислотНазвание кислот образуется так, что к названию предельного углеводорода прибавляется -овая кислота.
- 6. Номенклатура карбоновых кислот
- 7. Тривиальные названия важнейших кислотАлифатические предельные одноосновные кислотыНСООН муравьинаяСН3СООН уксуснаяС2Н5СООН пропионоваяС3Н7СООН маслянаяС5Н11СООН валериановаяС6Н13СООН капроноваяС15Н31СООН пальмитиноваяС17Н35СООН стеариновая
- 8. Тривиальные названия важнейших кислот2. Непредельные кислотыСН2=СН-СООН акриловаяСН3-(СН2)7-СН=СН-(СН2)7-СООН
- 9. Муравьиная кислота
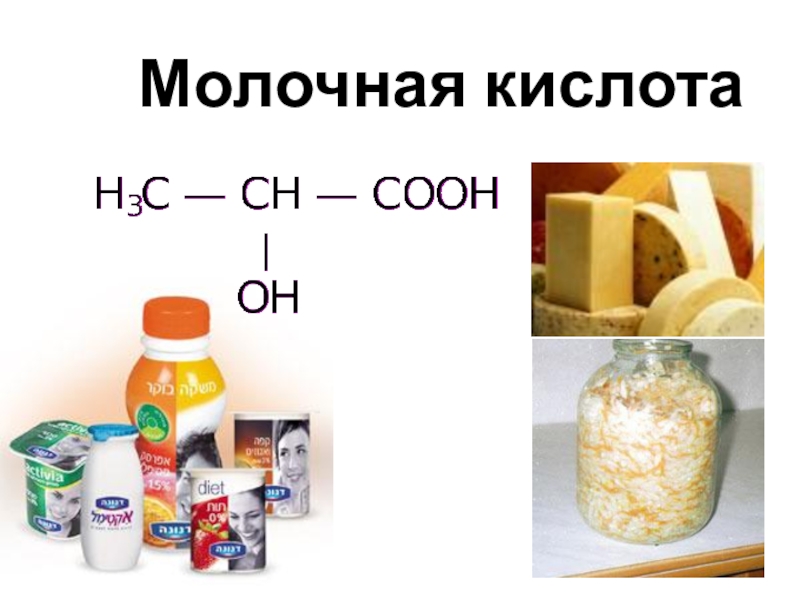
- 10. Молочная кислота
- 11. Масляная кислота – для получения ароматизирующих
- 12. Щавелевая кислота – HООCCООHдля производства пищевых добавок,в
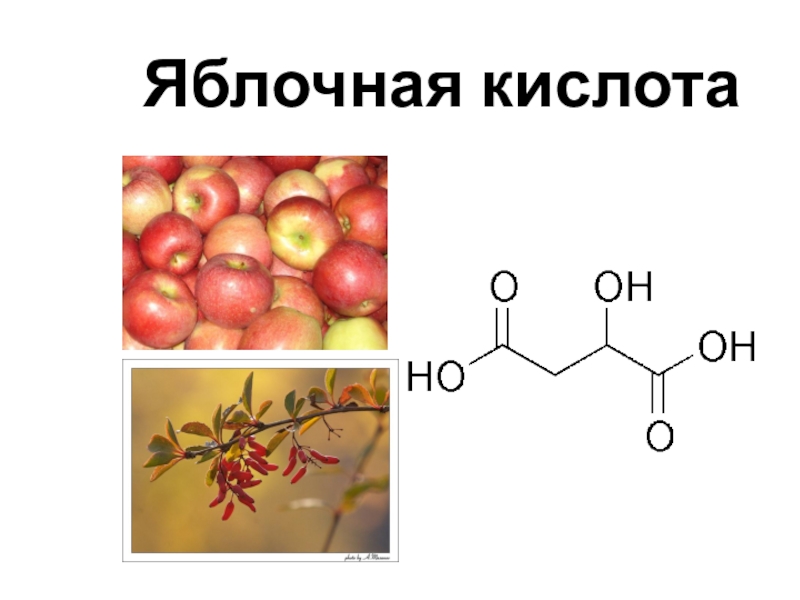
- 13. Яблочная кислота
- 14. Лимонная кислотаЕ330 до Е333 – это лимонная
- 15. САЛИЦИЛОВАЯ КИСЛОТААнтисептическое средство Ацетилсалициловая кислота таблетки ацетилсалициловой кислоты (аспирина)применяют для консервирования Ацетилсалициловая кислота
- 16. Стеариновая C17H35COOH и пальмитиновая кислота C15H31COOH –
- 17. Номенклатура В систематической номенклатуре кислот действуют следующие правила:1.
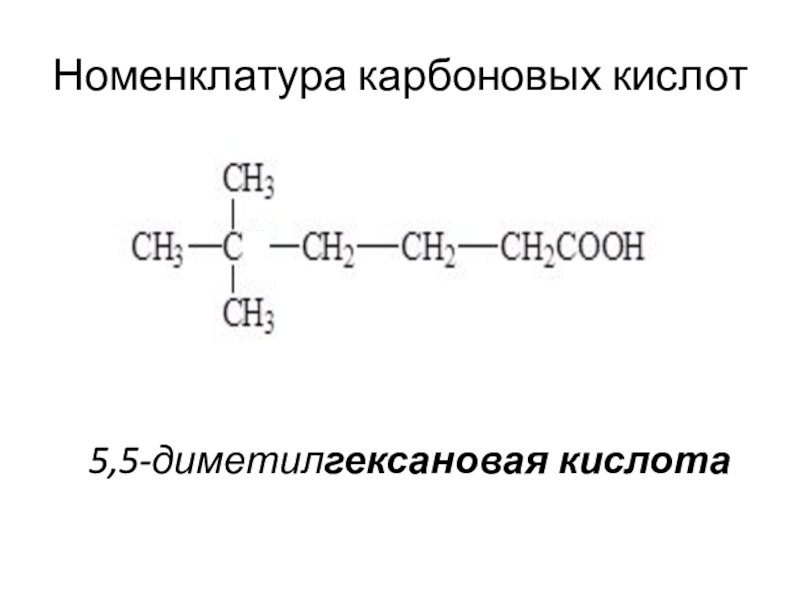
- 18. Номенклатура карбоновых кислот5,5-диметилгексановая кислота
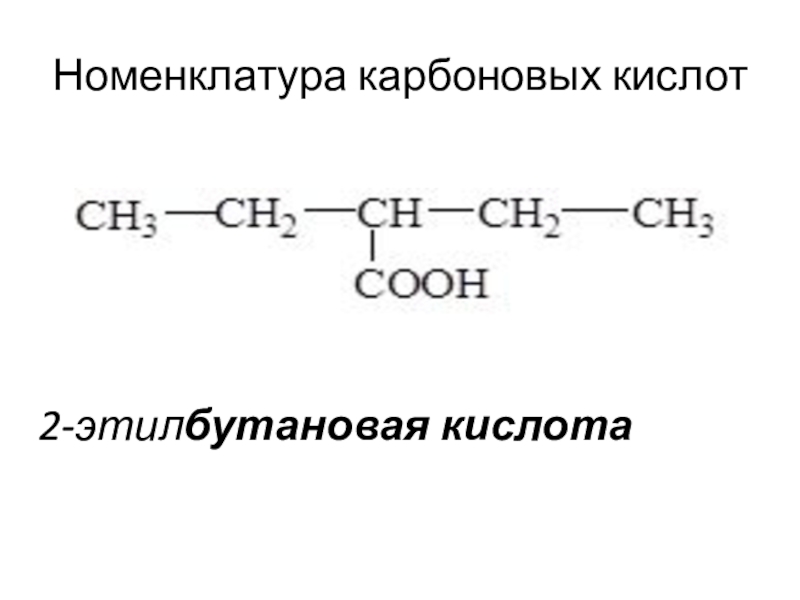
- 19. Номенклатура карбоновых кислот2-этилбутановая кислота
- 20. 4
- 21. Практическое задание (письменно в тетрадь!)Напишите структурные формулы карбоновых кислот:2,3,4-триметилпентановая кислота4,4,5 –триэтилнонановая кислота2-метил-3,3-дихлоргептановая кислотаВалериановая кислотаПальмитиновая кислота
- 22. Общие способы получения кислот1. Окисление непредельных углеводородов
- 23. Общие способы получения кислот2. Окисление спиртов подкисленным
- 24. Общие способы получения кислот3. При окислении аренов
- 25. Скачать презентанцию
Органическая химияТема. Карбоновые кислоты. Гомологический ряд предельных одноосновных карбоновых кислот. Получение.
Слайды и текст этой презентации
Слайд 2Органическая химия
Тема. Карбоновые кислоты. Гомологический ряд предельных одноосновных карбоновых кислот.
Получение.
Слайд 3Карбоновые кислоты
Карбоновые кислоты часто называют просто органическими кислотами за их
кислотные свойства.
Свойства карбоновых кислот обусловлены наличием в них карбоксильной группы
или карбоксила -СООНКарбоксильная группа образована сочетанием двух групп:
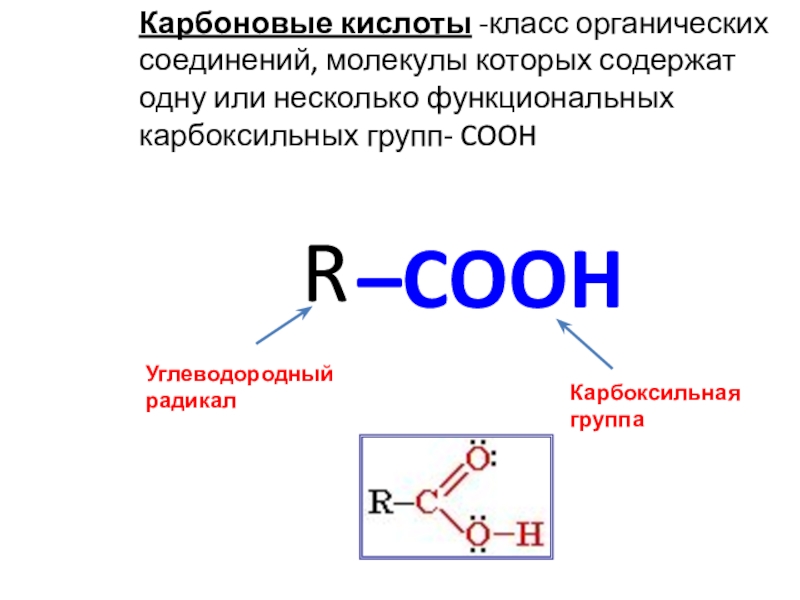
Слайд 4Карбоновые кислоты -класс органических соединений, молекулы которых содержат одну или
несколько функциональных карбоксильных групп- COOH
–COOH
Карбоксильная группа
R
Углеводородный радикал
Слайд 5Номенклатура карбоновых кислот
Название кислот образуется так, что к названию предельного
углеводорода прибавляется -овая кислота.
Слайд 7Тривиальные названия важнейших кислот
Алифатические предельные одноосновные кислоты
НСООН муравьиная
СН3СООН уксусная
С2Н5СООН пропионовая
С3Н7СООН
масляная
С5Н11СООН валериановая
С6Н13СООН капроновая
С15Н31СООН пальмитиновая
С17Н35СООН стеариновая
Слайд 8Тривиальные названия важнейших кислот
2. Непредельные кислоты
СН2=СН-СООН акриловая
СН3-(СН2)7-СН=СН-(СН2)7-СООН
олеиновая
3. Ароматические кислоты
С6Н5COOH бензойная
4. Двухосновные кислоты
НООС-СООН щавелевая
НООС-СН2-СООН малоновая
Слайд 11Масляная кислота –
для получения
ароматизирующих добавок, пластификато-
ров и флотореагентов.
бесцветная жидкость
с запахом прогорклого масла. Соли и эфиры масляной кислоты называются
бутиратамиСлайд 12 Щавелевая кислота – HООCCООH
для производства пищевых добавок,
в косметологии — как отбеливающий
компонент в кремах.
для уменьшения жесткости воды и для ее очистки от примесей,
(в составе самых разных порошков для чистки труб, моющих средств, а также «Антинакипина»).как инсектицид, особенно она востребована у пчеловодов,
для дубления кож, а также при окраске натуральных шелковых и шерстяных тканей,
Слайд 14Лимонная кислота
Е330 до Е333 – это лимонная кислота и ее
соли, которые на химическом языке называются цитратами.
консервант и антиоксидант, регулятор
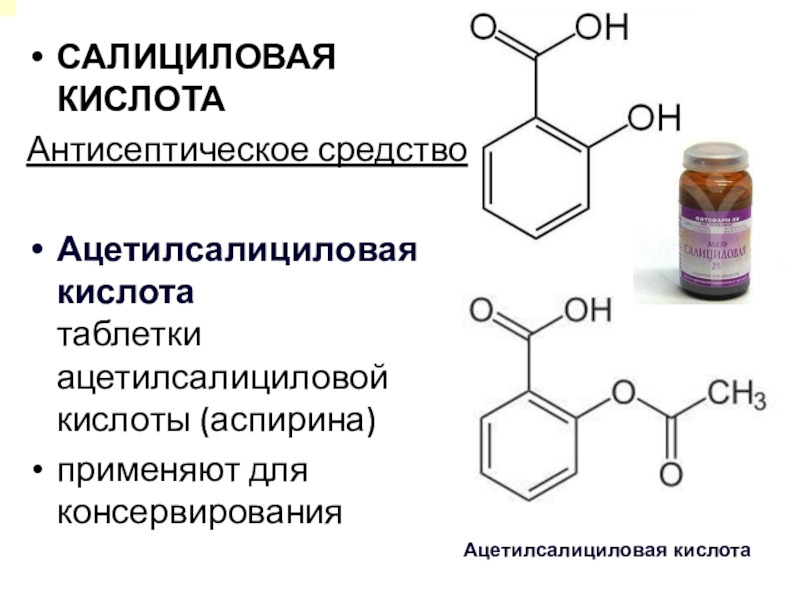
кислотности Слайд 15САЛИЦИЛОВАЯ КИСЛОТА
Антисептическое средство
Ацетилсалициловая кислота
таблетки ацетилсалициловой кислоты (аспирина)
применяют для консервирования
Ацетилсалициловая
кислота
Слайд 16
Стеариновая C17H35COOH и
пальмитиновая кислота C15H31COOH – в
качестве поверхностно-активных
веществ,
смазочных материалов в металлообработке.
Олеиновая кислота C17H33COOH –
флотореагент и
собиратель при обогащении руд цветных металлов.
Слайд 17Номенклатура
В систематической номенклатуре кислот действуют
следующие правила:
1. Главная цепь должна
начинаться и нумероваться с
карбоксильной группы.
2. В префиксе указываются положение
и названия заместителей.
3. После корня указывающего число атомов в цепи
идет суффикс, показывающий наличие или отсутствие
двойных, тройных связей, их положение.
4. После этого добавляется «– овая кислота». Если
карбоксильных групп несколько, то перед – овая
ставится числительное (ди –, три –… ).
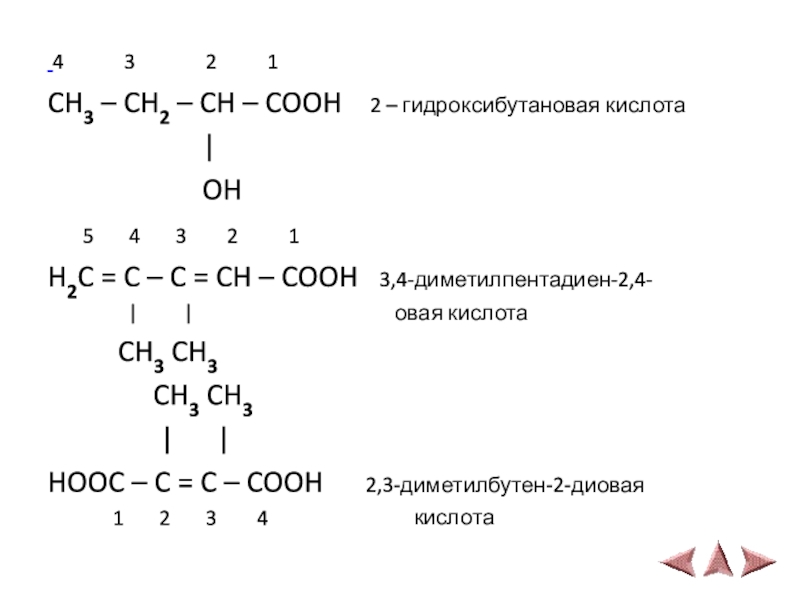
Слайд 20 4 3
2 1
CH3 – CH2 – CH – COOH 2 – гидроксибутановая кислота
|
OH
5 4 3 2 1
H2C = C – C = CH – COOH 3,4-диметилпентадиен-2,4-
| | овая кислота
CH3 CH3
CH3 CH3
| |
HOOC – C = C – COOH 2,3-диметилбутен-2-диовая
1 2 3 4 кислота
Слайд 21Практическое задание
(письменно в тетрадь!)
Напишите структурные формулы карбоновых кислот:
2,3,4-триметилпентановая кислота
4,4,5
–триэтилнонановая кислота
2-метил-3,3-дихлоргептановая кислота
Валериановая кислота
Пальмитиновая кислота
Слайд 22Общие способы получения кислот
1. Окисление непредельных углеводородов подкисленным раствором перманганата
калия или дихромата калия:
5СHR=CHR + 8KMnO4 + 12H2SO4 = 10RCOOH
+ 8MnSO4 + 4K2SO4 + 12H2O.Слева – раствор перманганата калия, справа – результат его взаимодействия с алкеном.
Слайд 23Общие способы получения кислот
2. Окисление спиртов подкисленным раствором перманганата или
дихромата калия:
3С2Н5ОН + 2K2Cr2O7 + 8H2SO4 = 3СН3СООН + 2Cr2(SO4)3
+ 2K2SO4 + 11H2O.Слева – раствор дихромата калия, справа – результат его взаимодействия с этиловым спиртом.



































![Автоматизация звука
[ Р ] в слогах, словах, фразе,
предложениях, тексте у детей](/img/tmb/6/577954/93493577f437aaf90501124d2c9eb7d6-800x.jpg)