Слайд 1Основа́ния — класс химических соединений.
Слайд 2Содержание.
Основания
Получение
Классификация
Номенклатура
Химические свойства
Слайд 3Основания
Основания (осно́вные гидрокси́ды) — сложные вещества, которые состоят из атомов металла
или иона аммония и гидроксогруппы (-OH). В водном растворе диссоциируют
с образованием катионов и анионов ОН−. Название основания обычно состоит из двух слов: «гидроксид металла/аммония». Хорошо растворимые в воде основания называются щелочами.
Согласно протонной теории кислот и оснований, основания — один из основных классов химических соединений, вещества, молекулы которых являются акцепторами протонов.
В органической химии по традиции основаниями называют также вещества, способные давать аддукты («соли») с сильными кислотами, например, многие алкалоиды описывают как в форме «алкалоид-основание», так и в виде «солей алкалоидов».
Слайд 4Получение.
Взаимодействие сильноосновного оксида с водой позволяет получить сильное основание или
щёлочь. Слабоосновные и амфотерные оксиды с водой не реагируют, поэтому
соответствующие им гидроксиды таким способом получить нельзя. Гидроксиды малоактивных металлов получают при добавлении щелочи к растворам соответствующих солей. Так как растворимость слабоосновных гидроксидов в воде очень мала, гидроксид выпадает из раствора в виде студнеобразной массы. Также основание можно получить при взаимодействии щелочного или щелочноземельного металла с водой. Гидроксиды щелочных металлов в промышленности получают электролизом водных растворов солей: Некоторые основания можно получить реакциями обмена: Основания металлов встречаются в природе в виде минералов, например: гидраргиллита Al(OH)3, брусита
Слайд 6Классификация
Основания классифицируются по ряду признаков.
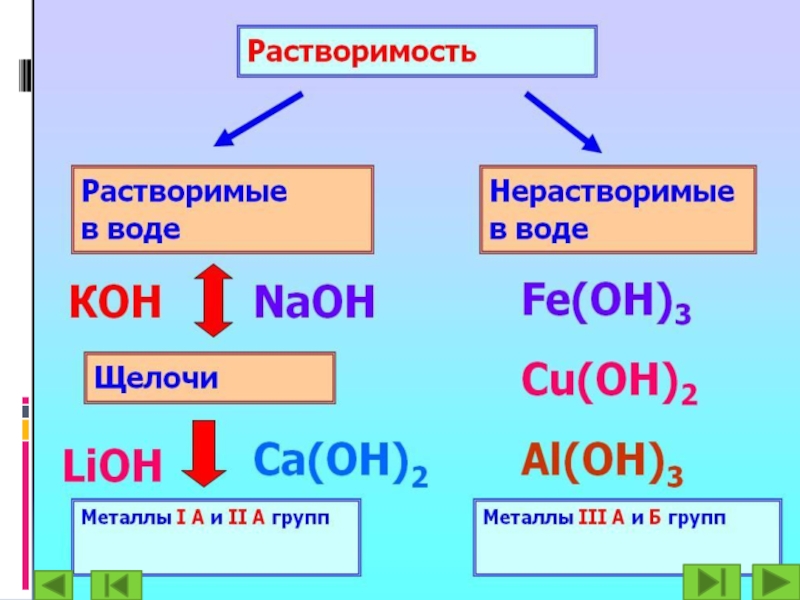
По растворимости в воде.
Растворимые основания
(щёлочи): гидроксид натрия NaOH, гидроксид калия KOH, гидроксид бария Ba(OH)2,
гидроксид стронция Sr(OH)2, гидроксид цезия CsOH, гидроксид рубидия RbOH.
Практически нерастворимые основания: Mg(OH)2, Ca(OH)2, Zn(OH)2, Cu(OH)2, Al(OH)3, Fe(OH)3, Be(OH)2.
Другие основания: NH3·H2O
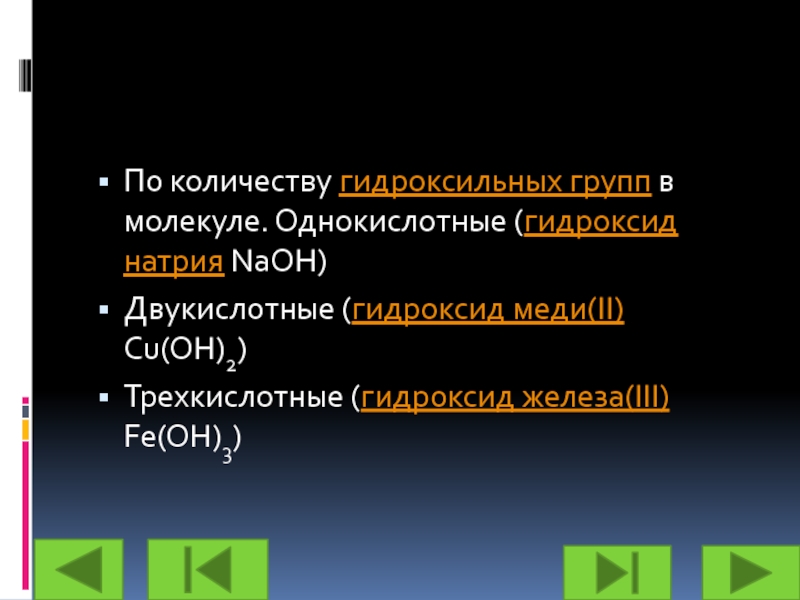
Слайд 8По количеству гидроксильных групп в молекуле. Однокислотные (гидроксид натрия NaOH)
Двукислотные
(гидроксид меди(II) Cu(OH)2)
Трехкислотные (гидроксид железа(III) Fe(OH)3)
Слайд 9По летучести. Летучие: NH3, CH3-NH2
Нелетучие: щёлочи, нерастворимые основания
Слайд 10По стабильности. Стабильные: гидроксид натрия NaOH, гидроксид бария Ba(OH)2
Нестабильные: гидроксид
аммония NH3·H2O (гидрат аммиак
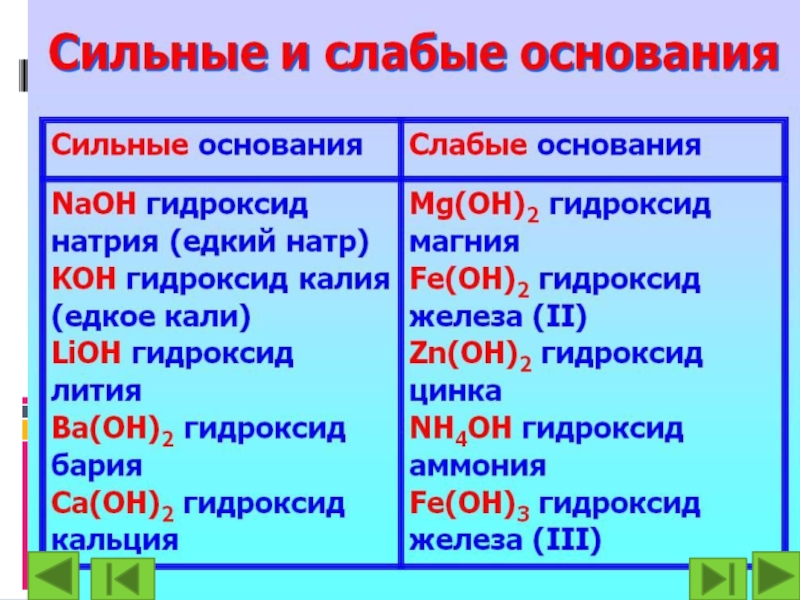
Слайд 11По степени электролитической диссоциации. Сильные (α > 30 %): щёлочи.
Слабые (α
< 3 %): нерастворимые основания.
Слайд 13По наличию кислорода. Кислородсодержащие: гидроксид калия KOH, гидроксид стронция Sr(OH)2
Бескислородные:
аммиак NH3, амины.
Слайд 14По типу соединения: Неорганические основания: содержат одну или несколько групп
-OH.
Органические основания: органические соединения, являющиеся акцепторами протонов: амины, амидины и
другие соединения.
Слайд 15Номенклатура
По номенклатуре IUPAC неорганические соединения, содержащие группы -OH, называются гидроксидами.
Примеры систематических названий гидроксидов:
NaOH — гидроксид натрия
TlOH — гидроксид таллия(I)
Fe(OH)2
— гидроксид железа(II)
Если в соединении есть оксидные и гидроксидные анионы одновременно, то в названиях используются числовые приставки:
TiO(OH)2 — дигидроксид-оксид титана
MoO(OH)3 — тригидроксид-оксид молибдена
Для соединений, содержащих группу O(OH), используют традиционные названия с приставкой мета-:
AlO(OH) — метагидроксид алюминия
CrO(OH) — метагидроксид хрома
Слайд 16Для оксидов, гидратированных неопределённым числом молекул воды, например Tl2O3•n H2O,
недопустимо писать формулы типа Tl(OH)3. Называть такие соединениями гидроксидами также
не рекомендуется. Примеры названий:
Tl2O3•n H2O — полигидрат оксида таллия(III)
MnO2•n H2O — полигидрат оксида марганца(IV)
Особо следует именовать соединение NH3•H2O, которое раньше записывали как NH4OH и которое в водных растворах проявляет свойства основания. Это и подобные соединения следует именовать как гидрат:
NH3•H2O — гидрат аммиака
N2H4•H2O — гидрат гидразина
Слайд 17Химические свойства
В водных растворах основания диссоциируют, что изменяет ионное равновесие:
это
изменение проявляется в цветах некоторых кислотно-основных индикаторов: лакмус становится синим,
метилоранж — жёлтым,
фенолфталеин приобретает
цвет фуксии.
При взаимодействии с кислотой происходит реакция нейтрализации и образуется соль и вода:
Примечание: реакция не идёт, если и кислота и основание слабые. При избытке кислоты или основания реакция нейтрализации идёт не до конца и образуются кислые или осно́вные соли, соответственно:
Слайд 18Амфотерные основания могут реагировать с щелочами с образованием гидроксокомплексов:
Основания реагируют
с кислотными или амфотерными оксидами с образованием солей:
Основания вступают в
обменные реакции (реагируют с растворами солей):
Слабые и нерастворимые основания при нагреве разлагаются на оксид и воду:
Некоторые основания (Cu(I), Ag, Au(I)) разлагаются уже при комнатной температуре. Основания щелочных металлов (кроме лития) при нагревании плавятся, расплавы являются электролитами.