Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основные понятия и законы теплотехники
Содержание
- 1. Основные понятия и законы теплотехники
- 2. Один опыт я
- 3. 1. Структура курса термодинамика и теплопередачаСогласно учебного
- 4. Слайд 4
- 5. Слайд 5
- 6. Термодинамика и теплопередачаТермодинамика и теплопередача – наука,
- 7. 2. Основные проблемы дисциплиныпарниковый эффекттепловое и химическое загрязнение окружающей среды.озоновые дыры.
- 8. Слайд 8
- 9. Слайд 9
- 10. Слайд 10
- 11. Слайд 11
- 12. Слайд 12
- 13. Слайд 13
- 14. Слайд 14
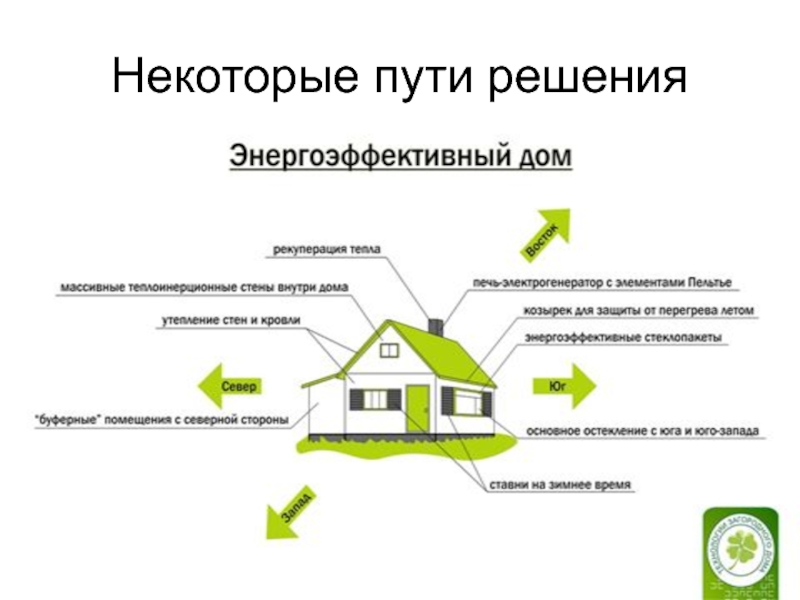
- 15. Некоторые пути решения
- 16. Слайд 16
- 17. Слайд 17
- 18. 3. Основные понятия и определенияИсторически термодинамика возникла
- 19. ИДЕАЛЬНЫЙ ГАЗ
- 20. ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКАБазируется на трёх основных законах (началах)
- 21. ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКАТермодинамика – раздел физики, изучающий общие
- 22. ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМАТермодинамической системой называется совокупность макроскопических тел,
- 23. Параметры состояния
- 24. Закон Бойля-МариоттаРоберт Бойль1627-1691английский химик, физик и теолог
- 25. Закон Гей-ЛюссакаЖозеф Луи Гей-Люссак1778-1850французский химик ифизик При
- 26. Закон ШарляЖан Александр Шарль1746-1823французский физик иизобретательПри постоянных
- 27. Закон Дальтона: давление смеси идеальных газов равно
- 28. Закон АвогадроСРЕДНЯЯ КИНЕТИЧЕСКАЯ ЭНЕРГИЯ поступательного движения одной
- 29. УРАВНЕНИЕ МЕНДЕЛЕЕВА – КЛАПЕЙРОНА уравнение состояния идеального
- 30. 4.Аналитическое выражение первого закона термодинамикиВНУТРЕННЕЙ ЭНЕРГИЕЙ вещества
- 31. Работа в термодинамике. Обмен энергией осуществляется
- 32. Количество теплотыТеплообмен происходит между телами или частями
- 33. Первое начало термодинамикиколичество теплоты, сообщенное системе, расходуется
- 34. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Q=dU+ A ПРИМЕНИТЕЛЬНО
- 35. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Q=dU+ A ПРИМЕНИТЕЛЬНО
- 36. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Q=dU+ A ПРИМЕНИТЕЛЬНО
- 37. 5. Второй закон термодинамикиФранцузская академия наук с
- 38. Слайд 38
- 39. Определения II закона термодинамики
- 40. Теорема Карно3. Формулировка Карно (II закона термодинамики):
- 41. 4. Формулировка ВТОРОГО НАЧАЛА ТЕРМОДИНАМИКИ на основе
- 42. Круговые процессы Круговым процессом (или циклом) называется
- 43. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Основные понятия и законы теплотехники
Структура курса термодинамика и теплопередача.
Основные проблемы
дисциплины.
Слайд 2 Один опыт я ставлю выше, чем
тысячу мнений, рожденных только воображением.
Математику уже за
то любить следует, что она ум в порядок приводит.Ежели ты хорошее сделаешь с трудом, труд минется, а хорошее останется, а ежели сделаешь что худое с услаждением, услаждение минется, а худое останется.
Кто малого не может, тому и большее невозможно.
Разум с помощью науки проникает в тайны вещества, указывает, где истина. Наука и опыт - только средства, только способы собирания материалов для разума.
М.В. Ломоносов
Слайд 31. Структура курса термодинамика и теплопередача
Согласно учебного плана дисциплина относится
к вариативной части блака1 и на её изучение отводится 3
з. е. (108 ч.) в т. ч.аудиторные занятия (контактная работа):
по очной форме обучения- 18/36 (лек./лаб.);
по заочной форме обучения- 4/4 (лек./лаб.);
самостоятельная работа:
по очной форме обучения – 54 час.
по заочной форме обучения – 100 час.
Форма промежуточной аттестации – диф. зач.
Слайд 6Термодинамика и теплопередача
Термодинамика и теплопередача – наука, которая изучает методы
получения, преобразования, передачи и использования теплоты, а также принципы действия
и конструктивные особенности тепловых машин, аппаратов и устройств.Термодинамика и теплопередача
Техническая термодинамика
Теория теплообмена
Тепловые процессы и аппараты
Слайд 72. Основные проблемы дисциплины
парниковый эффект
тепловое и химическое загрязнение окружающей среды.
озоновые
дыры.
Слайд 183. Основные понятия и определения
Исторически термодинамика возникла как наука, изучающая
переход теплоты в механическую работу, что диктовалось необходимостью дать теоретические
основы работы тепловых машинСлайд 19 ИДЕАЛЬНЫЙ ГАЗ можно рассматривать как
совокупность беспорядочно движущихся молекул-шариков, имеющих пренебрежимо малый собственный объем и
не взаимодействующих друг с другом на расстоянии.Слайд 20 ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА
Базируется на трёх основных законах (началах) термодинамики и уравнении
состояния:
I закон термодинамики - закон превращения и сохранения энергии;
II закон термодинамики – устанавливает условия , необходимые для превращения тепловой энергии в механическую в системах, состоящих из большого количества частиц;
III закон термодинамики – утверждает, что абсолютный нуль температуры недостижим.
Слайд 21 ТЕХНИЧЕСКАЯ ТЕРМОДИНАМИКА
Термодинамика – раздел физики, изучающий общие свойства макроскопических систем,
находящихся в состоянии термодинамического равновесия, и процессы перехода между этими
состояниямиОбъектом исследования является термодинамическая система.
Изолированная система - система не взаимодействующая с окружающей средой.
Адиабатная (теплоизолированная) система –имеет адиабатную оболочку, которая исключает обмен теплотой с окружающей средой.
Однородная система – система, имеющая во всех своих частях одинаковый состав и физические свойства.
Гомогенная система – однородная система по составу и физическому строению (лед, вода, газы).
Гетерогенная система – система, состоящая из нескольких гомогенных частей (фаз) с различными физическими свойствами, отделенных одна от другой видимыми поверхностями раздела (лед и вода, вода и пар).
Слайд 22ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА
Термодинамической системой называется совокупность макроскопических тел, которые могут обмениваться
энергией между собой и окружающей средой.
Термодинамические системы, которые не
обмениваются с внешней средой ни энергией, ни веществом называются замкнутыми (изолированными). Параметры состояния не всегда имеют определенные значения (одинаковые во всех точках системы). Состояние, в котором хотя бы один из параметров не имеет определенного значения, называется неравновесным.
Состояние термодинамической системы будет равновесным, если все параметры cостояния имеют определенные значения, не изменяющиеся с течением времени.
Любое изменение в термодинамической системе, связанное с изменением хотя бы одного из ее термодинамических параметров, называется термодинамическим процессом
Основа термодинамического метода – определение состояния термодинамической системы – совокупности макроскопических тел, которые взаимодействуют и обмениваются энергией как между собой, так и с другими телами (внешней средой).
Слайд 24Закон Бойля-Мариотта
Роберт Бойль
1627-1691
английский химик,
физик и теолог
Эдм Мариотт
1620-1684
французский физик
При постоянной массе газа и неизменной температуре произведение давления р
на объем V газа постояннопри Т=Const, m=Const
pV=Const - уравнение изотерм
Термодинамический процесс, протекающий при постоянной температуре, называется изотермическим процессом
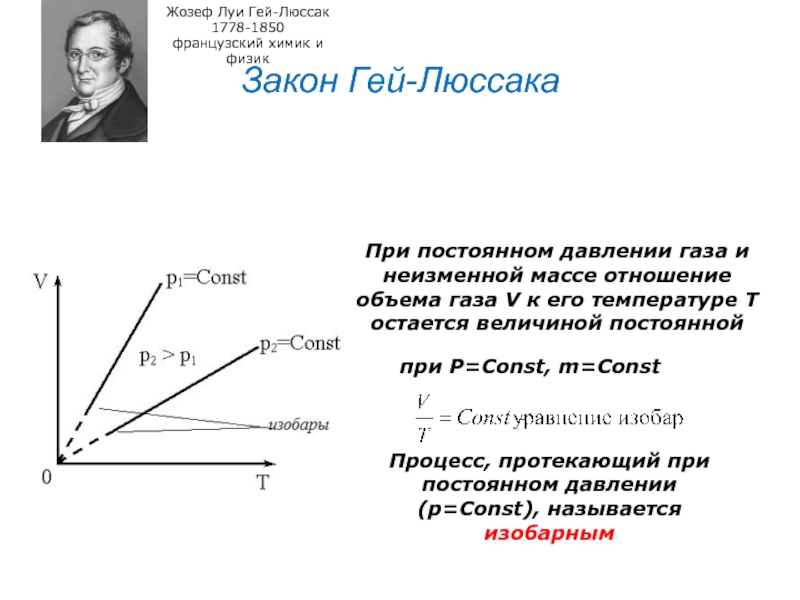
Слайд 25Закон Гей-Люссака
Жозеф Луи Гей-Люссак
1778-1850
французский химик и
физик
При постоянном давлении газа
и неизменной массе отношение объема газа V к его температуре
Т остается величиной постояннойпри Р=Const, m=Const
Процесс, протекающий при постоянном давлении (р=Const), называется изобарным
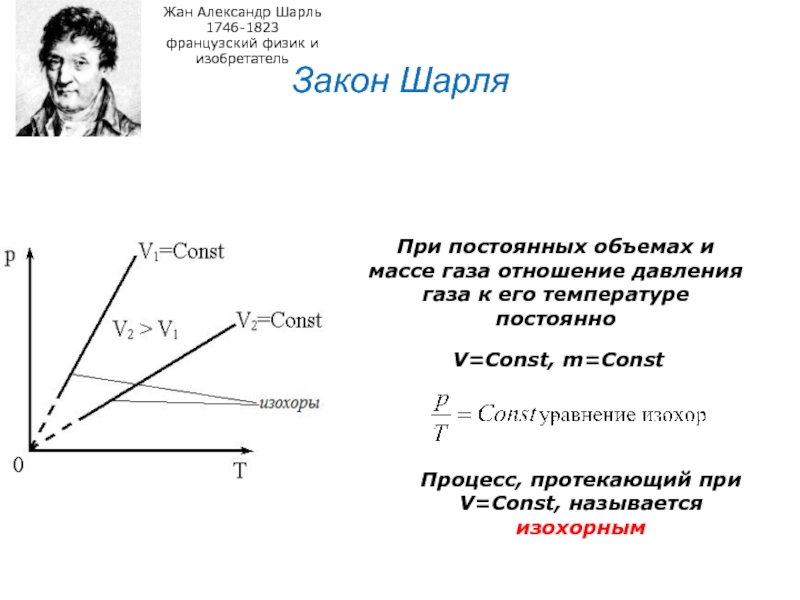
Слайд 26Закон Шарля
Жан Александр Шарль
1746-1823
французский физик и
изобретатель
При постоянных объемах и массе
газа отношение давления газа к его температуре постоянно
V=Const, m=Const
Процесс, протекающий
при V=Const, называется изохорнымСлайд 27Закон Дальтона: давление смеси идеальных газов равно сумме парциальных давлений
p1 , p2 ,…, pn входящих в нее газов
Парциальное
давление — давление, которое производил бы газ, входящий в состав газовой смеси, если бы он один занимал объем, равный объему смеси при той же температуреДжон Дальтон
1766-1844
английский физик
Слайд 28Закон Авогадро
СРЕДНЯЯ КИНЕТИЧЕСКАЯ ЭНЕРГИЯ поступательного движения
одной молекулы идеального газа
равна
k1,3810-23 Дж/К -
Постоянная Больцмана
.
Термодинамическая температура является мерой средней
кинетической энергии поступательного движения молекул идеального газаПри одинаковых условиях (при одинаковых давлениях и температуре) различные идеальные газы содержат в равных объемах одно и то же количество молекул
Подставляем
Делим почленно на V, и учитывая, что:
закон Авогадро
Слайд 29УРАВНЕНИЕ МЕНДЕЛЕЕВА – КЛАПЕЙРОНА
уравнение состояния идеального газа
m – масса газа,
–молярная масса газа (масса одного моля),
m/ = - количество
вещества (молей)Rµ – универсальная газовая постоянная 8.31 Дж/моль К
Согласно закону Авогадро: 1 моль любого вещества содержит одно и то же число молекул (число Авогадро )NA=6,022 1023 моль-1 и 1 моль идеального газа занимает при нормальных условиях объем V= 22,4 дм3= 22,410-3 м3
Слайд 304.Аналитическое выражение первого закона термодинамики
ВНУТРЕННЕЙ ЭНЕРГИЕЙ вещества называется энергия U,
зависящая от термодинамического состояния системы (вещества) (т.е. является функцией состояния
термодинамической системы) и включает в себя энергию всех видов внутренних движений в теле (системе).Для идеального газа учитывается только кинетическая энергия теплового поступательного и вращательного движения
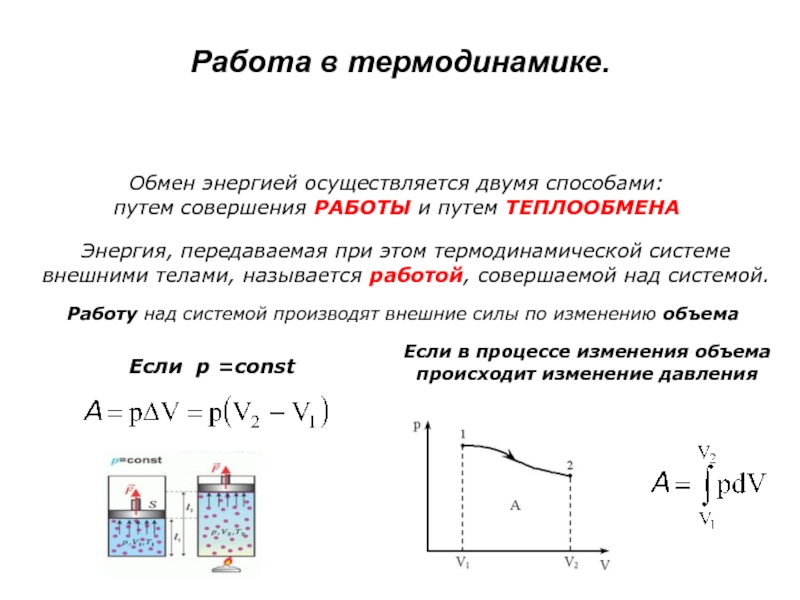
Слайд 31Работа в термодинамике.
Обмен энергией осуществляется двумя способами:
путем совершения
РАБОТЫ и путем ТЕПЛООБМЕНА
Энергия, передаваемая при этом термодинамической системе внешними
телами, называется работой, совершаемой над системой. Работу над системой производят внешние силы по изменению объема
Если p =const
Если в процессе изменения объема происходит изменение давления
Слайд 32Количество теплоты
Теплообмен происходит между телами или частями одного и того
же тела, нагретыми до различной температуры
Энергия (Q или Q), передаваемая
системе внешними телами путем теплообмена (без совершения работы), называется ТЕПЛОТОЙ (КОЛИЧЕСТВОМ ТЕПЛОТЫ (Дж)), получаемой системой от внешней среды
ТЕПЛОЕМКОСТЬЮ тела (вещества) называется физическая величина, численно равная количеству теплоты, которое необходимо подвести к телу, чтобы увеличить его температуру на один градус
УДЕЛЬНАЯ ТЕПЛОЕМКОСТЬ вещества – теплоемкость единицы массы вещества
В зависимости от вида процесса изменения состояния вещества различают теплоемкость при постоянном давлении Сv и при постоянном объеме Сp
Молярная теплоемкость Cμ
теплоемкость одного моля вещества
[Дж/(моль К)]
Слайд 33Первое начало термодинамики
количество теплоты, сообщенное системе, расходуется на изменение внутренней
энергии системы и на совершение системой работы против внешних сил
ПЕРВОЕ
НАЧАЛО ТЕРМОДИНАМИКИ – это закон сохранения и превращения энергии в термодинамических процессахДля изменения состояния системы, вызванного сообщением ей бесконечно малого количества теплоты Q
Если к системе подводится теплота, то δQ > 0
Если от системы отводится теплота, то δQ < 0
Если система совершает работу над внешними телами, то δA > 0
Если же над системой внешние силы совершают работу, то δA < 0
Слайд 34ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Q=dU+ A ПРИМЕНИТЕЛЬНО К ИЗОПРОЦЕССАМ В ИДЕАЛЬНЫХ
ГАЗАХ
Для изохорного процесса (V= Const) работа равна нулю, поскольку dV=0
A=pdV=0В изохорном процессе количество теплоты, переданное системе, идет на увеличение ее внутренней энергии, т.е. на увеличение температуры
для 1 моля вещества:
Для изотермического процесса (Т=Const) dU=0
В изотермическом процессе все тепло, получаемое системой, расходуется на совершение системой работы.
Слайд 35ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Q=dU+ A ПРИМЕНИТЕЛЬНО К ИЗОПРОЦЕССАМ В ИДЕАЛЬНЫХ
ГАЗАХ
АДИАБАТНЫМ называется, термодинамический процесс, при котором система не обменивается теплом
с окружающей средой, т.е. Q=0. Такая система называется теплоизолированной
Q=0
A–dU
Работа в адиабатном процессе совершается за счет убыли внутренней энергии системы
Уравнение адиабаты
Уравнение Пуассона
Слайд 36ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ Q=dU+ A ПРИМЕНИТЕЛЬНО К ИЗОПРОЦЕССАМ В ИДЕАЛЬНЫХ
ГАЗАХ
Для изобарного процесса (p=const)
Физический смысл R: численно равна работе,
совершаемой одним молем идеального газа при его изобарном нагревании на один градусУравнение Майера :
Слайд 375. Второй закон термодинамики
Французская академия наук с 1755 г. «раз
и навсегда» объявила что не принимает на рассмотрение проекты «вечных
двигателей»Двигатель, который позволял бы получать работу без энергетических затрат называется вечным двигателем первого рода.
Двигатель полностью превращающий в работу всю полученную от горячего источника теплоту, называется вечным двигателем второго рода
Слайд 39
Определения II закона термодинамики
1.Формулировка Клаузиуса: теплота самопроизвольно не может
переходить от тела с меньшей температурой к телу с большей
температурой2. Формулировка Томсона (Кельвина): невозможен такой периодический процесс единственным результатом которого было бы превращение теплоты в работу вследствие охлаждения тела
Слайд 40Теорема Карно
3. Формулировка Карно (II закона термодинамики):
Теорема Карно: КПД
обратимых машин, работающих при одинаковых температурах нагревателей и
холодильников, равны друг другу и не зависят от природы рабочего тела, а определяются только температурами нагревателя и холодильникадля повышения к.п.д. тепловой машины нужно увеличивать температуру нагревателя и уменьшать температуру холодильника
к.п.д. тепловой машины всегда меньше 1!
Слайд 414. Формулировка ВТОРОГО НАЧАЛА ТЕРМОДИНАМИКИ на основе понятия энтропии:
ЭНТРОПИЯ замкнутой (теплоизолированной) системы не может убывать при любых происходящих
в ней процессахЗАКОН ВОЗРАСТАНИЯ ЭНТРОПИИ
неравенство Клаузиуса
Энтропией S называется функция состояния системы и характеризует направление протекания процессов в термодинамической системе
Если система замкнутая (теплоизолированная), то изменение энтропии для
обратимого кругового процесса равно нулю S=0
необратимого - S>0
.
Слайд 42Круговые процессы
Круговым процессом
(или циклом) называется процесс, при котором
система, пройдя через ряд промежуточных состояний, возвращается в исходное
A>0, то
цикл называется прямымA<0, то цикл называется обратным
РАБОТА , равно как и ТЕПЛОТА — является функцией процесса,
который происходит с системой
Термодинамический процесс называется ОБРАТИМЫМ, если после его завершения в окружающей среде не произошло никаких изменений – физическая абстракция!
Все реальные процессы являются необратимыми!