Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основные принципы проточной цитомет р ии ИММУНОФЕНОТИПИРОВАНИЕ СУБПОПУЛЯЦИИ
Содержание
- 1. Основные принципы проточной цитомет р ии ИММУНОФЕНОТИПИРОВАНИЕ СУБПОПУЛЯЦИИ
- 2. Проточная цитометрияПроточная цитометрия — автоматизированный анализ клеток, проходящих в потоке жидкости перед источником света.
- 3. Проточные цитометрыЧетыре основных компонентаИсточник света — обычно
- 4. Слайд 4
- 5. Проточные цитометрыЧто измеряется?Малоугольное рассеяние света (FSC) —
- 6. Проточные цитометрыОсновные возможностиМультипараметрический анализВозможность одновременного измерения нескольких
- 7. Преимущества проточной цитометрииСтатистическая достоверность.Быстрота.Объективность.Количественное определение.Одновременный анализ
- 8. Недостатки проточной цитометрииНеобходимо наличие суспензии
- 9. Применение проточной цитометрииКлиническая практикаИммунофенотипированиеАнализ ДНК/клеточного циклаПодсчет
- 10. ИммунофенотипированиеОсновано на распознавании поверхностных антигенов мембраны моноклональными
- 11. ИммунофенотипированиеПодготовка клетокОбразцами обычно является периферическая кровь, костный
- 12. ИммунофенотипированиеПодготовка клетокИспользуются два основных метода.Метод лизирования с
- 13. ИммунофенотипированиеПодготовка клетокМетод лизирования с отмывкой- Внесите меченные
- 14. ИммунофенотипированиеПодготовка клетокМетод лизирования без отмывки- Внесите меченные
- 15. ИммунофенотипированиеПолучаемая информация является одновременно диагностической и
- 16. Панели антител для подсчета CD4Выбор используемой
- 17. Панели антител для подсчета CD4Выбор используемой
- 18. Примеры панелей антител для подсчета CD4Для ручных
- 19. Примеры панелей антител для подсчета CD4Для четырехцветовых систем:анти-CD4/анти-CD8/анти-CD45/анти-CD3;анти-CD19/анти-CD16+56/анти-CD45/анти-CD3.Для шестицветовых систем:анти-CD3/анти-CD16+56/анти-CD45/ анти-CD4/анти-CD19/анти-CD8.Панели антител для подсчета CD4
- 20. Стратегии гейтингаСуществует два типа стратегий гейтингаFSC против
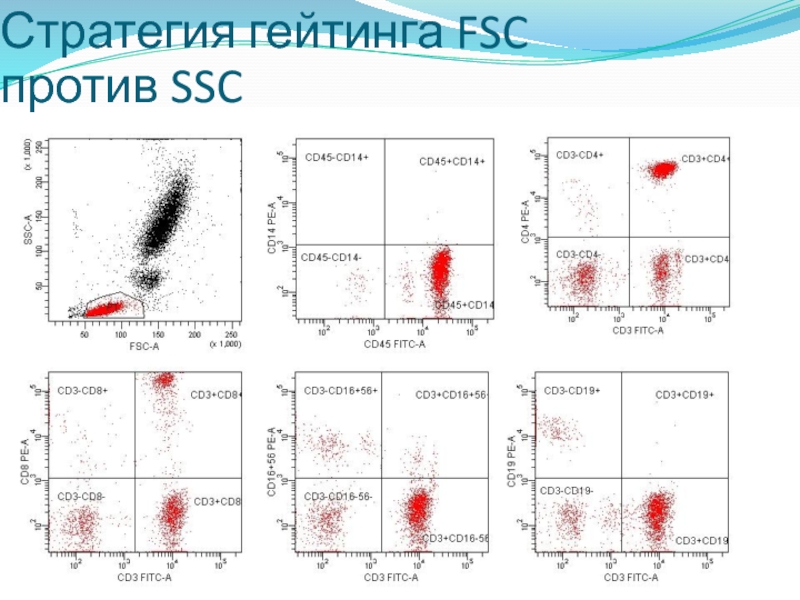
- 21. Стратегия гейтинга FSC против SSC
- 22. Стратегии гейтингаCD45 против SSCВыбор популяции, подлежащей анализу,
- 23. Стратегия гейтинга CD45 против SSC
- 24. РезюмеПроточная цитометрия является полуавтоматическим методом, который может
- 25. РезюмеИммунофенотипирование — методика, в которой для
- 26. ВопросыДайте определение проточной цитометрии;Опишите основные компоненты проточного
- 27. ВопросыОпишите возможные варианты применения проточной цитометрии в
- 28. Скачать презентанцию
Проточная цитометрияПроточная цитометрия — автоматизированный анализ клеток, проходящих в потоке жидкости перед источником света.
Слайды и текст этой презентации
Слайд 2Проточная цитометрия
Проточная цитометрия — автоматизированный анализ клеток, проходящих в потоке
жидкости перед источником света.
Слайд 3Проточные цитометры
Четыре основных компонента
Источник света — обычно лазер или дуговая
ртутная лампа.
Контейнер для образца, проточная ячейка
и оптическая система.
Электронная система
— преобразует световые импульсы в цифровые сигналы.Компьютерная система — управляет работой прибора, накапливает данные и выполняет стандартные аналитические операции.
Слайд 5Проточные цитометры
Что измеряется?
Малоугольное рассеяние света (FSC) — пропорциональное размеру клетки.
Боковое
рассеяние света (SSC) — пропорциональное зернистости клетки.
Флуоресцентные сигналы — обычно
от двух до восьми, но может быть
и большее количество.Слайд 6Проточные цитометры
Основные возможности
Мультипараметрический анализ
Возможность одновременного измерения нескольких параметров (размера, зернистости,
связанной флуоресценции) каждой клетки.
Гейтинг
Возможность установки селектора для определенной подвыборки событий
или анализируемой клеточной популяции.Слайд 7Преимущества
проточной цитометрии
Статистическая достоверность.
Быстрота.
Объективность.
Количественное определение.
Одновременный анализ нескольких параметров.
Чувствительность — менее 2000
молекул
на клетку.
Малое количество требуемого образца.
Слайд 8Недостатки
проточной цитометрии
Необходимо наличие суспензии
из отдельных клеток.
Потеря структуры ткани.
Медленная
сортировка клеток и получение данных по небольшому количеству клеток.
Стоимость оборудования.
Потребность
в обученном персонале.Ограничения по другим позициям.
Трудности в управлении данными.
Слайд 9Применение
проточной цитометрии
Клиническая практика
Иммунофенотипирование
Анализ ДНК/клеточного цикла
Подсчет ретикулоцитов
Исследовательская практика
Многие исследования, в
том числе требующие сортировки клеток; измерения клеточной активации, например потока
Ca++, изменений pH и мембранного потенциала; экспрессии онкогенов и т. п.Слайд 10Иммунофенотипирование
Основано на распознавании поверхностных антигенов мембраны моноклональными антителами
Применяется:
для классификации лейкемий
и лимфом;
мониторинга уровня CD4
у ВИЧ-инфицированных пациентов;
мониторинга отторжения органного трансплантата;
мониторинга
состояния пациентов
с аутоиммунными заболеваниями или
с состояниями первичного иммунодефицита.Слайд 11Иммунофенотипирование
Подготовка клеток
Образцами обычно является периферическая кровь, костный мозг или ткань
лимфатического узла, в зависимости от цели анализа.
Для определения CD4
используется
периферическая кровь.Слайд 12Иммунофенотипирование
Подготовка клеток
Используются два основных метода.
Метод лизирования с отмывкой.
Метод лизирования без
отмывки.
Должен использоваться
в интегрированных приборах на единой платформе, в которых
для подсчета абсолютного количества клеток применяются флуоресцентные микросферы.Слайд 13Иммунофенотипирование
Подготовка клеток
Метод лизирования с отмывкой
- Внесите меченные флуорохромом моноклональные антитела
в небольшое количество материала образца.
- Инкубируйте 20 минут, внести лизирующее
вещество на 10 минут, отмыть и ресуспендировать в фиксаторе.- Проведите анализ.
Слайд 14Иммунофенотипирование
Подготовка клеток
Метод лизирования без отмывки
- Внесите меченные флуорохромом моноклональные антитела
в точно определенное количество образца.
Инкубируйте 20 минут, внесите лизирующее/фиксирующее вещество
на 10 минутПроведите анализ.
Слайд 15Иммунофенотипирование
Получаемая информация является одновременно диагностической
и прогностической.
Используя панели специфических моноклональных
антител, получают профиль типов присутствующих клеток.
Абсолютные величины содержания клеток
в
периферической крови могут быть получены с использованием значений общего анализа крови (CBC) или с учетом известного количества флуоресцентных микросфер.Слайд 16Панели антител
для подсчета CD4
Выбор используемой для подсчета CD4 панели
моноклональных антител зависит от нескольких факторов.
Метод, используемый для определения CD4
Полуавтоматический
Ручной
Предполагаемая
стратегия гейтингаFSC против SSC или CD45 против SSC
Слайд 17Панели антител
для подсчета CD4
Выбор используемой для подсчета CD4 панели
моноклональных антител зависит от нескольких факторов.
Тип доступного прибора
Проточный цитометр с
определением
от двух до шести цветов.Лабораторный стационарный (напр., FACSCalibur), скоростной (напр., FACSCount), портативный (напр., PIMA).
Стоимость
Слайд 18Примеры панелей антител для подсчета CD4
Для ручных методов, вероятно, будет
использоваться только анти-CD4.
Для блокирования CD4 на моноцитах также используется анти-CD14.
Для двухцветовых систем:
анти-CD3/анти-CD4 и анти-CD3/анти-CD8;
анти-CD3/анти-CD16+56 и анти-CD3/анти-CD19.
Панели антител
для подсчета CD4
Слайд 19Примеры панелей антител для подсчета CD4
Для четырехцветовых систем:
анти-CD4/анти-CD8/анти-CD45/анти-CD3;
анти-CD19/анти-CD16+56/анти-CD45/анти-CD3.
Для шестицветовых систем:
анти-CD3/анти-CD16+56/анти-CD45/
анти-CD4/анти-CD19/анти-CD8.
Панели
антител
для подсчета CD4
Слайд 20Стратегии гейтинга
Существует два типа стратегий гейтинга
FSC против SSC
Отбор популяции, подлежащей
анализу, определяется характеристиками рассеяния света клеточными популяциями.
Этот метод часто комбинируется
с отдельным измерением флуоресценции CD45 против CD14
в процедуре обратного гейтинга.Требуется отдельный прогон анализа пробирки с контрольными антителами для установления уровня фоновой аутофлуоресценции.
Слайд 22Стратегии гейтинга
CD45 против SSC
Выбор популяции, подлежащей анализу, основан на сочетании
флуоресценции
CD45 и бокового рассеяния света под углом 90°
Требуется присутствие анти-CD45
во всех анализах.При анализе лимфоцитов клетки всех прочих типов исключаются из процесса исследования.
Затем за счет наличия или отсутствия специфических маркеров (например, CD3) определяются субпопуляции.
Изотипические контрольные материалы обычно не требуются, так как для определения уровней фоновой аутофлуоресценции могут быть использованы отрицательные значения популяций на диаграмме рассеяния.
Слайд 24Резюме
Проточная цитометрия является полуавтоматическим методом, который может быть использован для
определения как физических характеристик клеток, так и других их свойств
на основе связывания клеток с аналитами, которые либо обладают собственной флуоресценцией, либо связаны с молекулами флуоресцентного вещества.Проточные цитометры способны измерять одновременно несколько параметров каждой клетки.