устойчивостью.
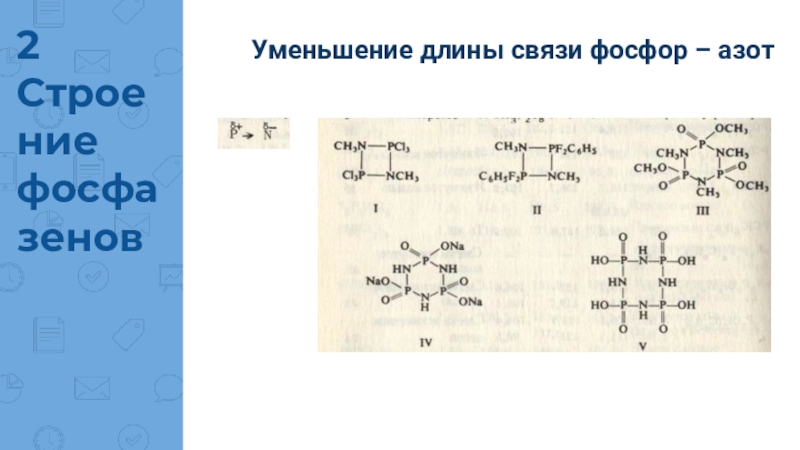
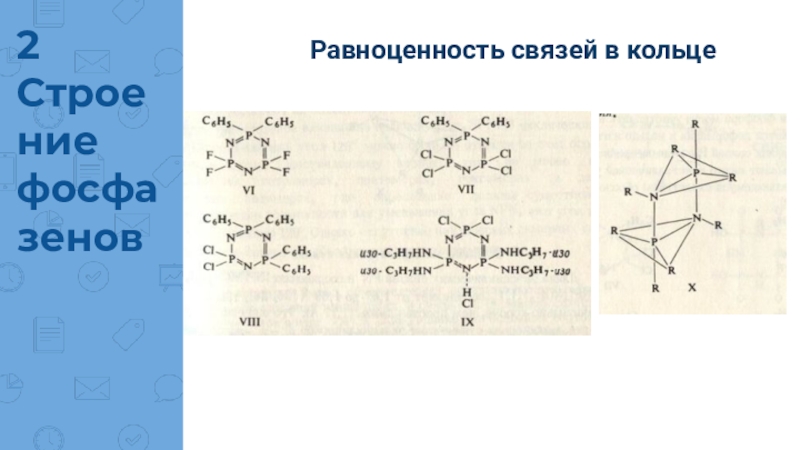
Связи PN в фосфазенах короче чисто ковалентных σ-связей Р—N. Наименьшие
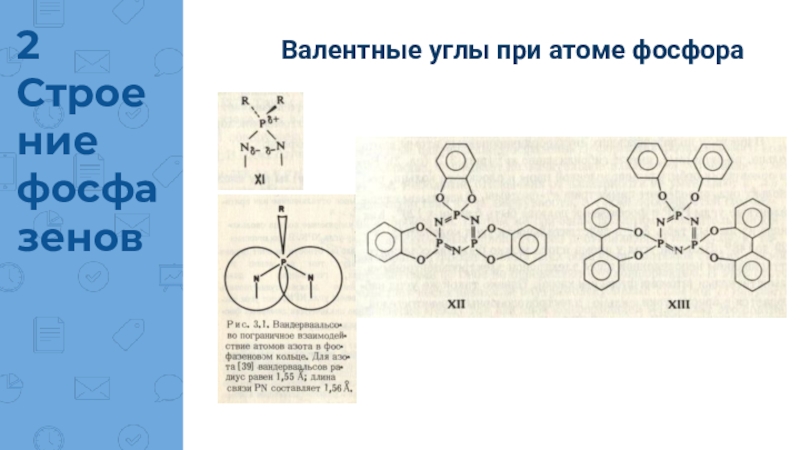
длины связей наблюдаются в присутствии наиболее электроотрицательных заместителей. Длины связей PN кольца обычно одинаковы, за исключением тех случаев, когда заместители расположены несимметрично.