Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Острые лейкозы
Содержание
- 1. Острые лейкозы
- 2. «Гематология – это острые лейкозы» Томас Бюхнер
- 3. Острые лейкозыОстрые лейкозы (ОЛ) представляют собой гетерогенную
- 4. Острые лейкозыВсе острые лейкозы клональны, то есть
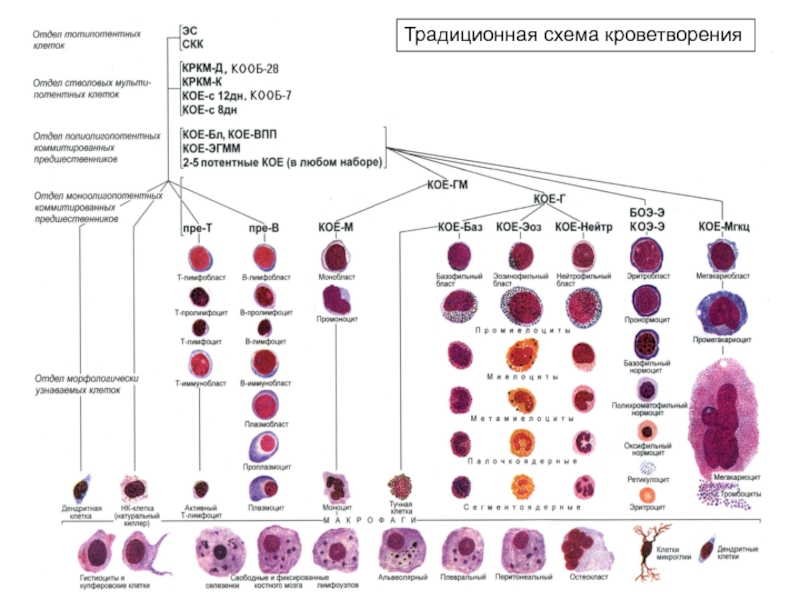
- 5. Традиционная схема кроветворения
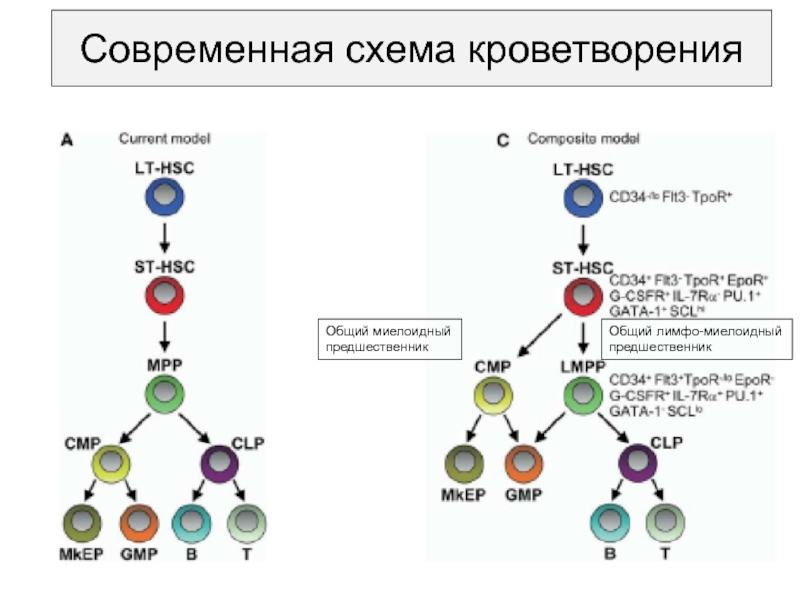
- 6. Современная схема кроветворенияОбщий миелоидныйпредшественникОбщий лимфо-миелоидныйпредшественник
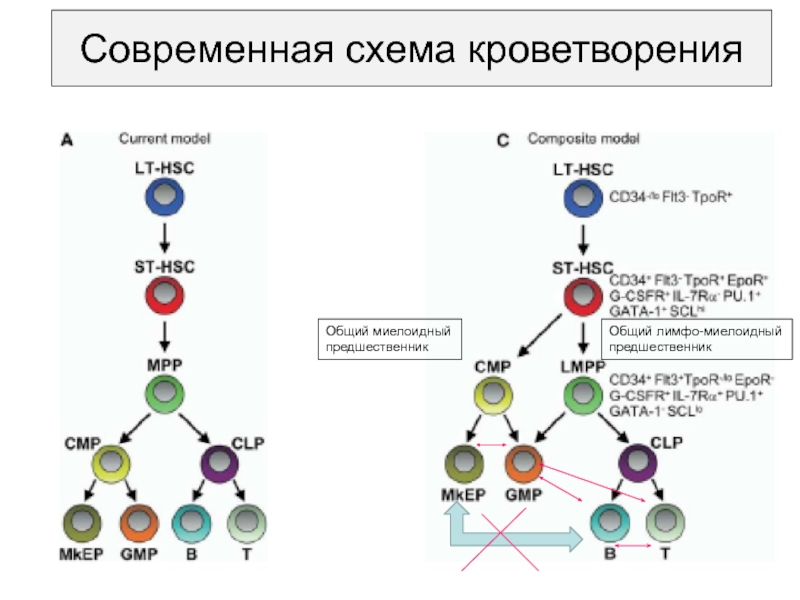
- 7. Современная схема кроветворенияОбщий миелоидныйпредшественникОбщий лимфо-миелоидныйпредшественник
- 8. Слайд 8
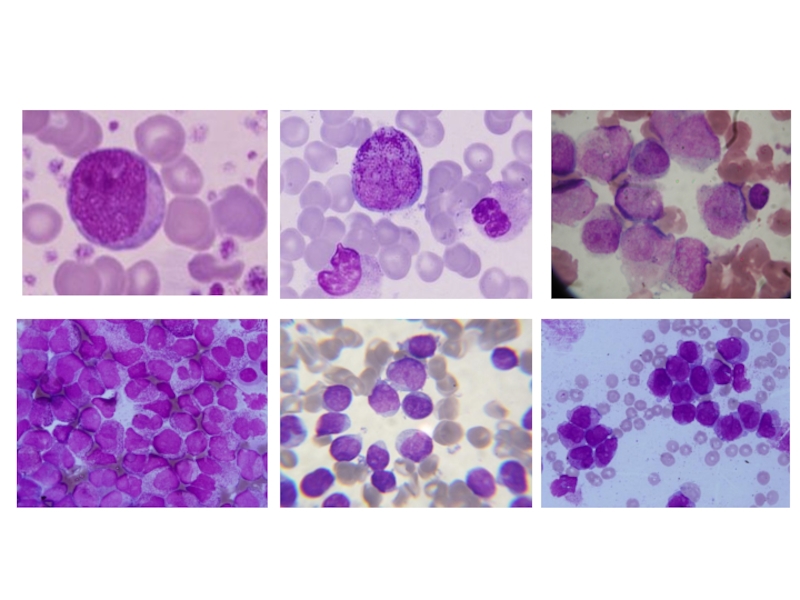
- 9. Трепанобиоптат (х10)
- 10. D.M. Parkin The Lancet Oncology 2: 533-543
- 11. ЭпидемиологияОстрый лейкоз - довольно редкое заболевание и
- 12. Подсчитано, что в США в 2013 году
- 13. По данным Российского Ракового Регистрав 2009 году
- 14. Медиана возраста диагностики ОМЛ составляет 65 лет
- 15. По расчетам в США в 2013 -
- 16. DORES et al BLOOD, 5 JANUARY 2012,
- 17. Результаты регистрационного исследования ( с апреля 2013)
- 18. Течение заболеванияДо появления современных цитостатических препаратов и
- 19. ЭтиологияВ большинстве случаев конкретная причина возникновения острого
- 20. ЭтиологияРоль вирусов в развитии лейкозов доказана в
- 21. ЭтиологияЧетко доказана взаимосвязь между ионизирующей радиацией при
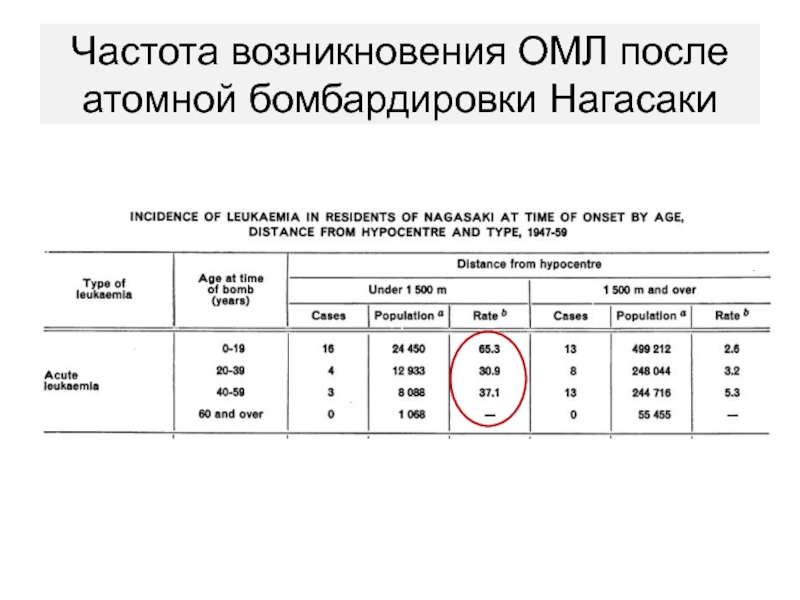
- 22. Частота возникновения ОМЛ после атомной бомбардировки Нагасаки
- 23. ЭтиологияВпервые взаимосвязь между предшествующей химиотерапией, лучевым лечением
- 24. ЭтиологияПри еженедельном использовании эпиподофиллотоксинов - этопозида или
- 25. ЭтиологияДоказано, что между курением и риском развития
- 26. ЭтиологияБензол при длительном воздействие на организм человека
- 27. Развитие ОЛ -следствие повреждения - мутации -
- 28. Развитие ОЛ -следствие повреждения - мутации -
- 29. ДиагностикаДиагностика острых лейкозов базируется на оценке морфологических
- 30. Иммунофенотипирование бластных клетокНе является принципиальным методом для
- 31. Ключевые маркеры, определяющие принадлежность бластных клеток к той или иной линии дифференцировки
- 32. Классификация ОЛНаиболее распространенной морфологической классификацией острых лейкозов
- 33. Слайд 33
- 34. Классификация ОЛОстрые миелоидные лейкозы и опухоли из
- 35. ОМЛ и опухоли из миелоидных предшественниковОМЛ подразделяется
- 36. ОМЛ, ассоциированный со стабильно выявляемыми генетическими аномалиямиОМЛ
- 37. ОМЛ с изменениями, характерными для миелодисплазииОМЛ, которые
- 38. Миелоидные опухоли, ассоциированные с предшествующей химиотерапииОМЛ или
- 39. ОМЛ неспецифицируемый (ФАБ-классификация)М0 - острый миелобластный
- 40. Опухоли из миелоидных предшественников Миелоидная саркома Пролиферации
- 41. Бифенотипические лейкозыДиагноз бифенотипического острого лейкоза устанавливается в
- 42. Острые лейкозы с «разнонаправленной» дифференцировкойОстрый недифференцируемый
- 43. Острые лимфобластные лейкозы в новой ВОЗ-классификации рассматриваются в
- 44. Опухоли из лимфоидных предшественниковB- лимфобластный лейкоз/лимфома B-лимфобластный
- 45. В-клеточныеПро-В (B I)CD19+, CD10-,
- 46. Иммунофенотипирование опухолевых клеток, хромосомный анализ,молекулярно-биологический анализ
- 47. При использовании этих методов было доказано, что1)
- 48. Эти положения позволили внедрить в лейкозологию такие
- 49. Клинические проявленияПроявления ОЛ довольно сходны при различных
- 50. При объективном обследованииможет не наблюдаться никаких симптомовувеличение
- 51. Лабораторные показателиВ анализах крови могут быть неспецифические
- 52. Дифференциальная диагностикаПроста, поскольку, если есть бластные клетки
- 53. Дифференциальная диагностикаУвеличение числа лейкоцитов со сдвигом формулы
- 54. Дифференциальная диагностикаИнфекционный мононуклеоз и некоторые другие вирусные
- 55. Дифференциальная диагностикаРАИБ-2Бластный криз хронического миелолейкоза (t(9;22)может обнаруживаться и при ОЛ)Лимфома из клеток мантийной зоны
- 56. Экстрамедуллярные пораженияНейролейкемияЕе возникновение обусловлено метастазированием лейкозных клеток
- 57. Нейролейкемияхарактеризуется менингеальным и гипертензивным синдромом: отмечается постоянная
- 58. НейролейкемияНаиболее часто нейролейкемия возникает при острых лимфобластных
- 59. Экстрамедуллярные пораженияЛейкемиды (инфильтрация кожи)Поражение сетчатки, десен, яичек,
- 60. Периоды заболевания (на фоне терапии) В течении
- 61. Динамика объема опухоли в процессе лечения острых лейкозовРецидивМорфологическая ремиссияЛейкемические клеткиВремяМинимальная резидуальнаяболезнь
- 62. Основополагающими принципами химиотерапии всех злокачественных опухолей человека,
- 63. Адекватность цитостатического воздействиядозы цитостатических препаратов способ и
- 64. Ключевые ожидаемые побочные эффектымиелосупрессия = анемия+ нейтропения
- 65. Что происходит с программной химиотерапией вследствие развития
- 66. Доза -интенсивностьКак в эксперименте, так и в
- 67. 1988-1993Неадекватное цитостатическое воздействие – неоспоримый
- 68. Лечение острых лейкозов должно осуществляться только в
- 69. Подготовка к химиотерапииСледует подчеркнуть, что практически никогда
- 70. Подготовка к химиотерапииПодготовить пациента к проведению индукционной
- 71. Основной целью лечения ОЛ- является эрадикация лейкемического
- 72. Основные этапы терапии ОЛиндукция ремиссии, консолидация ремиссии, поддерживающая терапия профилактика нейролейкемии (для некоторых вариантов ОЛ)
- 73. Индукция ремиссииЭто период начального лечения, целью которого
- 74. Консолидация ремиссииявляется вторым этапом терапии острых лейкозов,
- 75. Период поддерживающего леченияначинается после консолидации при разных
- 76. Принципиальным этапом при лечении некоторых вариантов ОЛ
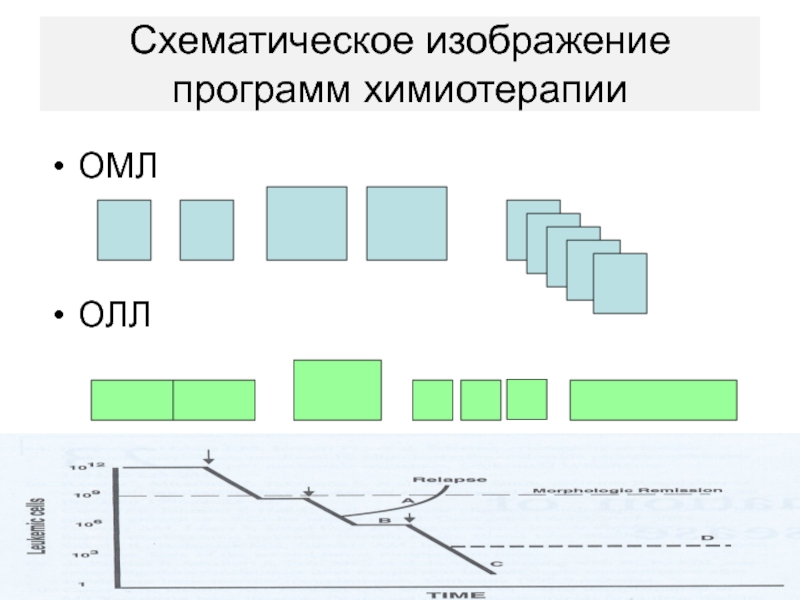
- 77. Схематическое изображение программ химиотерапииОМЛОЛЛ
- 78. Острые миелоидные лейкозыI / HDAraC +Dauno orMito
- 79. ОЛЛ – разные подходыКонсолидация+ i.th MTX, AraC,
- 80. ОЛЛ – разные подходыКонсолидация+ i.th MTX, AraC,
- 81. Как может изменить результаты лечения изменение принципа цитостатического воздействияОбщая выживаемостьБезрецидивная выживаемость45%38%ОЛЛ-2005ОЛЛ-200960%57%
- 82. Основные понятияПолная ремиссияМорфологическаяЦитогенетическая Молекулярнаяс неполным восстановлением показателей
- 83. Полная ремиссиято состояние кроветворной ткани, при котором
- 84. Резистентная форма ОЛконстатируется при отсутствии полной ремиссии
- 85. по международным критериям резистентность при ОМЛ можно
- 86. Ранняя смерть – смерть больного в период
- 87. Рецидив ОЛКонстатируется при обнаружении в пунктате костного
- 88. Успех в лечении ОЛ определяется прецизионностью диагноза
- 89. Прецизионность диагностики даже уже в рамках определенного
- 90. Целенаправленность воздействияОстрые промиелоцитарные лейкозыполностью транс-ретиноевая кислотатриоксид мышьякаPh-позитивные острые лейкозы – ингибиторы тирозинкиназ
- 91. Мониторинг минимальной резидуальной болезниРецидивМорфологическая ремиссияЛейкемические клеткиВремяМинимальная резидуальнаяболезнь
- 92. 10-4
- 93. Слайд 93
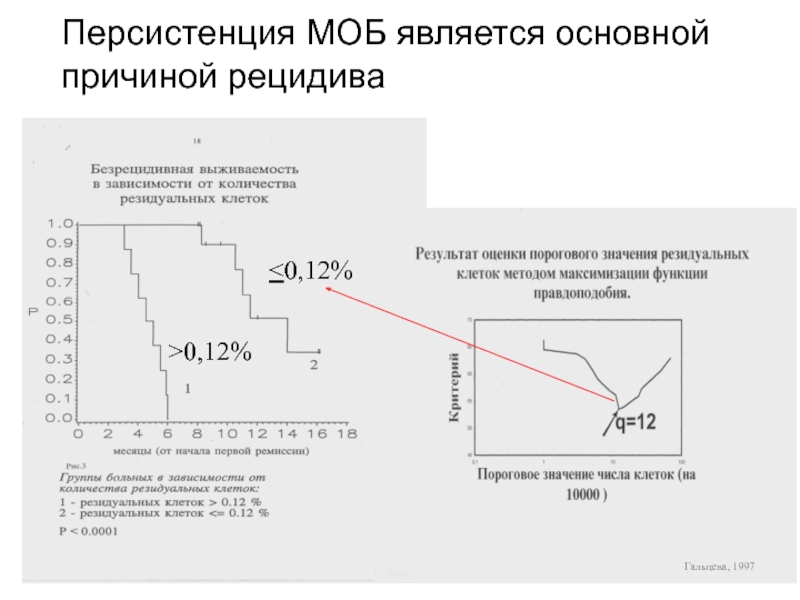
- 94. Персистенция МОБ является основной причиной рецидива0,12%Гальцева, 1997
- 95. Различный клиренс опухоли при разных острых лейкозахОЛЛОПЛIgH/TCRШуравина, Мисюрин, Давидян, Гальцева, Паровичникова, Савченко 2001-2012
- 96. Клиренс опухолевого клона на протоколе AIDA значимо
- 97. CBF-ОМЛ
- 98. ОЛЛ-2005 ОПЛ-2001ОМЛ-2006 ОМЛ-1011112222Результаты лечения ОЛ напрямую зависят от опыта команды
- 99. Catherine Mengis, Stefan Aebi, Andreas Tobler, Werner
- 100. Catherine Mengis, et al Journal of Clinical
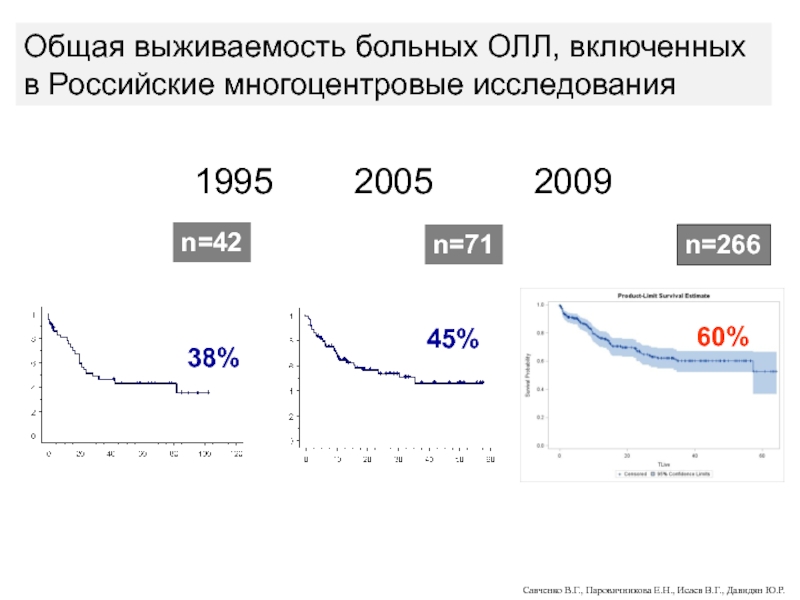
- 101. Общая выживаемость больных ОМЛ, включенных в Российские
- 102. 1995 2005 200938%45%60%n=42n=71n=266Савченко В.Г., Паровичникова Е.Н., Исаев
- 103. Добро пожаловать в КОМАНДУ!
- 104. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Острые лейкозы
Острые лейкозы (ОЛ) представляют собой гетерогенную группу опухолевых заболеваний
Слайд 4Острые лейкозы
Все острые лейкозы клональны, то есть возникают из одной
мутировавшей кроветворной клетки, которая может относиться как к очень ранним,
так и к коммитированным в направлении различных линий кроветворения клеткам-предшественницам.Принадлежность бластных клеток к той или иной линии кроветворения, степень их дифференцировки обусловливают клиническое течение острого лейкоза, терапию, эффективность проводимого лечения и, соответственно, прогноз заболевания
Слайд 6Современная схема кроветворения
Общий миелоидный
предшественник
Общий лимфо-миелоидный
предшественник
Слайд 7Современная схема кроветворения
Общий миелоидный
предшественник
Общий лимфо-миелоидный
предшественник
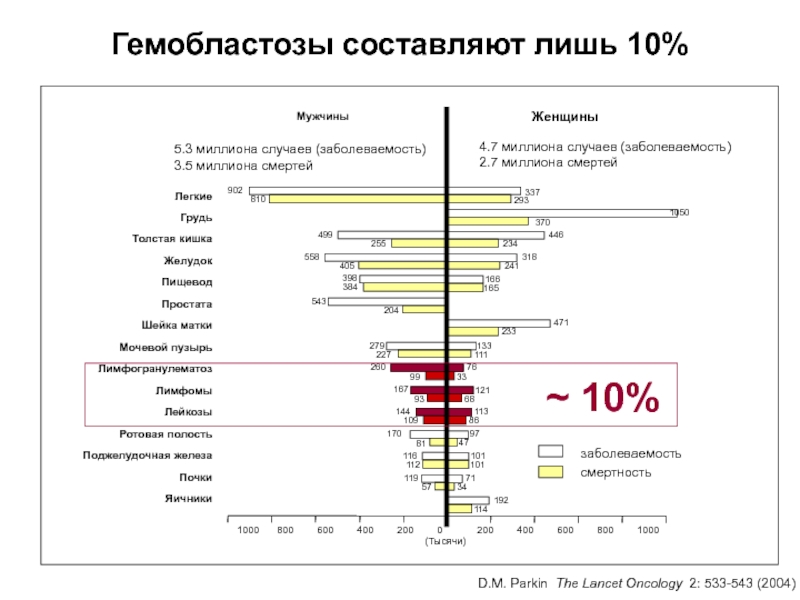
Слайд 10D.M. Parkin The Lancet Oncology 2: 533-543 (2004)
Гемобластозы составляют лишь
10%
Легкие
Грудь
Толстая кишка
Желудок
Пищевод
Простата
Шейка матки
Мочевой пузырь
Лимфогранулематоз
Лимфомы
Лейкозы
Ротовая полость
Поджелудочная железа
Почки
Яичники
1000 800 600 400 200 0 200 400 600 800 1000
Мужчины
Женщины
(Тысячи)
заболеваемость
смертность
337
293
1050
370
241
318
446
234
165
166
471
233
133
111
76
33
121
68
113
86
47
97
101
101
34
71
192
114
810
902
558
405
255
499
398
384
204
543
279
260
227
99
93
167
144
109
81
170
116
112
57
119
5.3 миллиона случаев (заболеваемость)
3.5 миллиона
смертей4.7 миллиона случаев (заболеваемость)
2.7 миллиона смертей
~ 10%
Слайд 11Эпидемиология
Острый лейкоз - довольно редкое заболевание и составляет лишь 3%
злокачественных опухолей человека. Однако среди гемобластозов острые лейкозы занимают одно
из первых мест по частоте встречаемости.Заболеваемость острыми лейкозами составляет в среднем 5 случаев на 100 000 населения в год.
75% всех случаев диагностируется у взрослых, и среднее соотношение миелоидных лейкозов (ОМЛ) и лимфоидных составляет (ОЛЛ) 6:1.
В детском возрасте 80-90% всех ОЛ составляют лимфобластные варианты, а после 40 лет наблюдается обратное соотношение - у 80% больных ОЛ выявляется миелоидный вариант заболевания.
ОМЛ - это болезнь пожилых людей, и медиана возраста при этом заболевании составляет 60-65 лет. При ОЛЛ медиана возраста составляет 10 лет
Слайд 12Подсчитано, что в США в 2013 году
установлен диагноз
ОМЛ у 14,590 больных (7,820 мужчин и 6,770 женщин), и
10,370
больных погибли от этого заболевания (заболеваемость ~ 3-4 на 100 тыс)
Что же в России?
http://seer.cancer.gov/statfacts/html/amyl.html
Слайд 13По данным Российского Ракового Регистра
в 2009 году диагноз острого миелоидного
лейкоза («острый миелолейкоз» по МКБ-10) установлен у 1 533 больных
т.о.,
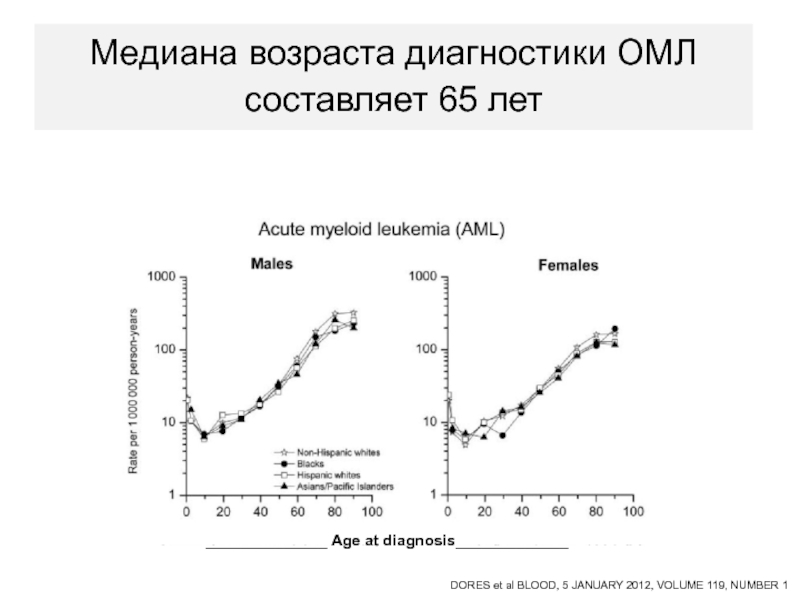
расчетный показатель заболеваемости в РФ составляет 0,84 случая на 100 тыс населения !!!???Слайд 14Медиана возраста диагностики ОМЛ составляет 65 лет
DORES et al
BLOOD, 5 JANUARY 2012, VOLUME 119, NUMBER 1
______________ Age at
diagnosis_____________Слайд 15По расчетам в США в 2013
- у 6,070 человек
(3,350 мужчин и 2,720 женщин) установлен диагноз ОЛЛ, и
-
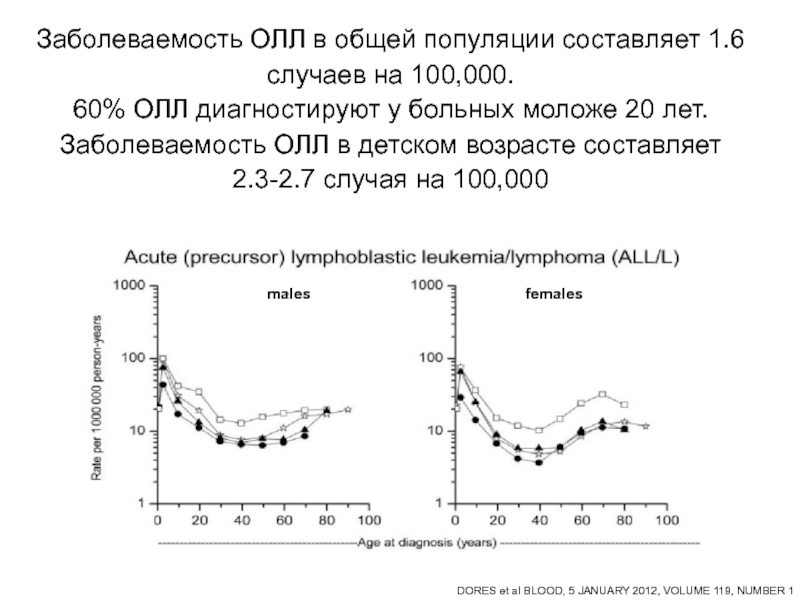
1,430 человек погибли от ОЛЛСлайд 16DORES et al BLOOD, 5 JANUARY 2012, VOLUME 119, NUMBER
1
Заболеваемость ОЛЛ в общей популяции составляет 1.6 случаев на 100,000.
60% ОЛЛ диагностируют у больных моложе 20 лет.
Заболеваемость ОЛЛ в детском возрасте составляет 2.3-2.7 случая на 100,000males
females
Слайд 18Течение заболевания
До появления современных цитостатических препаратов и программ лечения ОЛ
был быстро прогрессирующим и фатальным во всех случаях заболеванием со
средней продолжительностью жизни пациентов 2,5-3 месяца.У большинства больных причиной смерти являлись тяжелые инфекционные осложнения из-за агранулоцитоза и геморрагического синдрома вследствие тромбоцитопении, причиной которых являются вытеснение нормального кроветворения опухолевым
Слайд 19Этиология
В большинстве случаев конкретная причина возникновения острого лейкоза остается неизвестной.
При ряде врожденных заболеваний за счет повышенной хромосомной нестабильности определяется
высокая вероятность развития острого лейкоза: синдром Дауна = вероятность возникновения острого лейкоза в 20 раз выше, чем в здоровой популяции , т.е. изменения, связанные с 21-й парой хромосом, могут приводить к развитию лейкоза.
врожденный агранулоцитоз, синдром Эллиса-ван Кревелда, синдром Блюма, целиакия, анемия Фанкони, синдром Вискотта-Олдридча, Клайнфельтера, нейрофиброматоз Реклингаузена и т.д
Слайд 20Этиология
Роль вирусов в развитии лейкозов доказана в отношении некоторых видов
животных (коровы, приматы и т.д.).
Прямое доказательство вирусного происхождения ОЛ
у взрослых получено лишь для Т-клеточного лейкоза/лимфомы взрослых. Это заболевание встречается у населения Японии и жителей Карибского бассейна. Причиной развития болезни является вирус HTLV-I, причем от момента инфицирования до манифестации болезни происходит иногда несколько лет.Слайд 21Этиология
Четко доказана взаимосвязь между ионизирующей радиацией при взрыве атомной бомбы,
а также химио- и радиотерапией по поводу других опухолей с
повышенным риском возникновения острых лейкозов.Слайд 23Этиология
Впервые взаимосвязь между предшествующей химиотерапией, лучевым лечением каких-либо других опухолевых
заболеваний и увеличенным риском развития ОЛ была отмечена у пациентов,
излеченных от лимфогранулематоза. При использовании облучения в сочетании с программами, включавшими применение мустаргена, риск заболеть острым лейкозом составлет 10%. Кроме мустаргена, мутагенным эффектом обладают прокарбазин, хлорбутин, циклофосфан, ломустин, тенипозид, этопозид.Риск заболеть ОЛ был выше у рентгенологов, пациентов, которым проводили облучение по поводу «пяточных шпор», радикулита и т.д.
Слайд 24Этиология
При еженедельном использовании эпиподофиллотоксинов - этопозида или тенипозида - в
программах поддерживающего лечения детских ОЛЛ риск развития вторичного ОМЛ возрос
до 13 %. В отношении этих препаратов доказано, что не столько кумулятивная доза, сколько интенсивность дозового воздействия обусловливает повышение частоты заболеваемости ОМЛРиск развития вторичного ОМЛ наиболее высок в период от 2 до 9 лет после завершения предшествующей химиотерапии. В 85% случаев вторичные лейкозы возникают в сроки до 10 лет от окончания лечения
Слайд 25Этиология
Доказано, что между курением и риском развития острого лейкоза существует
дозовая зависимость, которая особенно очевидна для лиц старше 60 лет.
Ряд исследователей предполагает, что около 20% ОМЛ являются следствием куренияСлайд 26Этиология
Бензол при длительном воздействие на организм человека дает лейкемогенный эффект,
но при небольших концентрациях этого вещества, с которыми чаще всего
сталкиваются люди на производстве, не доказана взаимосвязь с повышенным риском возникновения ОЛ.Слайд 27Развитие ОЛ -
следствие повреждения - мутации - в генетическом материале
клоногенной кроветворной клетки. В результате этого происходит нарушение контроля за
клеточным циклом, изменение процесса транскрипции и продукции ряда ключевых белков.Вследствие бесконтрольной пролиферации в отсутствие дифференцировки происходит накопление патологических клеток.
Тот факт, что патогенез острых лейкозов связан с генетическими поломками, подтверждается обнаружением различных хромосомных аберраций (транслокаций, делеций, инверсий и т.д.) практически у всех больных ОЛ
Слайд 28Развитие ОЛ -
следствие повреждения - мутации - в генетическом материале
клоногенной кроветворной клетки. В результате этого происходит нарушение контроля за
клеточным циклом, изменение процесса транскрипции и продукции ряда ключевых белков.Вследствие бесконтрольной пролиферации в отсутствие дифференцировки происходит накопление патологических клеток.
Тот факт, что патогенез острых лейкозов связан с генетическими поломками, подтверждается обнаружением различных хромосомных аберраций (транслокаций, делеций, инверсий и т.д.) практически у всех больных ОЛ
Эпигенетические воздействия
Слайд 29Диагностика
Диагностика острых лейкозов базируется на оценке морфологических особенностей клеток костного
мозга и периферической крови.
Диагноз устанавливают лишь при обнаружении 20%
и более бластных клеток, характеризующихся нежносетчатой структурой ядерного хроматина, в костном мозге или периферической крови. Для точного определения варианта ОЛ необходимы иммунофенотипирование, цитохимическое, цитогенетическое, молекулярно-биологическое исследования.
Слайд 30Иммунофенотипирование бластных клеток
Не является принципиальным методом для ОМЛ, лишь подтверждает
диагноз ОЛ и позволяет определить аберрантный иммунофенотип для мониторинга МРБ
Лишь
в случае М0 и М7 использование иммунофенотипирования позволяет достоверно установить диагнозБез ИФТ невозможно установить диагноз ОЛ с разнонаправленной дифференцировкой
Ключевой метод диагностики острых лимфобластных лейкозов
Слайд 31Ключевые маркеры, определяющие принадлежность бластных клеток к той или иной
линии дифференцировки
Слайд 32Классификация ОЛ
Наиболее распространенной морфологической классификацией острых лейкозов была предложенная франко-американо-британской
группой в 1976 году FAB- классификация, пересмотренная и дополненная в
1991 году.В 2001 году международной группой экспертов была создана новая классификация гематологических опухолей – классификация ВОЗ. ФАБ-классификация стала ее составной частью.
В 2008 году ВОЗ-классификация была дополнена и издана под редакцией С.Свердлова
Слайд 34Классификация ОЛ
Острые миелоидные лейкозы и опухоли из миелоидных предшественников
Острые лейкозы
с «разнонаправленной» дифференцировкой
Опухоли из лимфоидных предшественников
Слайд 35ОМЛ и опухоли из миелоидных предшественников
ОМЛ подразделяется на :
1)
ОМЛ, ассоциированный со стабильно выявляемыми генетическими аномалиями;
2) ОМЛ с
изменениями, характерными для миелодисплазии; 3) миелоидные опухоли, ассоциированные с предшествующей химио- и/или радиотерапией;
4) ОМЛ неспецифицируемый (собственно ФАБ-классификация).
Опухоли из миелоидных предшественников
Слайд 36ОМЛ, ассоциированный со стабильно выявляемыми генетическими аномалиями
ОМЛ с t(8;21)(q22;q22) и
химерным транскриптом RUNX1-RUNX1T1 (AML1/ETO);
ОМЛ с инверсией 16(p13;q22) или t(16;16)(p13;1q22);
CBFbeta/MYH1Острые промиелоцитарные лейкозы с t(15;17)(q22;q12); PML/RARa
ОМЛ с t(9;11)(p22; q23); MLLT3-MLL
ОМЛ с t(6; 9)(p23;q34); DEK-NUP214
ОМЛ с inv3 (q21;q26.1) или с t(3; 3)(p23;q34) RPN-EVI1
ОМЛ с t(1; 12)(p13;q13); RBM15-MKL-1
ОМЛ с нормальным кариотипом и мутированным NPM1 - геном
ОМЛ с нормальным кариотипом и мутированным CEBPA- геном
Слайд 37ОМЛ с изменениями, характерными для миелодисплазии
ОМЛ, которые морфологически характеризуются мультилинейной
дисплазией костного мозга
которые развились либо на фоне предшествующего миелодиспластического синдрома,
либо миелопролиферативного заболевания при которых выявляются МДС-ассоциированные цитогенетические аномалии (-7/7q-, -5/5q-; 11q-; 9q-; t(17p);-13/13q-; -12p/t(12p); t(11;16); t(3;21);t(3;5) и др.)
NB. В анамнезе не должно быть радио-химиотерапии. Не определяются стабильно
выявляемые хромосомные аберрации
Слайд 38Миелоидные опухоли, ассоциированные с предшествующей химиотерапии
ОМЛ или МДС или МДС
или МПЗ, развившиеся как позднее осложнение цитостатической терапии и/или лучевого
воздействия (tAML, tMDS, tMDS/MPN)Слайд 39ОМЛ неспецифицируемый
(ФАБ-классификация)
М0 - острый миелобластный лейкоз минимально дифференцированный,
М1
- миелобластный без созревания,
М2 – миелобластный с созреванием,
М3
– промиелоцитарный (в первой категории)М4- миеломонобластный,
М5 – монобластный и моноцитарный,
М6 – эритробластный,
М7 – мегакариобластный,
острый базофильный лейкоз,
острый панмиелоз с миелофиброзом
Слайд 40Опухоли из миелоидных предшественников
Миелоидная саркома
Пролиферации миелоидных предшественников, ассоциированная
с синдромом Дауна
транзиторный аномальный миелопоэз
ОМЛ
Бластные плазмоцитоидные дендритноклеточные
опухолиСлайд 41Бифенотипические лейкозы
Диагноз бифенотипического острого лейкоза устанавливается в тех ситуациях, когда
цитохимически и морфологически не представляется возможным определить принадлежность клеток к
той или иной линии кроветворения, а при иммунофенотипировании на мембране этих клеток экспрессируются линейно-специфические маркеры как лимфоидные, так и миелоидные.Реже наблюдаются случаи, когда сосуществуют две популяции бластных клеток, иммунофенотипически принадлежащих к различным линиям кроветворения. Этот вариант острого лейкоза называют билинейным.
Слайд 42Острые лейкозы
с «разнонаправленной» дифференцировкой
Острый недифференцируемый лейкоз
ОЛ смешанного фенотипа с
t(9;22)(q34;q11.2); BCR-ABL1 ОЛ смешанного фенотипа с t(v;11q23); реарранжировка гена MLL ОЛ смешанного
фенотипа, B-лф/миелоидный ОЛ смешанного фенотипа, T-лф/миелоидный ОЛ смешанного фенотипа, редкие фенотипы Другие острые лейкозы разнонаправленной дифференцировки Лимфобластный лейкоз/лимфома из натуральных киллеровСлайд 43Острые лимфобластные лейкозы
в новой ВОЗ-классификации рассматриваются в разделе опухолей из
предшественников Т- и В-лимфоцитов
1) лимфобластный лейкоз/лимфома из В-предшественников (острый лимфобластный
лейкоз из предшественников В-клеток – синоним); 2) лимфобластный лейкоз/лимфома из Т-предшественников (острый лимфобластный лейкоз из предшественников Т-клеток – синоним).
Возможно равноценное использование описанных определений, и авторы классификации лишь полагают, что при проценте бластных клеток в костном мозге 25 и более целесообразно говорить об остром лейкозе, а менее 25% - о лимфобластной лимфоме. Но чаще всего эти терминологические сложности умозрительны, поскольку терапия одинакова.
Слайд 44Опухоли из лимфоидных предшественников
B- лимфобластный лейкоз/лимфома
B-лимфобластный лейкоз/лимфома , NOS
B-лимфобластный лейкоз/лимфома с повторяющимися хромосомными аномалиями
B -лимфобластный лейкоз/лимфома с
t(9:22) (q34;q11.2); BCR/ABL B -лимфобластный лейкоз/лимфома с t(v;11q23); MLL rearranged
B -лимфобластный лейкоз/лимфома с t(12;21) (p13;q22); TEL/AML1(ETV6-RUNX1)
B -лимфобластный лейкоз/лимфома с гипердиплоидией
B -лимфобластный лейкоз/лимфома с гиподиплоидией (гиподиплоидный ОЛЛ)
B -лимфобластный лейкоз/лимфома с t(5;14)(q31;q32)(IL3-IGH)
B -лимфобластный лейкоз/лимфома с t(1;19)(q23;p13.3); E2A-PBX1;TCF3/PBX1)
T -лимфобластный лейкоз/лимфома
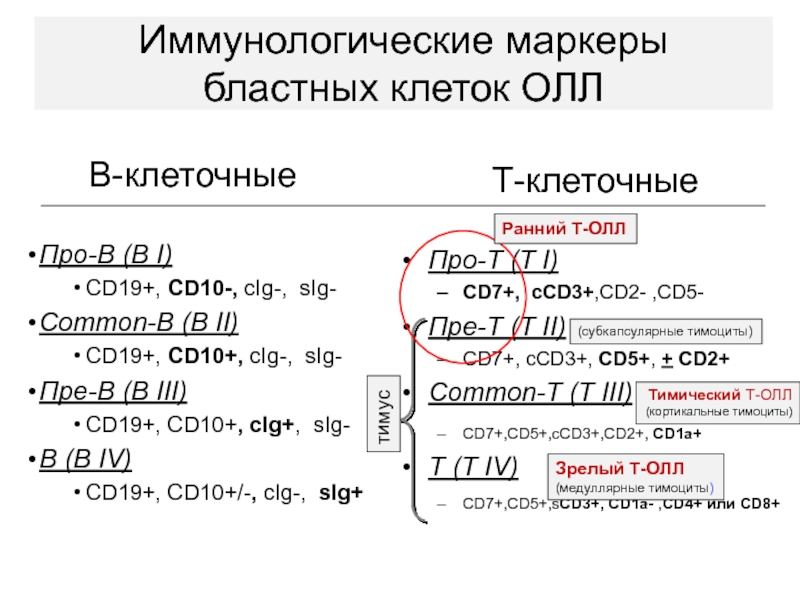
Слайд 45 В-клеточные
Про-В (B I)
CD19+, CD10-, сIg-, sIg-
Common-В
(B II)
CD19+, CD10+, сIg-, sIg-
Пре-В (B III)
CD19+, CD10+, сIg+,
sIg- В (B IV)
CD19+, CD10+/-, сIg-, sIg+
Т-клеточные
Про-Т (T I)
CD7+, cCD3+,CD2- ,CD5-
Пре-Т (T II)
CD7+, сCD3+, CD5+, + CD2+
Common-Т (T III)
CD7+,CD5+,cCD3+,CD2+, CD1a+
Т (T IV)
CD7+,CD5+,sCD3+, CD1a- ,CD4+ или CD8+
Иммунологические маркеры
бластных клеток ОЛЛ
Ранний Т-ОЛЛ
Тимический Т-ОЛЛ
(кортикальные тимоциты)
Зрелый Т-ОЛЛ
(медуллярные тимоциты)
(субкапсулярные тимоциты)
тимус
Слайд 46Иммунофенотипирование опухолевых клеток,
хромосомный анализ,
молекулярно-биологический анализ
стали ключевыми
методами и диагностики, и мониторинга результатов терапии острых лейкозов
Слайд 47При использовании этих методов было доказано, что
1) острые лейкозы клональны;
2) лейкозные клетки часто несут на своей поверхности маркеры, характеризующие
определенные этапы дифференцировки нормальных гемопоэтических клеток; 3) на нормальных клетках гемопоэза никогда не определяется аберрантная экспрессия антигенов;
4) существует группа ОЛ, клетки которых несут маркеры разных линий кроветворения (миелопоэза и лимфопоэза) или уровня дифференцировки (так называемые ранние и поздние маркеры);
5) в период морфологически доказанной ремиссии можно обнаружить клетки с характерным лейкемическим иммунофенотипом или генотипом;
6) молекулярные маркеры при некоторых формах острых лейкозов могут определяться в течение длительного времени после прекращения терапии вне связи с рецидивом заболевания.
Слайд 48Эти положения позволили внедрить в лейкозологию такие понятия как клональная
ремиссия, минимальная остаточная болезнь, цитогенетическая и молекулярная ремиссия, молекулярный и
цитогенетический рецидивСлайд 49Клинические проявления
Проявления ОЛ довольно сходны при различных формах. В основном
они связаны с замещением нормальной гемопоэтической ткани опухолевыми клетками (анемия,
тромбоцитопения, гранулоцитопения), инфильтрацией ими различных органов и продукцией различных цитокинов.Дебют ОЛ может быть острым cо значительным повышением температуры тела, резкой слабостью, интоксикацией, кровоточивостью, тяжелыми инфекциями.
Однако нередко диагноз устанавливают случайно при профилактическом осмотре или в случае госпитализации по другой причине. У пожилых больных нередко на фоне анемии появляется или усугубляется стенокардия, возникают нарушения ритма, в связи с чем их госпитализируют в кардиологическое отделение.
Слайд 50При объективном обследовании
может не наблюдаться никаких симптомов
увеличение периферических лимфатических узлов,
печени, селезенки (наиболее характерно для острых лимфобластных лейкозов, но может
быть при моно- и миеломонобластном лейкозе),гиперплазия десен (при миеломоно- и монобластных вариантах),
инфильтрация кожи (при лимфобластных, миеломоно- и монобластных вариантах),
геморрагический синдром различной степени тяжести - от петехиальных высыпаний до тяжелых кровотечений (особенно при промиелоцитарном лейкозе),
боли в костях, артралгии,
неврологическая симптоматика (менингеальные знаки - головная боль, ригидность затылочных мышц, симптом Кернига, парез лицевого, глазодвигательного и других нервов, парезы нижних конечностей и т.д.) (чаще при острых лимфобластных лейкозах).
Слайд 51Лабораторные показатели
В анализах крови могут быть неспецифические изменения: трехростковая цитопения,
или анемия, или только лейкопения или лейкоцитоз, или тромбоцитопения.
Бластные
клетки могут не определяться в анализе периферической крови и, наоборот, составлять 90-95% всех лейкоцитов. Количество лейкоцитов также варьирует от менее 0,1 до 500,0*109/л.
Примерно в 15% случаев в дебюте заболевания определяется более 100,0*109/л.
Слайд 52Дифференциальная диагностика
Проста, поскольку, если есть бластные клетки в пунктате или
в периферической крови, диагноз ОЛ очевиден.
Трудности возникают на первых
этапах - при анализе мазков периферической крови, когда бластных клеток нет, или обнаруживают так называемые «омоложенные» или «моноцитоидные» клетки . Слайд 53Дифференциальная диагностика
Увеличение числа лейкоцитов со сдвигом формулы влево при различных
инфекционных процессах может вызывать сомнения в диагнозе ОЛ, но в
таких случаях никогда не обнаруживаются типичные бластные клетки.Увеличение числа лейкоцитов при тяжелых инфекциях, сепсисе (например, менингококковом) может сопровождаться снижением числа тромбоцитов, анемией, геморрагическим синдромом, тем не менее, никогда не выявляются характерные бластные клетки.
Слайд 54Дифференциальная диагностика
Инфекционный мононуклеоз и некоторые другие вирусные инфекции (клиническая симптоматика
-повышение температуры тела, боли в горле, увеличение лимфатических узлов, печени,
селезенки - может напоминать таковую при ОЛ). НО: характерно обнаружение мононуклеаров с широкой фиолетовой цитоплазмой с перинуклеарным просветлением. Помочь в диагностике может выявление IgM-антител или увеличение выше 1000 титра IgG-антител к EBVСлайд 55Дифференциальная диагностика
РАИБ-2
Бластный криз хронического миелолейкоза (t(9;22)может обнаруживаться и при ОЛ)
Лимфома
из клеток мантийной зоны
Слайд 56Экстрамедуллярные поражения
Нейролейкемия
Ее возникновение обусловлено метастазированием лейкозных клеток в паутинную и
мягкую мозговые оболочки головного и спинного мозга.
В ряде случаев
наблюдается лейкозная инфильтрация периферических нервов с разнообразными двигательными и чувствительными нарушениями, или обнаруживается очаговое поражение вещества головного мозга. Слайд 57Нейролейкемия
характеризуется менингеальным и гипертензивным синдромом: отмечается постоянная головная боль, возможна
рвота, вялость, выявляется отек дисков зрительных нервов, может быть нистагм,
косоглазие, другие признаки поражения черепно-мозговых нервов, выявляется ригидность затылочных мышц, симптом Кернига.В цереброспинальной жидкости при этом обычно наблюдается цитоз (15/3 и более, что составляет 5 и более клеток в 1 мкл цереброспинальной жидкости), и морфологически эти клетки являются бластами (их часто описывают как моноцитоидные).
Слайд 58Нейролейкемия
Наиболее часто нейролейкемия возникает при острых лимфобластных лейкозах. Если не
осуществлять ее профилактику, она может проявиться у 30-50% больных.
При
миелоидных лейкозах нейролейкемия довольно редка в дебюте болезни, тем не менее встречается при миеломоно- и монобластных вариантах, особенно при тех формах лейкозов, когда обнаруживают поломку 16 хромосомы – inv(16) (у 30% таких больных при отсутствии профилактики возникает нейролейкемия). Слайд 59Экстрамедуллярные поражения
Лейкемиды (инфильтрация кожи)
Поражение сетчатки, десен, яичек, яичников
Описаны поражения
лимфатических узлов, легких, кишечника, сердечной мышцы, мочеточников.
При острых миелоидных
лейкозах экстармедуллярные поражения мягких тканей ранее называли “хлоромой”. В настоящее время для обозначения поражения мягких тканей и органов используют термин миелоидная или гранулоцитарная саркома Слайд 60Периоды заболевания
(на фоне терапии)
В течении острых лейкозов выделяют:
первый острый период (дебют или манифестация);
резистентное течение;
ремиссию
;рецидив.
Клиническая манифестация опухоли происходит, когда ее масса составляет 1012 клеток
Слайд 61Динамика объема опухоли в процессе лечения острых лейкозов
Рецидив
Морфологическая ремиссия
Лейкемические
клетки
Время
Минимальная
резидуальная
болезнь
Слайд 62Основополагающими принципами химиотерапии всех злокачественных опухолей человека, в том числе
острых лейкозов, являются:
1) принцип дозы-интенсивности, то есть необходимости использования адекватных
доз цитостатических препаратов в сочетании с четким соблюдением временных межкурсовых интервалов;2) принцип использования сочетаний цитостатических средств с целью получения наибольшего эффекта и уменьшения вероятности развития лекарственной резистентности;
3) принцип этапности терапии
Слайд 63Адекватность цитостатического воздействия
дозы цитостатических препаратов
способ и кратность их введения
сочетание
препаратов
временные интервалы
Специфичность воздействия
цитостатические препараты
«таргетные» препараты
Слайд 64Ключевые ожидаемые
побочные эффекты
миелосупрессия = анемия+ нейтропения (длительность и глубина) +
тромбоцитопения
повреждение эндотелия
(тромбогенность, дистресс-синдром)
коагуляционные нарушения
повреждение слизистых (объем поражения)
иммунодефицит (Т-клеточный дисбаланс,
блокада макрофагального звена, фагоцитоза, гуморальный иммунодефицит)Слайд 65Что происходит с программной химиотерапией вследствие развития осложнений:
Удлинение интервалов между
курсами
Уменьшение доз цитостатических препаратов
Прекращение протокольного лечения и переход на пациент-ориентированную
терапиюНарушение закона «дозы-интенсивности»
Слайд 66Доза -интенсивность
Как в эксперименте, так и в результате клинических исследований
было доказано, что снижение дозы препаратов на 20% в программах
химиотерапии ведет к уменьшению эффективности лечения на 50%Увеличение дозы в 2 раза при лечении опухолей с высокой фракцией роста сопровождается 10-кратным увеличением гибели опухолевых клеток (но!токсичность).
Использование сочетаний цитостатических препаратов еще более повышает процент гибели опухолевых клеток. Например, число детей, излеченных от острого лимфобластного лейкоза, увеличивалось в линейной зависимости по мере изменения числа используемых цитостатических препаратов с 3 до 7.
Слайд 67
1988-1993
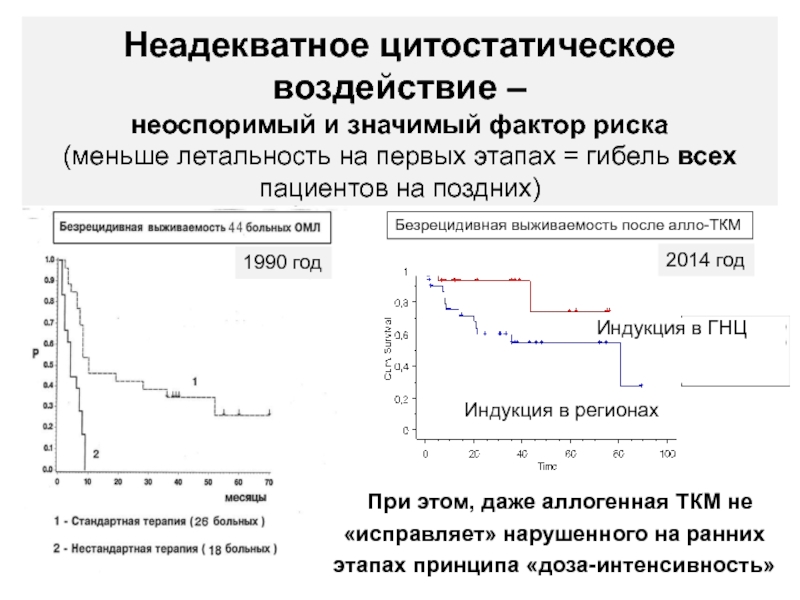
Неадекватное цитостатическое воздействие –
неоспоримый и значимый фактор риска
(меньше летальность
на первых этапах = гибель всех пациентов на поздних)
1990 год
2014
Индукция
в ГНЦ При этом, даже аллогенная ТКМ не «исправляет» нарушенного на ранних этапах принципа «доза-интенсивность»
Индукция в регионах
Безрецидивная выживаемость после алло-ТКМ
2014 год
Слайд 68Лечение острых лейкозов должно осуществляться только в специализированных гематологических отделениях!!!
Ни
в коем случае не вводить никакие цитостатические средства (преднизолон, цитарабин
и т.д.) на этапах диагностики и перевода в специализированное отделение = > неадекватная предлеченность – нациоанльный фактор рискаЭффективное лечение острых лейкозов – эталон работы отделения гематологии
Слайд 69Подготовка к химиотерапии
Следует подчеркнуть, что практически никогда нет необходимости в
день поступления пациента начинать индукционное лечение
Прежде всего, следует установить
как можно более точный диагноз (не только лимфобластный или миелоидный вариант острого лейкоза, но и их морфологические подтипы, обязательно получить материал для иммунофенотипирования, цитогенетического и молекулярного исследования)Слайд 70Подготовка к химиотерапии
Подготовить пациента к проведению индукционной терапии (купировать анемию,
инфекционные, геморрагические осложнения, электролитные нарушения, обеспечить водную нагрузку, профилактировать тумор-лизис
аллопуринолом и т.д.) .Как правило, на предварительные этапы обследования и подготовки уходит 1-3 дня. Но ни в коем случае не рекомендуется откладывать начало химиотерапии на более долгий срок.
Слайд 71Основной целью лечения ОЛ-
является эрадикация лейкемического клона, восстановление нормального
кроветворения и в результате этого - достижение длительной безрецидивной выживаемости
больныхЭто достигается за счет использования миелотоксических противоопухолевых препаратов, которые быстро уменьшают объем опухолевой массы, вызывая глубокую аплазию костного мозга. Именно в период аплазии возникает так называемое состояние клональной конкуренции, когда пролиферативное преимущество получают клетки нормального кроветворного клона, которые и восстанавливают здоровое поликлональное кроветворение.
Слайд 72Основные этапы терапии ОЛ
индукция ремиссии,
консолидация ремиссии,
поддерживающая терапия
профилактика
нейролейкемии (для некоторых вариантов ОЛ)
Слайд 73Индукция ремиссии
Это период начального лечения, целью которого является максимально быстрое
и существенное уменьшение опухолевой массы и достижение полной ремиссии, (обычно
1-2 курса).Именно в этот период на фоне применения цитостатических средств количество лейкемических клеток в костном мозге уменьшается на 95-99.9% (на 2-3 порядка), т.е. в момент констатации полной ремиссии в костном мозге морфологически определяется менее 5% опухолевых клеток.
Слайд 74Консолидация ремиссии
является вторым этапом терапии острых лейкозов, если достигнута полная
ремиссия, то есть закреплением достигнутого противоопухолевого эффекта.
В настоящее время в
большинстве случаев консолидация является наиболее агрессивным и высокодозным этапом при лечении острых лейкозов. Задачей этого периода является по возможности еще большее уменьшение числа остающихся после индукции лейкемических клеток.
Слайд 75Период поддерживающего лечения
начинается после консолидации
при разных вариантах острых лейкозах
длительность и интенсивность поддерживающей терапии различны, но принцип ее одинаков
для всех видов ОЛ - продолжение цитостатического воздействия в меньших дозах, чем в период индукции ремиссии, на возможно остающийся опухолевый клон.Слайд 76Принципиальным этапом при лечении некоторых вариантов ОЛ (лимфобластных, промиелоцитарных, миеломоно-
и монобластных) являются профилактика или при необходимости лечение нейролейкемии. Этот
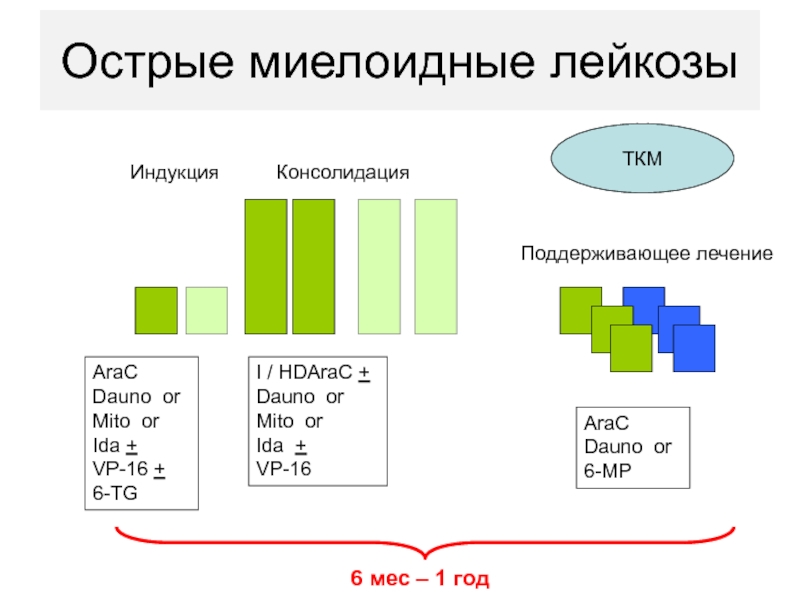
этап распределяется на все периоды программного лечения - индукцию ремиссии, консолидацию и поддерживающее лечение.Слайд 78Острые миелоидные лейкозы
I / HDAraC +
Dauno or
Mito or
Ida +
VP-16
ТКМ
Индукция
Консолидация
Поддерживающее
лечение
AraC
Dauno or
Mito or
Ida +
VP-16 +
6-TG
AraC
Dauno or
6-MP
6 мес – 1 год
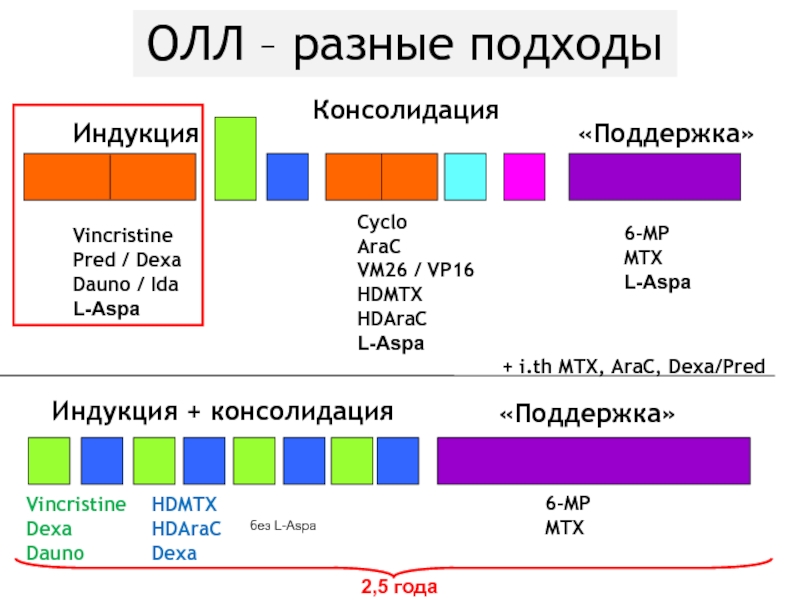
Слайд 79ОЛЛ – разные подходы
Консолидация
+ i.th MTX, AraC, Dexa/Pred
Индукция
Индукция + консолидация
Vincristine
Pred
/ Dexa
Dauno / Ida
L-Aspa
Vincristine
Dexa
Dauno
Cyclo
AraC
VM26 / VP16
HDMTX
HDAraC
L-Aspa
HDMTX
HDAraC
Dexa
«Поддержка»
«Поддержка»
6-MP
MTX
L-Aspa
6-MP
MTX
без L-Aspa
2,5 года
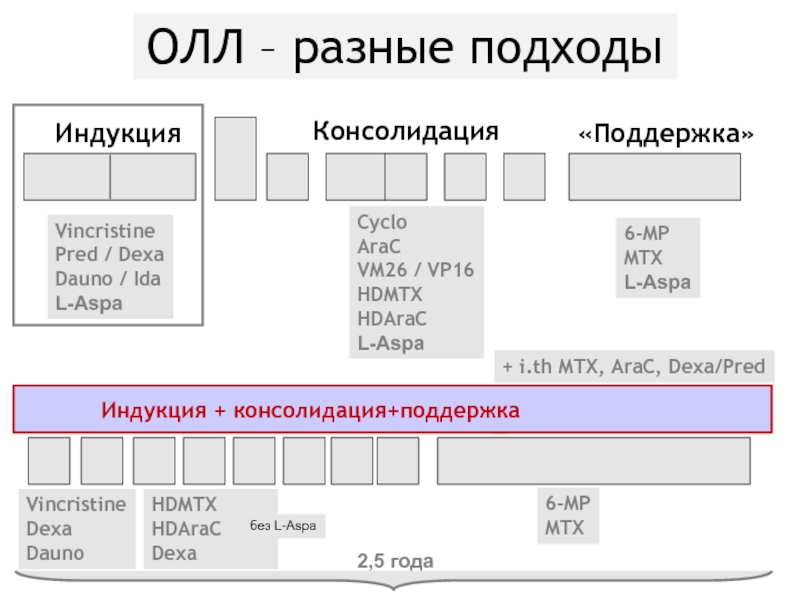
Слайд 80ОЛЛ – разные подходы
Консолидация
+ i.th MTX, AraC, Dexa/Pred
Индукция
Vincristine
Pred / Dexa
Dauno
/ Ida
L-Aspa
Vincristine
Dexa
Dauno
Cyclo
AraC
VM26 / VP16
HDMTX
HDAraC
L-Aspa
HDMTX
HDAraC
Dexa
«Поддержка»
6-MP
MTX
L-Aspa
6-MP
MTX
без L-Aspa
2,5 года
Индукция + консолидация+поддержка
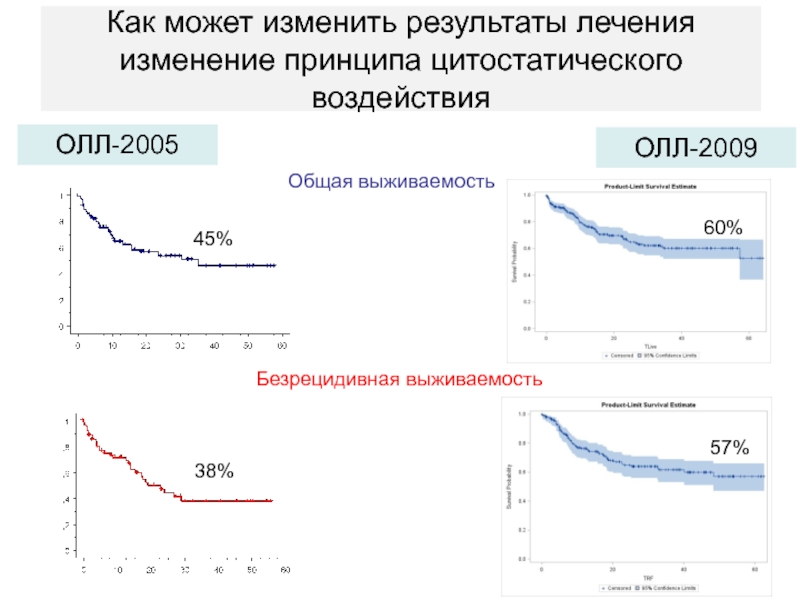
Слайд 81Как может изменить результаты лечения изменение принципа цитостатического воздействия
Общая выживаемость
Безрецидивная
выживаемость
45%
38%
ОЛЛ-2005
ОЛЛ-2009
60%
57%
Слайд 82Основные понятия
Полная ремиссия
Морфологическая
Цитогенетическая
Молекулярная
с неполным восстановлением показателей периферической крови, когда
число нейтрофилов менее 1*109/л , а тромбоцитов менее 100*109/л
Резистентность
первичная
вторичная
Рецидив гематологический
ранний цитогенетический
поздний молекулярный
Слайд 83Полная ремиссия
то состояние кроветворной ткани, при котором в пунктате костного
мозга обнаруживается 5% и менее бластных клеток при нормальном соотношении
всех ростков кроветворения, при количестве нейтрофилов в периферической крови более 1,0*109/л, при количестве тромбоцитов более или равном 100*109/л, при отсутствии экстрамедуллярных очагов лейкемического роста.Указанные показатели должны сохраняться в стабильном состоянии в течение 1 месяца и более.
Слайд 84Резистентная форма ОЛ
констатируется при отсутствии полной ремиссии после завершения индукционной
терапии (обычно это два курса химиотерапии при ОМЛ и две
фазы индукции при ОЛЛ).Слайд 85по международным критериям резистентность при ОМЛ можно оценивать лишь через
7 дней после завершения курса полихимиотерапии. Если больной погибает в
течение курса химиотерапии и в течение 7 дней после него, определить, резистентная у него форма лейкоза или нет, нельзя, и больных относят к категории неудач в лечении как неопределенный исход.Слайд 86Ранняя смерть – смерть больного в период индукционной терапии (1-2
курса индукции для ОМЛ и 1-2 фазы индукции для ОЛЛ).
Этот
критерий является обобщающим для понятия гибели больного в процессе индукционной терапии и объединяет два понятия: 1. Смерть в аплазии - смерть больного, пережившего после окончания курса 7 дней, в период миелотоксического агранулоцитоза и аплазии кроветворной ткани, доказанной пункцией костного мозга;
2. Неопределенность эффекта
1) смерть больного в течение 7 дней после завершения химиотерапии;
2) смерть больного в период проведения курса химиотерапии;
3) смерть больного, пережившего после окончания курса химиотерапии 7 дней, у которого в периферической крови не выявляются бластные клетки, но пункция костного мозга не выполнена.
Слайд 87Рецидив ОЛ
Констатируется при обнаружении в пунктате костного мозга более 5%
бластных клеток.
Рецидивом также является и внекостномозговое поражение (нейролейкемия, поражение
яичек, увеличение селезенки и т.д.) даже при отсутствии изменений крови и костного мозга. Слайд 88Успех в лечении ОЛ определяется
прецизионностью диагноза
целенаправленностью воздействия
четкостью
выполнения современных протоколов, включая ТКМ как этап лечения, в рамках
кооперативного взаимодействияадекватностью сопроводительного лечения
мониторингом МРБ
опытом команды
научными исследованиями
Слайд 89Прецизионность диагностики даже уже в рамках определенного диагноза ОЛ позволяет
определить адекватную
терапевтическую тактику
Всегда (!) –
престройки 11q23
или мутаций MLL-гена перестройки 3q26 (EVI1 ген)
моносомный кариотип
комплексный кариотип
в программу лечения необходимо включать трансплантацию аллогенного костного мозга
Слайд 90Целенаправленность воздействия
Острые промиелоцитарные лейкозы
полностью транс-ретиноевая кислота
триоксид мышьяка
Ph-позитивные острые лейкозы –
ингибиторы тирозинкиназ
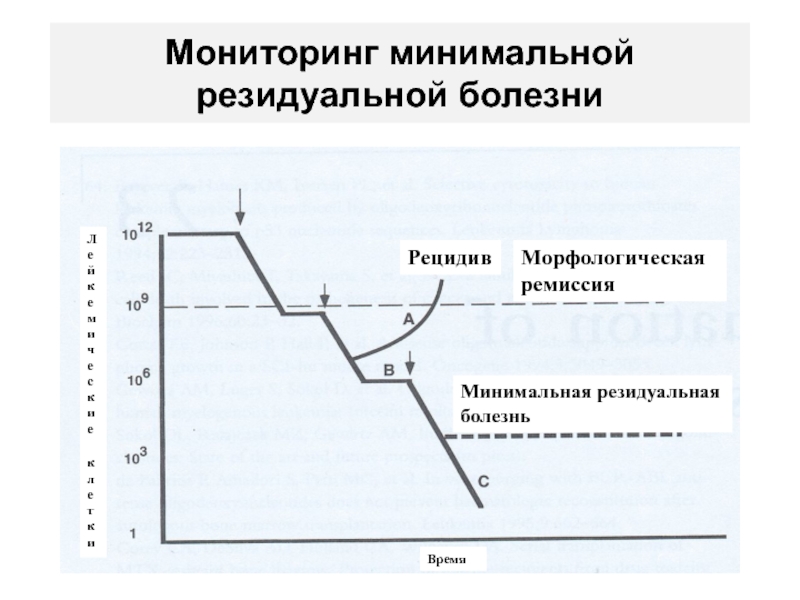
Слайд 91Мониторинг минимальной резидуальной болезни
Рецидив
Морфологическая ремиссия
Лейкемические
клетки
Время
Минимальная резидуальная
болезнь
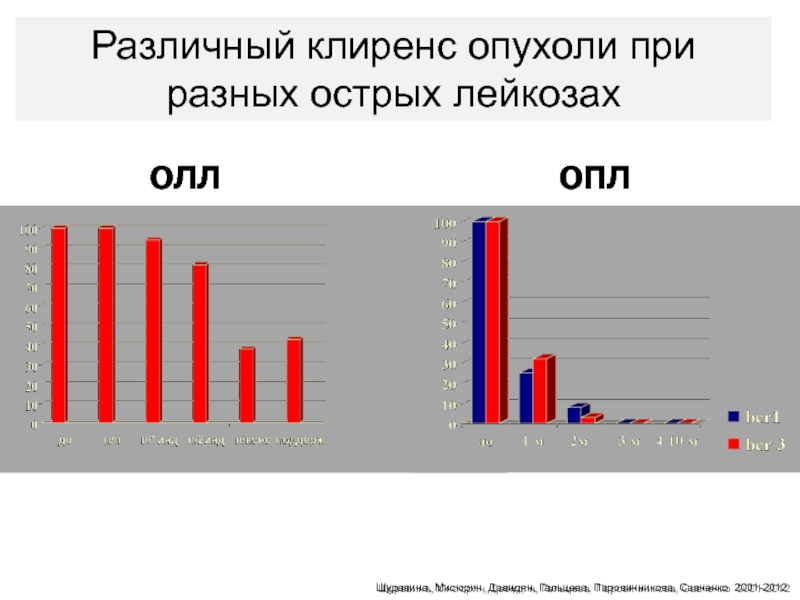
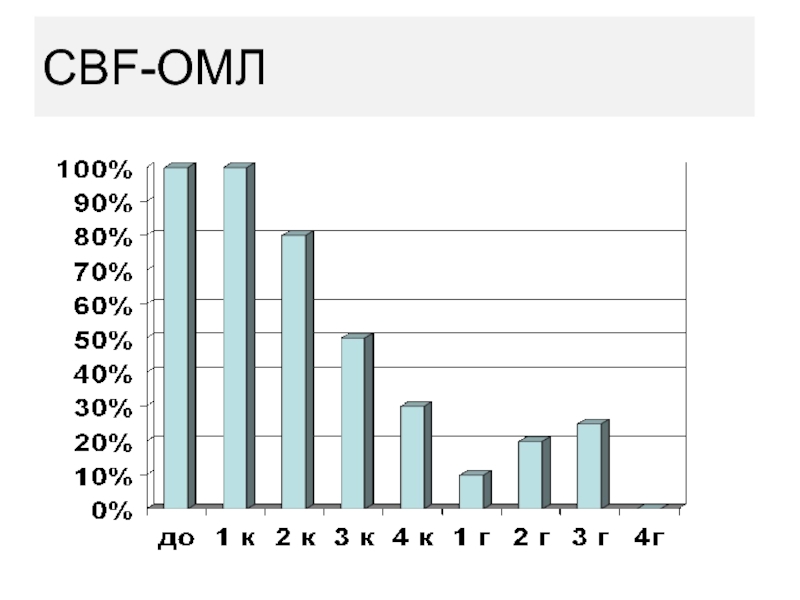
Слайд 95Различный клиренс опухоли при разных острых лейкозах
ОЛЛ
ОПЛ
IgH/TCR
Шуравина, Мисюрин, Давидян, Гальцева,
Паровичникова, Савченко 2001-2012
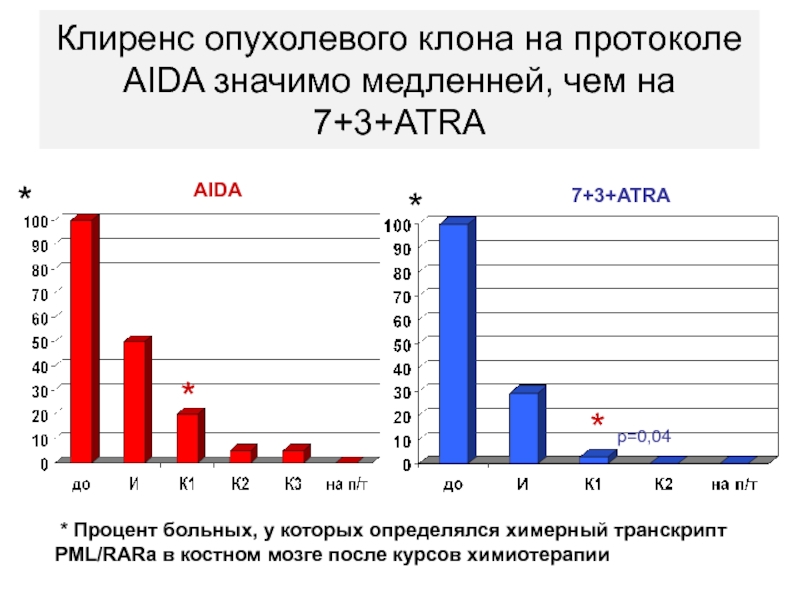
Слайд 96Клиренс опухолевого клона на протоколе AIDA значимо медленней, чем на
7+3+ATRA
* Процент больных, у которых определялся химерный транскрипт PML/RARa
в костном мозге после курсов химиотерапии*
* р=0,04
AIDA
7+3+ATRA
*
*
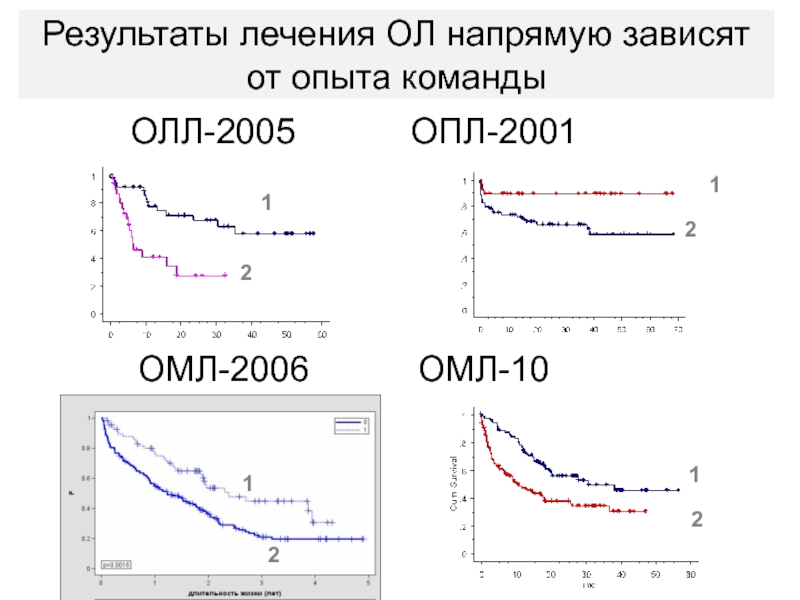
Слайд 98ОЛЛ-2005 ОПЛ-2001
ОМЛ-2006 ОМЛ-10
1
1
1
1
2
2
2
2
Результаты лечения ОЛ напрямую зависят от опыта команды
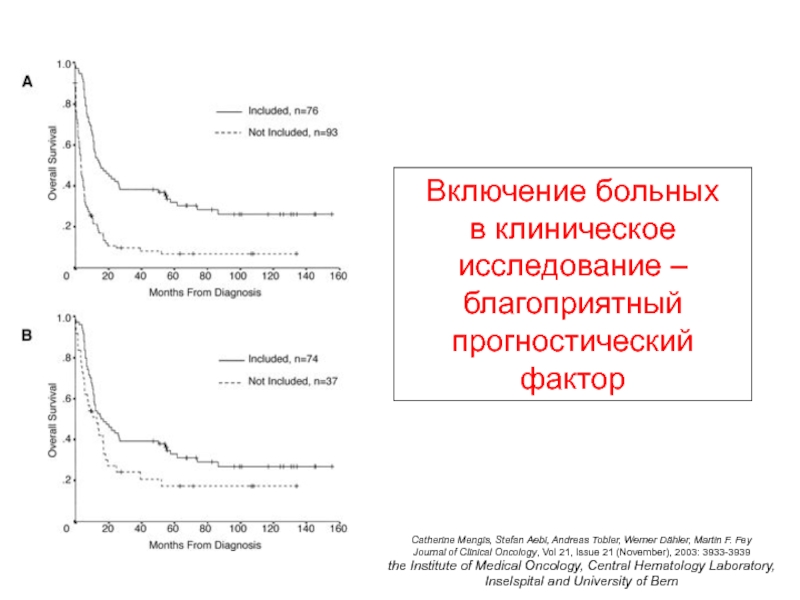
Слайд 99Catherine Mengis, Stefan Aebi, Andreas Tobler, Werner Dähler, Martin F.
Fey
Journal of Clinical Oncology, Vol 21, Issue 21 (November),
2003: 3933-3939
the Institute of Medical Oncology, Central Hematology Laboratory,Inselspital and University of Bern
Включение больных
в клиническое исследование –
благоприятный
прогностический фактор
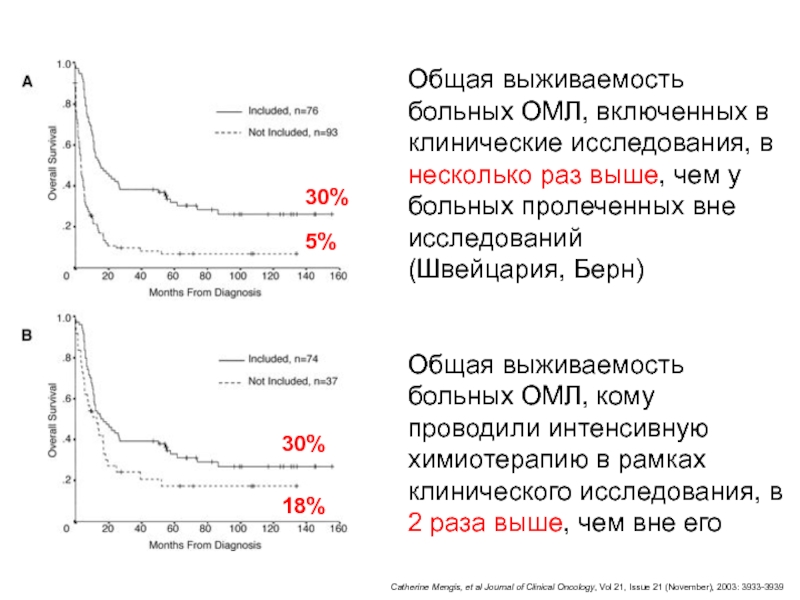
Слайд 100Catherine Mengis, et al Journal of Clinical Oncology, Vol 21,
Issue 21 (November), 2003: 3933-3939
Общая выживаемость больных ОМЛ, включенных в
клинические исследования, в несколько раз выше, чем у больных пролеченных вне исследований(Швейцария, Берн)
Общая выживаемость больных ОМЛ, кому проводили интенсивную химиотерапию в рамках клинического исследования, в 2 раза выше, чем вне его
30%
30%
5%
18%
Слайд 101Общая выживаемость больных ОМЛ, включенных в Российские многоцентровые исследования
20%
25,5%
24,3%
23%
ОМЛ-92
ОМЛ-95 ОМЛ-01
ОМЛ-06
ОМЛ-10мeд.в.=
38 лет
мeд.в.=
45 лет
35%
n=243
n=396
n=392
n=143
n=199
Савченко В.Г., Паровичникова Е.Н., Исаев В.Г., Соколов А.Н.