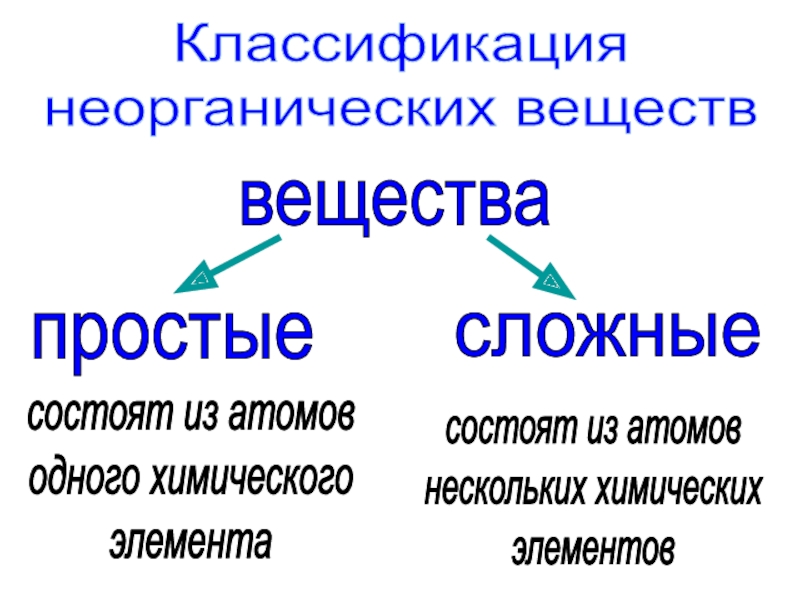
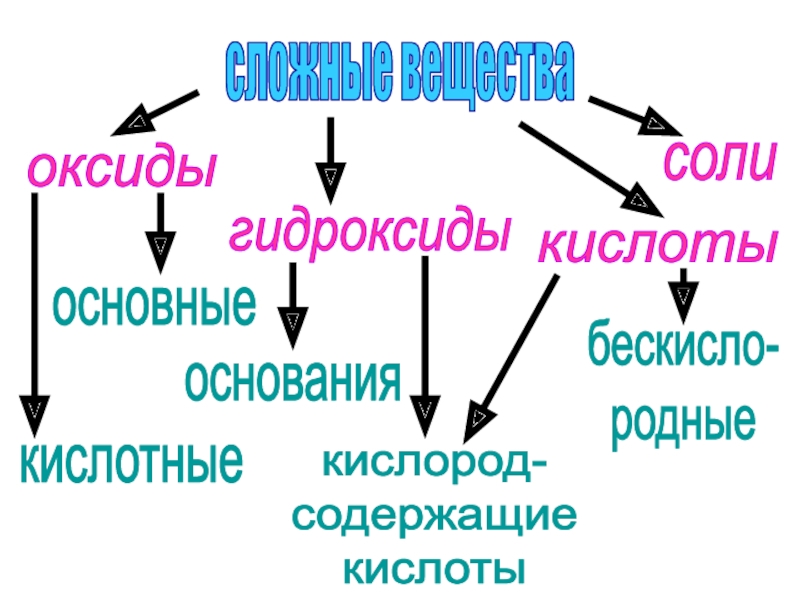
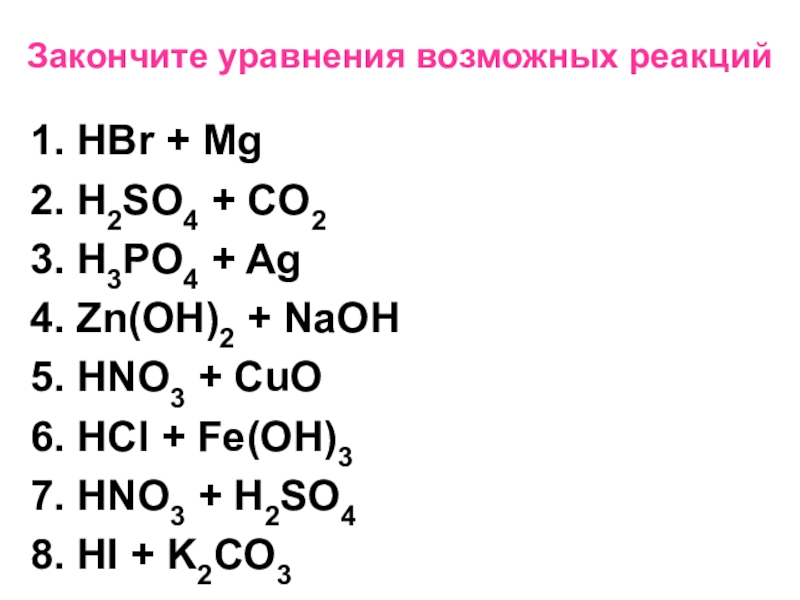
и смесей:
спиртовой раствор йода, железная руда, водород, медная
руда, чернила,
дистиллированная вода, железо, воздух, сера, медь, морская вода, сладкий чай, сахар, кислород.Чистые вещества
Смеси
Водород
Дистиллированная вода
Железо
Сера
Медь
Сахар
Кислород
Спиртовой раствор йода
Железная руда
Медная руда
Чернила
Воздух
Морская вода
Сладкий чай