Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Соотношение кинетических и термодинамических параметров реакции
Содержание
- 1. Соотношение кинетических и термодинамических параметров реакции
- 2. CООТНОШЕНИЕ КИНЕТИЧЕСКИХИ ТЕРМОДИНАМИЧЕСКИХ ПАРАМЕТРОВРЕАКЦИЙпереходноесостояниеСвязь ΔG= и ΔGреакц. ?
- 3. Соотношение Бренстедаk = βKpαlgk = lgβ +
- 4. Йоханн Николаус Бренстед Автор протонной теории кислот и оснований
- 5. Принцип Бэлла-Эванса-Поляни (БЭП)EA = A + B
- 6. Капица и Семенов
- 7. Слайд 7
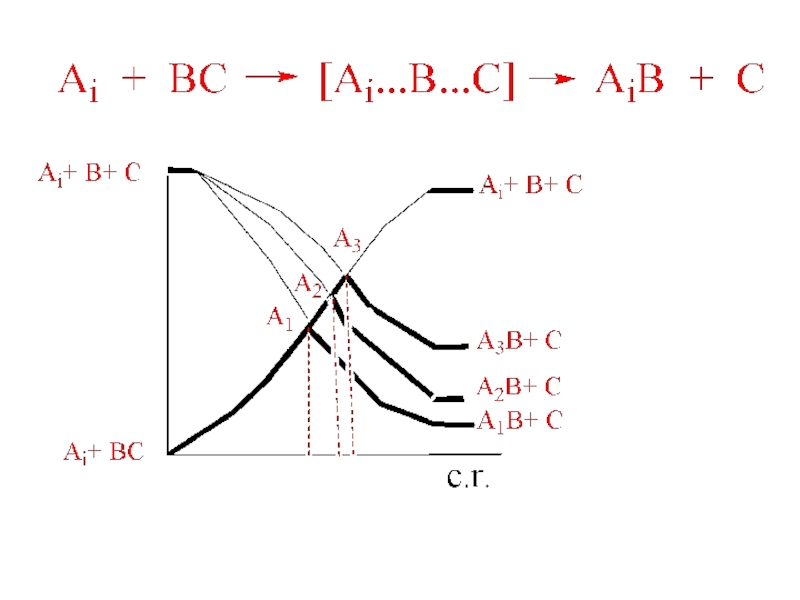
- 8. Постулат Хэммонда 1955 г.«Если два состояния
- 9. lg(kX/kH) = ρ σXРеагент Br2
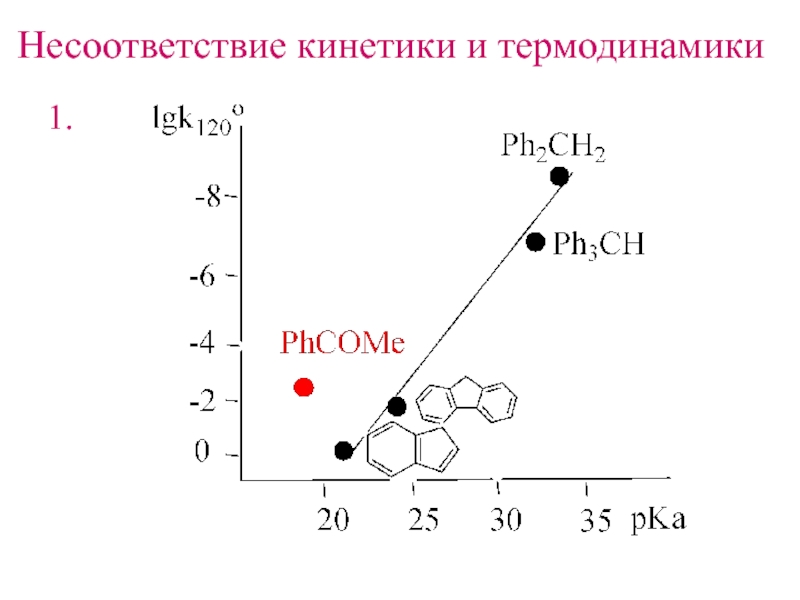
- 10. Несоответствие кинетики и термодинамики1.
- 11. Причины:
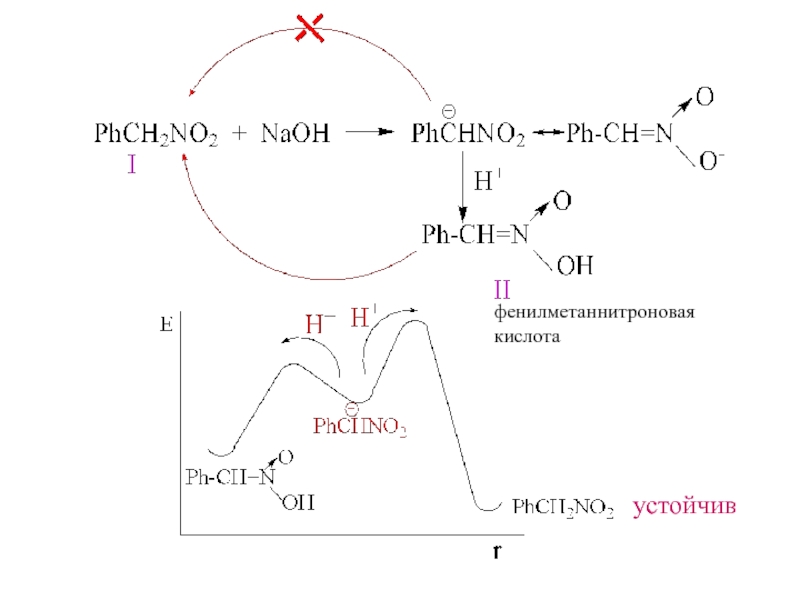
- 12. фенилметаннитроноваякислотаустойчив
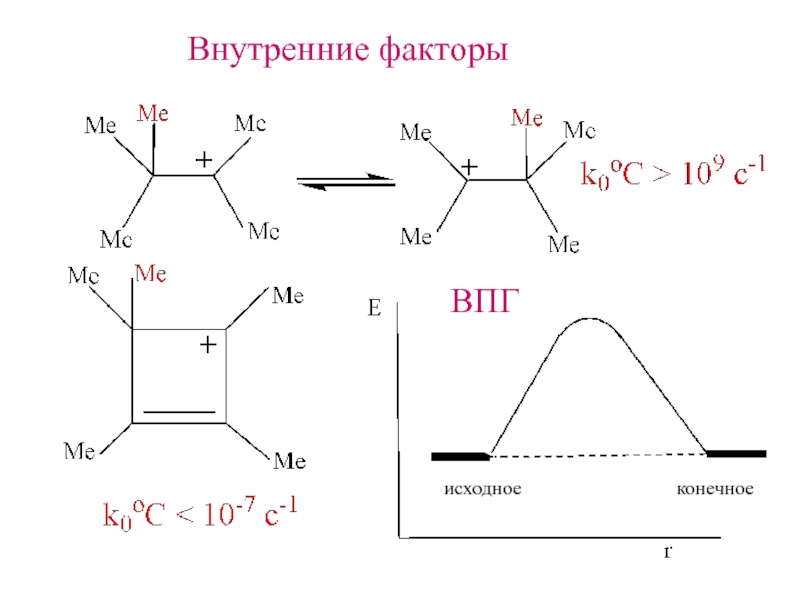
- 13. Внутренние факторыВПГисходное
- 14. Подход МаркусаΔG= = ΔGo= + ΔGp/2
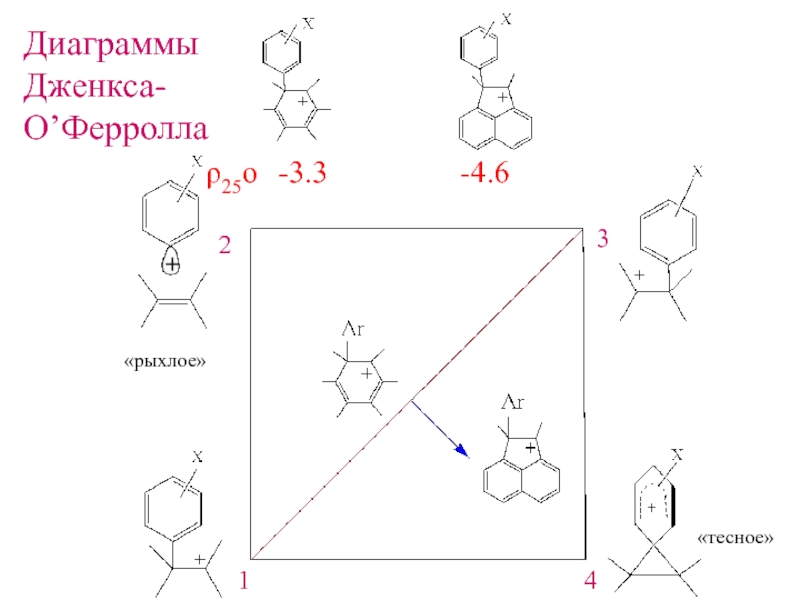
- 15. «рыхлое»«тесное»ρ25ο -3.3 -4.6ДиаграммыДженкса-О’Ферролла1234
- 16. Слайд 16
- 17. Слайд 17
- 18. Слайд 18
- 19. Скачать презентанцию
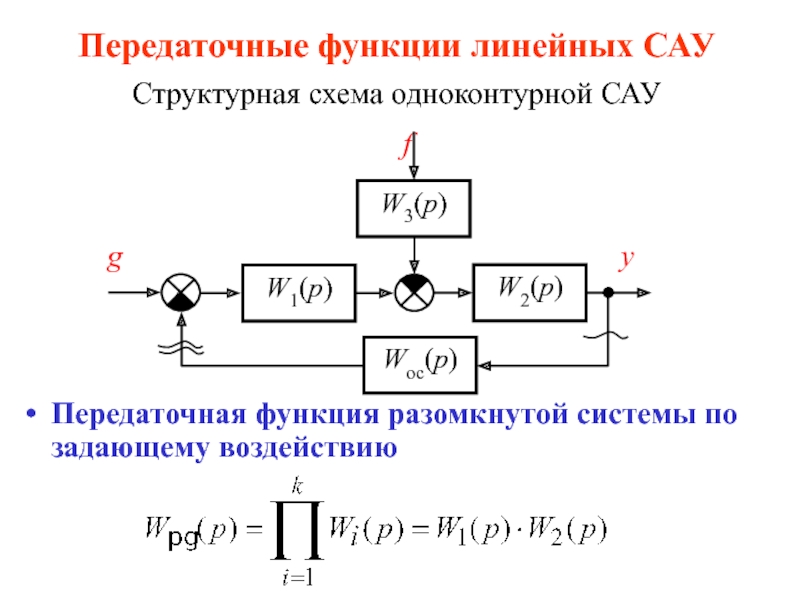
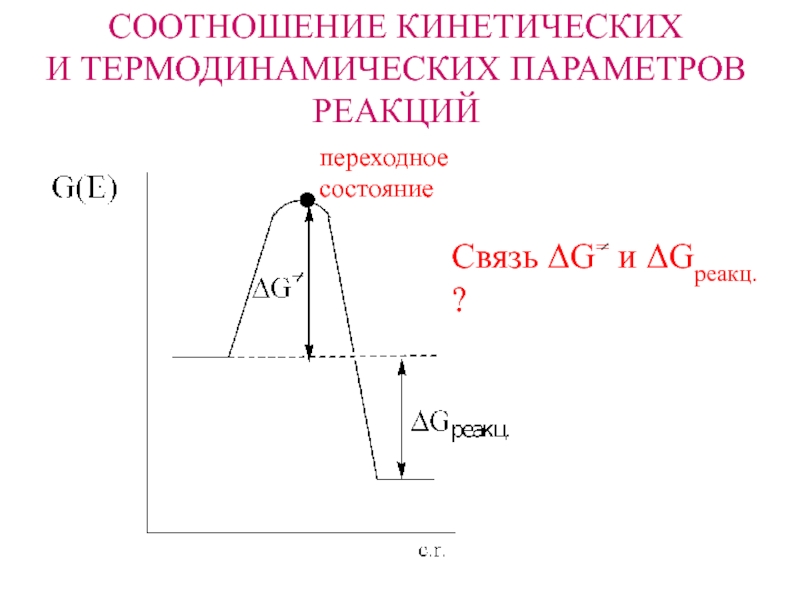
CООТНОШЕНИЕ КИНЕТИЧЕСКИХИ ТЕРМОДИНАМИЧЕСКИХ ПАРАМЕТРОВРЕАКЦИЙпереходноесостояниеСвязь ΔG= и ΔGреакц. ?
Слайды и текст этой презентации
Слайд 1Теоретические основы органической
химии
Соотношение кинетических и
термодинамических параметров реакций
Лекция 27
(электронно-лекционный курс)
Проф. Бородкин
Г.И.
Слайд 2CООТНОШЕНИЕ КИНЕТИЧЕСКИХ
И ТЕРМОДИНАМИЧЕСКИХ ПАРАМЕТРОВ
РЕАКЦИЙ
переходное
состояние
Связь ΔG= и ΔGреакц. ?
Слайд 3Соотношение Бренстеда
k = βKpα
lgk = lgβ + αlgKp
α, β −
const
k - константа скорости
K – константа равновесия
(для однотипных реакций)
Слайд 5Принцип Бэлла-Эванса-Поляни (БЭП)
EA = A + B ΔH
Н.Н. Семенов (30-годы,
свободные радикалы) :
EA = 11.5 - 1/4 ΔH экзотерм. реак.
EA
= 11.5 + 3/4 ΔH эндотерм. реак.Слайд 8Постулат Хэммонда 1955 г.
«Если два состояния (переходное и промежу-
точный
комплекс) имеют приблизительно
одинаковую энергию, то их взаимопревращение
должно включать небольшие изменения
структуры»
Расширенный постулат
экзо
эндо
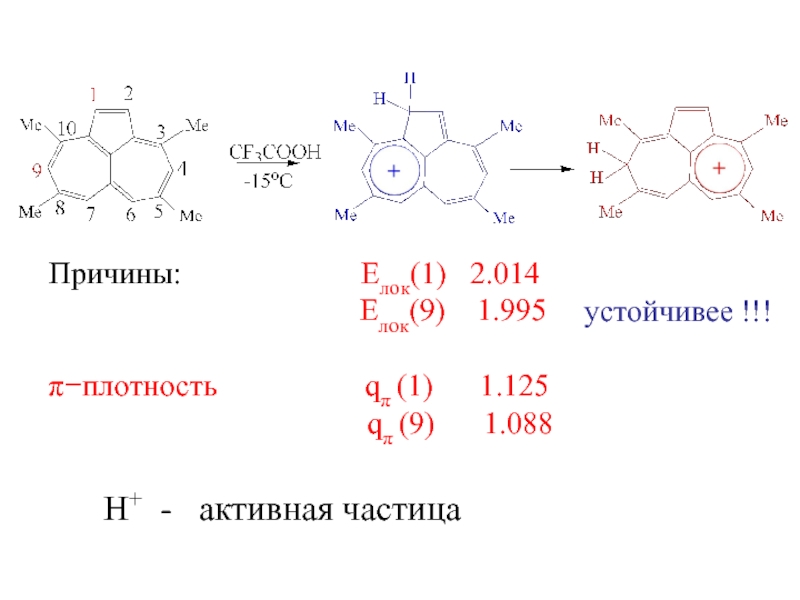
Слайд 11Причины:
Елок(1) 2.014
Елок(9) 1.995π−плотность qπ (1) 1.125
qπ (9) 1.088
H+ - активная частица
устойчивее !!!
Слайд 14Подход Маркуса
ΔG= = ΔGo= + ΔGp/2 + (ΔGp2)/ (16
ΔGo=)
[ΔG= (λ) – внутренний
барьер реакции]
ΔG=
ΔGp
−4λ
4λ
λ
3λ
экзотерм.
эндотерм.
α
β
tg α = -λ/4λ = -1/4
tg β = 3λ/4λ = 3/4
dΔG=
dΔGp
=
1
2
+
2ΔGp
16ΔGo=
= 0
Min:






![Соотношение кинетических и термодинамических параметров реакции Подход МаркусаΔG= = ΔGo= + ΔGp/2 + (ΔGp2)/ (16 ΔGo=)[ΔG= (λ) Подход МаркусаΔG= = ΔGo= + ΔGp/2 + (ΔGp2)/ (16 ΔGo=)[ΔG= (λ) – внутреннийбарьер реакции]ΔG=ΔGp−4λ4λλ3λэкзотерм.эндотерм.αβtg α =](/img/thumbs/6c200b265b76dba214a3f4d997a429f9-800x.jpg)