Слайд 1
ТЕМА 9: ОРГАНИЗАЦИЯ ВНУТРИАПТЕЧНОГО
КОНТРОЛЯ КАЧЕСТВА ЛЕКАРСТВ
Цель: сформировать у студентов знания по системе
обеспечения качества ЛС в РК и по видам
внутриаптечного контроля лекарственных
средств и оценке качества ЛС, изготовляемых в
аптеке.
Лекторы: доцент Шопабаева А.Р.
доцент НФаУ Хименко С.В.
Слайд 2 ПЛАН
Обеспечение качества ЛС как международная проблема.
Система обеспечения качества ЛС
(Система – далее) в РК.
Государственная регистрация и сертификация ЛС как
механизм государственного контроля качества препаратов.
Аптека в структуре Системы.
Слайд 3Обеспечение качества ЛС как международная проблема
Слайд 4Cубстандартный – препарат, произведенный легальным производителем с правильной маркировкой, но
который во время его производства, транспортировки, хранения утратил соответствие требованиям,
утвержденным АНД (аналитико-нормативной документацией)
Фальсифицированный или контрафактный – препарат, который преднамеренно и противоправно был оформлен этикеткой, которая неверно указывает на достоверность препарата и/или его производителя
Незарегистрированный – препарат, который не прошел официальной процедуры государственной регистрации по занесению его в Государственный реестр ЛС
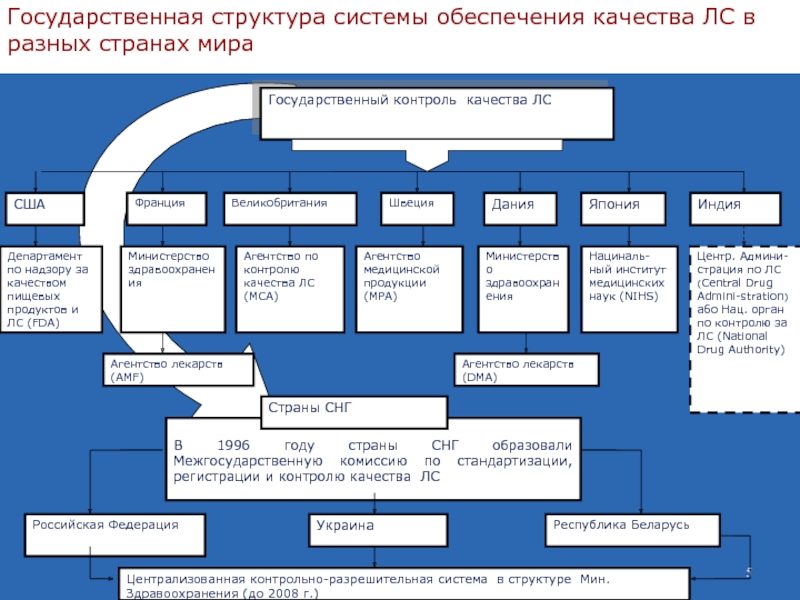
Слайд 5Государственная структура системы обеспечения качества ЛС в разных странах мира
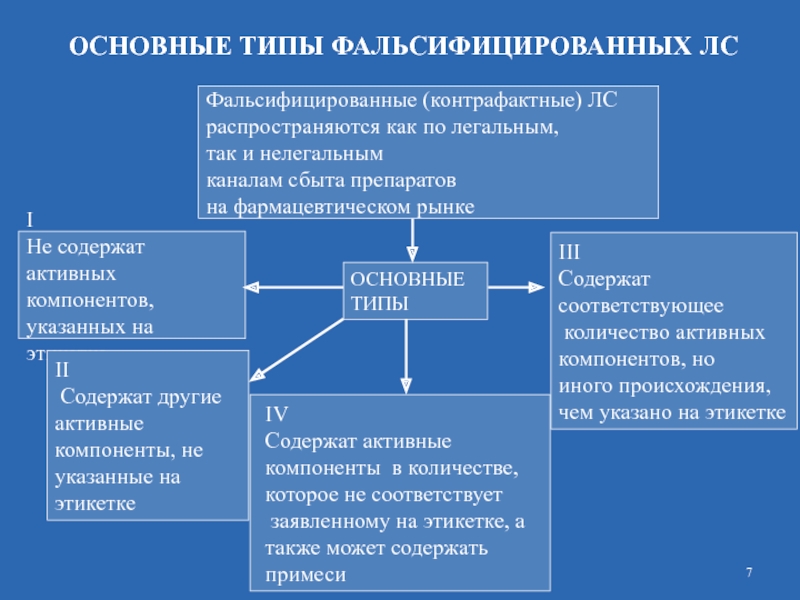
Слайд 7Фальсифицированные (контрафактные) ЛС
распространяются как по легальным,
так и нелегальным
каналам сбыта препаратов
на фармацевтическом рынке
І
Не содержат активных
компонентов,
указанных
на этикетке
ОСНОВНЫЕ
ТИПЫ
ІІІ
Содержат
соответствующее
количество активных
компонентов, но
иного происхождения,
чем указано на этикетке
ІV
Содержат активные компоненты в количестве, которое не соответствует
заявленному на этикетке, а также может содержать примеси
ІІ
Содержат другие активные
компоненты, не
указанные на этикетке
ОСНОВНЫЕ ТИПЫ ФАЛЬСИФИЦИРОВАННЫХ ЛС
Слайд 8
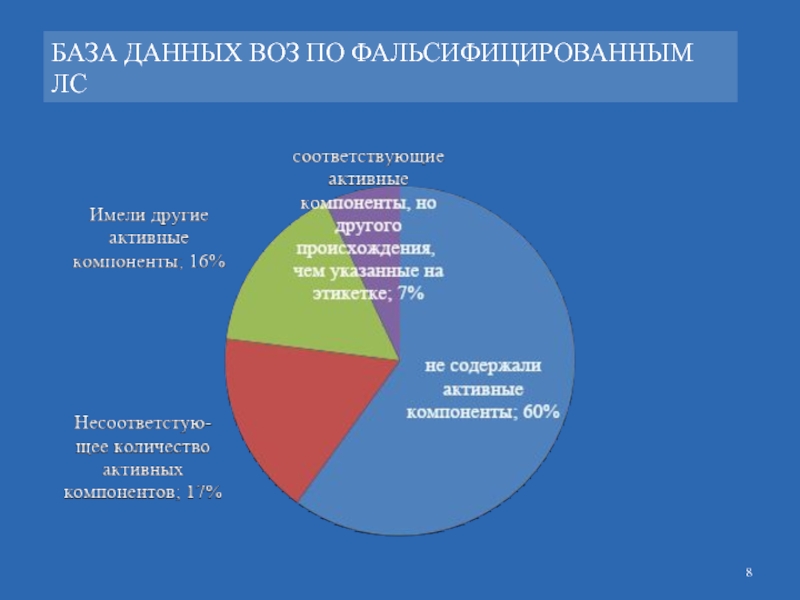
БАЗА ДАННЫХ ВОЗ ПО ФАЛЬСИФИЦИРОВАННЫМ ЛС
Слайд 9
Официально проблема фальсификации ЛС ВОЗ стала рассматриваться с 1982 года.
По указанному вопросу ВОЗ сотрудничает с:
Международной ассоциацией фармацевтических работников;
Международной системой
сотрудничества фармацевтических инспекций (PIC/S);
мировой организацией по охране интеллектуальной собственности;
Интерполом.
Слайд 10 PIC/S - это международный инструмент взаимодействия между странами и регуляторными
органами в сфере контроля качества ЛС (национальными фармацевтическими инспекторатами), обеспечивающими
совместно активное и конструктивное сотрудничество в сфере надлежащей производственной практики (GMP), инспектирования и лицензирования.
Слайд 11В 1995 году ВОЗ разработала “Программу помощи национальным системам здравоохранения
в борьбе с некачественными и фальсифицированными ЛС”.
Была создана:
Мировая база
данных ВОЗ по случаям выявления фальсифицированных ЛС
Методика выявления фальсифицированных и субстандартных ЛС
Глобальная сеть (110 стран) работников национальных систем здравоохранения, ответственных за работу по выявлению фальсифицированных и субстандартных ЛС.
Слайд 12
СИСТЕМА ОБЕСПЕЧЕНИЯ КАЧЕСТВА ЛС
В КАЗАХСТАНЕ
Слайд 13Согласно международному опыту и требованиям ВОЗ национальные Системы должны функционировать
в условиях обеспечения качества ЛС на всех этапах их жизненного
цикла:
разработка →
доклинические и клинические испытания → производство →
оптовая реализация →
отпуск конечному потребителю
Слайд 14Гарантирование качества ЛС на указанных этапах должно обеспечивать лицензирование согласно
правилам и нормам надлежащих практик (GCP→GLP→GMP→GDP→GPP),
а также стандартам ISO
серии 9000
Для поддержания качества ЛС во время их оптовой и розничной реализации в развитых странах в деятельность фирм и аптек дополнительно вводятся Надлежащая практика закупок („Good Pharmaceutical Procurement Practice” – GPPР) и Надлежащая практика хранения („Good Storage Practice” – GSP).
Слайд 15Задачи Системы – обеспечение качества субстанций, ЛС и ИМН, БАД
на этапах создания, ввоза на территорию Казахстана, производства, оптовой и
розничной реализации.
Система имеет 3 организационных уровня:
Общегосударственный;
Региональный;
Субъекты хозяйственной деятельности
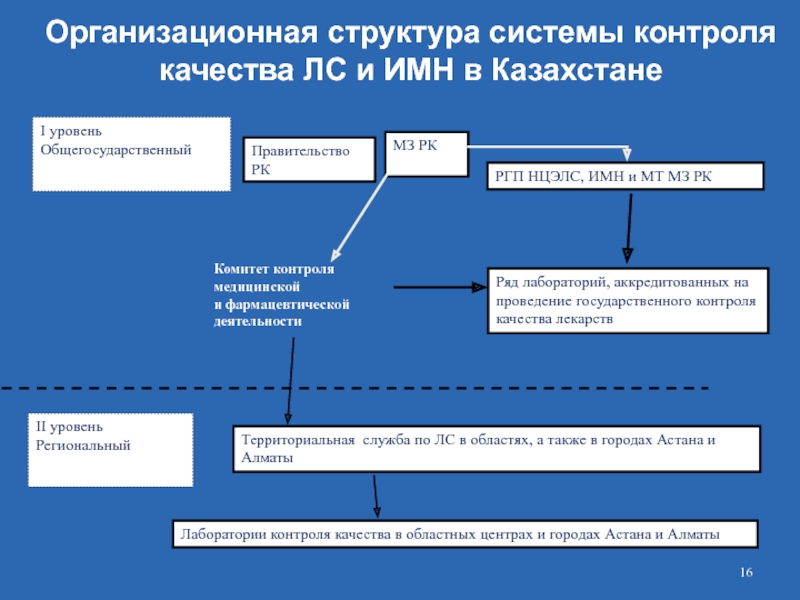
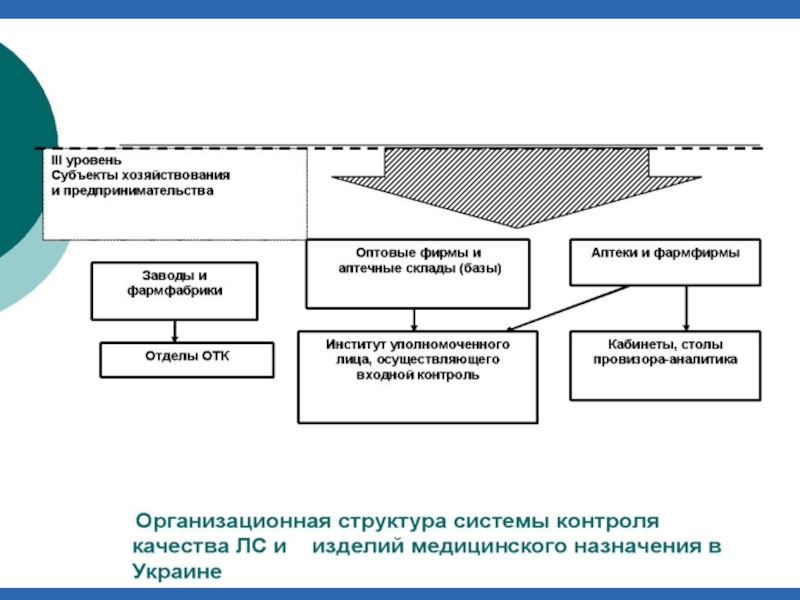
Слайд 16Организационная структура системы контроля качества ЛС и ИМН в Казахстане
I
уровень
Общегосударственный
Правительство РК
МЗ РК
РГП НЦЭЛС, ИМН и МТ МЗ РК
Ряд лабораторий,
аккредитованных на проведение государственного контроля качества лекарств
II уровень
Региональный
Территориальная служба по ЛС в областях, а также в городах Астана и Алматы
Лаборатории контроля качества в областных центрах и городах Астана и Алматы
Комитет контроля медицинской и фармацевтической деятельности
Слайд 18РГП «Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и
медицинской техники» МЗ РК является государственной экспертной организацией в сфере
обращения лекарственных средств.
Основной целью Национального центра является осуществление деятельности в области здравоохранения по обеспечению безопасности, эффективности и качества лекарственных средств.
Слайд 19
Территориальные подразделения, предприятия представлены органами по подтверждению соответствия и испытательными
лабораториями, аккредитованными в государственной системе технического регулирования РК.
Слайд 20Государственная регистрация и сертификация
ЛС как механизм государственного контроля
качества
ЛС
Слайд 22 Составными Системы сертификации ВОЗ являются:
национальная система лицензирования;
соблюдение производителями
ЛС требований надлежащей производственной практики, соответствующие требованиям GMP WHO;
регистрация ЛС;
национальная
фармацевтическая инспекция по контролю за ЛС .
Слайд 24
Аптека в структуре Системы контроля
Слайд 25Организация внутриаптечного контроля изготовленных лекарственных препаратов
Слайд 26Правила проведения внутриаптечного контроля изготовленных лекарственных препаратов (далее - Правила)
устанавливают требования к обеспечению качества лекарственных препаратов, изготовленных в аптеке,
и организации проведения внутриаптечного контроля.
Действие Правил распространяется на все аптеки, в том числе гомеопатические, независимо от их формы собственности и ведомственной принадлежности, которые изготовляют лекарственные препараты.
Постановление Правительства Республики Казахстан от 19 января 2012 года № 114 Об утверждении Правил проведения внутриаптечного контроля изготовленных лекарственных препаратов.
Слайд 27 3. Руководитель аптеки приказом назначает фармацевта (провизора-аналитика), ответственного за
организацию и проведение контроля качества изготовляемых ЛП в аптеке и
снижения риска допущения ошибок при изготовлении ЛП.
4. Руководитель аптеки обеспечивает рабочее место специалиста типовым набором средств измерений, испытательным оборудованием, лабораторной посудой, вспомогательными материалами, применяемыми при проведении аналитических работ в аптеках, в соответствии с установленным перечнем согласно приложению 1 к настоящим Правилам, а также нормативными правовыми актами РК, регламентирующими порядок изготовления и проведения контроля качества лекарственных препаратов, изготовленных в аптеке, и справочной литературой.
Постановление Правительства Республики Казахстан от 19 января 2012 года № 114 Об утверждении Правил проведения внутриаптечного контроля изготовленных лекарственных препаратов.
Слайд 28Рабочее место фармацевта-аналитика размещается в специальном помещении вблизи от асептического
блока, дефектарской и ассистентской.
Фармацевт-аналитик, впервые назначенный на эту должность, должен
пройти курс стажировки в аккредитованной испытательной лаборатории на договорной основе или в аптеке, на рабочем месте у фармацевта-аналитика, имеющего стаж работы не менее 3 лет.
Фармацевт-аналитик должен повышать квалификацию 1 раз в 5 лет на курсах повышения квалификации.
Слайд 29 5. ЛП, изготовленные в аптеке (в том числе внутриаптечная заготовка,
фасованная продукция, концентраты и полуфабрикаты), подвергаются внутриаптечному контролю.
6. Внутриаптечный
контроль выполняется проведением следующего:
1) предупредительных мероприятий;
2) приемочного контроля исходных материалов, используемых для изготовления лекарственных препаратов;
3) обязательного письменного контроля;
4) выборочного опросного контроля;
5) обязательного органолептического контроля;
6) выборочного физического контроля;
7) химического контроля;
8) контроля при отпуске.
Постановление Правительства Республики Казахстан от 19 января 2012 года № 114 Об утверждении Правил проведения внутриаптечного контроля изготовленных лекарственных препаратов.
Слайд 307. Результаты органолептического, физического и химического контроля ЛП регистрируются в
Журнале регистрации результатов органолептического, физического и химического контроля внутриаптечной заготовки,
ЛП, изготовленных по индивидуальным рецептам (требованиям медицинских организаций), концентратов, полуфабрикатов, тритураций, спирта этилового и фасовки по форме согласно приложению 2 к настоящим Правилам.
Журнал должен быть пронумерован, прошнурован, скреплен печатью территориального органа в сфере обращения ЛП, ИМН и МТ
Постановление Правительства Республики Казахстан от 19 января 2012 года № 114 Об утверждении Правил проведения внутриаптечного контроля изготовленных лекарственных препаратов.
Слайд 31 8. При проведении внутриаптечного контроля качество ЛП, в том
числе гомеопатических, изготовляемых в аптеке, устанавливается по комплексу показателей, дающих
полную характеристику ЛП.
Для оценки качества лекарственных препаратов, изготовляемых в аптеке, применяются два термина: "удовлетворяет" ("годная продукция"), "не удовлетворяет" ("бракованная").
Изготовленные лекарственные препараты в случаях признания по результатам внутриаптечного контроля как "не удовлетворительные" ("бракованные") подлежат изъятию и уничтожению.
Постановление Правительства Республики Казахстан от 19 января 2012 года № 114 Об утверждении Правил проведения внутриаптечного контроля изготовленных лекарственных препаратов.
Слайд 32 9. Аптеки с правом изготовления лекарственных препаратов ежегодно по
итогам года составляют отчет аптеки о работе по контролю качества
лекарственных препаратов (в том числе гомеопатических) по форме согласно приложению 3 к настоящим Правилам, который в срок до 10 января следующего за отчетным года направляется в территориальные органы в сфере обращения лекарственных средств, изделий медицинского назначения, медицинской техники.
Постановление Правительства Республики Казахстан от 19 января 2012 года № 114 Об утверждении Правил проведения внутриаптечного контроля изготовленных лекарственных препаратов.
Слайд 33ОРГАНИЗАЦИЯ РАБОТЫ ПО КОНТРОЛЬНО-АНАЛИТИЧЕСКОМУ ОБСЛУЖИВАНИЮ АПТЕКИ
10. Для осуществления контроля за
производственной деятельностью, выполнением аптекой предупредительных мероприятий, а также за качеством
изготовляемых ЛП аптека заключает с органом по сертификации ЛС или с одной из аккредитованных испытательных лабораторий договор о контрольно-аналитическом обслуживании и обеспечении необходимыми химическими реактивами, титрованными растворами, приготовленными испытательной лабораторией по требованию аптеки.
Оплата стоимости контрольно-аналитического обслуживания и обеспечения необходимыми химическими реактивами, титрованными растворами производится на счет аптеки в соответствии с договором.
Постановление Правительства Республики Казахстан от 19 января 2012 года № 114 Об утверждении Правил проведения внутриаптечного контроля изготовленных лекарственных препаратов.
Слайд 34Предупредительные мероприятия
14. Предупредительные мероприятия направлены на снижение риска возникновения ошибок
и на обеспечение качества изготовляемых ЛП.
Предупредительные мероприятия заключаются в
выполнении:
1) условий асептического изготовления ЛП;
2) обеспечения исправности и точности весо-измерительных приборов, проведение ежегодной их поверки;
3) получения, сбора, хранения воды очищенной, воды для инъекций и маркировки емкости в виде указания на бирке;
4) сроков, условий хранения реактивов, эталонных и титрованных растворов и правильном их оформлении ;
5) определения отклонений в проверяемых ЛП;
6) обработки, заполнения, оформления штангласов, бюреточной установки и нанесения на них необходимой информации.
Слайд 36ЛИТЕРАТУРА
Постановление Правительства Республики Казахстан от 19 января 2012 года №
114 Об утверждении Правил проведения внутриаптечного контроля изготовленных лекарственных препаратов.
Слайд 37КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Единые правила оформления лекарственных форм, изготовленных в аптеках.
2. Маркировка лекарственных
средств.
3. Виды этикеток.
4. Предупредительные надписи.
5. Контроль при отпуске лекарственных средств.
6. Отпуск лекарственных средств.