Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ТЕМА : Растворение. Растворимость веществ в воде
Содержание
- 1. ТЕМА : Растворение. Растворимость веществ в воде
- 2. Растворы играют важную роль в природе, науке
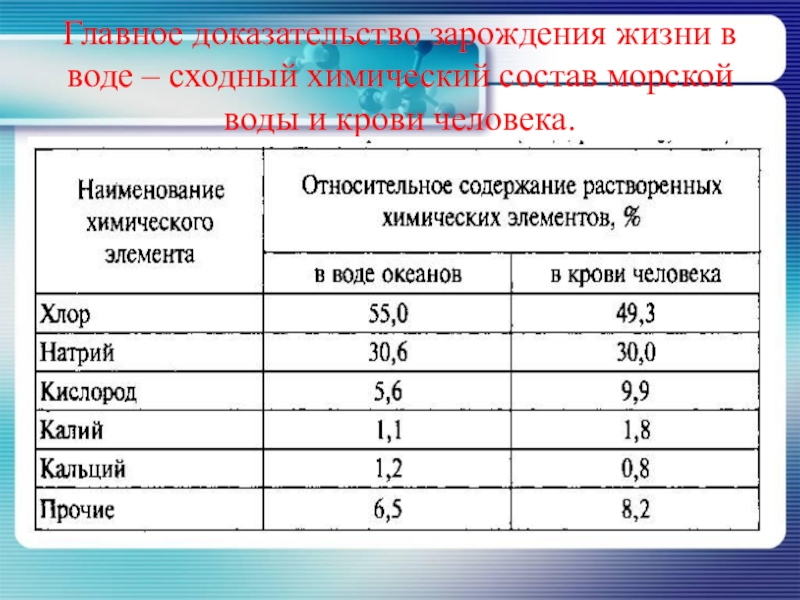
- 3. Главное доказательство зарождения жизни в воде – сходный химический состав морской воды и крови человека.
- 4. А знаете ли вы,
- 5. Какие растворы Вам известны?
- 6. РастворыВодаЛекарственные настойкиАцетонЗолотые украшения
- 7. Что же такое раствор?
- 8. Раствор – однородная система, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия.
- 9. Изучение свойств растворов занимает важное место в
- 10. Изучение свойств растворов занимает важное место в
- 11. Гидраты – соединения, образованные взаимодействием вещества с водой.Кристаллогидраты – соли, в состав которых входит вода.
- 12. Какие признаки химических реакций Вы знаете?
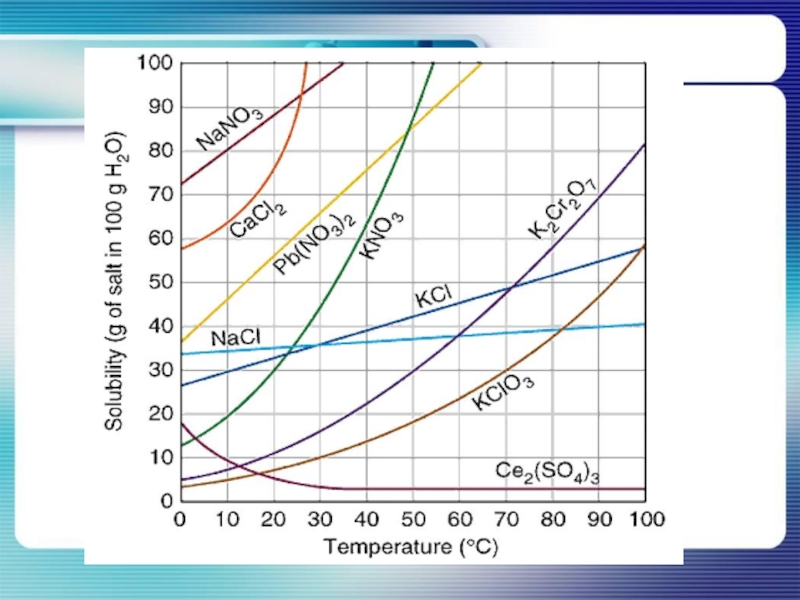
- 13. От чего зависит растворимость веществ?
- 14. Растворимость веществ зависит от:Природы веществаПрироды растворителяТемпературы
- 15. Растворы (при данной температуре)Насыщенные Ненасыщенные ПеренасыщенныеВещество больше
- 16. Слайд 16
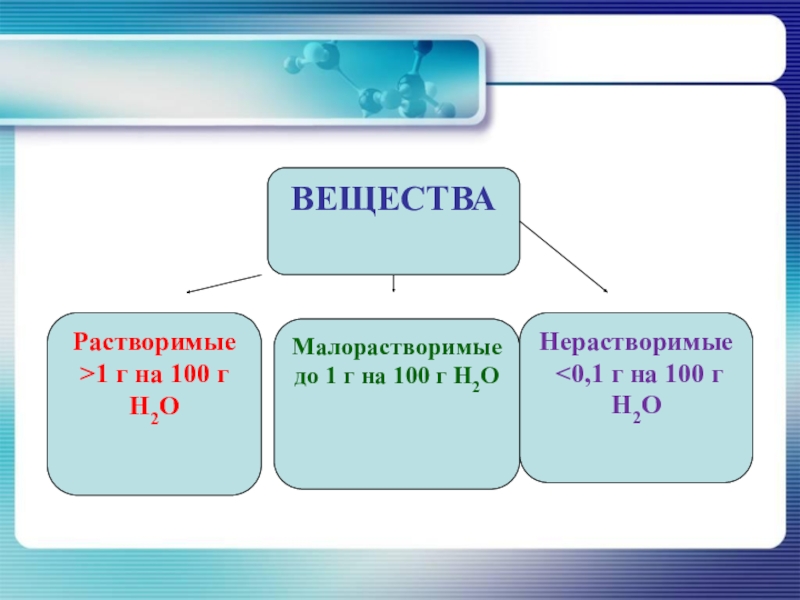
- 17. ВЕЩЕСТВАРастворимые>1 г на 100
- 18. Слайд 18
- 19. Тест на закрепление1. Растворимость веществ не зависит
- 20. ответы1. В 2. Б3. А4. Г5. А
- 21. Домашнее задание: §35, упр. 2, 3, 4 - устно
- 22. Скачать презентанцию
Растворы играют важную роль в природе, науке и технике. Особую роль на нашей планете играет вода.
Слайды и текст этой презентации
Слайд 2Растворы играют важную роль в природе, науке и технике. Особую
роль на нашей планете играет вода.
Слайд 3Главное доказательство зарождения жизни в воде – сходный химический состав
морской воды и крови человека.
Слайд 4
А знаете ли вы, что в 1м3 морской
воды растворено 0,01мг золота. Общее количество золота в морях и
океанах огромно. Если бы его удалось извлечь, то на каждого жителя нашей планеты пришлось бы более 1 тонны золота.Слайд 8 Раствор – однородная система, состоящая из частиц растворённого
вещества, растворителя и продуктов их взаимодействия.
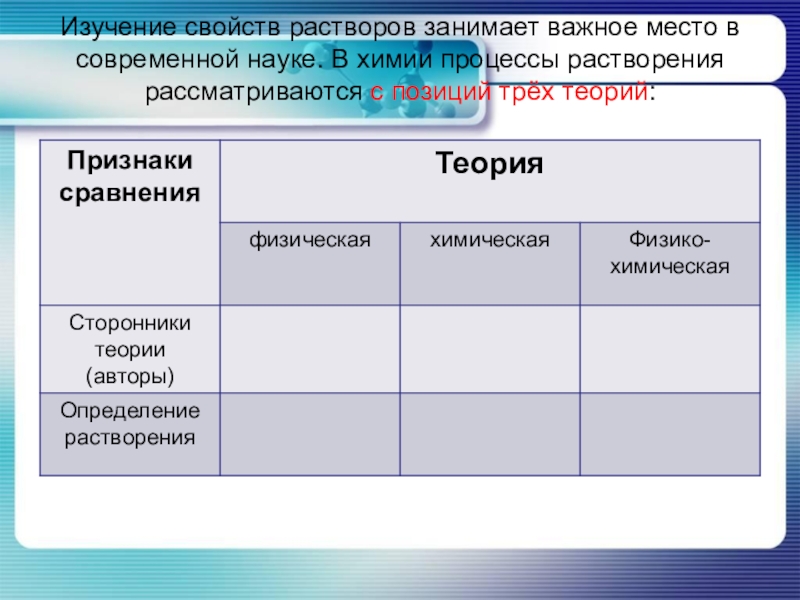
Слайд 9Изучение свойств растворов занимает важное место в современной науке. В
химии процессы растворения рассматриваются с позиций трёх теорий:
Слайд 10Изучение свойств растворов занимает важное место в современной науке. В
химии процессы растворения рассматриваются с позиций трёх теорий:
Слайд 11Гидраты – соединения, образованные взаимодействием вещества с водой.
Кристаллогидраты – соли,
в состав которых входит вода.
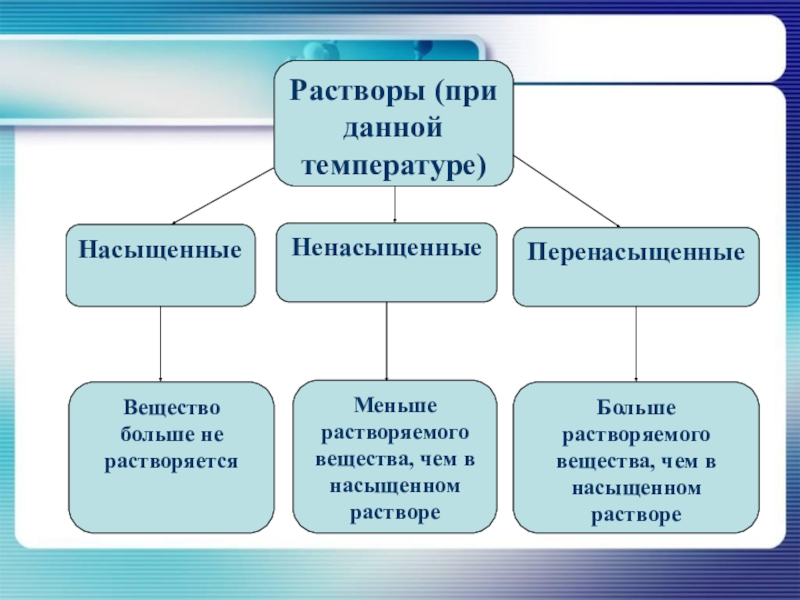
Слайд 15Растворы (при данной температуре)
Насыщенные
Ненасыщенные
Перенасыщенные
Вещество больше не растворяется
Меньше
растворяемого вещества, чем в насыщенном растворе
Больше растворяемого вещества, чем в
насыщенном раствореСлайд 19Тест на закрепление
1. Растворимость веществ не зависит от:
А) природы растворителя Б) температуры В) давления
Г)природы вещества2. К нерастворимому основанию относится:
А) NaOH Б) Mg(OH)2 В) KOH Г) Ba(OH)2
3. Вещество больше не растворяется при данной температуре – это раствор:
А) насыщенный Б) ненасыщенный В) пересыщенный
Г) недосыщенный
4. Основоположник химической теории растворения:
А) Вант-Гофф Б) Оствальд В) Аррениус Г) Менделеев
5. Соединение, образованное взаимодействием вещества с водой – это:
А) гидрат Б) кристаллогидрат В) аллотропия Г) изотоп