Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Типы химических реакций
Содержание
- 1. Типы химических реакций
- 2. Вещества можно классифицироватьПо составуПо агрегатному состояниюПо происхождению
- 3. «Подарки» природы
- 4. «Подарки» природыСераУгольКремнийСереброЗолотоПлатина
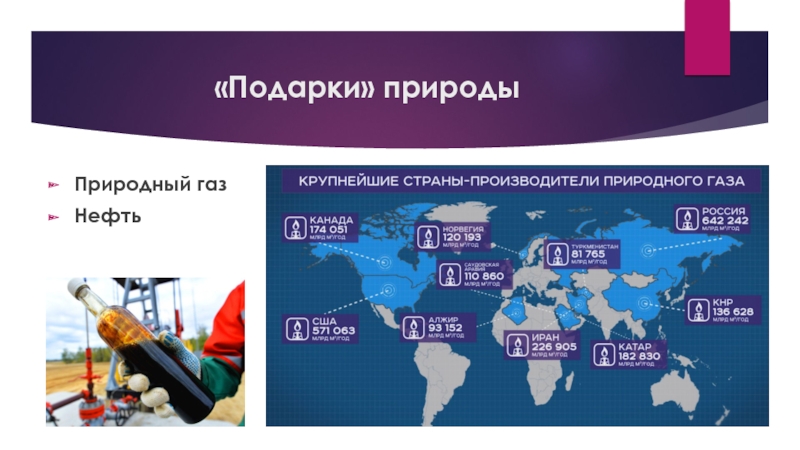
- 5. «Подарки» природыПриродный газНефть
- 6. «Подарки» природыВода Кремнезем (кварц, опал, аметист)Глинозем,боксит, корундКрасный и бурый железняки
- 7. «Подарки» природыКаменная соль (галенит)Сода (натрит)Известняк (мел, мрамор)Апатиты, фосфориты
- 8. Используя эти «подарки», получите следующие вещества:ВодородАлюминийЖелезоГашеную известьУгольную кислотуФосфорную кислотуФосфат натрия
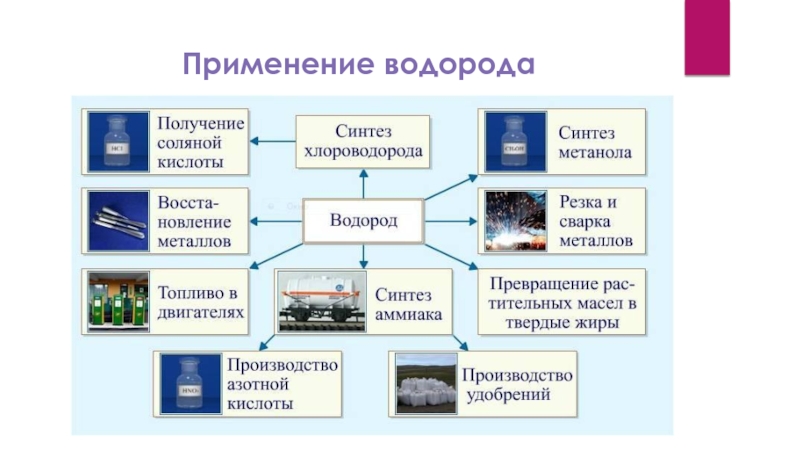
- 9. Применение водорода
- 10. Слайд 10
- 11. Слайд 11
- 12. Слайд 12
- 13. Средний американец выпивает 180 л газированной воды в
- 14. Слайд 14
- 15. Слайд 15
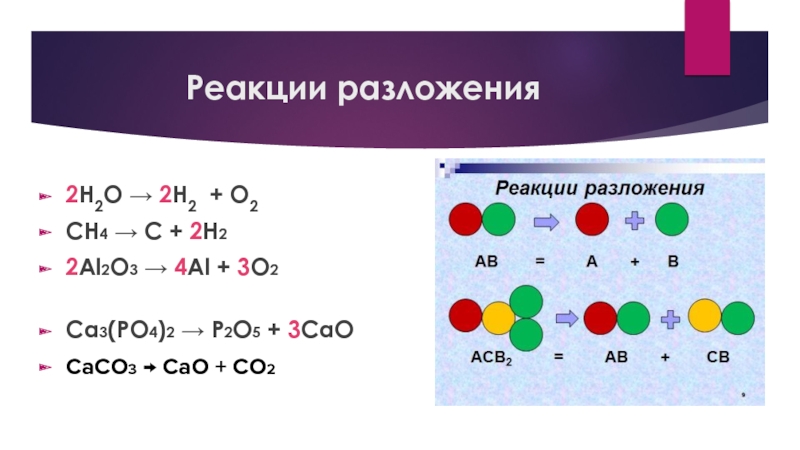
- 16. Реакции разложения2H2O → 2H2 + O2
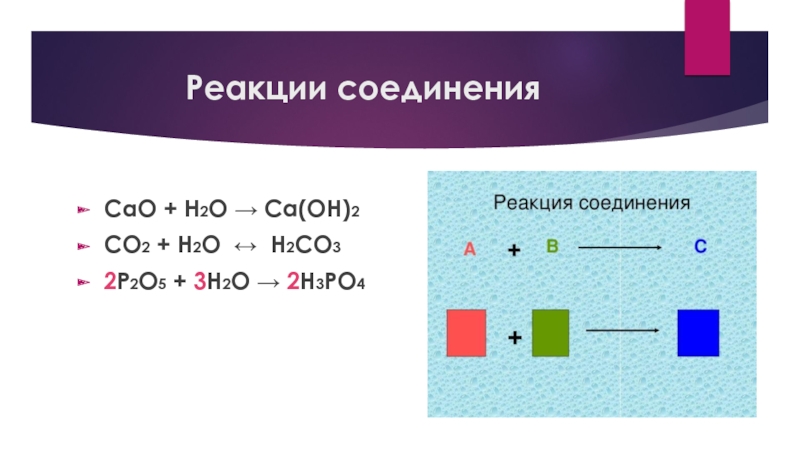
- 17. Реакции соединенияCaO + H2O → Ca(OH)2СО2 + Н2О ↔ Н2СО32P2O5 + 3Н2О → 2H3PO4
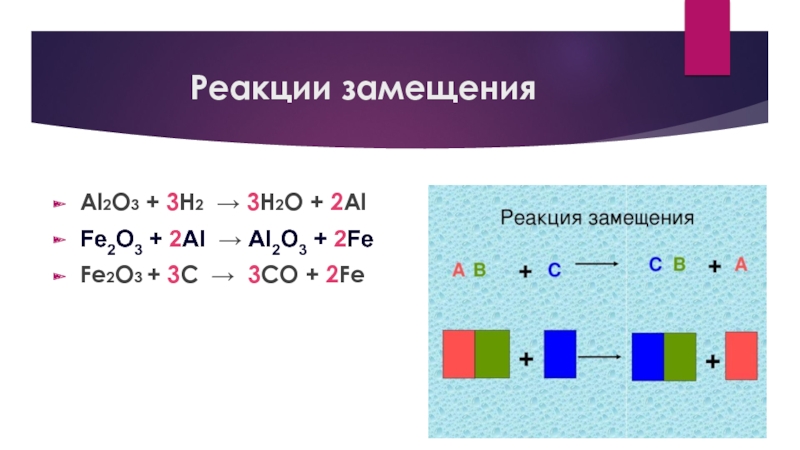
- 18. Реакции замещенияAl2O3 + 3H2 → 3H2O +
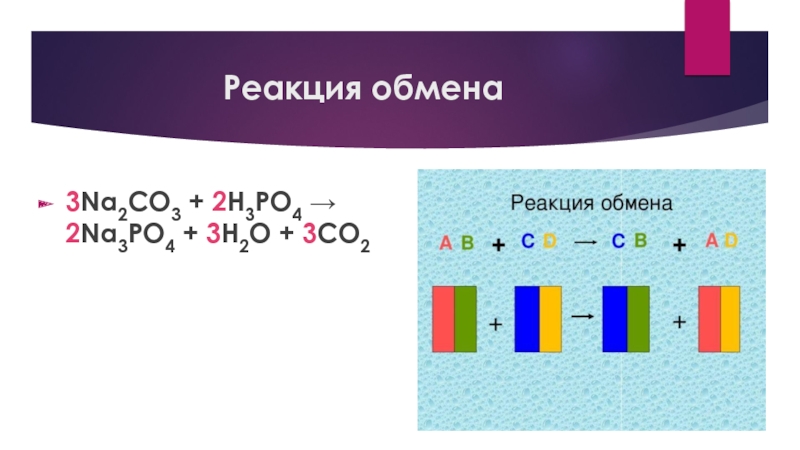
- 19. Реакция обмена3Na2CO3 + 2H3PO4 → 2Na3PO4 + 3H2O + 3CO2
- 20. Домашнее задание §34 № 1 повторить формулы для расчета количества вещества
- 21. Скачать презентанцию
Вещества можно классифицироватьПо составуПо агрегатному состояниюПо происхождению
Слайды и текст этой презентации
Слайд 6 «Подарки» природы
Вода
Кремнезем (кварц, опал, аметист)
Глинозем,боксит, корунд
Красный и бурый
железняки
Слайд 7 «Подарки» природы
Каменная соль (галенит)
Сода (натрит)
Известняк (мел, мрамор)
Апатиты, фосфориты
Слайд 8Используя эти «подарки», получите следующие вещества:
Водород
Алюминий
Железо
Гашеную известь
Угольную кислоту
Фосфорную кислоту
Фосфат натрия
Слайд 13Средний американец выпивает 180 л газированной воды в год; средний россиянин —
50 л, средний китаец — 20 л воды в год
Слайд 16Реакции разложения
2H2O → 2H2 + O2
CH4 → С +
2H22Al2О3 → 4Al + 3О2
Ca3(PO4)2 → P2O5 + 3CaO
CaCO3 → CaO + CO2