Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Типы химических реакций
Содержание
- 1. Типы химических реакций
- 2. Химические реакции или химические явления
- 3. По каким признакам можно определить химические реакции?
- 4. Каковы условия возникновения реакций? Растворение;Измельчение;Смешивание веществ;Нагревание.
- 5. Химические реакцииКак классифицировать?
- 6. Реакции соединения2Аl+ 3I2 = 2 AlI3NH3 + HCl = NH4Cl1.
- 7. Реакции, в которых из нескольких
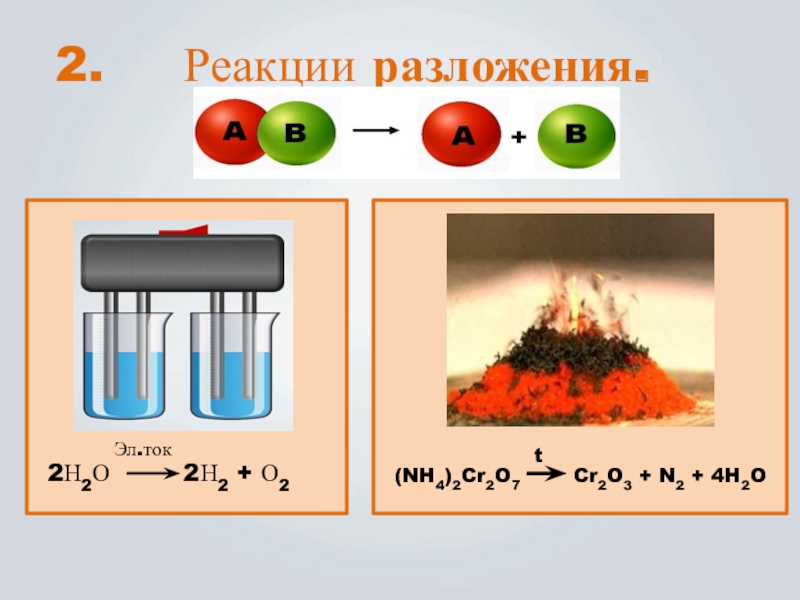
- 8. Реакции разложения.(NH4)2Cr2O7 Cr2O3 +
- 9. Реакции, в которых из
- 10. Реакции замещения.SnCl2 + Zn = ZnCl2 + SnH2SO4 + Zn = ZnSO4 + H2↑3.
- 11. Реакции, протекающие между простыми
- 12. Реакции обмена.Pb(NO3)2 +2KI = PbI2↓+2KNO32 NaOH + H2SO4 = Na2SO4 + 2H2O4.
- 13. Реакции, происходящие между сложными веществами, в результате которых они меняются своими составными частями, наз. реакциями обмена.
- 14. Реакции обмена, протекающие в растворах,
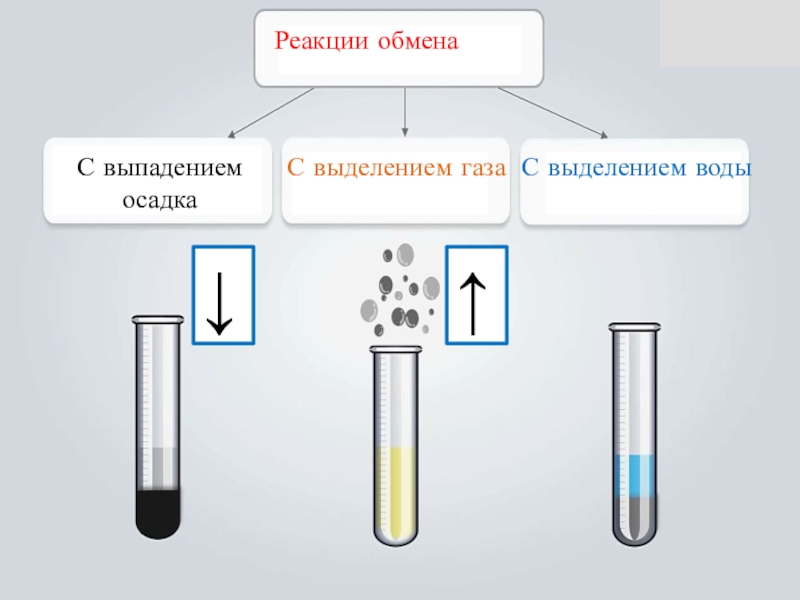
- 15. Реакции обменаС выпадением осадкаС выделением газаС выделением воды↓↑
- 16. Типы химических реакций
- 17. Проверка знаний Zn + O2 = 2
- 18. Домашнее задание: Выучить записи в тетради;определить тип реакций(зад. 1 – 3)
- 19. Задание № 1. Расставьте коэффициенты. Какие реакции
- 20. алюминий + хлор = хлорид алюминияоксид азота
- 21. Задание № 3. Закончите уравнения реакций, определите
- 22. Скачать презентанцию
Химические реакции или химические явления – это процессы, в результате которых из одних веществ образуются другие.Что такое химическая реакция?
Слайды и текст этой презентации
Слайд 2 Химические реакции или химические явления – это процессы,
в результате которых из одних веществ образуются другие.
реакция?Слайд 3По каким признакам можно определить химические реакции?
Выделение газа;
Образование осадка;
Выделение (поглощение)
тепла и света;
Появление или изменение запаха;
Изменение цвета.
Слайд 7 Реакции, в которых из нескольких простых или сложных
веществ образуется одно более сложное вещество, наз. реакциями соединения.
t
Слайд 9 Реакции, в которых из одного сложного вещества
получается два или несколько простых или сложных веществ, наз. реакциями
разложения.t
Слайд 11 Реакции, протекающие между простыми и сложными
веществами, при которых атомы простого вещества замещают атомы одного из
элементов в сложном веществе, наз. реакциями замещения.Слайд 13Реакции, происходящие между сложными веществами, в результате которых они меняются
своими составными частями, наз. реакциями обмена.
Слайд 14 Реакции обмена, протекающие в растворах, идут до конца
только в том случае, если образуется осадок, газ или вода.
Слайд 17Проверка знаний
Zn + O2 = 2 ZnO
2 Al(OH)3 =
Al2O3 + 3 H2O
Mg(ОН)2 + 2 HCl = MgCl2
+ H2О2 Au2O3 = 2 Au + 3 O2
2Fe + 3 Cl2 = 2 FeCl3
6) 2 Al + 3 CuCl2 = 3 Cu + 2 AlCl3
Соединение
Разложение
Обмен
Разложение
Соединение
Замещение
Слайд 19Задание № 1. Расставьте коэффициенты. Какие реакции относятся к реакциям
разложения?
Al2S3 + H2O → Al(OH)3 + H2S
KMnO4 → K2MnO4 +
MnO2 + O2KClO3 → KCl + O2
Al4C3 + H2O → Al(OH)3 + CH4
NH3 → N2 + H2
H3PO4 + CaSO4 → H2SO4 + Ca3(PO4)3
Слайд 20алюминий + хлор = хлорид алюминия
оксид азота (II) + кислород
= оксид азота (IV)
оксид азота (V) + вода = азотная
кислотацинк + соляная кислота = хлорид цинка + водород
гидроксид магния + бромоводородная кислота = бромид магния + вода
хлорид меди (II) + хром = хлорид хрома (II) + медь
Задание № 2. Запишите уравнения реакций и определите тип реакции.
Слайд 21Задание № 3. Закончите уравнения реакций, определите тип реакций.
1)
нитрат серебра + цинк →
2) гидроксид калия + фосфорная кислота
→3) сульфид железа (II) + соляная кислота →
4) хлорид бария + гидроксид алюминия →
5) оксид меди (II) + серная кислота →
6) оксид железа (III) + магний →