Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Транспортні антибіотики - іонофори
Содержание
- 1. Транспортні антибіотики - іонофори
- 2. Антибіотики іонофори – мембранні пори для пасивного транспорту іонов (діри для іонів)
- 3. Транспортні антибіотики підвищують іонну проникність мембранРяд мікроорганізмів
- 4. ВластивістьІон Характеристики чотирьох біологічно важливих лужних та лужноземельних катіонів.
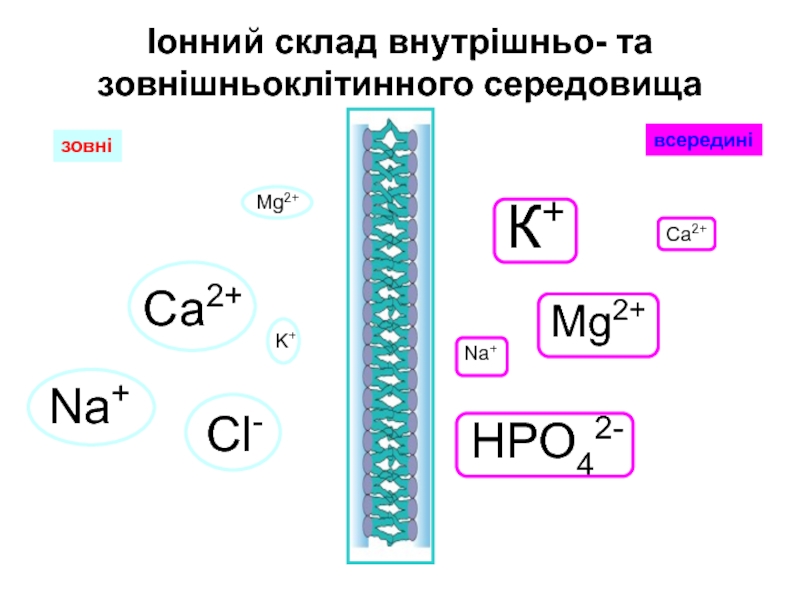
- 5. Іонний склад внутрішньо- та зовнішньоклітинного середовищазовнівсерединіК+Mg2+HPO42-Na+Na+Са2+Cl-Mg2+Са2+K+
- 6. [M(H2O)n]m+ + L [ML]m+ + n(H2O)Комплексоутворення
- 7. Для дициклогексил-18-корони-6 взаємодія з катіонами лужних металів
- 8. гідрофільні донорні атоми макроцикла повернуті всередину до
- 9. Іонофори (тобто переносники іонів, від “іони” та
- 10. 1. Нейтральні іонофори, що не містять здатних
- 11. Макротетралідні актини Цей тип іонофорів (18-членні кільця)
- 12. Енніатини відносяться до групи циклічних гексадепсипептидів, що
- 13. Антибіотик валіноміцин – пептидний іонофор зв’язує К+Streptomyces fulvissimus
- 14. Валіноміцин перешкоджає окиснювальному фосфо-рилюванню в мітохондріях шляхом
- 15. ВаліноміцинВаліноміцин звязує К+ у 1000разів міцніше, ніж
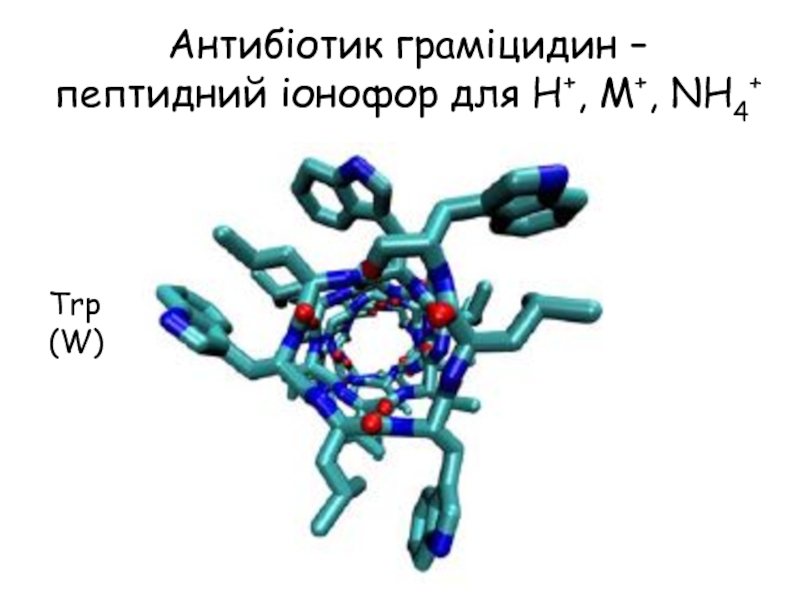
- 16. Антибіотик граміцидин – пептидний іонофор для H+, M+, NH4+Trp(W)
- 17. ГраміцидиниГраміцидин А Граміцидини – це лінійні пентадекапептиди,
- 18. Іонофор I дифундує через ліпідний бар’єр
- 19. Транспортні антибіотики як каналоутворювачі Антибіотик граміцидин А
- 20. Міжклітинні канали (щілинні контакти)1. Міжклітинні канали слугують
- 21. Вивчення зв’язування іонів лужних металів макроциклічними лігандами
- 22. Слайд 22
- 23. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Транспортні антибіотики підвищують
іонну проникність мембран
Ряд мікроорганізмів синтезує низькомолекулярні сполуки,
у присутності яких біомембрани стають більш проникними для певних іонів.
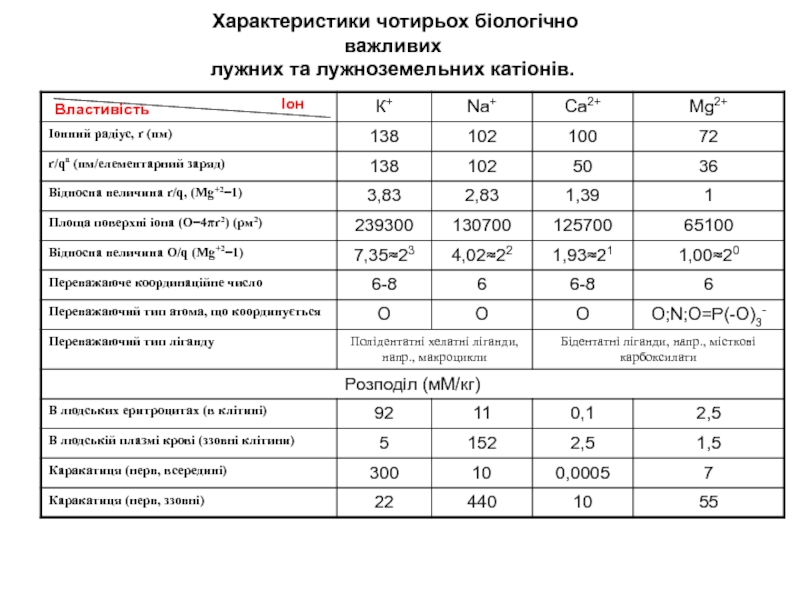
Слайд 4Властивість
Іон
Характеристики чотирьох біологічно важливих
лужних та лужноземельних катіонів.
Слайд 5Іонний склад внутрішньо- та зовнішньоклітинного середовища
зовні
всередині
К+
Mg2+
HPO42-
Na+
Na+
Са2+
Cl-
Mg2+
Са2+
K+
Слайд 6[M(H2O)n]m+ + L [ML]m+ + n(H2O)
Комплексоутворення лужних та лужноземельних
металів
Зростає ентропія
Підвищується кінетична стабільність
Для Са2+ та Mg2+ ефективні відкритоланцюгові ліганди
(напр., ЕДТА) відомі дуже давно, а ефективне комплексування лужних металів стало
можливим лише при появі краун-ефірів та криптандів.
[18]краун-6
дибензо[30]краун-10
криптанд[2,2,2]
Поліефіри типу корон дають можливість синтезувати поліефіри з різним розміром
кільця, що дозволяє корелювати іонну селективність з розміром порожнини у кільці.
Як і слід було очікувати, сполуки з меншими розмірами кільця (14- та 15-членні)
надають перевагу Na+, тоді як для К+ найбільш підходящими є 19-членні кільця,
а для Cs+ - кільця з 21-24 атомами.
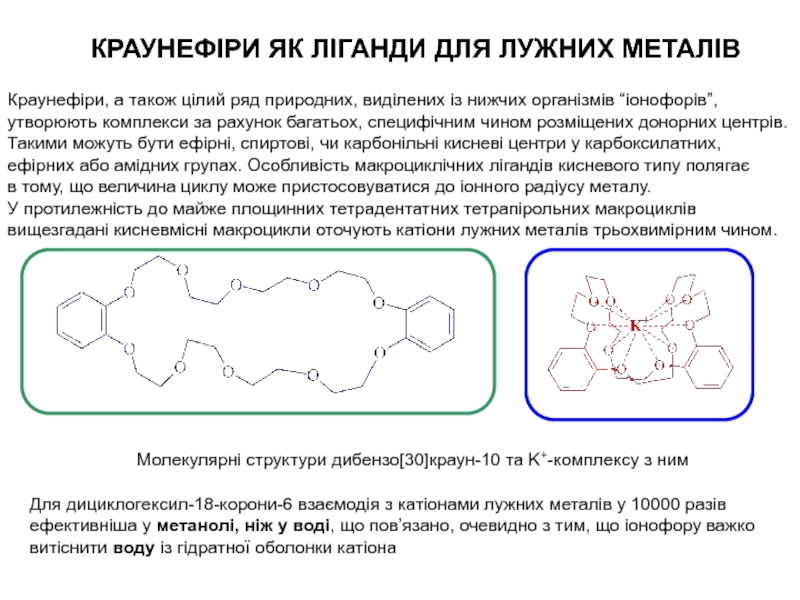
Слайд 7Для дициклогексил-18-корони-6 взаємодія з катіонами лужних металів у 10000 разів
ефективніша у метанолі, ніж у воді, що пов’язано, очевидно з
тим, що іонофору важко витіснити воду із гідратної оболонки катіона
Краунефіри, а також цілий ряд природних, виділених із нижчих організмів “іонофорів”,
утворюють комплекси за рахунок багатьох, специфічним чином розміщених донорних центрів.
Такими можуть бути ефірні, спиртові, чи карбонільні кисневі центри у карбоксилатних,
ефірних або амідних групах. Особливість макроциклічних лігандів кисневого типу полягає
в тому, що величина циклу може пристосовуватися до іонного радіусу металу.
У протилежність до майже площинних тетрадентатних тетрапірольних макроциклів
вищезгадані кисневмісні макроцикли оточують катіони лужних металів трьохвимірним чином.
КРАУНЕФІРИ ЯК ЛІГАНДИ ДЛЯ ЛУЖНИХ МЕТАЛІВ
Молекулярні структури дибензо[30]краун-10 та K+-комплексу з ним
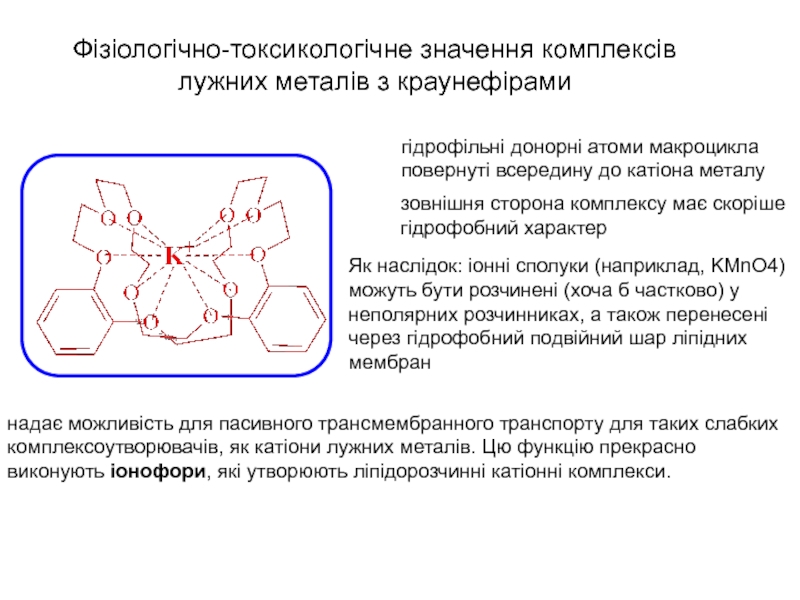
Слайд 8гідрофільні донорні атоми макроцикла
повернуті всередину до катіона металу
зовнішня
сторона комплексу має скоріше
гідрофобний характер
Як наслідок: іонні сполуки
(наприклад, KMnO4) можуть бути розчинені (хоча б частково) у
неполярних розчинниках, а також перенесені
через гідрофобний подвійний шар ліпідних
мембран
надає можливість для пасивного трансмембранного транспорту для таких слабких
комплексоутворювачів, як катіони лужних металів. Цю функцію прекрасно
виконують іонофори, які утворюють ліпідорозчинні катіонні комплекси.
Фізіологічно-токсикологічне значення комплексів
лужних металів з краунефірами
Слайд 9Іонофори (тобто переносники іонів, від “іони” та грецького
phoros – той,
що несе) – це сполуки з такою молекулярною
структурою, яка
обумовлює їх здатність переносити невеликі іони через ліпідні бар’єри (мембрани)
Молекули іонофорів містять велику кількість атомів кисню,
що регулярно розміщені у молекулярному остові
іонофори є, як правило, хімічно та метаболічно стійкими
іонофори або вже мають готову макроциклічну структуру,
або здатні утворювати макроциклічні кільця за допомогою
водневих зв’язків
Їх молекулярні маси знаходяться в межах від 200 до 2000
ІОНОФОРИ
Слайд 10
1. Нейтральні іонофори, що не містять здатних до дисоціації протонів
Типові циклічні ковалентні сполуки, чиї кільця містять від 18 до
40 атомів Кільця містять, як правило, субодиниці, що повторюються, з регулярним
чередуванням центрів оптичної асиметрії.
Комплекси, що вони утворюють, мають загальний позитивний заряд
2. Карбоксилвмісні іонофори,
Формально лінійні ланцюги, які містять гетероциклічні кільця з
карбоксильними групами з одного кінця молекули та однією або двома
гідроксильними групами з другого кінця
при утворенні комплексів карбоксильна група депротонується і утворює
кільце типу “голова до хвоста” за допомогою водневих зв’язків з кінцевою
гідроксильною групою
такі процеси є рН-залежними
комплекси, що вони утворюють є нейтральними
Групи іонофорів
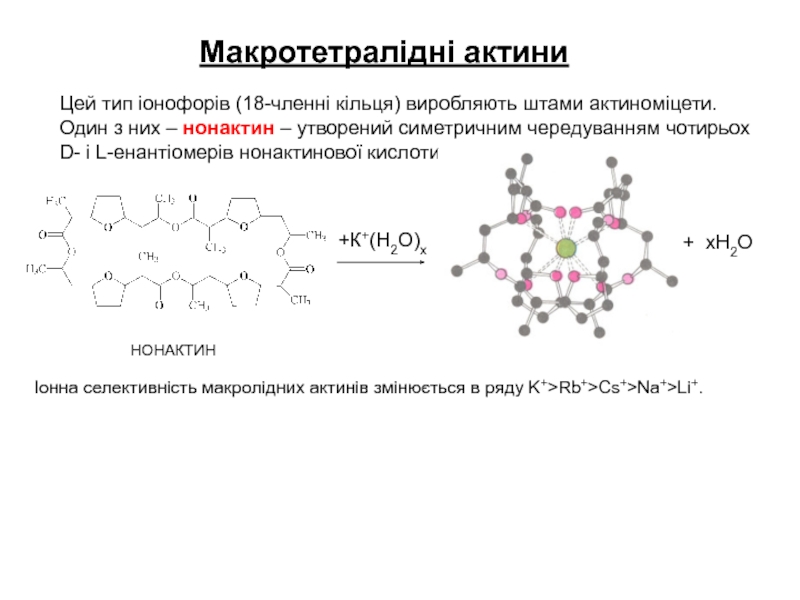
Слайд 11Макротетралідні актини
Цей тип іонофорів (18-членні кільця) виробляють штами актиноміцети.
Один з них – нонактин – утворений симетричним чередуванням чотирьох
D- і L-енантіомерів нонактинової кислоти.
НОНАКТИН
+К+(Н2О)х
+ хН2О
Іонна селективність макролідних актинів змінюється в ряду K+>Rb+>Cs+>Na+>Li+.
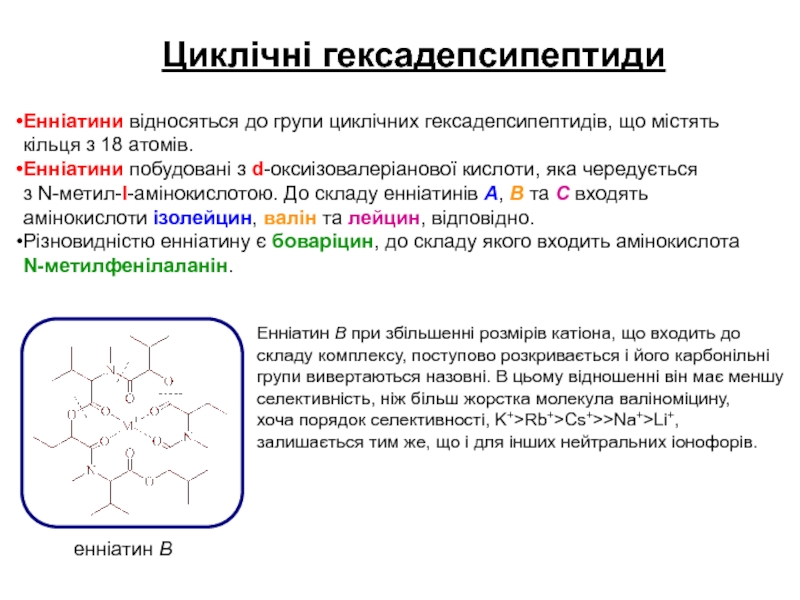
Слайд 12Енніатини відносяться до групи циклічних гексадепсипептидів, що містять
кільця з
18 атомів.
Енніатини побудовані з d-оксиізовалеріанової кислоти, яка чередується
з
N-метил-l-амінокислотою. До складу енніатинів А, В та С входять амінокислоти ізолейцин, валін та лейцин, відповідно.
Різновидністю енніатину є боваріцин, до складу якого входить амінокислота
N-метилфенілаланін.
енніатин В
Енніатин В при збільшенні розмірів катіона, що входить до
складу комплексу, поступово розкривається і його карбонільні
групи вивертаються назовні. В цьому відношенні він має меншу
селективність, ніж більш жорстка молекула валіноміцину,
хоча порядок селективності, K+>Rb+>Cs+>>Na+>Li+,
залишається тим же, що і для інших нейтральних іонофорів.
Циклічні гексадепсипептиди
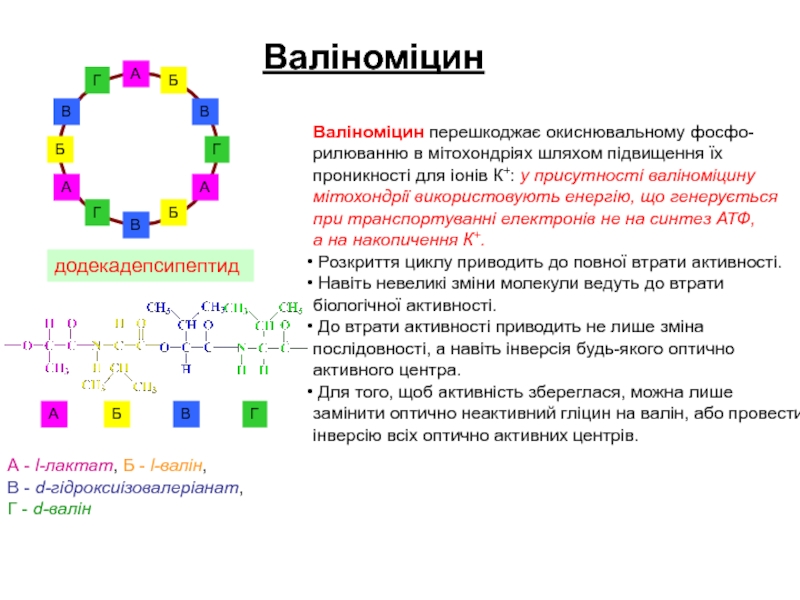
Слайд 14Валіноміцин перешкоджає окиснювальному фосфо-
рилюванню в мітохондріях шляхом підвищення їх
проникності
для іонів К+: у присутності валіноміцину
мітохондрії використовують енергію, що генерується
при
транспортуванні електронів не на синтез АТФ,а на накопичення К+.
Розкриття циклу приводить до повної втрати активності.
Навіть невеликі зміни молекули ведуть до втрати
біологічної активності.
До втрати активності приводить не лише зміна
послідовності, а навіть інверсія будь-якого оптично
активного центра.
Для того, щоб активність збереглася, можна лише
замінити оптично неактивний гліцин на валін, або провести
інверсію всіх оптично активних центрів.
А - l-лактат, Б - l-валін,
В - d-гідроксиізовалеріанат,
Г - d-валін
додекадепсипептид
Валіноміцин
А
А
А
А
Б
Б
Б
Б
В
В
В
В
Г
Г
Г
Г
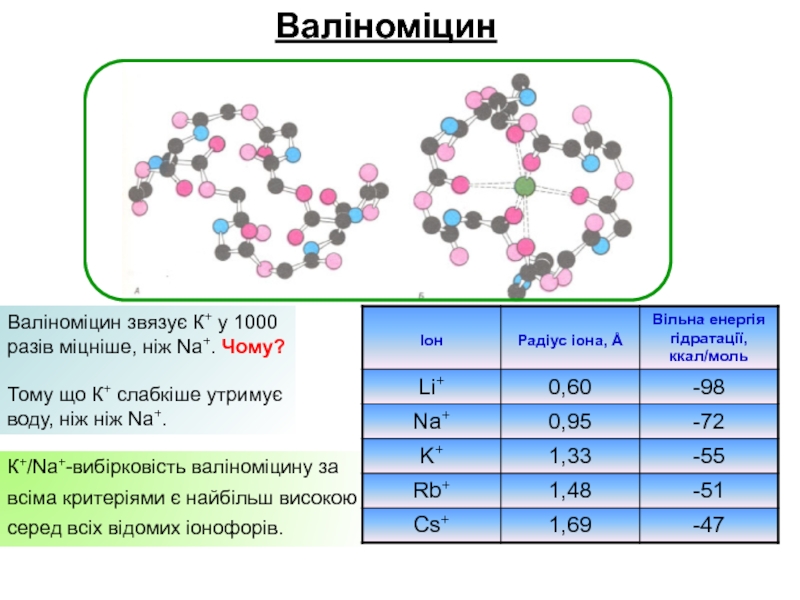
Слайд 15Валіноміцин
Валіноміцин звязує К+ у 1000
разів міцніше, ніж Na+. Чому?
Тому що
К+ слабкіше утримує
воду, ніж ніж Na+.
К+/Na+-вибірковість валіноміцину за
всіма критеріями
є найбільш високою серед всіх відомих іонофорів.
Слайд 17Граміцидини
Граміцидин А
Граміцидини – це лінійні пентадекапептиди, які виробляються штамом
В.brevis.
Можливими є наступні структурні варіанти: на початку ланцюга
– валін або ізолейцин, а фенілаланін, тирозин або триптофан – на дванадцятому місці в
ланцюгу, який складається з 15-ти залишків.
Спостерігається також типове для багатьох іонофорів чередування D- та L-конфігурацій,
Kінцеві групи блокуються формільною (R-NH-C(O)H) або
етаноламідною (R-CO-NH-CH2-CH2OH) групами.
Не зважаючи на те, що граміцидин подібний до вище описаних іонофорів за своєю
структурою і впливом на мембрани, він не утворює ліпідорозчинних комплексів і може
не виконувати функції істинного рухливого “іонофороподібного” носія.
l
d
d
d
d
d
d
l
l
l
l
l
l
l
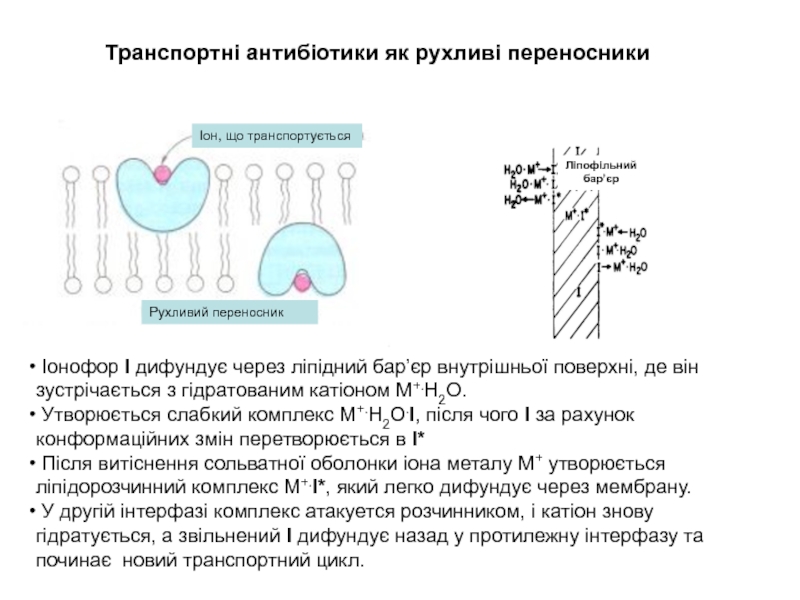
Слайд 18 Іонофор I дифундує через ліпідний бар’єр внутрішньої поверхні, де
він
зустрічається з гідратованим катіоном М+.Н2О.
Утворюється слабкий комплекс
М+.Н2О.I, після чого I за рахунокконформаційних змін перетворюється в I*
Після витіснення сольватної оболонки іона металу М+ утворюється
ліпідорозчинний комплекс M+.I*, який легко дифундує через мембрану.
У другій інтерфазі комплекс атакуется розчинником, і катіон знову
гідратується, а звільнений I дифундує назад у протилежну інтерфазу та
починає новий транспортний цикл.
Транспортні антибіотики як рухливі переносники
Рухливий переносник
Іон, що транспортується
Ліпофільний
бар’єр
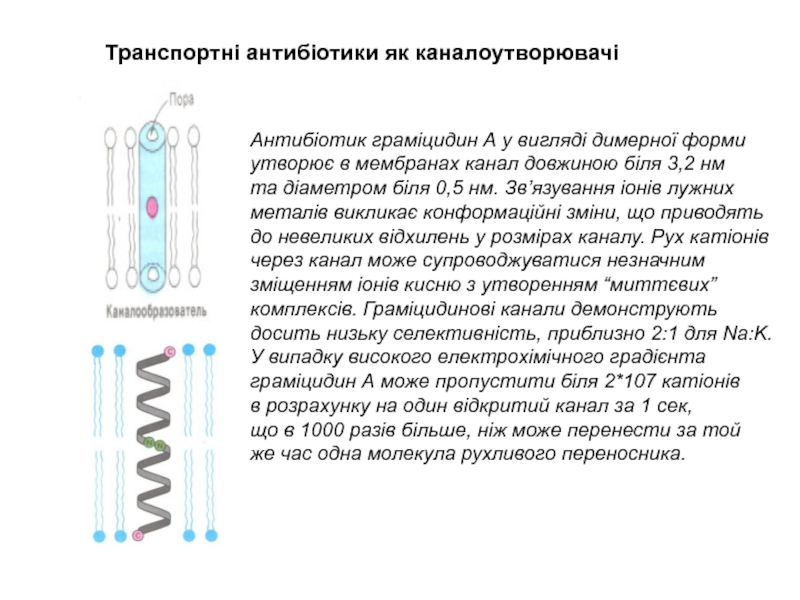
Слайд 19Транспортні антибіотики як каналоутворювачі
Антибіотик граміцидин А у вигляді димерної
форми
утворює в мембранах канал довжиною біля 3,2 нм
та
діаметром біля 0,5 нм. Зв’язування іонів лужних металів викликає конформаційні зміни, що приводять
до невеликих відхилень у розмірах каналу. Рух катіонів
через канал може супроводжуватися незначним
зміщенням іонів кисню з утворенням “миттєвих”
комплексів. Граміцидинові канали демонструють
досить низьку селективність, приблизно 2:1 для Na:K.
У випадку високого електрохімічного градієнта
граміцидин А може пропустити біля 2*107 катіонів
в розрахунку на один відкритий канал за 1 сек,
що в 1000 разів більше, ніж може перенести за той
же час одна молекула рухливого переносника.
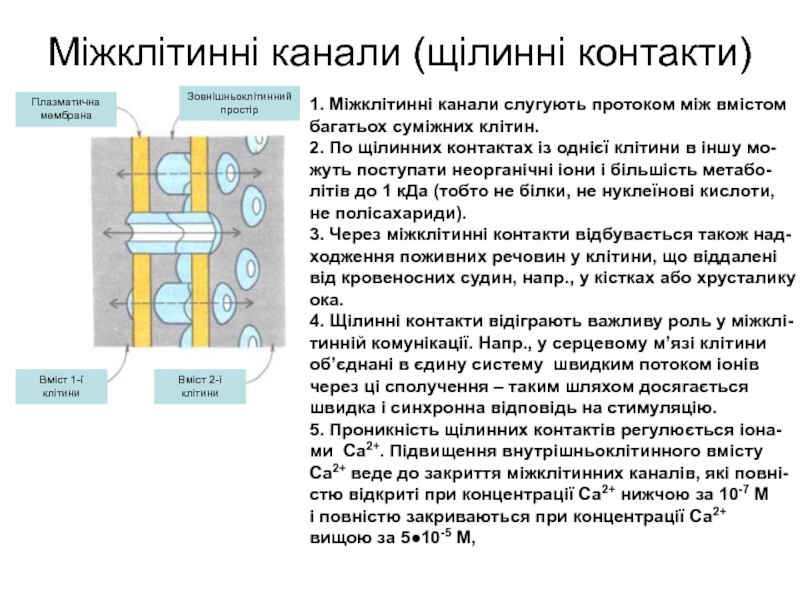
Слайд 20Міжклітинні канали (щілинні контакти)
1. Міжклітинні канали слугують протоком між вмістом
багатьох суміжних клітин.
2. По щілинних контактах із однієї клітини в
іншу мо-жуть поступати неорганічні іони і більшість метабо-
літів до 1 кДа (тобто не білки, не нуклеїнові кислоти,
не полісахариди).
3. Через міжклітинні контакти відбувається також над-
ходження поживних речовин у клітини, що віддалені
від кровеносних судин, напр., у кістках або хрусталику
ока.
4. Щілинні контакти відіграють важливу роль у міжклі-
тинній комунікації. Напр., у серцевому м’язі клітини
об’єднані в єдину систему швидким потоком іонів
через ці сполучення – таким шляхом досягається
швидка і синхронна відповідь на стимуляцію.
5. Проникність щілинних контактів регулюється іона-
ми Са2+. Підвищення внутрішньоклітинного вмісту
Са2+ веде до закриття міжклітинних каналів, які повні-
стю відкриті при концентрації Са2+ нижчою за 10-7 М
і повністю закриваються при концентрації Са2+
вищою за 5●10-5 М,
Плазматична
мембрана
Зовнішньоклітинний
простір
Вміст 1-ї
клітини
Вміст 2-ї
клітини
Слайд 21Вивчення зв’язування іонів лужних металів макроциклічними лігандами
різних типів та
транспорту утворених комплексів через штучні та
природні мембрани дозволило сформулювати
ряд висновків:молекули іонофорів містять електрофільні групи, які конкурують
з молекулами розчинника (води) за зв’язування катіонів. Під час
комплексоутворення відбувається заміщення гідратної оболонки катіона
донорними атомами ліганду.
ліганд містить або утворює порожнину для катіону, причому
селективність зв’язування досягається за рахунок точної відповідності
розмірів порожнини розмірам катіона. Окрім того, для іонної вибірковості
суттєву роль відіграє також симетрія розміщення ліганд них груп
іонофор має гнучку структуру і здатний до конформаційних змін
всі іонофори мають гідрофобну зовнішню поверхню, завдяки якій
жиророзчинний комплекс, що утворюється, здатний до дифузії через
ліпідний подвійний шар мембрани.



![Транспортні антибіотики
- іонофори [M(H2O)n]m+ + L [ML]m+ + n(H2O)Комплексоутворення лужних та лужноземельних металівЗростає [M(H2O)n]m+ + L [ML]m+ + n(H2O)Комплексоутворення лужних та лужноземельних металівЗростає ентропіяПідвищується кінетична стабільністьДля Са2+ та Mg2+](/img/tmb/4/353259/ffc1eef48a36bedee2f34c19d96259ce-800x.jpg)