Слайд 2Основные вопросы:
1. Растворы. Коллигативные
свойства растворов.
2. Закон Рауля и
его следствия.
Осмос и осмотическое давление.
3. Теория растворов сильных
электролитов.
4. Протолитическая теория кислот и
оснований.
5. Буферные растворы и системы.
Механизм действия и количественные
характеристики буферных систем.
Слайд 3Растворы -
Растворитель -
Растворённое вещество -
Слайд 4Вода - самый распространённый растворитель
Слайд 5Биол.
жидкости:
кровь
лимфа
слюна
моча
пот и др.
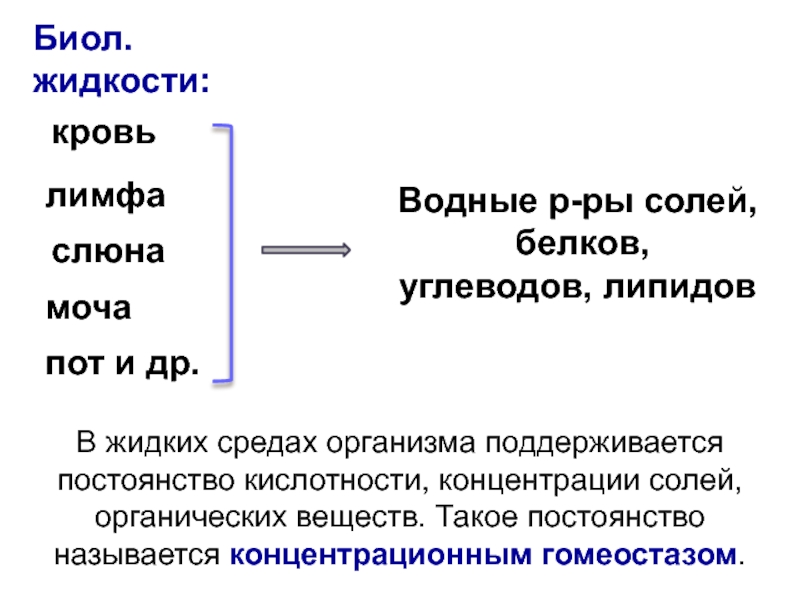
В жидких средах организма поддерживается постоянство кислотности,
концентрации солей, органических веществ. Такое постоянство называется концентрационным гомеостазом.
Слайд 6
Содержание и распределение воды в организме человека
Их состав сильно отличается
:
~ 60 % от общей массы тела человека составляет вода.
(На 70 кг веса приходится 45 л воды).
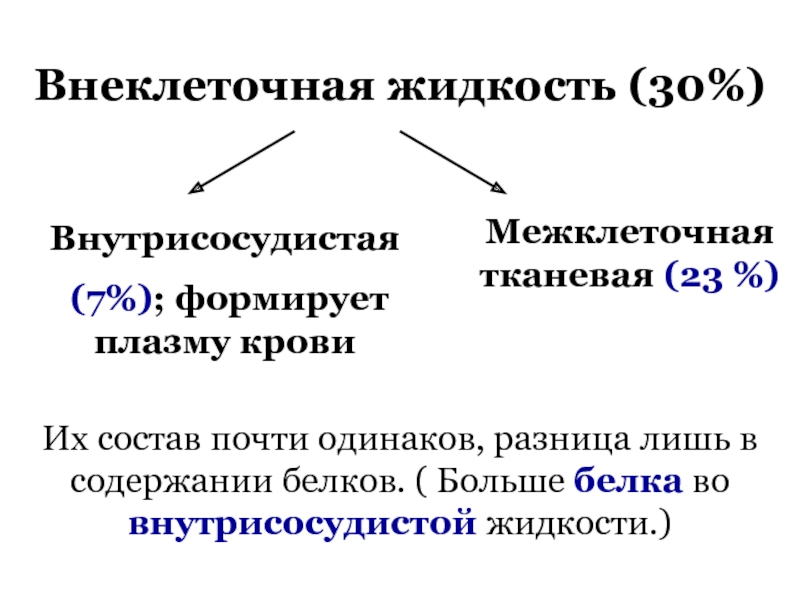
Слайд 8Внеклеточная жидкость (30%)
Их состав почти одинаков, разница лишь в содержании
белков. ( Больше белка во внутрисосудистой жидкости.)
Слайд 9В биохимических процессах вода выступает как :
3. Продукт реакции
1. Растворитель
2.
Реагент
Слайд 101. Вода- универсальный
растворитель
Существование межмолекулярных водородных связей определяет аномальные физические
свойства воды:
Молекула воды полярна; μ(Н2О) = 1,86 D
Вода – хороший
«термостат» для белков и нуклеиновых
кислот, структура и функции которых зависят от температуры.
1. Высокая теплоемкость –
главный фактор в поддержании температуры теплокровных животных (+36 - +37) град.
Слайд 113. Высокая теплота испарения воды с кожных
покровов предохр. организм от перегрева
4. Высокое поверхностное натяжение
5. Низкая
вязкость
6. Более высокая плотность в жидком состоянии, чем в твердом , защищает организмы от влияния низких т-р
7. Высокая диэлектрическая проницаемость ε = 80 (уникальный р-ль для в-в с ионной и полярной связью)
2. Высокая т-ра кипения ( )
Слайд 122. Вода – реагент в биохимических реакциях
кислотно-основных (автопротолиз воды)
Н2О + Н2О Н3О+ + ОН –
окисления-восстановления (окисление
воды при фотосинтезе:
6 Н2О + 6СО2 С6Н12О6 + 6О 2
гидратации (белков и нуклеиновых
кислот)
гидролиза (гидролиз АТФ)
Слайд 133. Вода - продукт биохимических реакций.
- 241,8 кДж/моль (57 ккал/моль)
2
Н2+О2 2Н2О + Q
Вывод: Н2О – универсальный р-ль, наличие
аномальных свойств ее играет важную физиологическую и биологическую роль. Биохимические процессы в организме протекают в водных р-рах или при ее (воды) участии, как реагента или продукта р-ции.
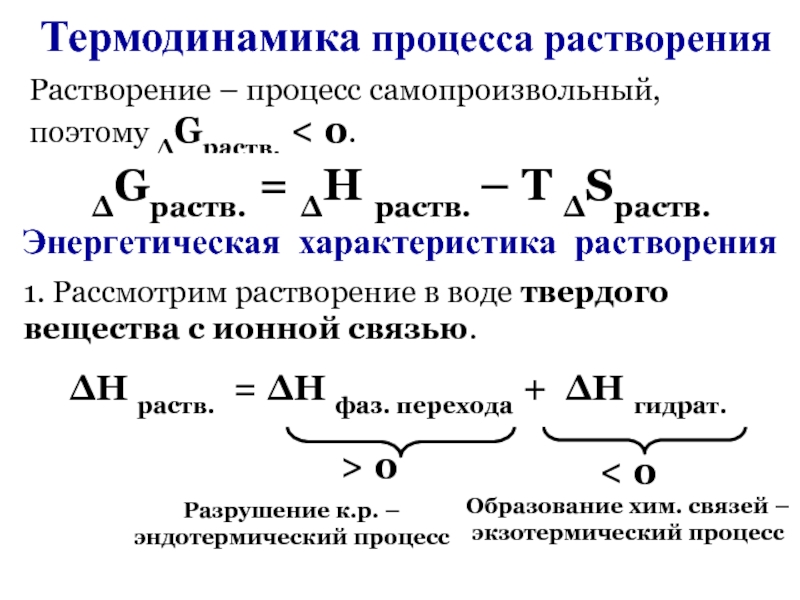
Слайд 15Термодинамика процесса растворения
Растворение – процесс самопроизвольный, поэтому ∆Gраств. < 0.
∆Gраств. = ∆Н раств. – Т ∆Sраств.
Энергетическая характеристика растворения
1. Рассмотрим
растворение в воде твердого вещества с ионной связью.
∆Н раств. = ∆Н фаз. перехода + ∆Н гидрат.
Слайд 161. Если |∆Н ф. п. | > |∆Н гидр. |,
то ∆Н раств. > 0, эндо-процесс, р-р охлаждается (КNO3,
NH4NO3)
2. Если |∆Н ф. п. |< |∆Н гидр. |,
то ∆Н раств. < 0, экзо-процесс, р-р нагревается (NaOH )
Т.о. при растворении тв./ж.
0 < ∆ Н раств. < 0
Слайд 17Энтропийная характеристика растворения
∆Sраств. = ∆S фаз. перехода + ∆S
гидр.
Т.о., |∆S ф. п. |> |∆S гидр. |, поэтому ∆Sраств.
тв. в-в > 0
Слайд 182. Растворение в воде газообразного вещества.
∆Sраств. газов
0,
∆Gраств. = ∆Н раств. – Т ∆Sраств.
∆Gраств. < 0 и ∆Sраств. < 0;
∆Н раств. газов < 0
∆Нраств.=∆G раств. + Т ∆Sраств.
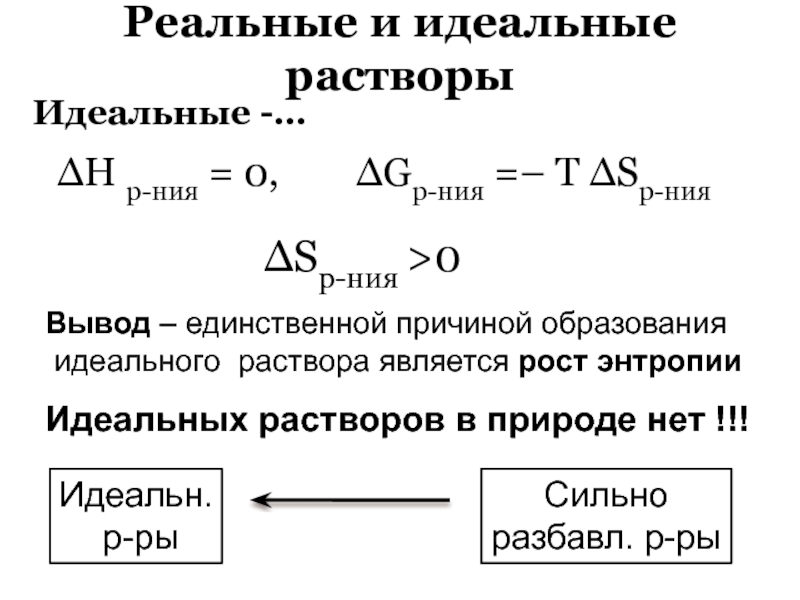
Слайд 19Реальные и идеальные растворы
Идеальные -…
Вывод – единственной причиной образования
идеального
раствора является рост энтропии
Идеальных растворов в природе нет !!!
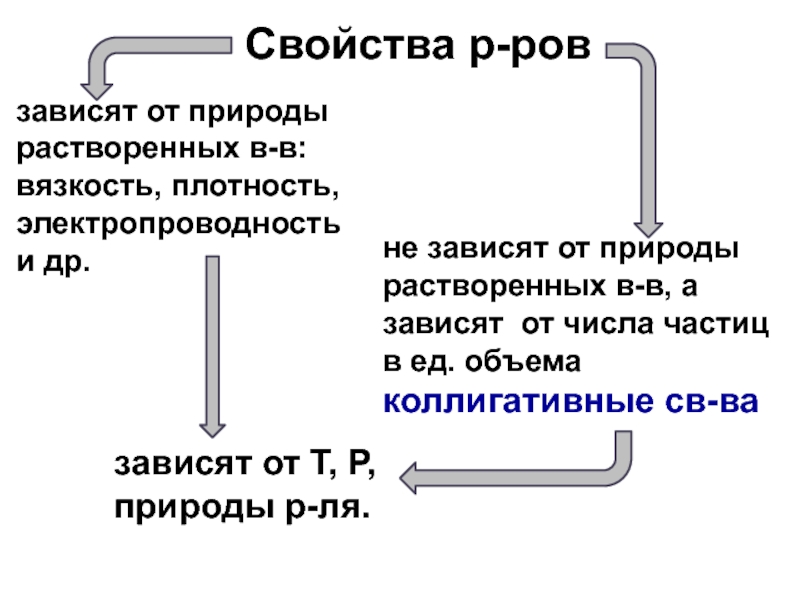
Слайд 21Коллигативные свойства
растворов
осмотическое давление
понижение давления насыщенного пара р-ля над
р-ом по сравнению с давлением насыщенного пара р-ля над чистым
р-лем.
повышение т-ры кипения раствора
по сравнению с т-рой кипения чистого р-ля
понижение т-ры кристаллизации р-ра по сравнению с т-рой замерзания чистого р-ля.
Слайд 22Коллигативные свойства разбавленных р-ров неэлектролитов
Диффузия – самопроизв. двухстор. процесс…
Осмос -
явление одностор. дифф…
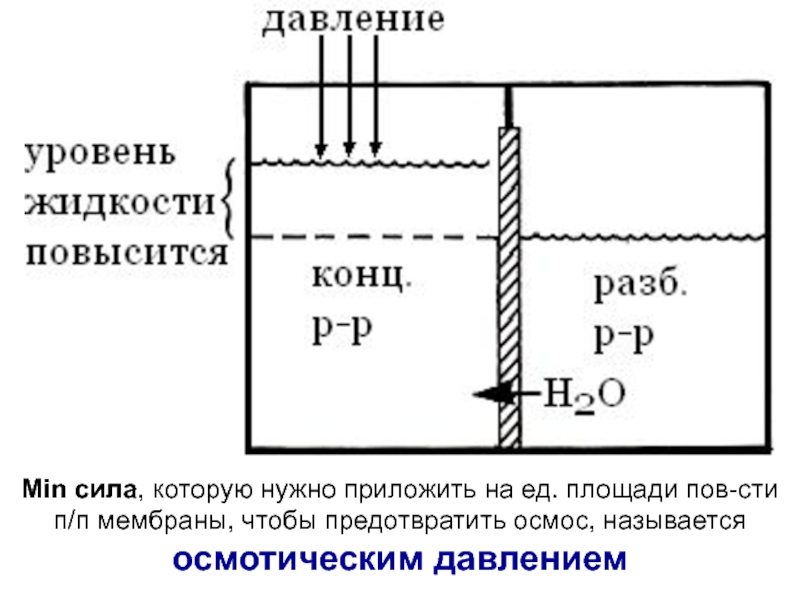
Слайд 23Min сила, которую нужно приложить на ед. площади пов-сти п/п
мембраны, чтобы предотвратить осмос, называется осмотическим давлением
Слайд 24Р осм. = СМRT – уравнение Вант-Гоффа
(1886 г; эксперим.)
1м3 = 1000 л; 1Па = 10-3 кПа
СМ = моль/л, Росм.= кПа.
Слайд 25РVгаза= nRT
уравнение Менделеева-Клапейрона.
Слайд 26Закон Вант-Гоффа : Осмотическое давление р-ра равно тому давлению, которое
оказывало бы растворенное в-во, если бы оно, находясь в газообразном
состоянии, занимало бы объем равный объему р-ра.
чем М, тем ↓ Росм. (белки)
Пример: 1 М р-р С6Н12О6 . Чему равно Росм.?
Слайд 27распределение воды между внутриклеточной жидкостью и внеклеточной
Осмос и осмотические
явления в биологических системах
Осмос и Росм. определяют:
распределение воды между
сосудистым руслом и внесосудистым пространством.
Слайд 28Осмолярность – суммарное количество
осмотически активных частиц (орг. и
неорг.
в-в) в 1л р-ра, моль/л
В клинической практике Росм биол. жидк.
измеряют
в единицах осмолярности и осмоляльности
Осмоляльность - … в 1кг растворителя,
моль/кг р-ля (определяется криометрией)
Слайд 29Она обусловлена:
низкомолекулярными веществами-электролитами: соли Na+, K+, Mg2+ , Ca2+
низкомолекулярными веществами
неэлектролитами:
глюкоза, мочевина.
ВМС – белки.
Осмоляльность плазмы
крови
равна 292 ммоль/кг
Росм крови = 740-780 кПа
Форменные элементы крови на Росм. не влияют.
Слайд 30Приблизительные величины вкладов компонентов
плазмы крови в поддержании ее осмоляльности
Слайд 31Вывод:
Na+ и связанные с ним анионы - основной ион
внеклеточной жидкости.
К+ и связанные с ним анионы
- основной ион внутриклеточной жидкости.
Росм. внутри и вне клетки одинаково, т.е. осмоляльность внутриклеточной жидкости равна осмоляльности плазмы крови ~ 292 ммоль /кг Н2О. Такое состояние – изоосмия.
Нарушение изоосмии вызывает патологию
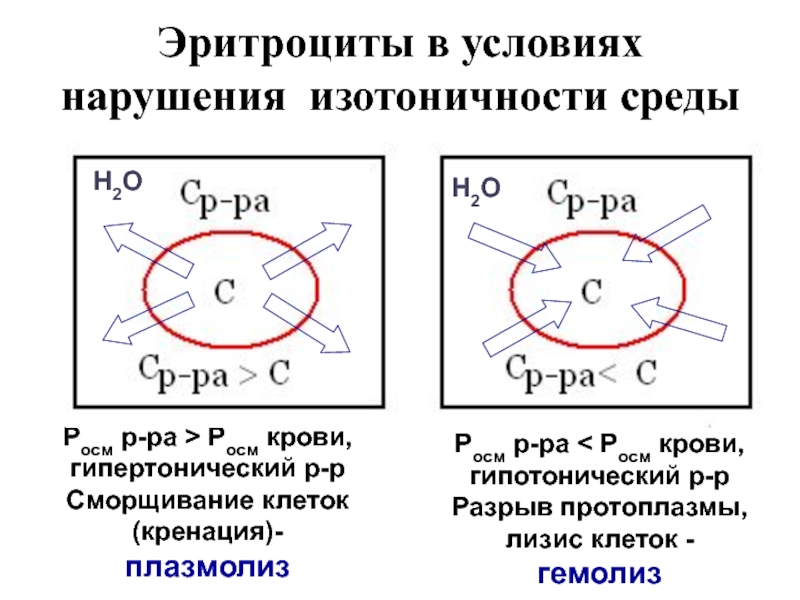
Слайд 32Эритроциты в условиях нарушения изотоничности среды
Росм р-ра > Росм крови,
гипертонический р-р
Сморщивание клеток (кренация)- плазмолиз
Росм р-ра < Росм крови, гипотонический
р-р
Разрыв протоплазмы, лизис клеток - гемолиз
Слайд 33Р-ры, изотоничные плазме крови:
0,85-0,9 % (0,15М) NaCl;
5% (0,3М) С6Н12О6
Вывод:
распределение воды между клетками и внеклеточной жидкостью …
Росм р-ра =
Росм крови - изотонический р-р
Физиол. р-р близок плазме крови не только по Росм , но и по солевому составу, рН, по буферным св-вам.
Слайд 34Распределение жидкости между сосудистым пространством и межтканевой жидкостью.
Стенки капилляров
Слайд 35Онкотическое давление – та часть осмотического давления плазмы крови, которая
обусловлена белками и проявляется на стенках капилляров.
Оно сост. ~
0,5% от общего и равно ~ 0,04 атм
Норма: ток воды внутрь сосудов уравновеш.
противоположным током воды, обусл. гидростат. давлением крови, которое создаётся работой сердца.
Слайд 36дегидратация: обезвоживание организма при
кровопотерях, рвоте, при лихорадке, пневмонии,
применении
мочегонных препаратов и др.
Вывод: Распределение жидкости между сосудистым руслом и
межтканевой жидкостью зависит от соотношения между гидростатическим и онкотическим давлением плазмы крови.
гипергидратация: конц. белка в крови; онкотич. давл.; накопление жидкости в межклеточном пр-ве; онкотические отёки (при голодании; некот. забол. почек)
Патология: равенство нарушается;
вода перераспределяется;
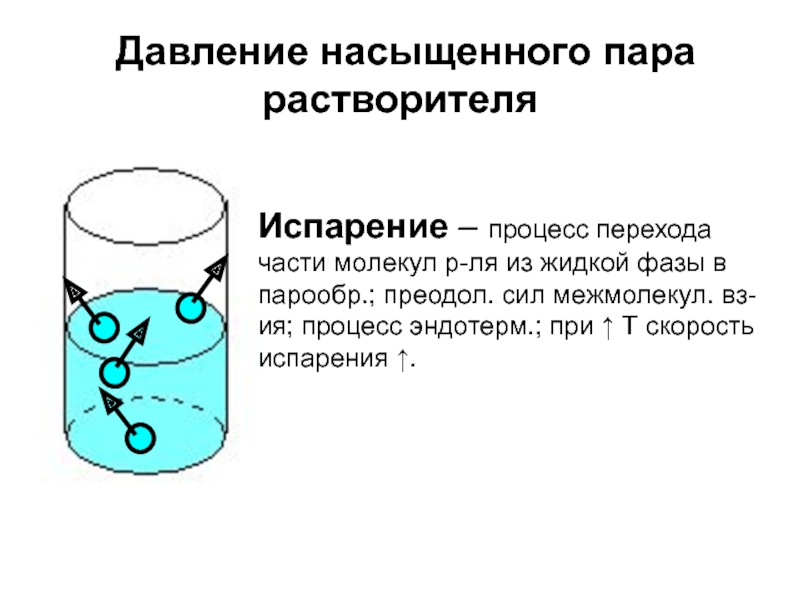
Слайд 37 Давление насыщенного пара растворителя
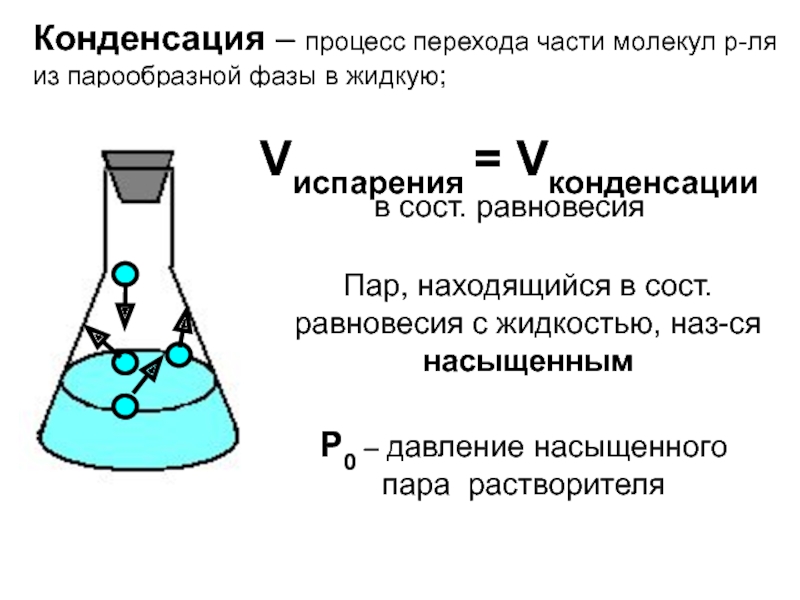
Слайд 38Конденсация – процесс перехода части молекул р-ля
из парообразной фазы
в жидкую;
Пар, находящийся в сост. равновесия с жидкостью, наз-ся насыщенным
Р0
– давление насыщенного пара растворителя
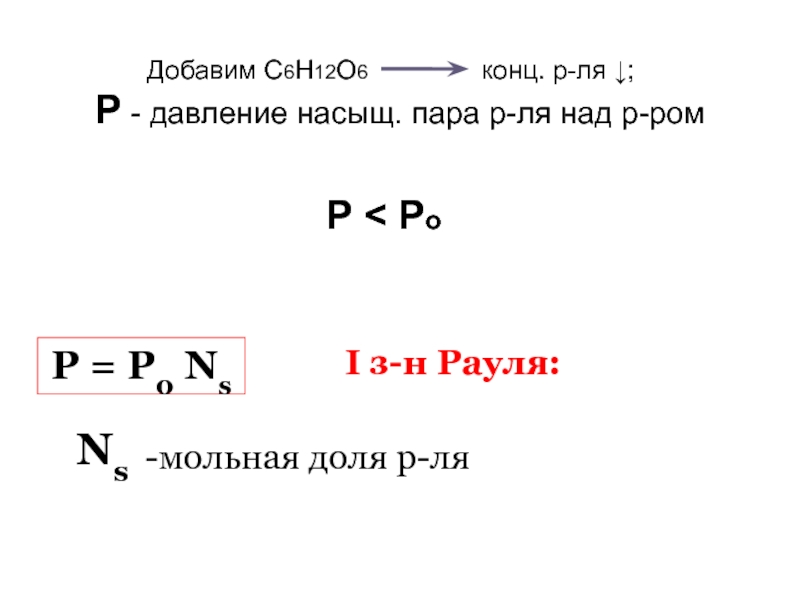
Слайд 40Р0 – Р = ΔР ; ΔР- абсолютное понижение давления
насыщ. пара р-ля над р-ом
NS + Ni= 1,
NS =1- Ni
P= P0(1- Ni) = P0 - P0 Ni; P0 – P = P0 Ni ;
ΔР=Р0 N i
I з-н Рауля:
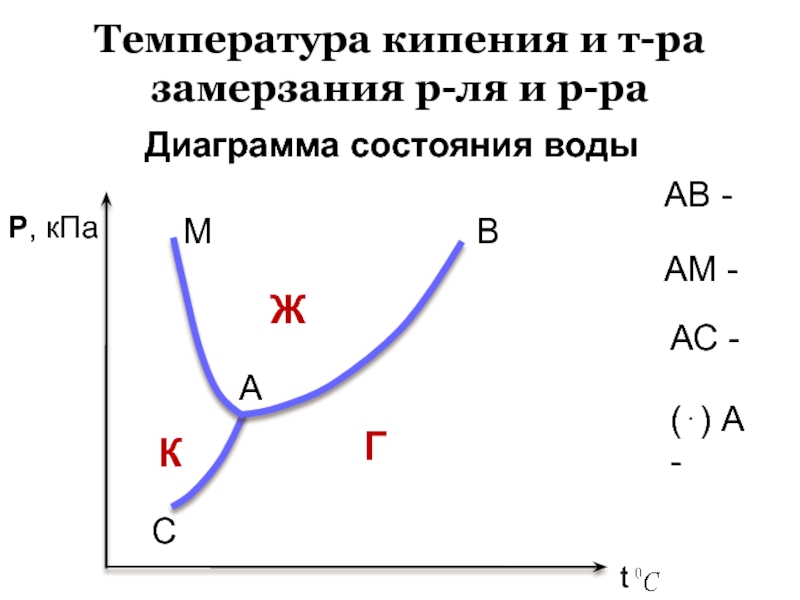
Слайд 41Температура кипения и т-ра замерзания р-ля и р-ра
АВ -
АМ -
АС
-
() А -
Диаграмма состояния воды
М
В
С
А
Ж
Г
К
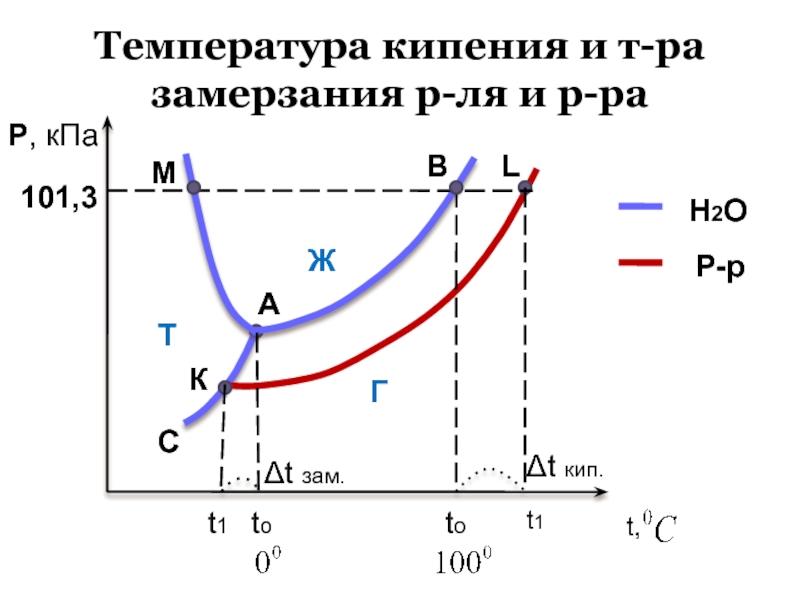
Слайд 42Температура кипения и т-ра замерзания р-ля и р-ра
t,
t зам.
Н2О
Р-р
К
Р,
кПа
to
to
t1
t1
101,3
t кип.
А
С
В
L
М
Слайд 43II закон Рауля (1882) : Повышение tкип. и понижение
tзам. растворов пропорционально моляльности растворенного в-ва.
Е - эбуллиоскопическая постоянная,
К - криоскопическая постоянная,
tкип. =ЕСm , tзам. = KСm
Сm - моляльность раствора,
Для Н2О: Е= 0,53 кгград / моль,
К=1,86 кгград / моль.
Слайд 45Коллигативные свойства разбавленных растворов электролитов
Росм = См R T
P
= P0 Ns
Ткип.= Е Сm
Тзам.= К Сm
Для р-ров неэлектролитов
Слайд 46Для р-ров электролитов
tзам.(оп.) = 3,36
Слайд 47Вант-Гофф ввел изотонический коэффициент – i (i>1), 1887 г.
Тзам.=
i К Сm
Физич. смысл i: показывает во сколько
раз число частиц в р-ре эл-та больше числа
частиц в р-ре неэл-та
Росм = i См R T
P = i P0N0
Ткип.= i Е Сm
Слайд 48СН3СООН СН3СОО- + Н+ ; теор. i=2
практ. i =1,05
KA K+ + A- ; n = 2
N – общее число раств-ных молекул слаб. эл-та
N - число распавшихся молекул
Nn – общее число ионов (кат. и анионов)
(N - N) - число не распавшихся молекул
(Nn + (N - N))–общее число частиц
в р-ре
Слайд 49 i= (n-1) + 1
-количественная характеристика процесса
диссоциации слабых электролитов; = f(c)
Слайд 50[H+] = [CH3COO-] = С
С- исходная молярная концентрация к-ты, моль/л;
С
- число продиссоциировавших молекул;
(С- С) – число непродиссоциировавших молекул;
Слайд 51для слабых эл-тов 0 и (1- ) 1,
тогда
З-н разведения Оствальда (1888 г.)
Слайд 52Теория электролитической диссоциации (ТЭД) эл-тов Аррениуса -это теория слабых эл-тов.
Факторы, влияющие на :
1. природа в-ва
растворителя (дип.
момент, диэлектр. проницаемость)
характер хим. связи в молекуле растворенного в-ва.
2. концентрация вещества ( с С, ↓)
3. температура (с Т, )
4. наличие одноименных ионов
(пр. Ле-Шателье):
Слайд 53 а) НCl, H+, х.р. ,
б) СН3СООNa,
СН3СОО- , х.р. ,
в) NaOH, OH-,
х.р. ,
= f (C, Т)
К дис. зависит:
от природы электролита
от температуры: Т , К дис.
Кдис. ≠ f (C) , поэтому можно сравнивать силу эл-тов. Чем больше Кдис., тем сильнее эл-т.
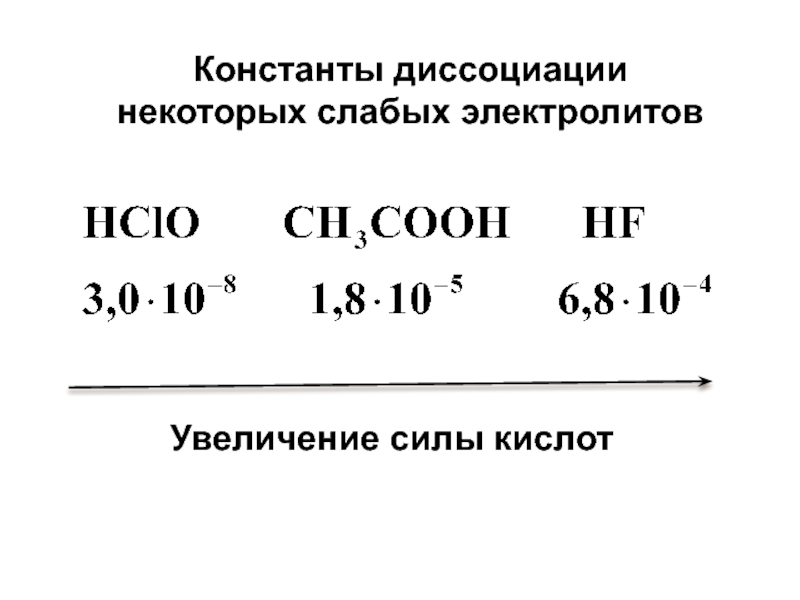
Слайд 54Константы диссоциации
некоторых слабых электролитов
Увеличение силы кислот
Слайд 55Теория сильных электролитов (1923 г, Дебай, Хюккель)
1. Сильные эл-ты в
водных р-рах диссоциируют полностью, т.е. для них = 1
или 100 %. Понятия и Кд к сильным эл-там неприменимы.
2. В растворах ионы за счет сильного ион-дипольного вз-ия с молекулами Н2О окружены гидратными оболочками.
3. Сильное ион-ионное вз-ие создает ионные атмосферы (каждый гидратированный ион окружен гидратированными ионами противоположного заряда).
Слайд 56Для реальных р-ров fa < 1.
В сильно разбавленных
р-рах fa 1.
Активность ( ) –
это та эффективная концентрация сильного эл-та, которая проявляется в хим. р-ях, в коллигативных св-вах, при переносе эл. заряда.
Слайд 57fa зависит от :
концентрации раствора
С , fa
С 0, fa 1
2. природы иона (заряд
и радиус):
Z, fa ;
r, fa , если Z = cоnst;
3. температуры: Т, fa
4. природы растворителя (, )
5. ионной силы раствора (I ): I, fa
Слайд 58Ионная сила раствора (I) - …
для разбавленных р-ров Сm ~
Cм
I биол-их жидкостей, например плазмы крови ~0,15 моль/кг .
Изотонический р-р 0,85% (0,15 М) р-р NaCl , I= 0,15 моль/кг.
Сm (NaCl) = 0,15 моль/ кг
Слайд 59Для разбавленных р-ров, в которых I ≤ 0,01:
Предельный з-н Дебая-Хюккеля
Для
р-ров электролитов одинаковозарядных (MgSO4):
Слайд 60Пример: Определить fa 0,001 М р-ра К2SO4.
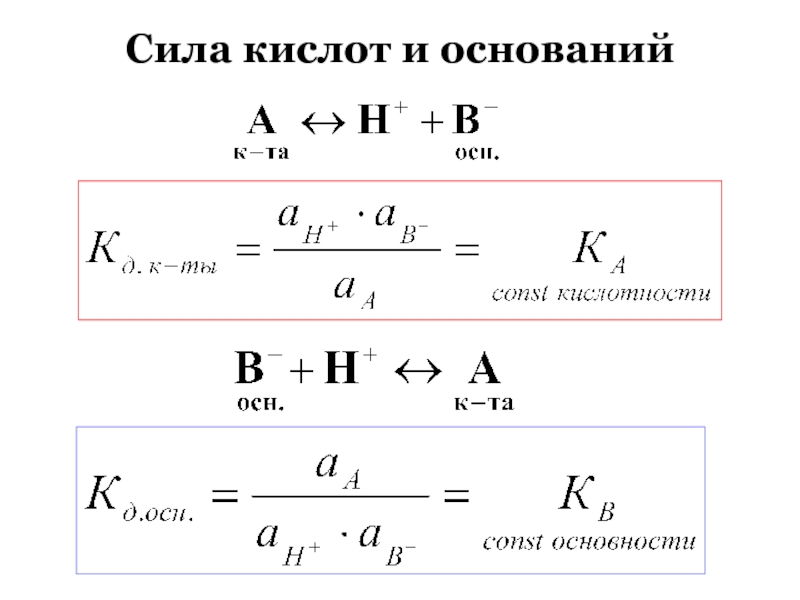
Протонная теория
кислот и оснований.
Теория Бренстеда – Лоури (1923 г.)
Основные положения
:
Кислота - любая частица (молекула, ион) отдающая протон, т.е. донор протонов. Основание – частица, присоединяющая протон, т.е. акцептор протонов.
Слайд 61Классификация кислот и оснований
Кислоты:
нейтральные НCl
H+ + Cl-
анионные HCO3 - H+ + CO3 2 -
катионные NH4+ H+ + NH3
Основания:
нейтральные NH3 + H+ NH4+
анионные Сl- + H+ HCl
катионные H2N – NH2 + H+
H2N – NH3+; N2H5+ + H+ H3N+ – NH3+
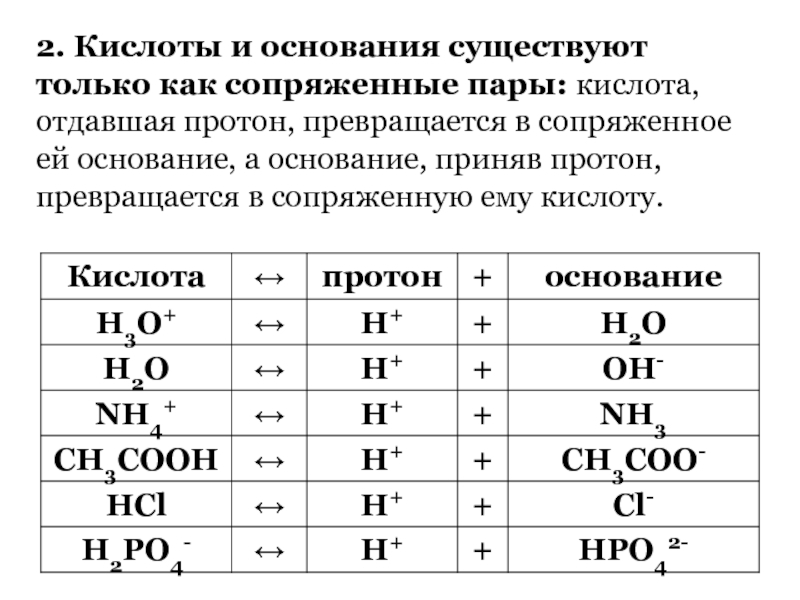
Слайд 622. Кислоты и основания существуют только как сопряженные пары: кислота,
отдавшая протон, превращается в сопряженное ей основание, а основание, приняв
протон, превращается в сопряженную ему кислоту.
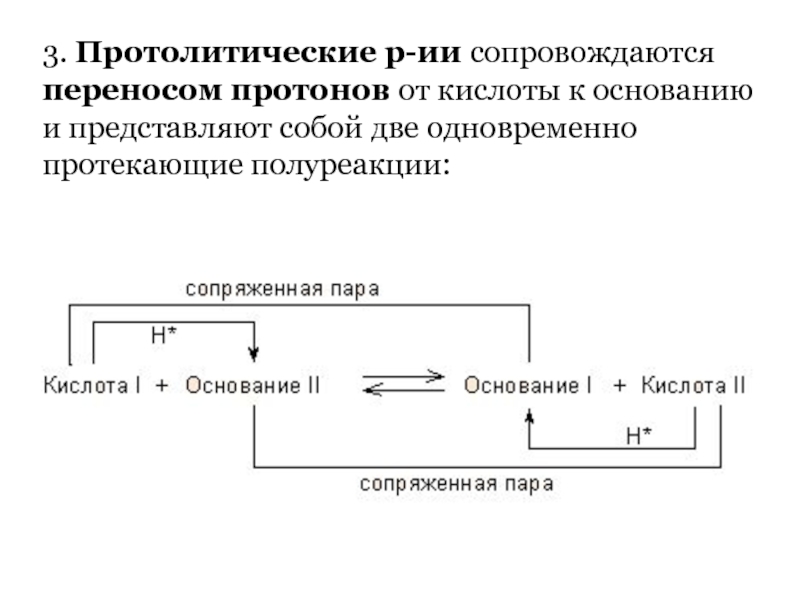
Слайд 633. Протолитические р-ии сопровождаются переносом протонов от кислоты к основанию
и представляют собой две одновременно протекающие полуреакции:
Слайд 64Типы протолитических реакций
1. нейтрализация
2. гидролиз
3. электролитическая диссоциация
Слайд 654.Кислотно-основные св-ва в-во проявляет в конкретной хим. р-ции. В зависимости
от партнера в-ва могут быть амфолитами.
Характеристика воды как амфолита
5. Протон
в водных растворах гидратирован, существует в виде иона –гидроксония Н3О+
Слайд 67Пример: СН4+Н+СН5+ в жестких условиях, но Кв (СН4) >10-20 ,
поэтому метан основанием не считают.
Условно считают, что соединение является
кислотой или основанием если его Ка (Кв ) > 10-20 в данном растворителе.
Слайд 68Классификация растворителей
1. апротонные (нет Н+) : СS2, CCl4 и др.
амфипротонные
(Н2О)
2. протолитические :
протогенные – отдают Н+
(Н2SO4, CH3COOH)
протофильные
- присоединяют Н+
(NH3 жидкий)
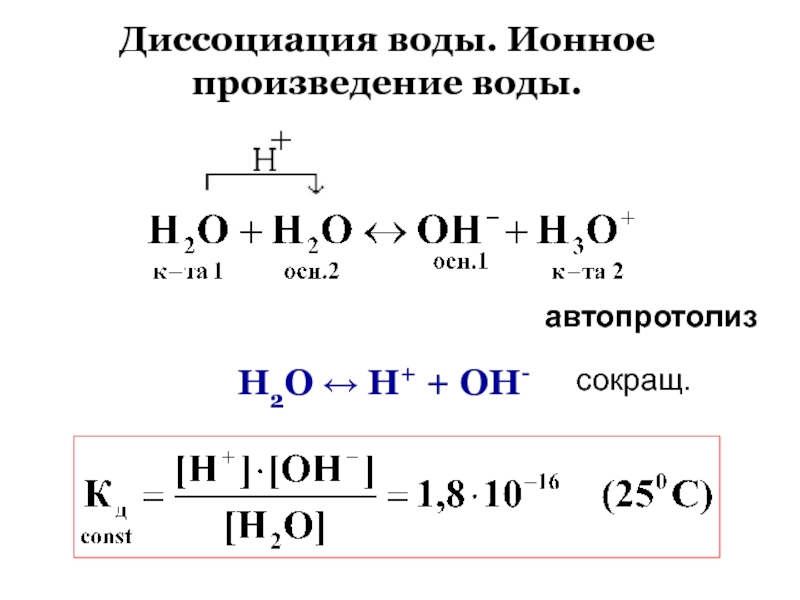
Слайд 69Диссоциация воды. Ионное произведение воды.
Н2О Н+ + ОН-
автопротолиз
сокращ.
Слайд 70(Н2О) =1,8 10-9 , это значит, что из
50 000 000
молекул распадается - 1
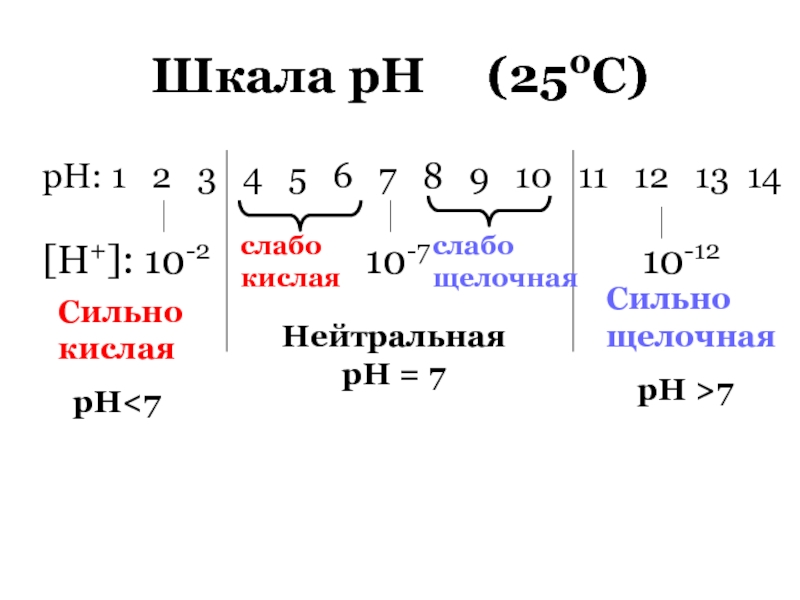
Слайд 72Водородный показатель (рН)
1909 г. Серенсен
Слайд 74Расчет рН растворов
I. Сильных кислот и оснований fa
1
Слайд 76Если неизвестно:
[СН3СОО-]=[Н+]
Слайд 77Кислотность биологических жидкостей
Общая кислотность – соответствует общей конц. сильных
и слабых к-т; опр-ся м. объёмного анализа – м. титрования
Потенциальная
кислотность - равна конц. непродиссоциировавших молекул слабых к-т и рассчит-ся по разности общей и активной кислотностей
Биол. жидк. содержат к-ты:
соляную
угольную
пировиноградную
молочную и др.
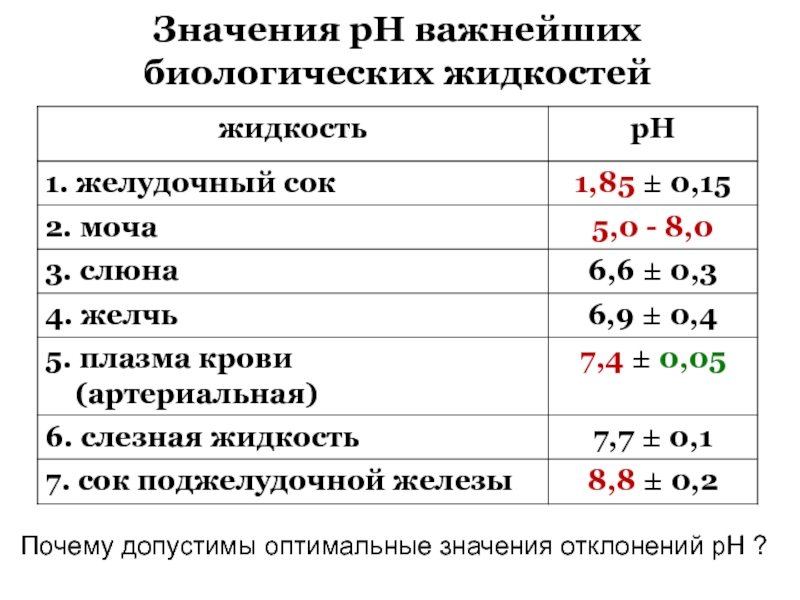
Слайд 78Значения рН важнейших биологических жидкостей
Почему допустимы оптимальные значения отклонений рН
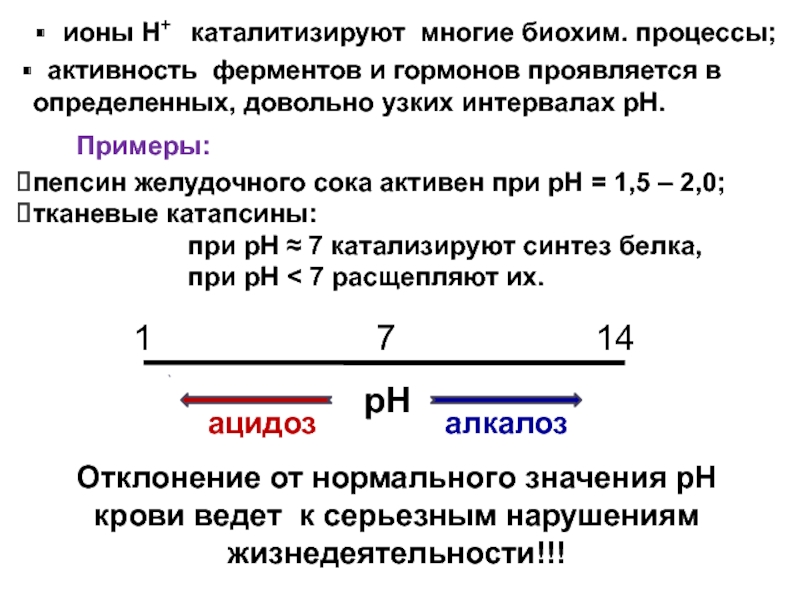
Слайд 79ионы Н+ каталитизируют многие биохим. процессы;
тканевые катапсины:
при
рН 7 катализируют синтез белка,
при рН < 7 расщепляют их.
Отклонение от нормального значения рН крови ведет к серьезным нарушениям жизнедеятельности!!!
активность ферментов и гормонов проявляется в определенных, довольно узких интервалах рН.
пепсин желудочного сока активен при рН = 1,5 – 2,0;
Примеры:
Слайд 80физиологические – это процессы метаболизма, дыхания и мочевыделения
Защитные мех-мы
поддержания
постоянства рН:
физико-химические мех-мы регуляции кислотно-основного равновесия в организме с
помощью буферных систем организма.
В результате процессов метаболизма
в организме человека ежесуточно образуется к-во к-ты, эквивалентное 2,5 л НСl (конц.)
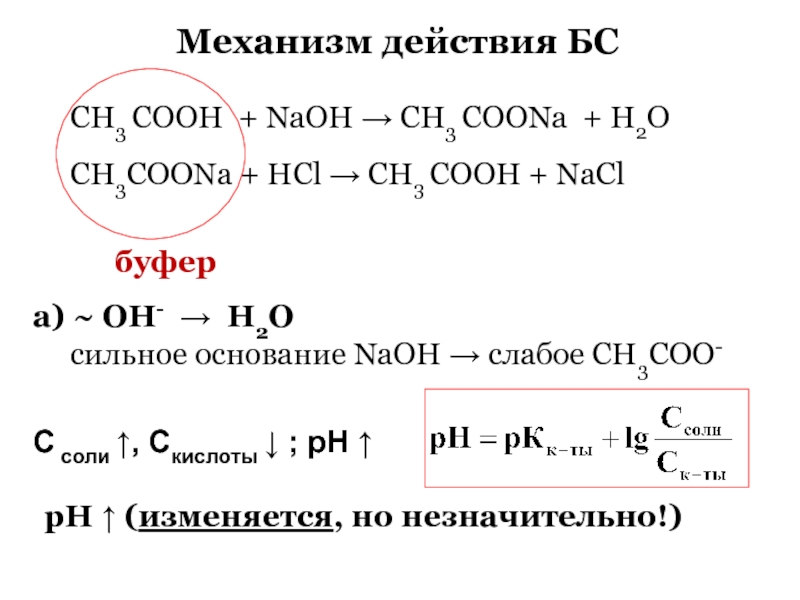
Слайд 81Буферные системы (бс)
Бс – это с-мы, которые сохраняют постоянство значения
рН при добавлении небольших количеств
сильных кислот и оснований, а
также при разведении.
Слайд 82Классификация бс
I. кислотные:
ацетатная: СН3СООН + СН3СООNa
гидрокарбонатная
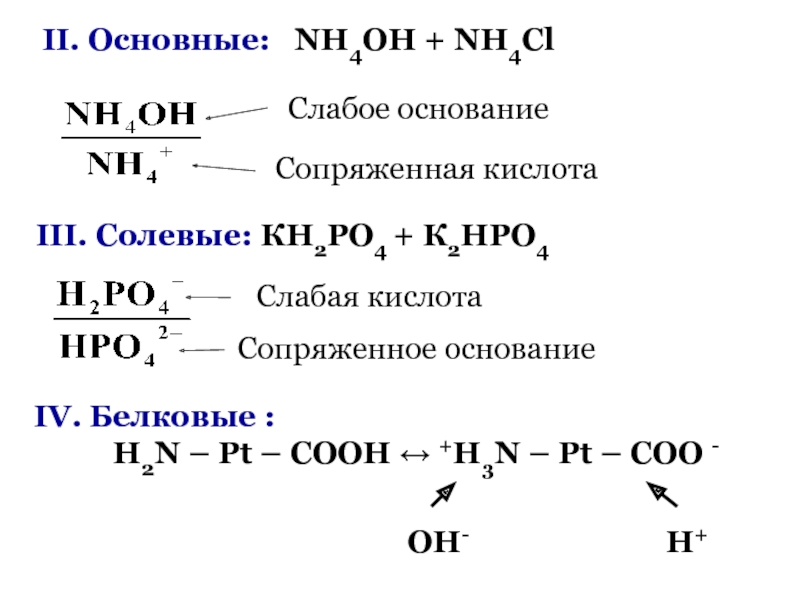
Слайд 83II. Основные: NH4OH + NH4Cl
III. Солевые: КН2РО4 + К2НРО4
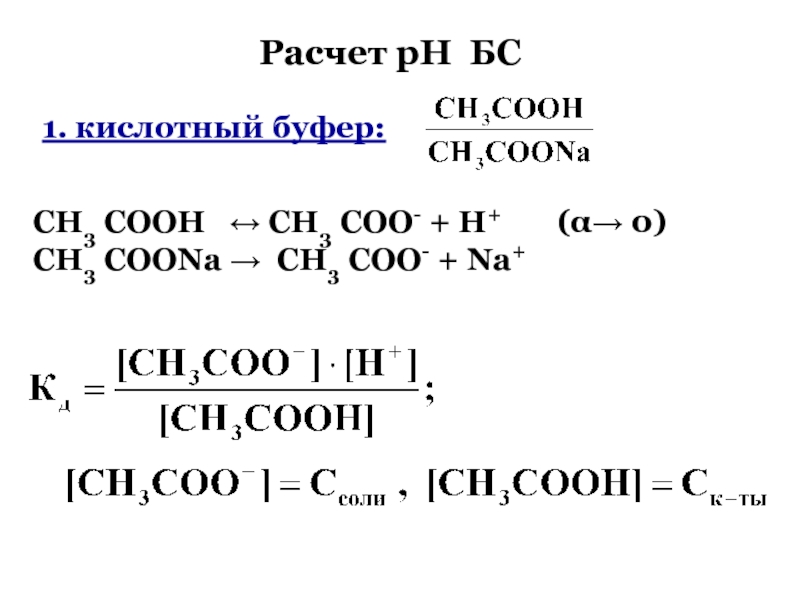
Слайд 84Расчет рН бс
СН3 СООН СН3 СОО- +
Н+ ( 0)
СН3 СООNa СН3 СОО-
+ Na+
Слайд 85ур-ие Гендерсона-Гассельбал(ь)ха
Слайд 86БС устойчиво поддерживает рН р-ра в пределах:
рН = рК
1 для кислот;
рН= 14 - (рК 1) для
оснований
Пример: рН плазмы крови = 7,4 ;
рК СН3СООН = 4,75, рК Н2РО4- = 6,8
Слайд 87 рН БС зависит:
от величины рК (т.е. от Кд),
а следовательно и от Т, т.к. Кд= f (Т)
от
соотношения концентраций компонентов;
рН БС не зависит от разбавления, т.к. Кд остаётся const
Кд ≠ f (С)
Слайд 88Механизм действия БС
а) ~ OH- Н2О
сильное основание NaOH слабое СН3СОО-
рН (изменяется, но
незначительно!)
С соли , Скислоты ; рН
Слайд 89б) ~Н+ в слабую СН3 СООН
Вывод: В БС кислотный компонент
нейтрализует щелочь, а основной компонент нейтрализует сильную кислоту, поэтому рН
БС практически не изменяется.
Скислоты , С соли ; рН (незначительно!)
Слайд 90Буферная емкость (БЕ)
БЕ – это к-во экв-тов ионов Н+ или
ОН-, которые надо добавить к 1 л буферного р-ра, чтобы
изменить его рН на единицу
Слайд 91БЕ зависит:
от абсолютных зн-ний конц-ии компонентов
(влияет разбавление).
от соотношения концентраций компонентов
Буф. р-ры с
равными концентрациями компонентов хар-ся max устойчивостью рН
При разбавлении р-ра БЕ уменьшается!
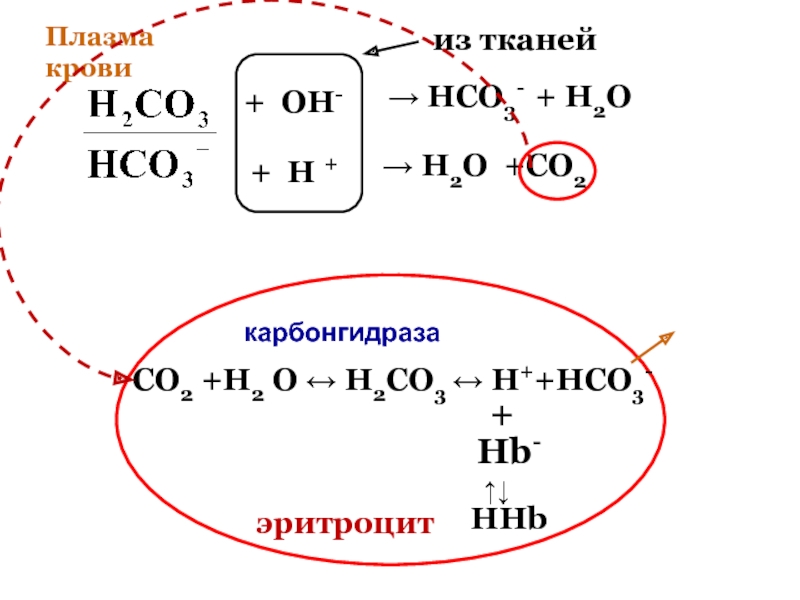
Слайд 92Буферные системы крови
Пределы изменения рН крови совместимые с жизнью
БС нейтрализуют
значит. часть кислот и оснований, поступ. в кровь.
Слайд 934. Гемоглобиновая буферная система
HHb + O2 HHbO2
Гемоглобиновый буфер
HHb
+ OH - Hb - + H2O
Hb - +
H + HHb
Оксигемоглобиновый буфер
HHbO2 + OH - HbO2 - + H2O
HbO2- + H + HHbO2
Слайд 94БС вносят различный вклад в БЕ крови.
Гидрокарбонатная БС основная –
53 % БЕ крови
Гемогл. БС эффективно функционирует в сочетании
с
гидрокарбонатной
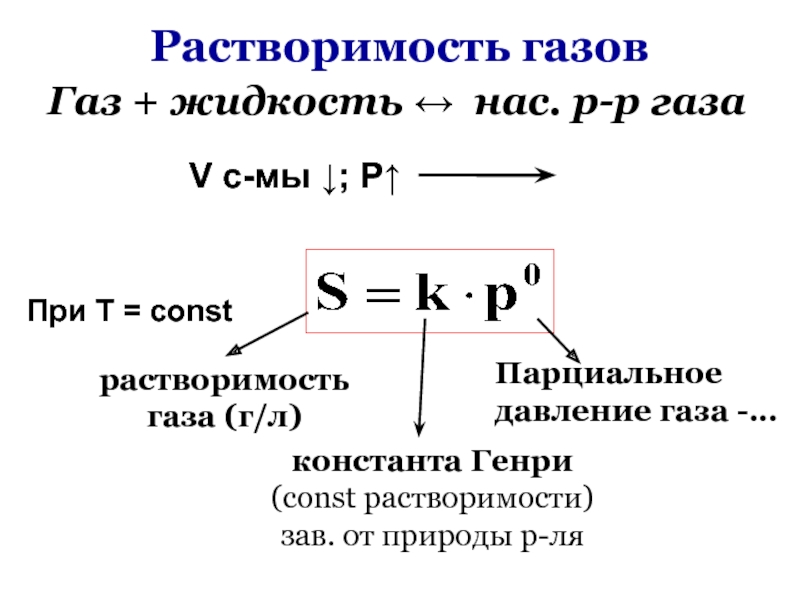
Слайд 96Растворимость газов
Газ + жидкость нас. р-р газа
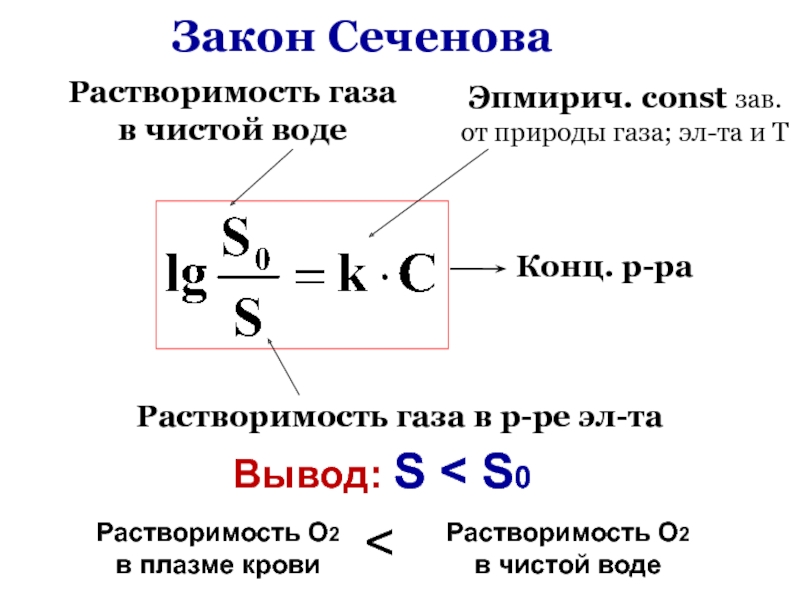
Слайд 98На глубине Р
растворимость
О2 в крови
Кессонная болезнь – мгновенное
выделение газов из плазмы крови
за счёт резкого растворимости из-за Р.
Пузырьки выд-ся газа могут вызвать закупорку
сосудов.
Горная болезнь – разряженная атмосфера и связанное с этим содержания О2 в крови из-за растворимости





































![Учение о растворах [H+] = [CH3COO-] = СС- исходная молярная концентрация к-ты, моль/л;С - [H+] = [CH3COO-] = СС- исходная молярная концентрация к-ты, моль/л;С - число продиссоциировавших молекул;(С- С) – число](/img/thumbs/6af3046e0bfd1b40d9e0f18ef13aeba8-800x.jpg)



















![Учение о растворах Если неизвестно:[СН3СОО-]=[Н+] Если неизвестно:[СН3СОО-]=[Н+]](/img/thumbs/de202eee6eb47bfedea707d30bd7e87d-800x.jpg)