Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
углеводороды
Содержание
- 1. углеводороды
- 2. Углерод и кремний являются важнейшими элементами природы.
- 3. Слова «организм» и «органический» имеют один корень.
- 4. Когда учёные научились определять химический состав веществ,
- 5. Органические вещества.
- 6. Слайд 6
- 7. Раздел химии, изучающий строение, свойства, превращения, способы
- 8. В молекуле простейшего органического вещества — метана
- 9. Выдающийся русский химик А. М. Бутлеров назвал
- 10. Бутлеров Александр Михайлович(1828—1886) Русский химик, профессор
- 11. этанБлижайший «родственник» метана — этан имеет формулу
- 12. Метан и этан — представители углеводородов —
- 13. МЕТАНЭТАН
- 14. Этилен (непредельный углеводород)Кроме предельных углеводородов, есть и
- 15. Нетрудно заметить, что молекула этого соединения содержит
- 16. Для предельных углеводородов характерны реакции замещения. Например,
- 17. Для непредельных углеводородов характерны ре акции присоединения
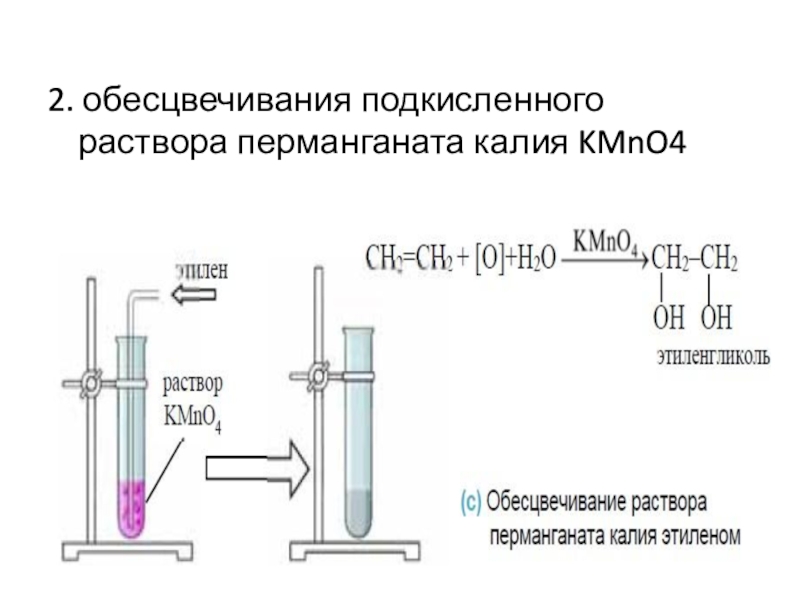
- 18. 2. обесцвечивания подкисленного раствора перманганата калия KMnO4
- 19. Предельные углеводороды — это не только топливо,
- 20. Своё название полиэтилен получил потому, что является
- 21. Природными источниками углеводородов являются природный газ, нефть
- 22. Также одним из основных источников углеводородов является
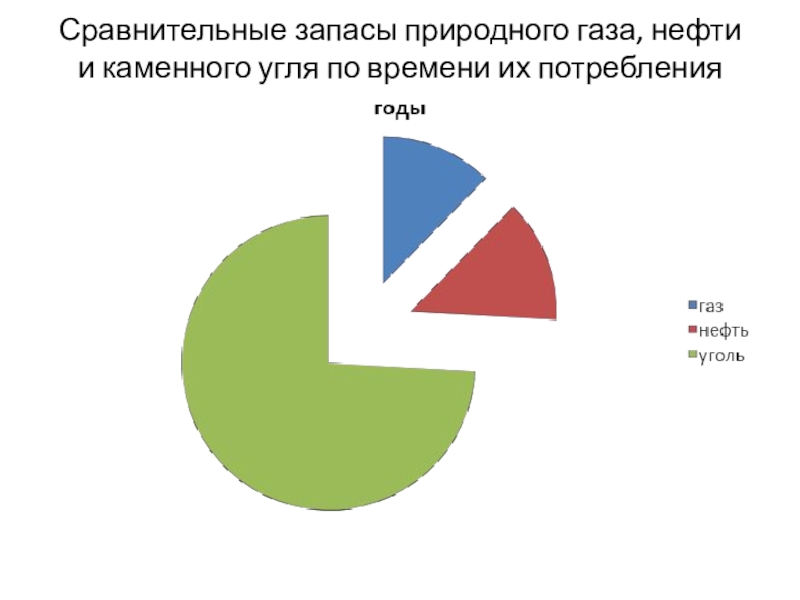
- 23. Сравнительные запасы природного газа, нефти и каменного угля по времени их потребления
- 24. Использование каменного угля в качестве сырья основано
- 25. аммиачную воду, содержащую кроме растворённого аммиака, также фенол и некоторые другие вещества
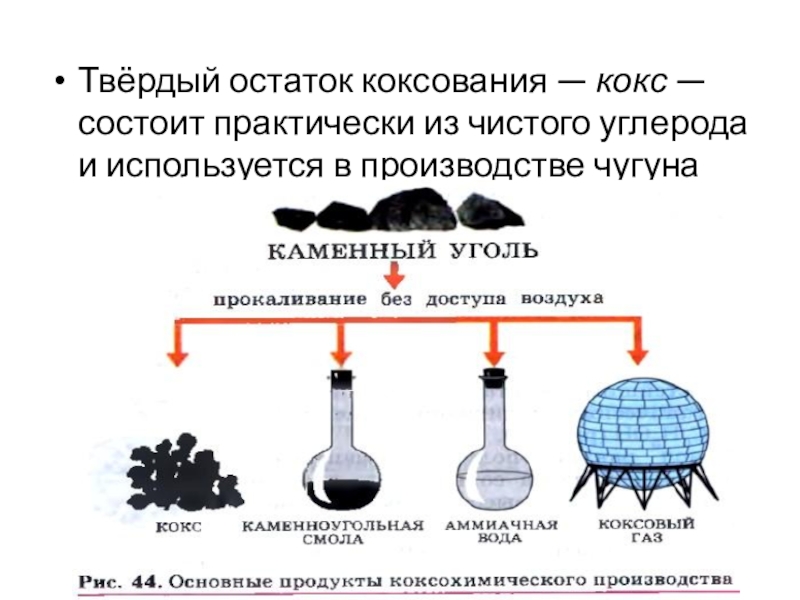
- 26. Твёрдый остаток коксования — кокс — состоит
- 27. Продажа излишков углеводородов позволяет России участвовать в
- 28. Домашнее задание (ответить на вопросы)1. Назовите области
- 29. Скачать презентанцию
Углерод и кремний являются важнейшими элементами природы. Углерод — главный элемент живой природы. Кремний, наряду с кислородом, образует почти 4/5 массы литосферы и составляет основу неживой природы.
Слайды и текст этой презентации
Слайд 3Слова «организм» и «органический» имеют один корень. Около 200 лет назад
выдающийся шведский химик Й. Я. Берцелиус предложил называть вещества растительного и животного
происхождения органическими соединениями.Слайд 4Когда учёные научились определять химический состав веществ, они обнаружили, что
в молекулах любых органических соединений, не только природных, но и искусственных,
и синтетических, обязательно содержатся атомы углерода (схема 1). С тех пор ми веществами стали называть все соединения углерода, кроме тех, с которыми вы познакомились раньше, в курсе неорганической химии.Слайд 7Раздел химии, изучающий строение, свойства, превращения, способы получения и области применения органических
веществ, называют
органической химией.
Слайд 8В молекуле простейшего органического вещества — метана СН4 атом углерода
четырёхвалентен, а валентность атома водорода, как и в любых других органических
веществах, равна единице.Слайд 9Выдающийся русский химик А. М. Бутлеров назвал химическим строением порядок соединения
атомов в молекулах согласно их валентности. Теория химического строения А. М. Бутлерова
сыграла в органической химии такую же огромную роль, как Периодический закон Д. И. Менделеева в неорганической химии.Слайд 10Бутлеров Александр Михайлович(1828—1886)
Русский химик, профессор Казанского университета (1857—1868),
с 1869
по 1885 г. — про фес сор Петербургско го уни
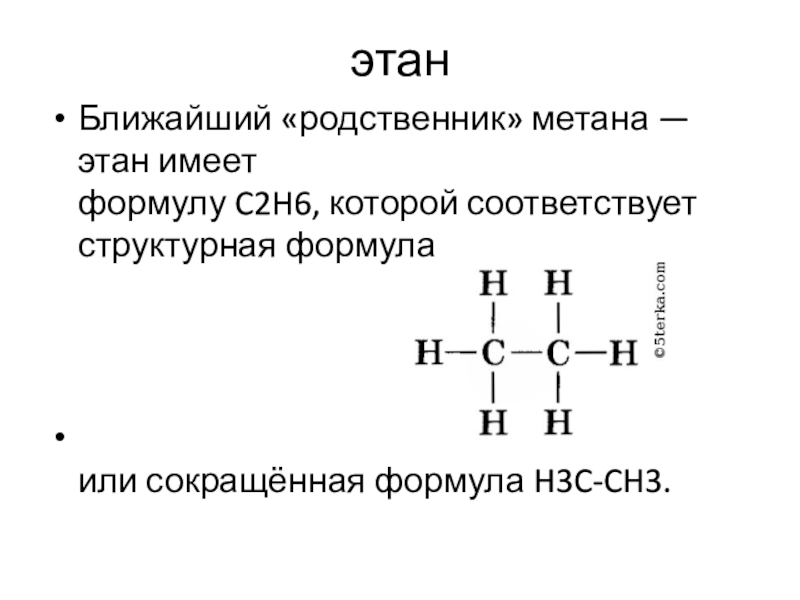
вер си те та. Ака демик Пе тер бург ской ака де мии на ук (с 1874 г.). Со зда тель те ории хи ми ческо го стро ения ор га ни че ских со еди нений (1861). Пред ска зал и изу чил изоме рию мно гих ор га ни че ских со еди нений. Син те зи ро вал мно гие ве ще ст ва.Слайд 11этан
Ближайший «родственник» метана — этан имеет
формулу C2H6, которой соответствует структурная
формула
или сокращённая формула H3C-CH3.
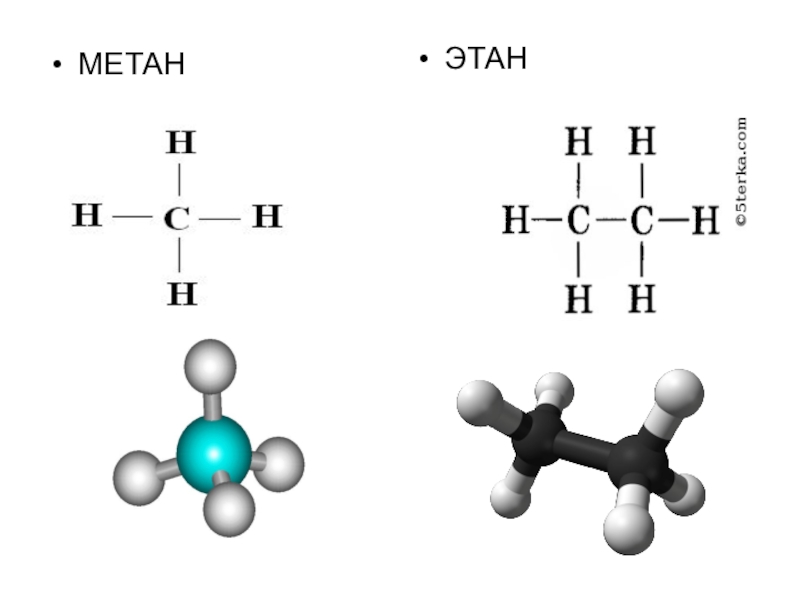
Слайд 12Метан и этан — представители углеводородов — органических соединений, построенных
двумя химическими элементами: углеродом и водородом. В молекулах метана и этана
атомы углерода имеют простые (одинарные) связи, которые соединены с максимально возможным числом атомов водорода, т. е. насыщены ими до предела. Поэтому такие углеводороды называют насыщенными или предельными. Метан и этан — основные компоненты природного газа.Слайд 14Этилен (непредельный углеводород)
Кроме предельных углеводородов, есть и непредельные, молекулы которых
содержат кратные (двойные или тройные) химические связи. Простейшим представителем непредельных углеводородов
является этилен C2H4.Слайд 15Нетрудно заметить, что молекула этого соединения содержит на два атома
водорода меньше, чем молекула
этана, и имеет двойную связь.
Сокращённая структурная
формула этилена CH2-CH2. Этилен получают дегидрированием этана:
– H2
C2 H6 ⎯⎯⎯→C2H4
Слайд 16Для предельных углеводородов характерны реакции замещения.
Например, атомы водорода в
молекуле метана можно последовательно заместить на атомы галогенов, например хлора:
CH4 + Cl2 CH3Cl + HCl,хлорметан CH3Cl + Cl2 CH2Cl2 + HCl,
дихлорметан CH2Cl2 + Cl2 CHCl3 + HCl,
трихлорметан CHCl3 + Cl2 CCl4 + HCl. тетрахлорметан
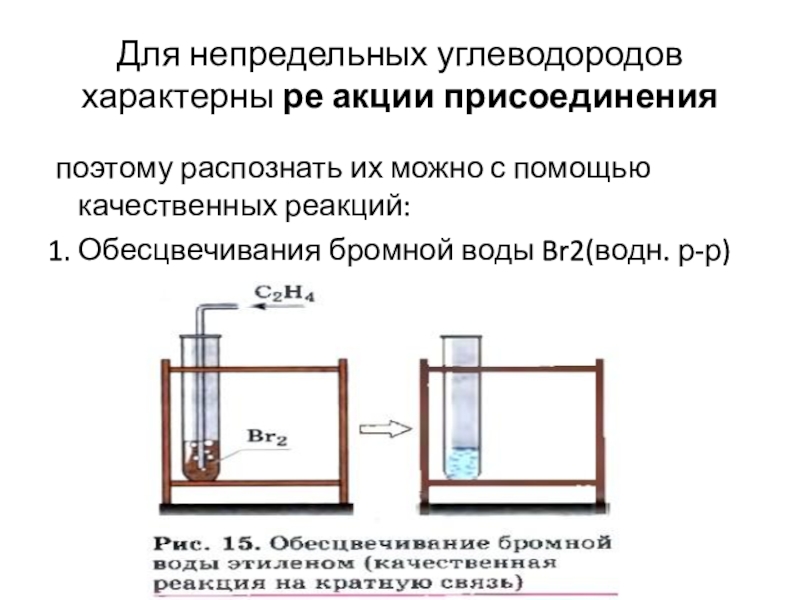
Слайд 17Для непредельных углеводородов характерны ре акции присоединения
поэтому распознать их
можно с помощью качественных реакций:
1. Обесцвечивания бромной воды Br2(водн.
р-р)
Слайд 19Предельные углеводороды — это не только топливо, но и ценное
химическое сырьё. Так, из этана получают ценный продукт этилен, а
из этилена реакцией полимеризации — всем известный полиэтилен.Реакция полимеризации является особым случаем реакции присоединения. Полимеризацию этилена отражает следующая схема:
... + CH2=CH2 + CH2=CH2 + ... ⎯⎯⎯ p t , → ⎯⎯→ ... -CH2-CH2-CH2-CH2- ... или в сокращённом виде:
nCH2=CH2 ⎯⎯⎯ p t , → ( -CH2-CH2- )n. этилен полиэтилен
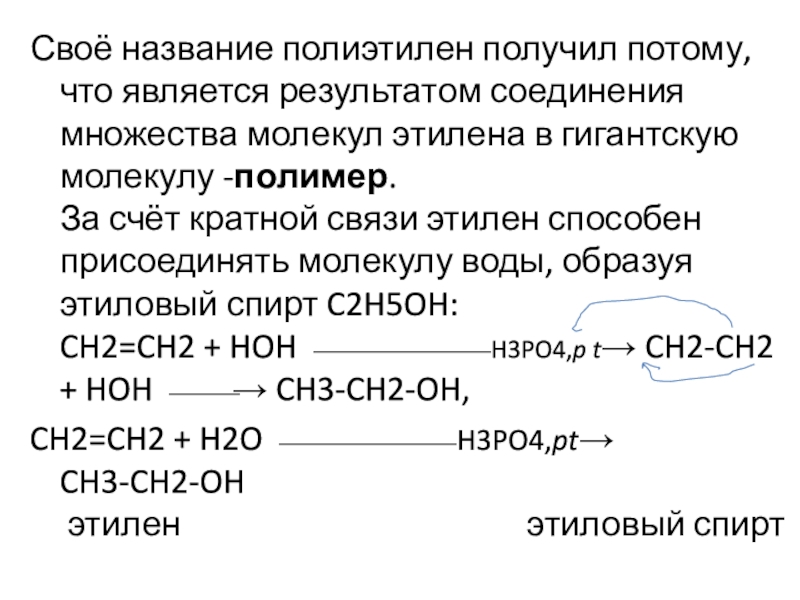
Слайд 20Своё название полиэтилен получил потому, что является результатом соединения множества
молекул этилена в гигантскую молекулу -полимер. За счёт кратной связи этилен
способен присоединять молекулу воды, образуя этиловый спирт C2H5OH: CH2=CH2 + HOH ⎯⎯⎯⎯⎯ H3PO4,p t→ CH2-CH2 + HOH ⎯⎯→ CH3-CH2-OH,CH2=CH2 + H2O ⎯⎯⎯⎯⎯ H3PO4,pt→ CH3-CH2-OH этилен этиловый спирт
Слайд 21Природными источниками углеводородов являются природный газ, нефть и уголь. Из нефти
путём её переработки получают нефтепродукты: бензин, керосин, лигроин, газойль и
мазут. И нефть, и природный газ — сырьё для производства пластмасс, искусственных волокон и кожи, синтетического каучука, моющих средств, высших спиртов и др.Слайд 22Также одним из основных источников углеводородов является каменный уголь, который у
вас ассоциируется с твёрдым топливом. Каменный уголь представляет собой окаменелые остатки
доисторических растений. Наряду с природным газом и нефтью, он является ценным сырьём для химической промышленности. Запасы каменного угля на планете значительно превышают запасы газа и нефти, (поэтому химические производства, основанные на переработке угля, имеют большое будущее.Слайд 24Использование каменного угля в качестве сырья основано на коксовании — нагревании
без доступа воздуха при температуре около 1000 °С в специальных
установках, называемых коксовыми батареями.В результате этого процесса получают: коксовый газ, состоящий преимущественно из метана; каменноугольную смолу, содержащую несколько сотен различных органических соединений, в том числе бензол, фенол и др.;
Слайд 25аммиачную воду, содержащую кроме растворённого аммиака, также фенол и некоторые
другие вещества
Слайд 26Твёрдый остаток коксования — кокс — состоит практически из чистого
углерода и используется в производстве чугуна
Слайд 27Продажа излишков углеводородов позволяет России участвовать в международном разделении труда и
служит важнейшим источником пополнения государственного бюджета страны.
Слайд 28Домашнее задание (ответить на вопросы)
1. Назовите области применения полиэтилена. В
случае затруд нения обратитесь к Интернету.
2. Рассчитайте массовые доли углерода
в молекулах этана
и этилена. Как массовая доля углерода в этих соединениях
влияет на характер пламени при их горении?3. Как распознать газообразные этан и этилен? Назовите два способа.
4. Почему метан и этан горят бесцветным пламенем, а этилен — светящимся?
5. Подготовьте сообщение о способах транспортировки углеводородного сырья и его значении для международной кооперации.