Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
УМКД БИОХИМИЯ Факультет физической культуры и спорта Направление - 032100
Содержание
- 1. УМКД БИОХИМИЯ Факультет физической культуры и спорта Направление - 032100
- 2. БИБЛИОГРАФИЧЕСКИЙ СПИСОКОсновной Биохимия. Учебник для институтов физической
- 3. ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ Федеральное государственное образовательное
- 4. Содержание:ЧАСТЬ 1. СТАТИЧЕСКАЯ БИОХИМИЯСтроение, свойства, биологическая роль
- 5. Содержание:ЧАСТЬ 2. ДИНАМИЧЕСКАЯ БИОХИМИЯ Переваривание углеводов в
- 6. СПОРТИВНАЯ БИОХИМИЯСодержаниеЧАСТЬ 3. СПОРТИВНАЯ БИОХИМИЯТема 11. Биохимия
- 7. Биохимия – наука о молекулярных основах жизниБиохимия
- 8. ЧАСТЬ 1. СТАТИЧЕСКАЯ БИОХИМИЯ- Строение, свойства, биологическая
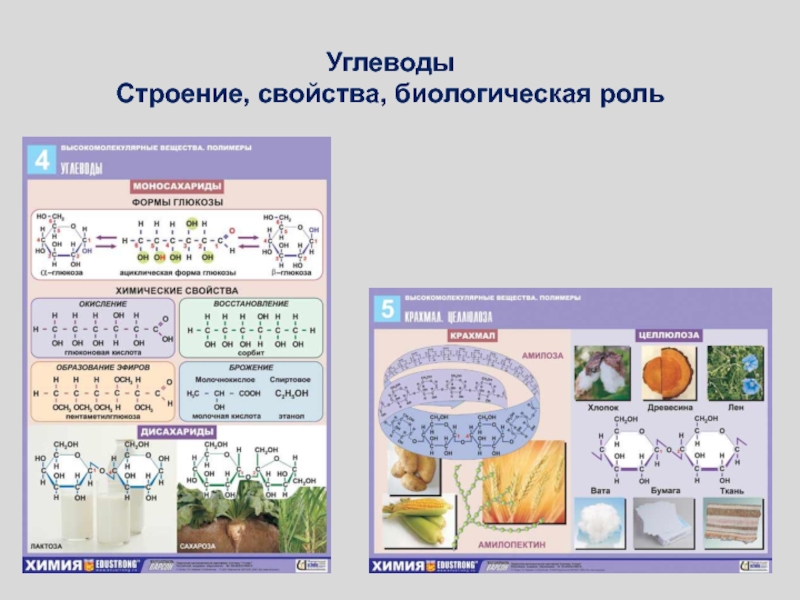
- 9. УглеводыСтроение, свойства, биологическая роль
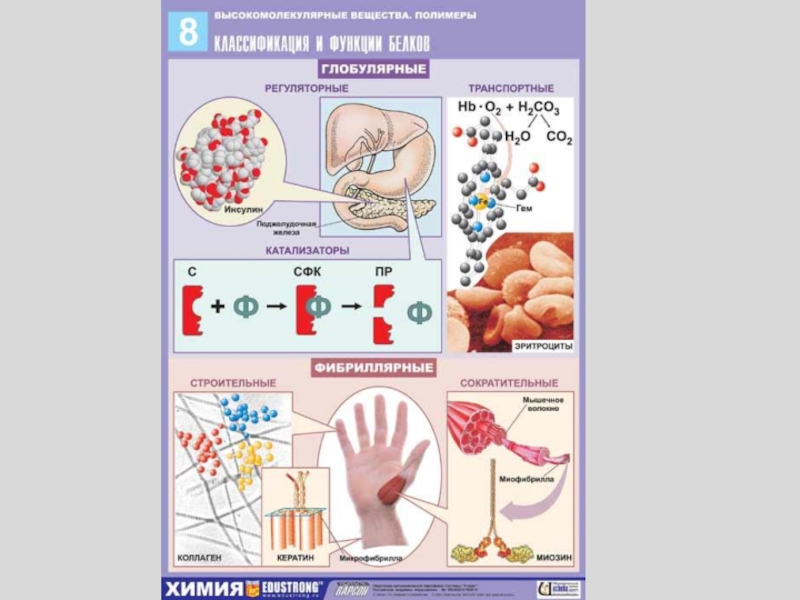
- 10. Биологические функции углеводов Энергетическая функция (главный вид
- 11. Слайд 11
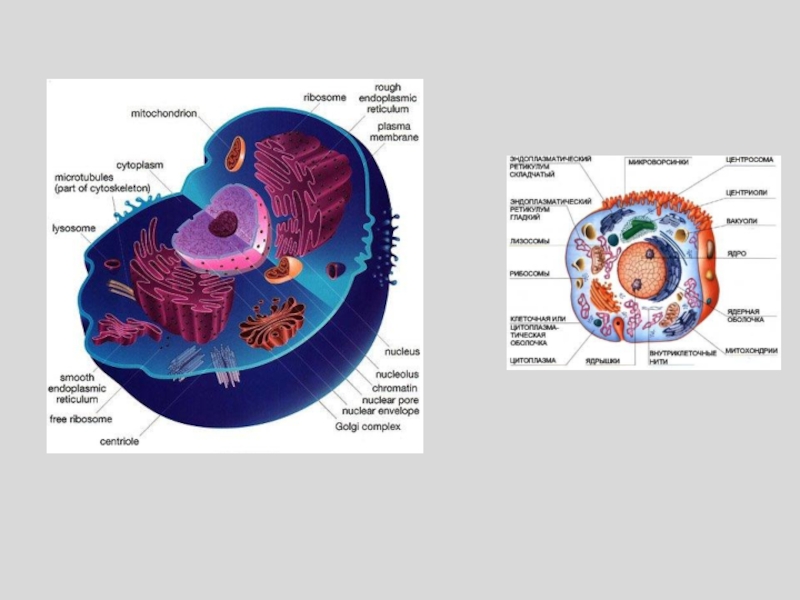
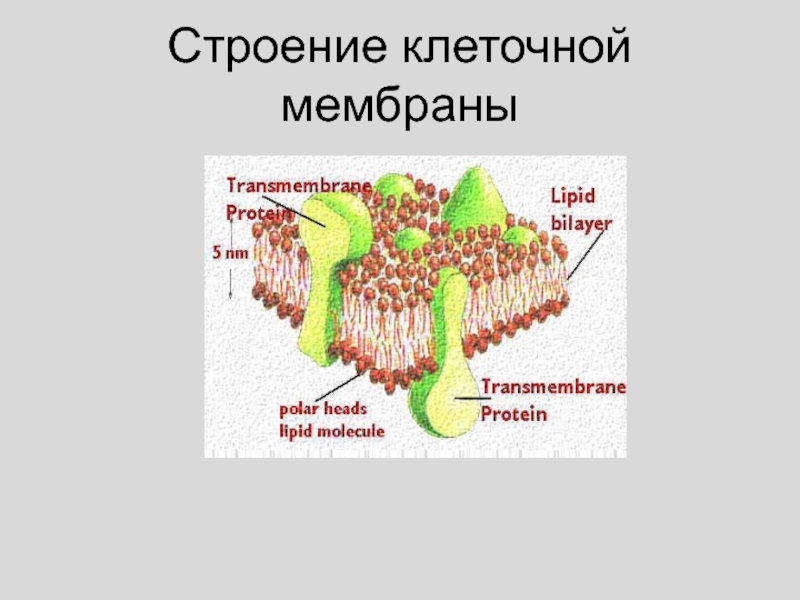
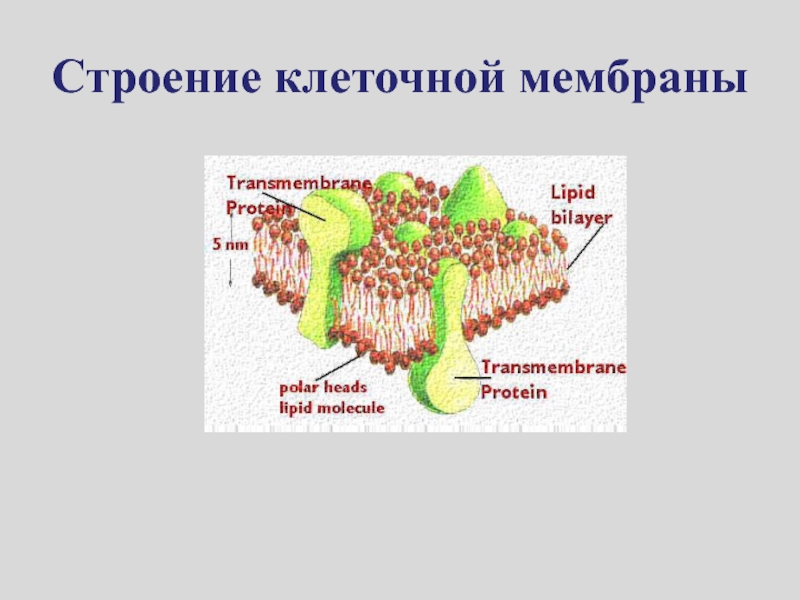
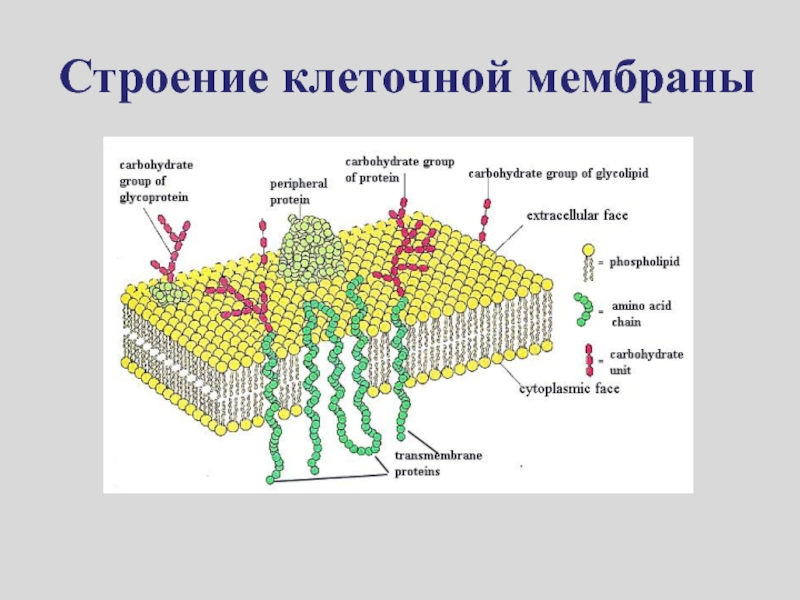
- 12. Строение клеточной мембраны
- 13. Слайд 13
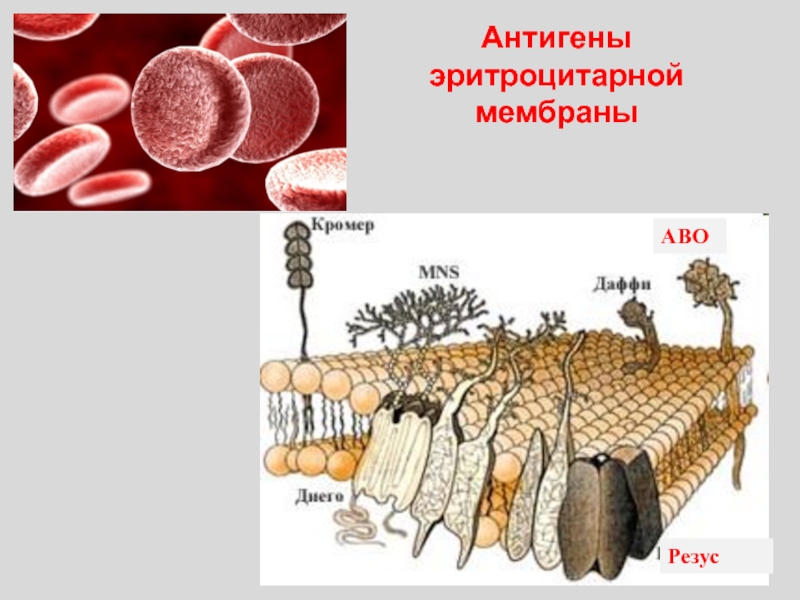
- 14. Антигены эритроцитарной мембраны
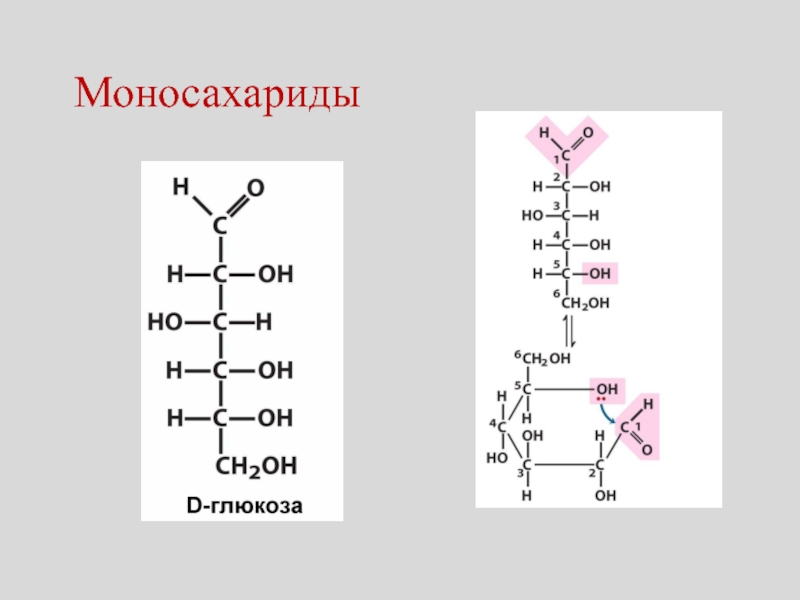
- 15. Моносахариды
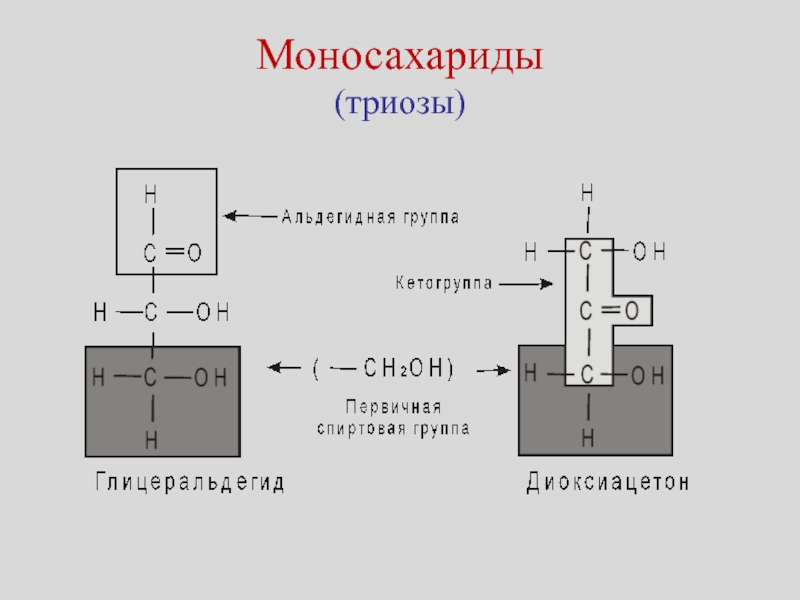
- 16. Моносахариды (триозы)
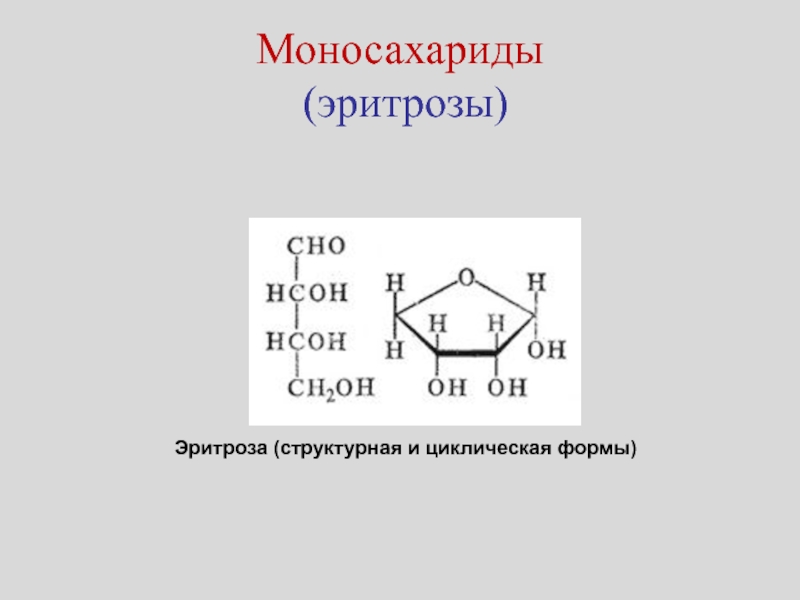
- 17. Эритроза (структурная и циклическая формы)Моносахариды (эритрозы)
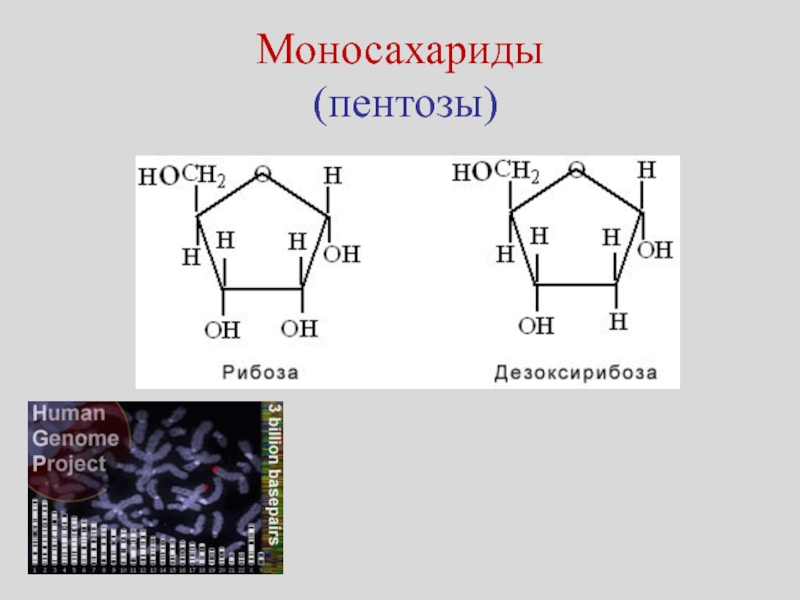
- 18. Моносахариды (пентозы)
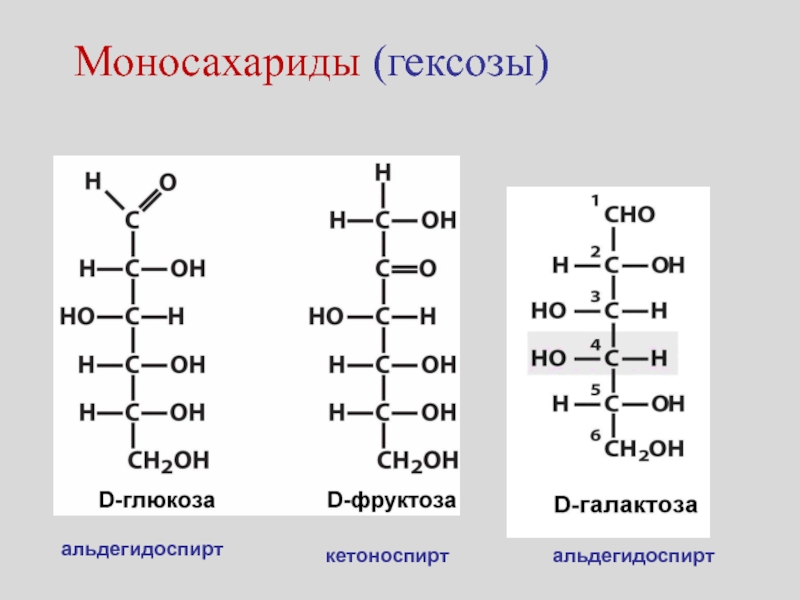
- 19. Моносахариды (гексозы)альдегидоспирткетоноспиртальдегидоспирт
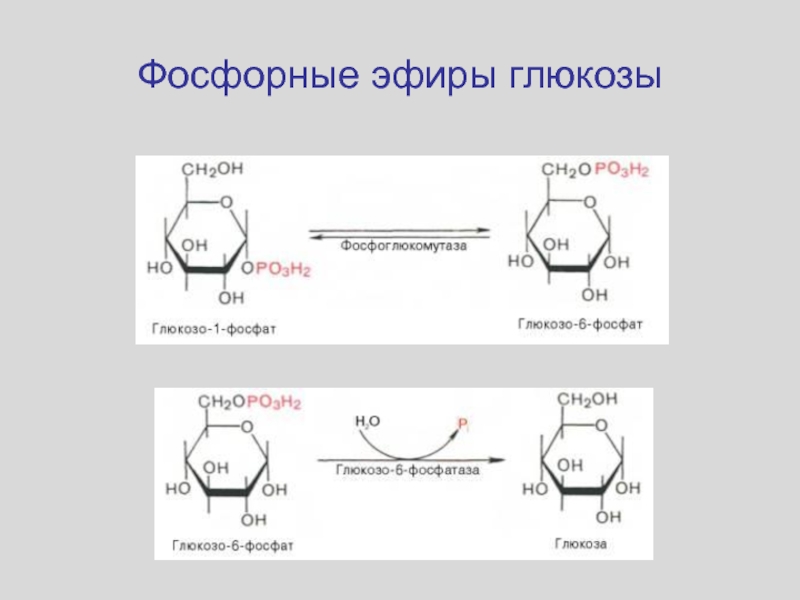
- 20. Фосфорные эфиры глюкозы
- 21. Глюкоза + Глюкоза = МальтозаГлюкоза + Галактоза = ЛактозаГлюкоза + Фруктоза = СахарозаОлигосахариды
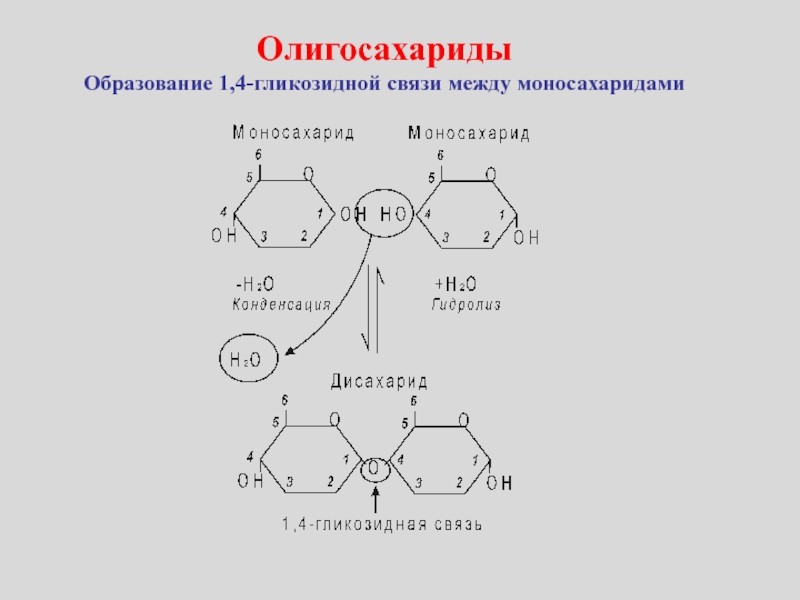
- 22. ОлигосахаридыОбразование 1,4-гликозидной связи между моносахаридами
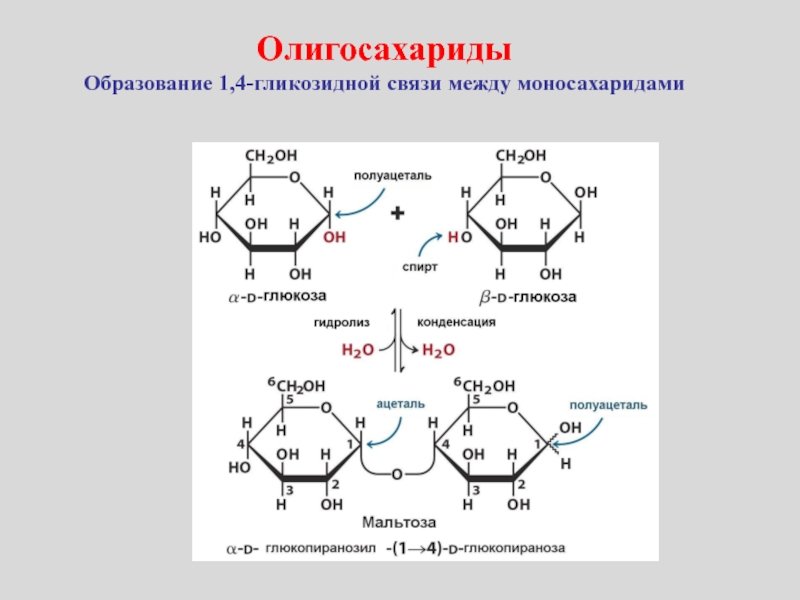
- 23. ОлигосахаридыОбразование 1,4-гликозидной связи между моносахаридами
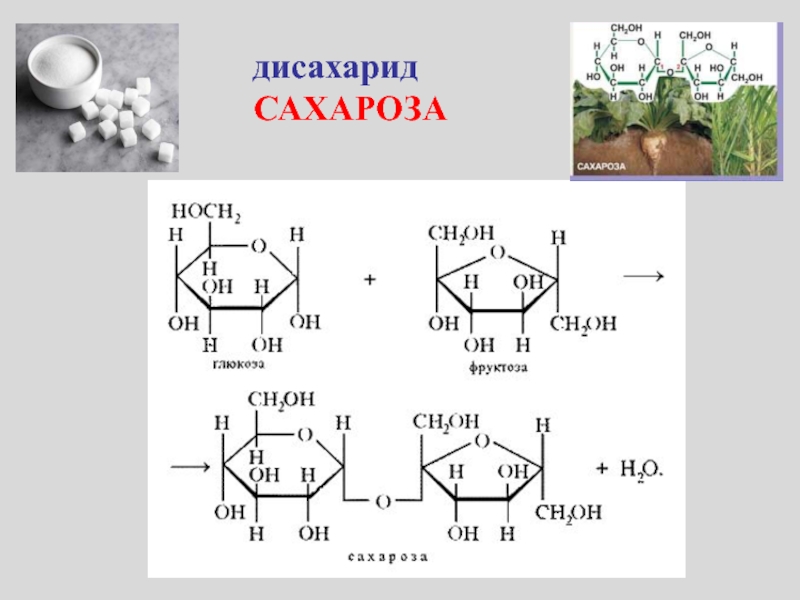
- 24. дисахарид САХАРОЗА
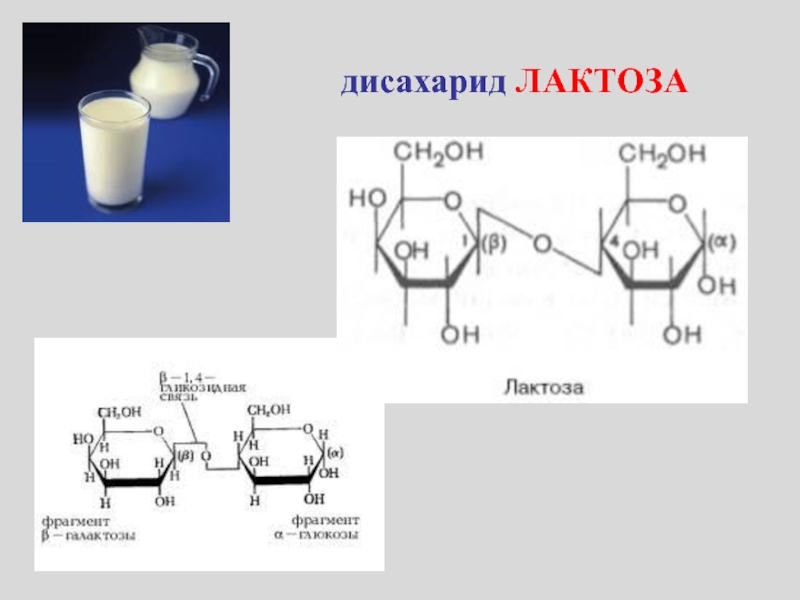
- 25. дисахарид ЛАКТОЗА
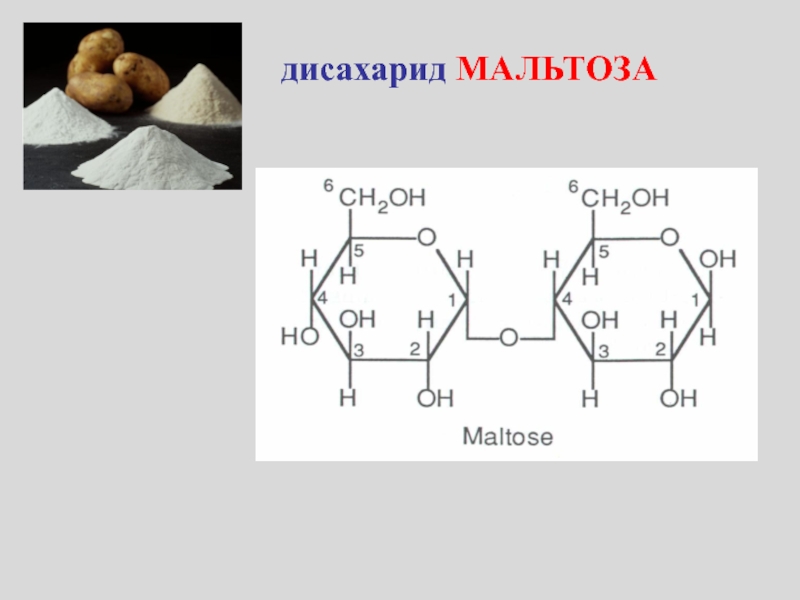
- 26. дисахарид МАЛЬТОЗА
- 27. Цепи полисахаридовСтроение, свойства, биологическая роль гомо- и гетерополисахаридовПОЛИСАХАРИДЫ:- Гомополисахариды- Гетерополисахариды
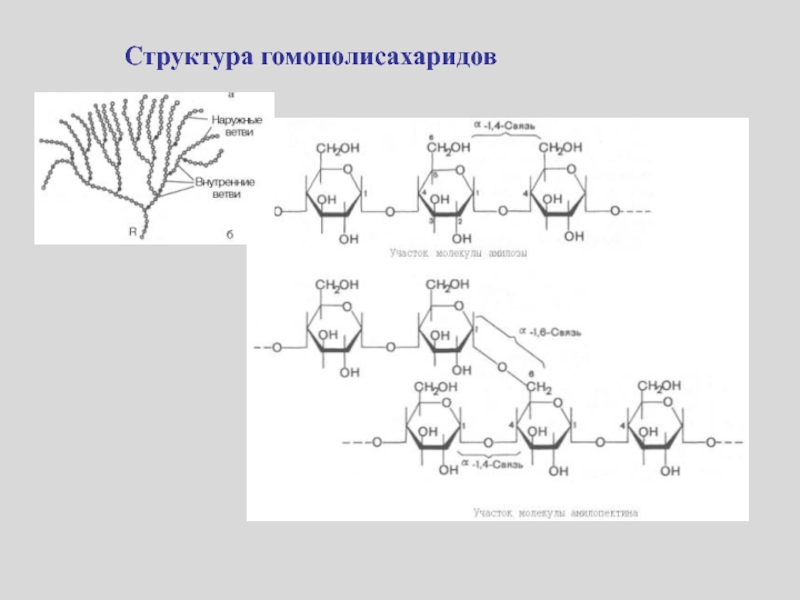
- 28. Структура гомополисахаридов
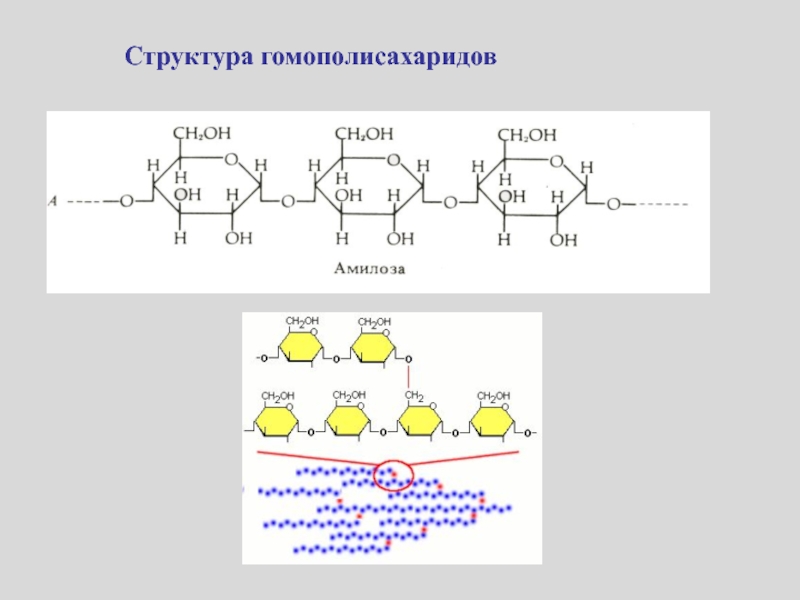
- 29. Структура гомополисахаридов
- 30. Ветвление полисахаридовСтроение, свойства, биологическая роль гомо- и гетерополисахаридов
- 31. КрахмалСтроение, свойства, биологическая роль гомо- и гетерополисахаридовГомополисахариды
- 32. Гомополисахариды
- 33. Клетчатка(целлюлоза)Целлюлоза (клетчатка) – наиболее широко распространенный структурный
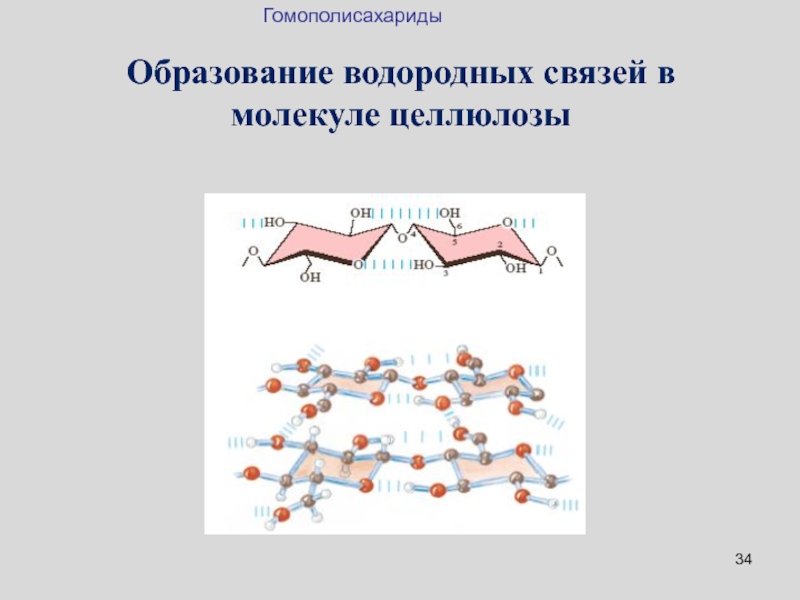
- 34. Образование водородных связей в молекуле целлюлозы Гомополисахариды
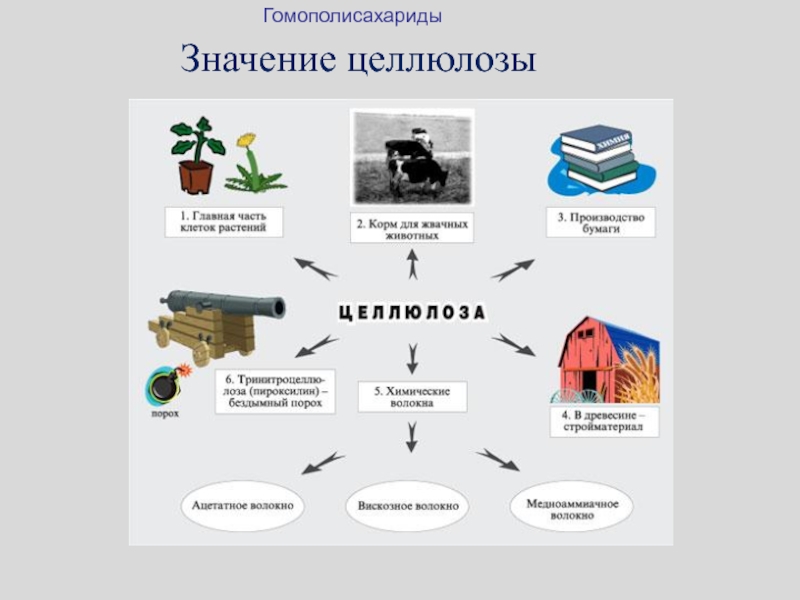
- 35. Значение целлюлозыГомополисахариды
- 36. Значение целлюлозыГомополисахариды
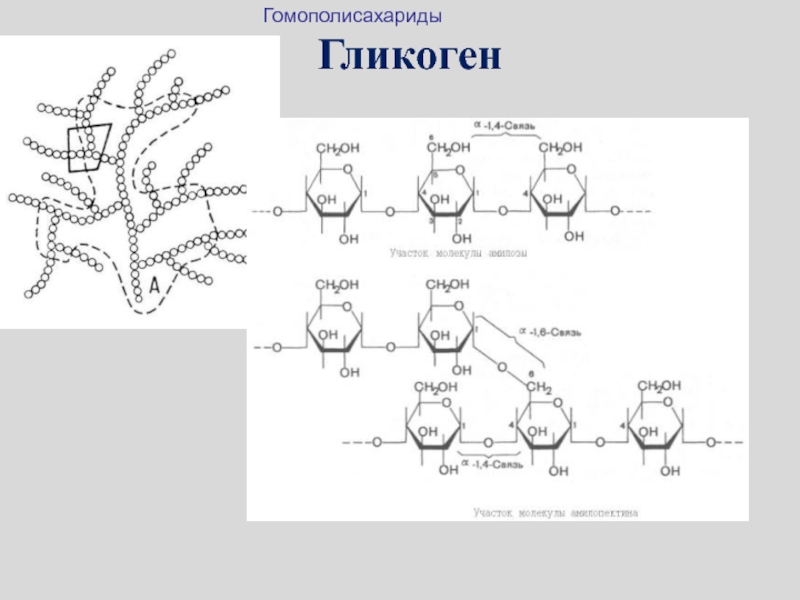
- 37. ГликогенГомополисахариды
- 38. ГликогенВКЛЮЧЕНИЯ ГЛИКОГЕНА В КЛЕТКАХ ПЕЧЕНИ В цитоплазме
- 39. ВКЛЮЧЕНИЯ ГЛИКОГЕНА В КЛЕТКАХ ПЕЧЕНИ Окраска
- 40. Хитин (C8H13NO5)n(фр. chitine, от др.-греч. χιτών: хитон — одежда,
- 41. Цепи полисахаридовСтроение, свойства, биологическая роль гомо- и гетерополисахаридовПОЛИСАХАРИДЫ:- Гомополисахариды- Гетерополисахариды
- 42. Структура природной Гиалуроновой кислоты. ГК – биополимер,
- 43. Дерма (собственно кожа) — это средний слой
- 44. Гиалуроновая кислота – тот редкий тип веществ,
- 45. Строение, свойства, биологическая роль гомо- и гетерополисахаридовГетерополисахариды: гиалуроновая кислота
- 46. Гепарин представляет собой сульфатированный гликозаминогликан, обычно используемый
- 47. МастоцитыТучные клетки.Тучные клетки (мастоциты, лаброциты) — высокоспециализированные
- 48. Хондроитинсульфаты — полимерные сульфатированные гликозаминогликаны. Являются специфическими компонентами
- 49. Слайд 49
- 50. Слайд 50
- 51. Химия белков
- 52. Слайд 52
- 53. Слайд 53
- 54. 124563
- 55. Слайд 55
- 56. В настоящее время наибольшим признанием пользуется жидкостно-мозаичная
- 57. Строение клеточной мембраны
- 58. Строение клеточной мембраны
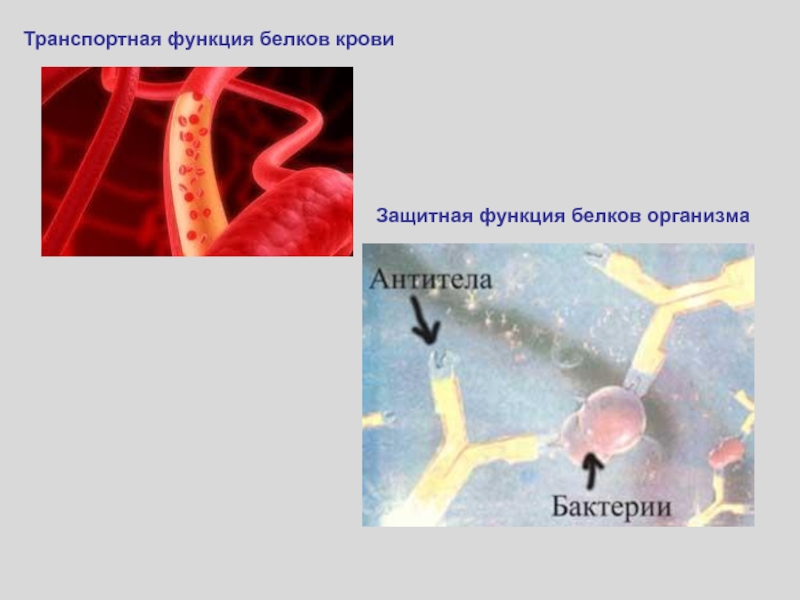
- 59. Транспортная функция белков кровиЗащитная функция белков организма
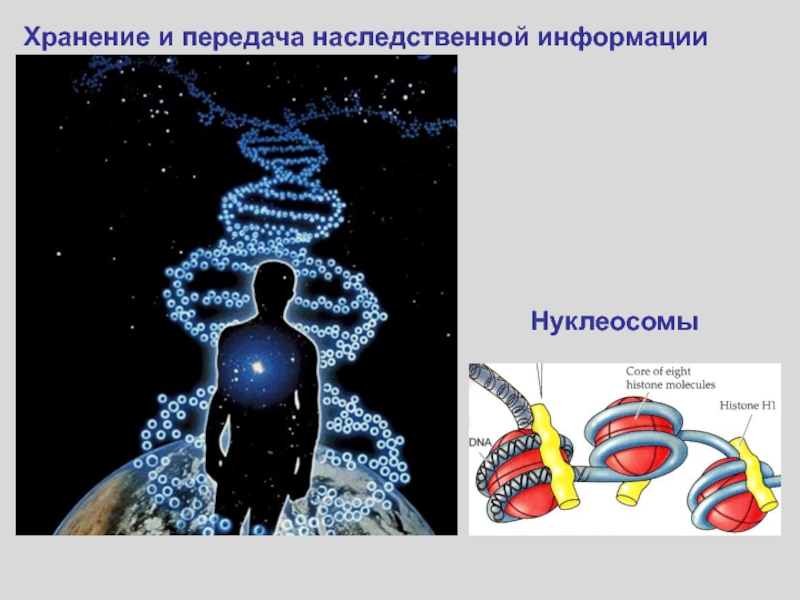
- 60. НуклеосомыХранение и передача наследственной информации
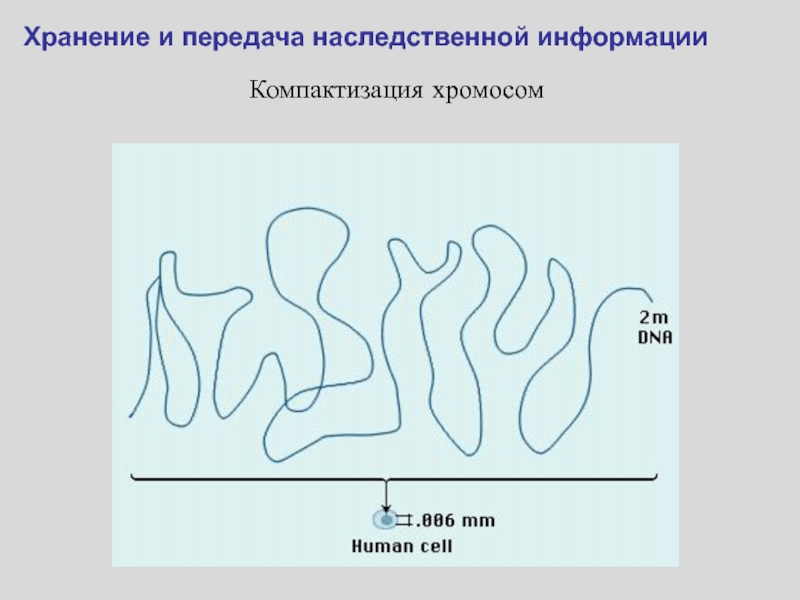
- 61. Компактизация хромосомХранение и передача наследственной информации
- 62. Химический состав белка:С – 50-55%О2 – 21-23%N – 15-17%Н2 – 6-7%S – 0,3 – 2,5%
- 63. Слайд 63
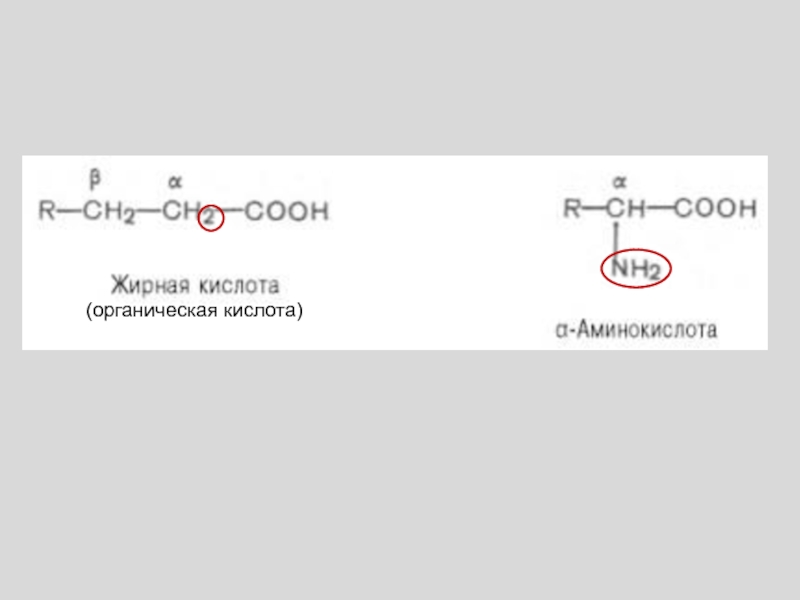
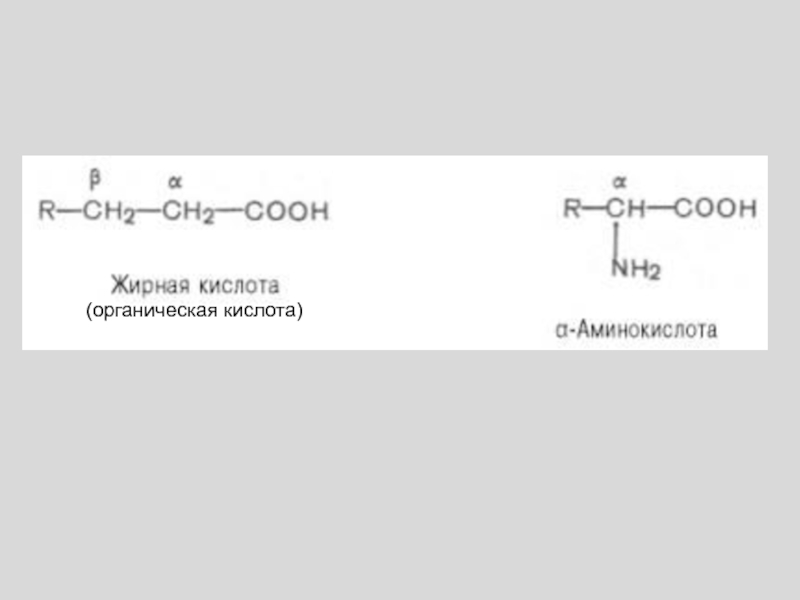
- 64. (органическая кислота)
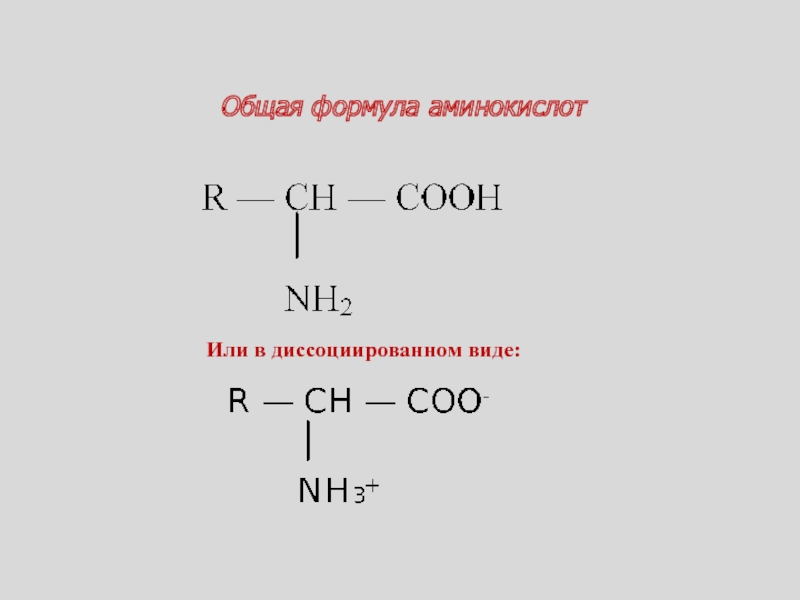
- 65. Общая формула аминокислотИли в диссоциированном виде:
- 66. Ациклические:Циклические(ароматические)АминокислотыНейтральные (моноаминомонокарбоновые)Неполярные (гидрофобные)Полярные (гидрофильные)2. ЗаряженныеПоложительно заряженные(диаминомонокарбоновые)Отрицательно заряженные(моноаминодикарбоновые)
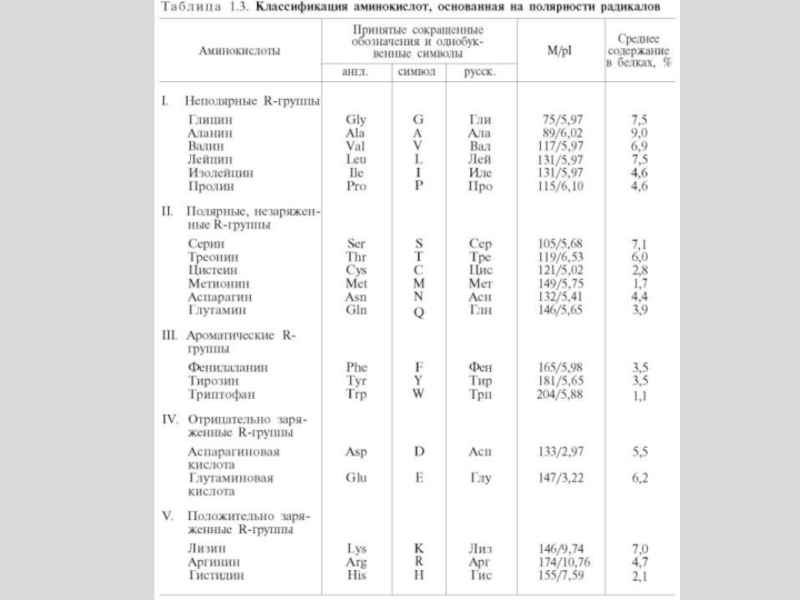
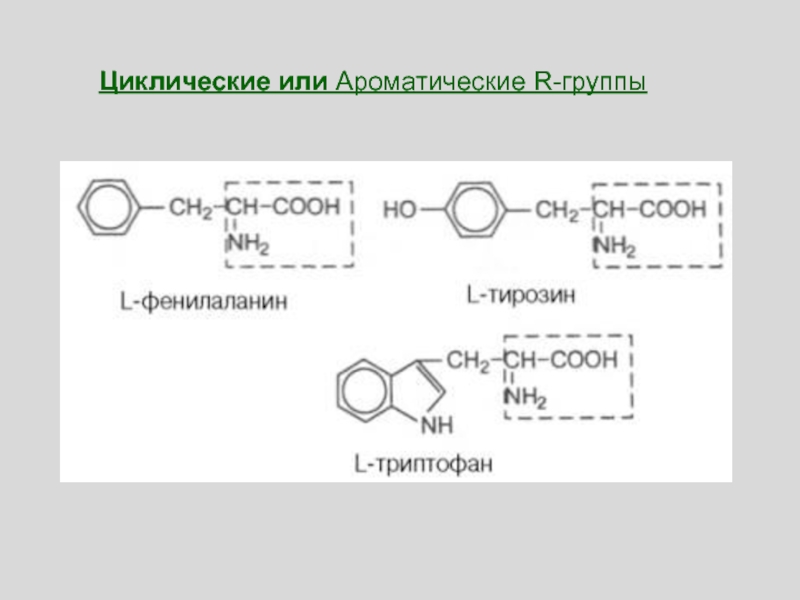
- 67. Циклические или Ароматические R-группы
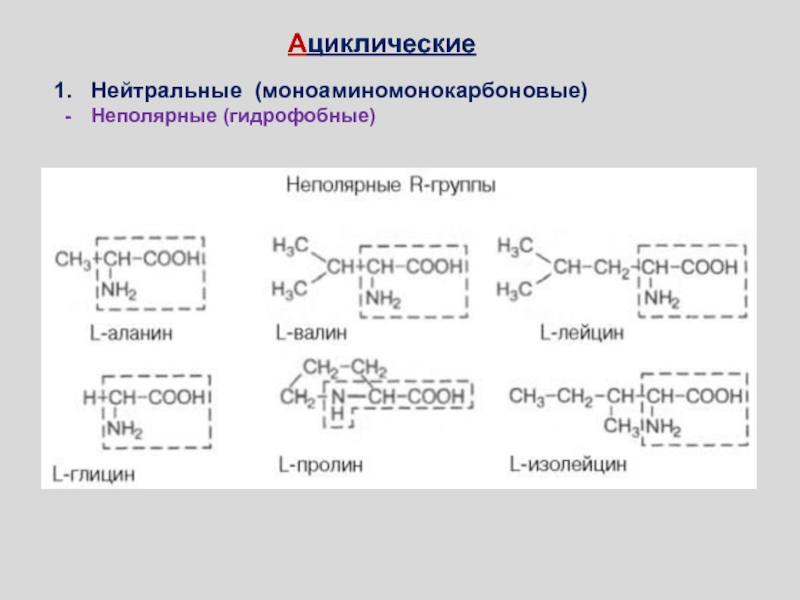
- 68. АциклическиеНейтральные (моноаминомонокарбоновые)Неполярные (гидрофобные)
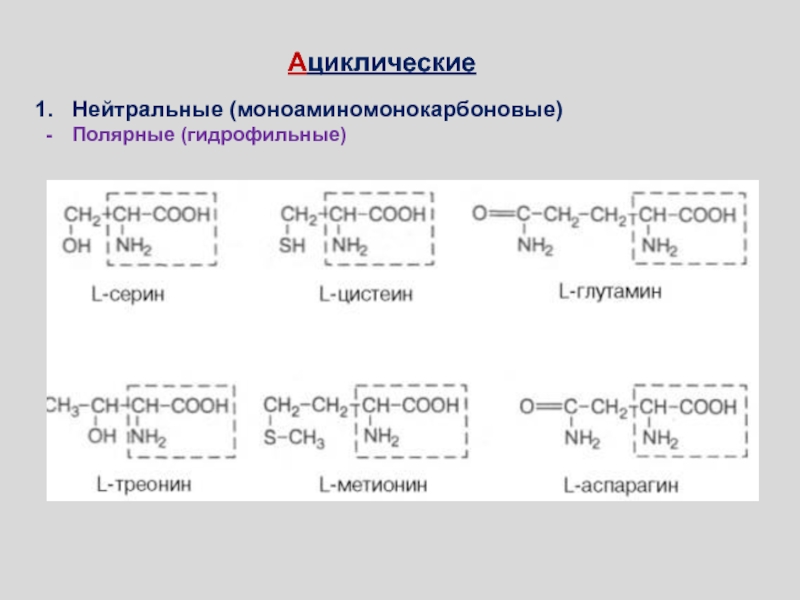
- 69. Полярные, незаряженные R-группы АциклическиеНейтральные (моноаминомонокарбоновые)Полярные (гидрофильные)
- 70. 2. ЗаряженныеОтрицательно заряженные (моноаминодикарбоновые)Ациклические
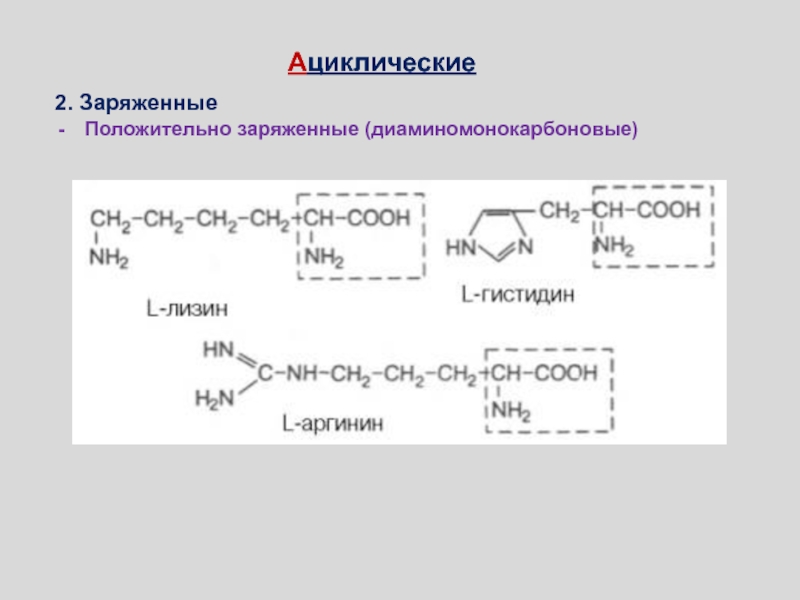
- 71. 2. ЗаряженныеПоложительно заряженные (диаминомонокарбоновые)Ациклические
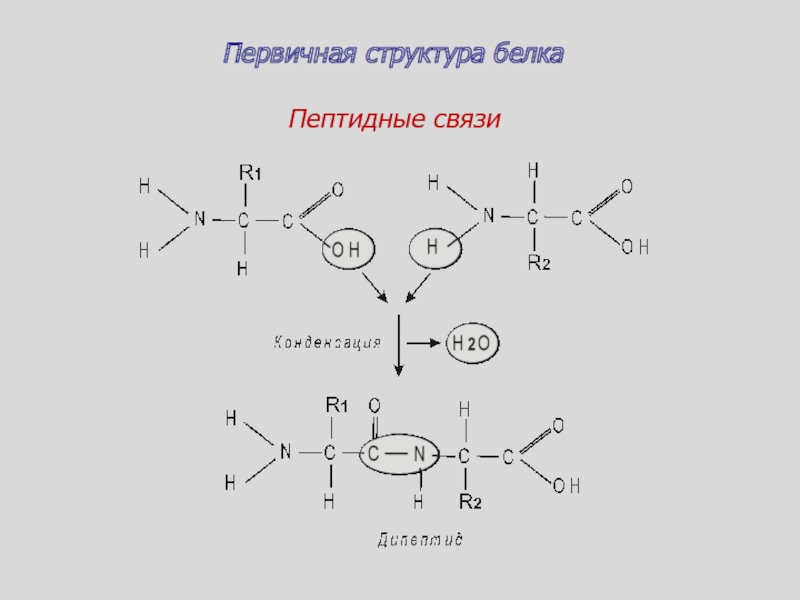
- 72. Пептидные связиПервичная структура белка
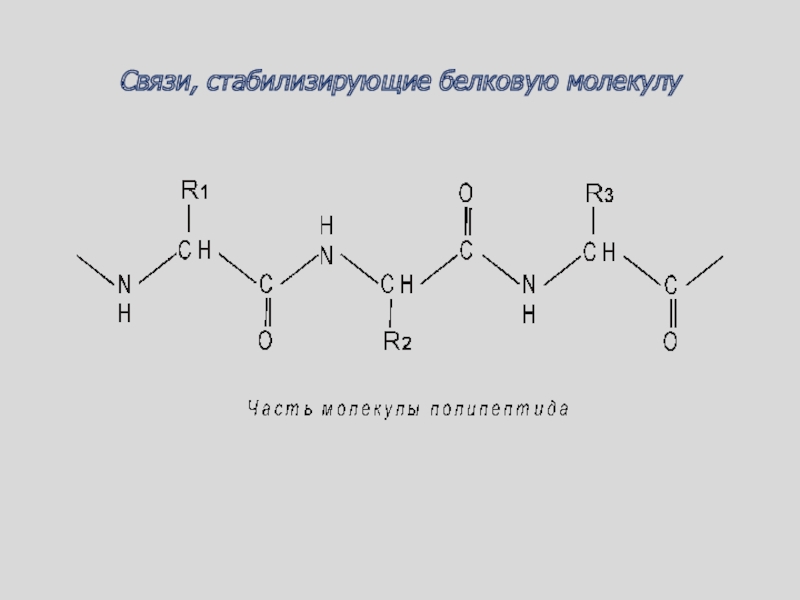
- 73. Связи, стабилизирующие белковую молекулу
- 74. Последовательность аминокислот для каждого белка уникальна и
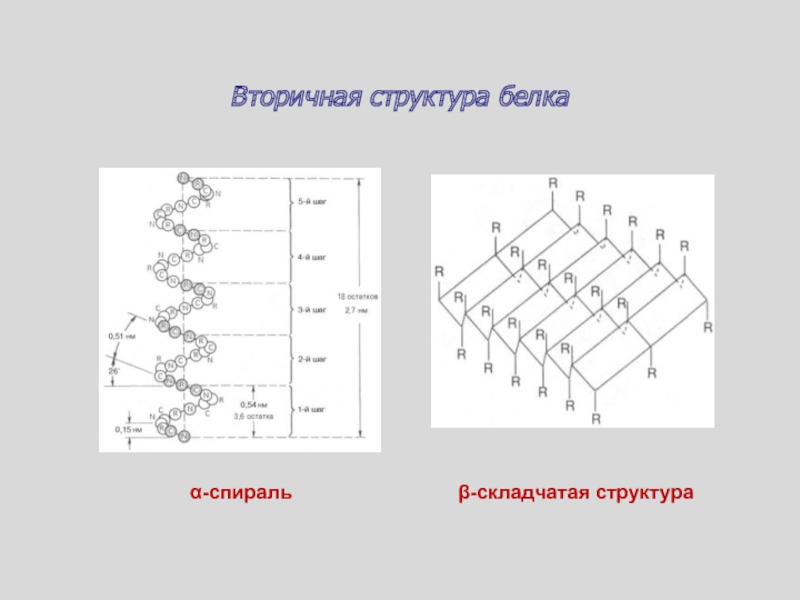
- 75. Вторичная структура белка α-спиральβ-складчатая структура
- 76. Пример бета-листа, сложенного из 4 антипараллельных нитей.
- 77. Связи, стабилизирующие белковую молекулуВодородная связь Локализованное электростатическое
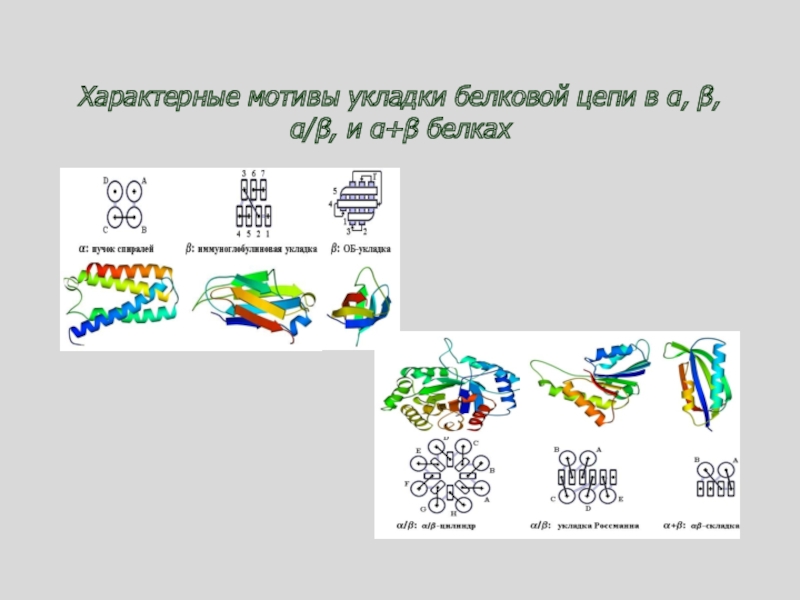
- 78. Характерные мотивы укладки белковой цепи в α, β, α/β, и α+β белках
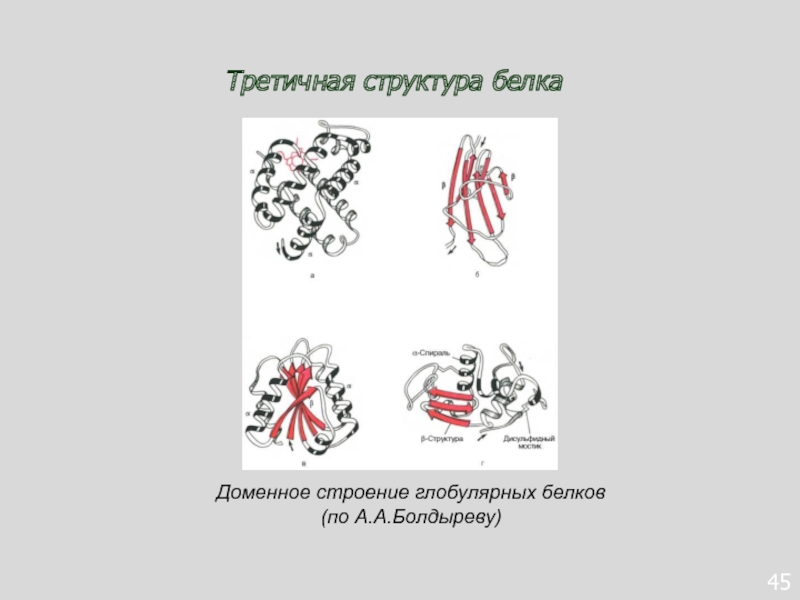
- 79. 45Третичная структура белка Доменное строение глобулярных белков (по А.А.Болдыреву)
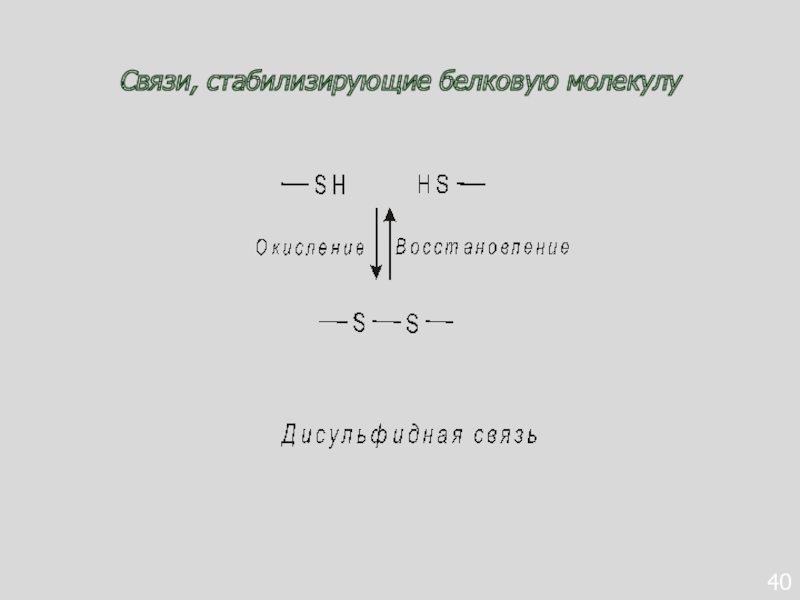
- 80. 40Связи, стабилизирующие белковую молекулу
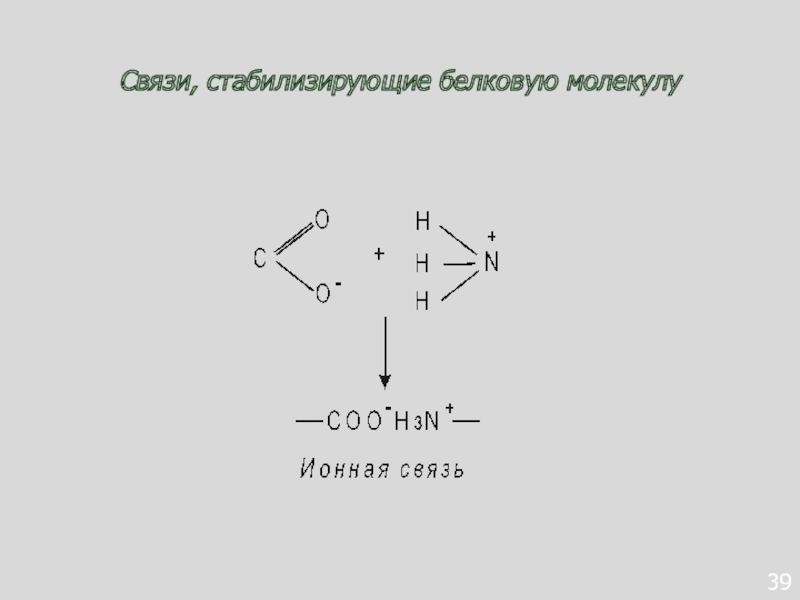
- 81. 39Связи, стабилизирующие белковую молекулу
- 82. Типы нековалентных связей, стабилизирующих третичную структуру белка.а
- 83. Четвертичная структура белка Гемоглобинсостоит из четырех субъединиц
- 84. Для справкиДиализ — освобождение коллоидных растворов и
- 85. Нейтральная цвиттерионная форма аминокислоты –NH2, основная группа,
- 86. На диссоциацию аминокислот оказывает влияние pH среды.
- 87. Слайд 87
- 88. НуклеосомыХранение и передача наследственной информацииСложные белки:нуклеопротеины
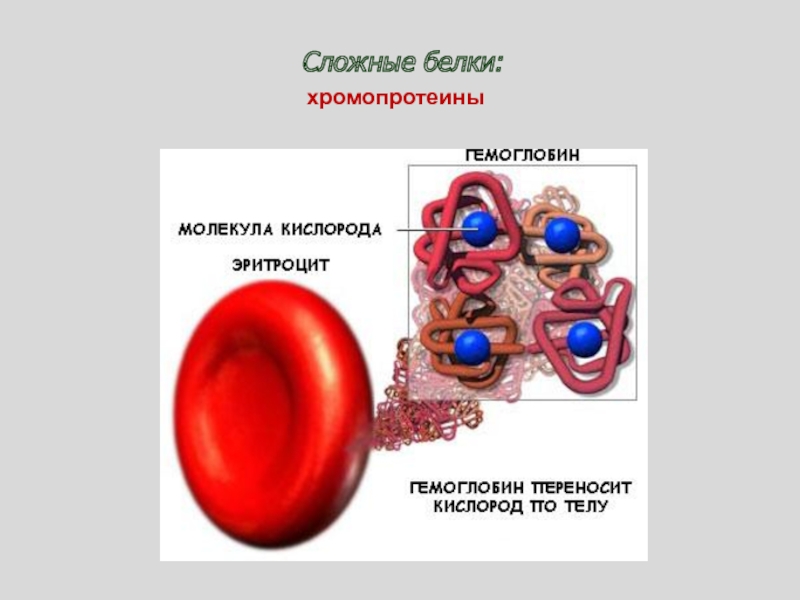
- 89. Сложные белки:хромопротеины
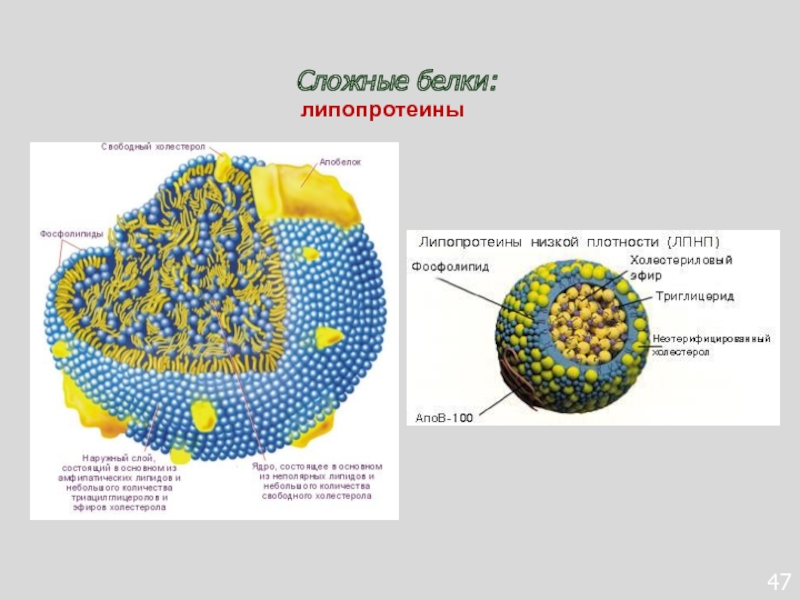
- 90. 47Сложные белки:липопротеины
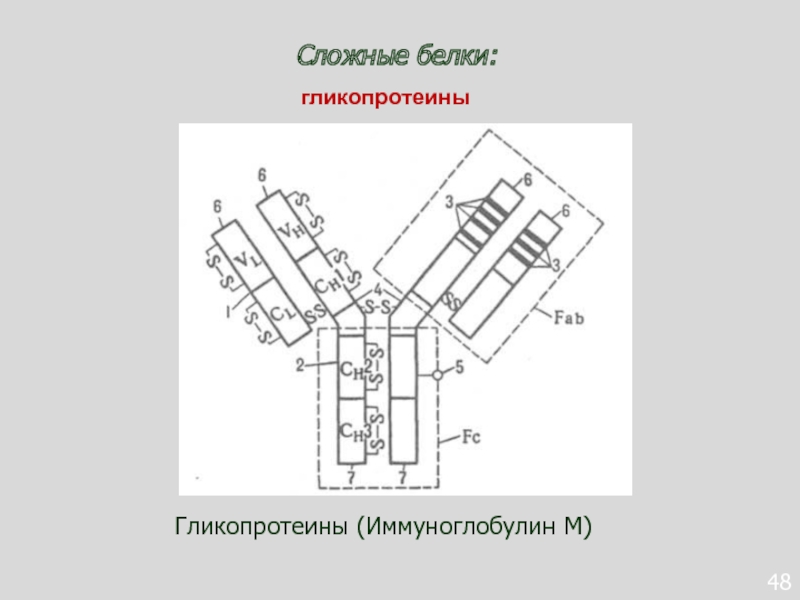
- 91. 48Сложные белки:Гликопротеины (Иммуноглобулин М)гликопротеины
- 92. Строение, свойства, биологическая роль белков49СТАТИЧЕСКАЯ БИОХИМИЯСложные белкиСхематическое
- 93. Строение, свойства, биологическая роль белков50СТАТИЧЕСКАЯ БИОХИМИЯСложные белки (металлопротеины) Цитохром с Ферритин
- 94. Строение, свойства, биологическая роль белков51СТАТИЧЕСКАЯ БИОХИМИЯСложные белки
- 95. Слайд 95
- 96. Слайд 96
- 97. Слайд 97
- 98. ЛИПИДЫ
- 99. ЖИРЫРезервный жироткладывается в жировой тканиЗапасается в организме
- 100. Биологическая роль липидов Структурная функция или строительнаяРегуляторнаяТранспортнаяЭнергетическая функцияЗапаснаяСпецифические функции
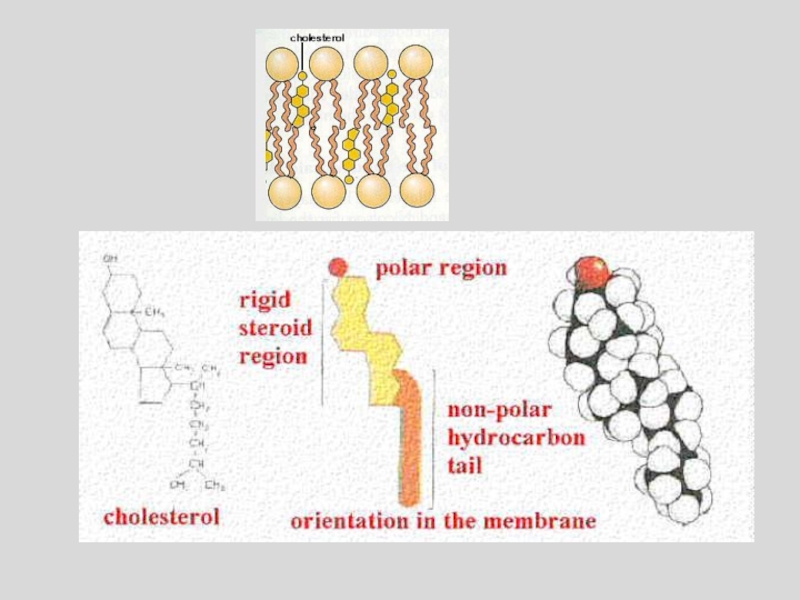
- 101. Строение клеточной мембраны
- 102. Строение клеточной мембраны
- 103. 47Сложные белки:липопротеины
- 104. Омыляемые – - в своём составе содержат
- 105. Процесс гидролиза сложных эфиров в щелочной среде
- 106. В живых организмах происходит ферментативный гидролиз жиров.
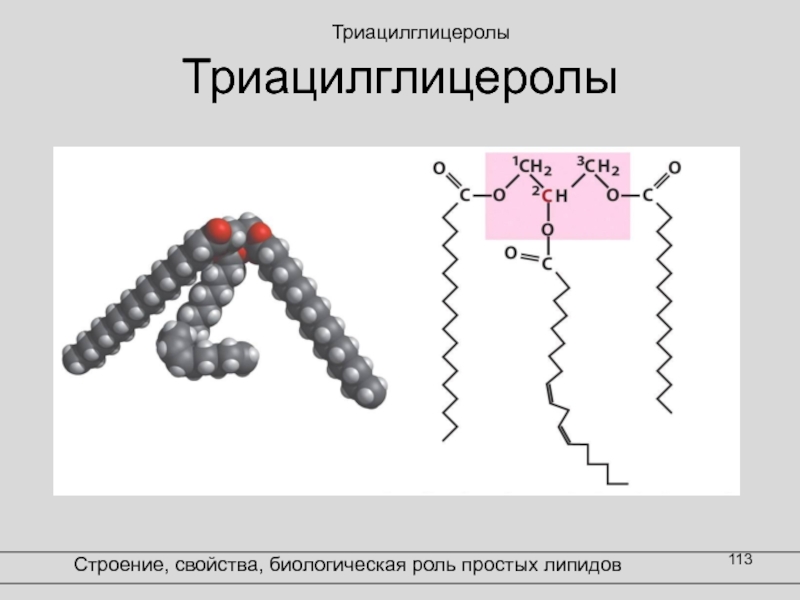
- 107. Простые липиды: триацилглицеролы
- 108. (органическая кислота)
- 109. 25Жирные кислотыСТАТИЧЕСКАЯ БИОХИМИЯ
- 110. Высшие жирные кислотыСтроение, свойства, биологическая роль простых
- 111. Строение клеточной мембраны
- 112. Насыщенные и ненасыщенные жирные кислотыСтроение, свойства, биологическая
- 113. ТриацилглицеролыСтроение, свойства, биологическая роль простых липидов
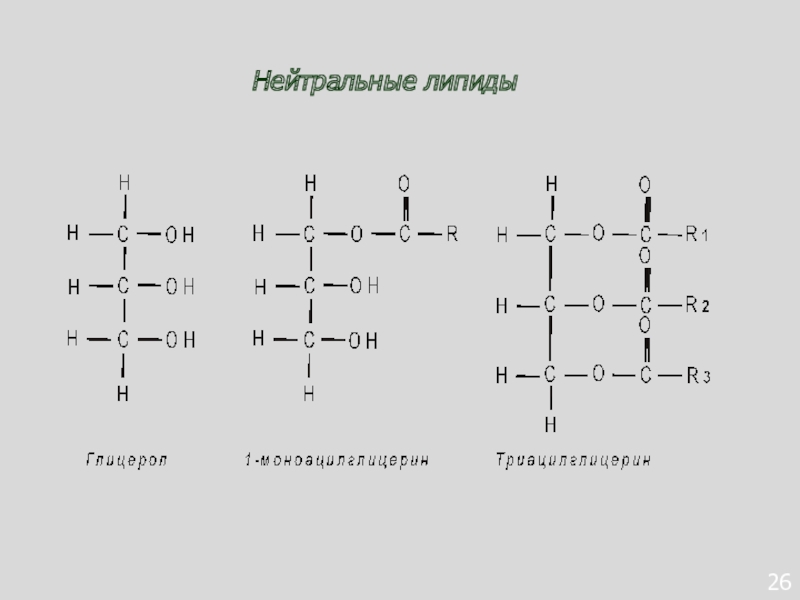
- 114. 26Нейтральные липиды
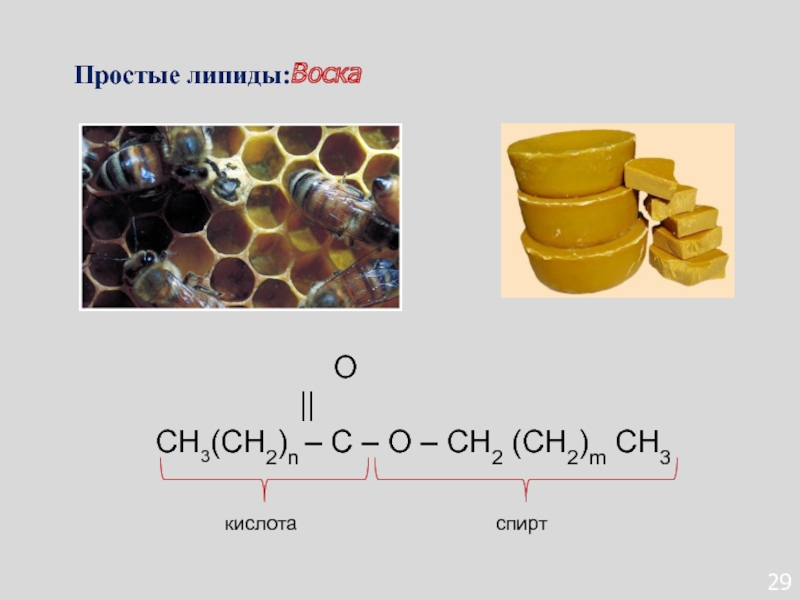
- 115. 29
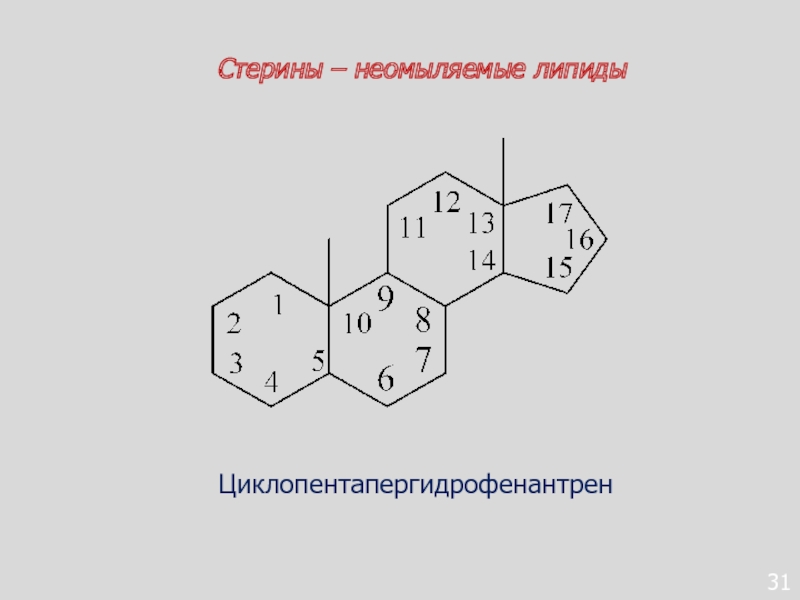
- 116. 31Стерины – неомыляемые липидыЦиклопентапергидрофенантрен
- 117. Стерины – неомыляемые липидыЗоостерины – в тканях животныхФитотерины – в тканях растенийМикостерины – в грибах
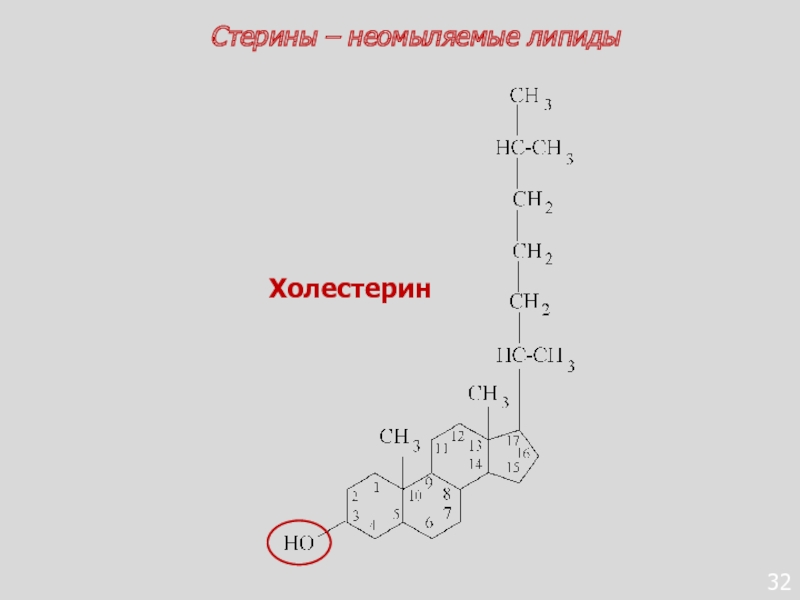
- 118. 32Холестерин Стерины – неомыляемые липиды
- 119. Слайд 119
- 120. Общее строение фосфолипидов Заместители R1 и R² —
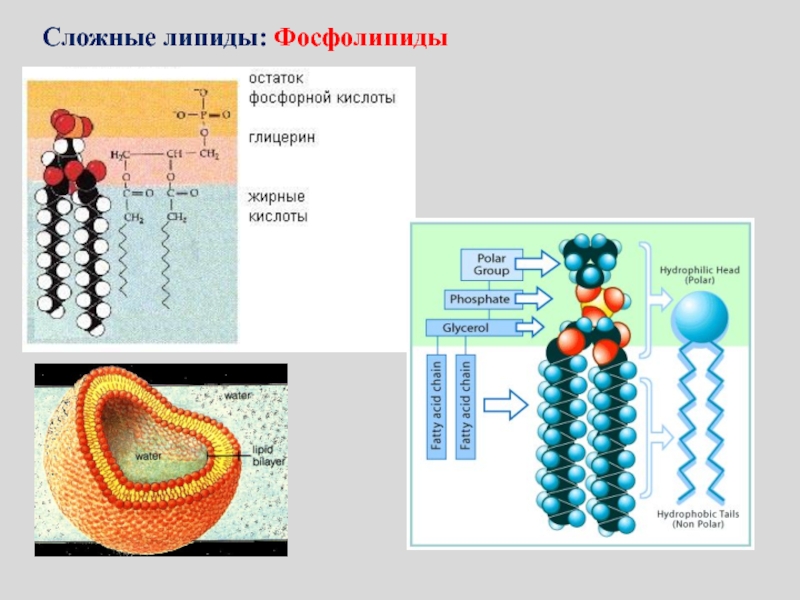
- 121. Сложные липиды: Фосфолипиды
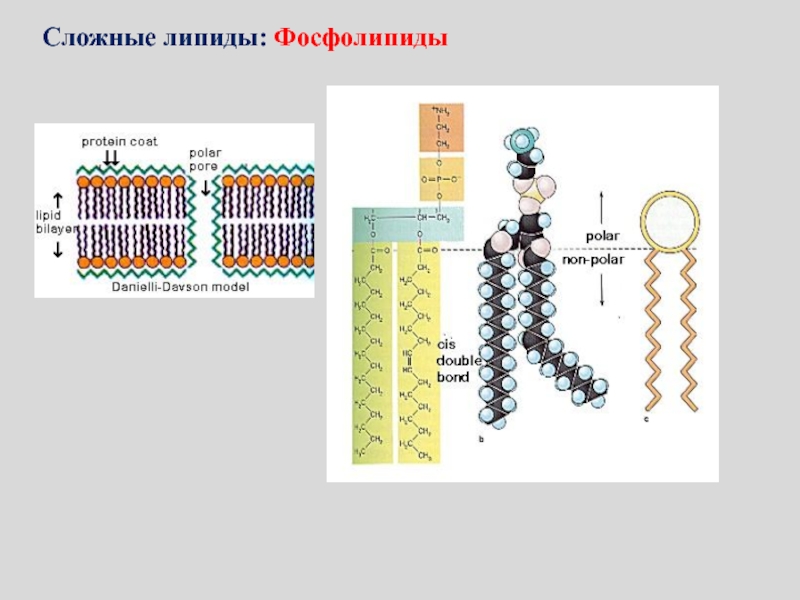
- 122. Сложные липиды: Фосфолипиды
- 123. Строение гликолипида (галактозилцерамида)(в основе спирт сфингозин)Сложные липиды: Гликолипиды
- 124. В настоящее время наибольшим признанием пользуется жидкостно-мозаичная
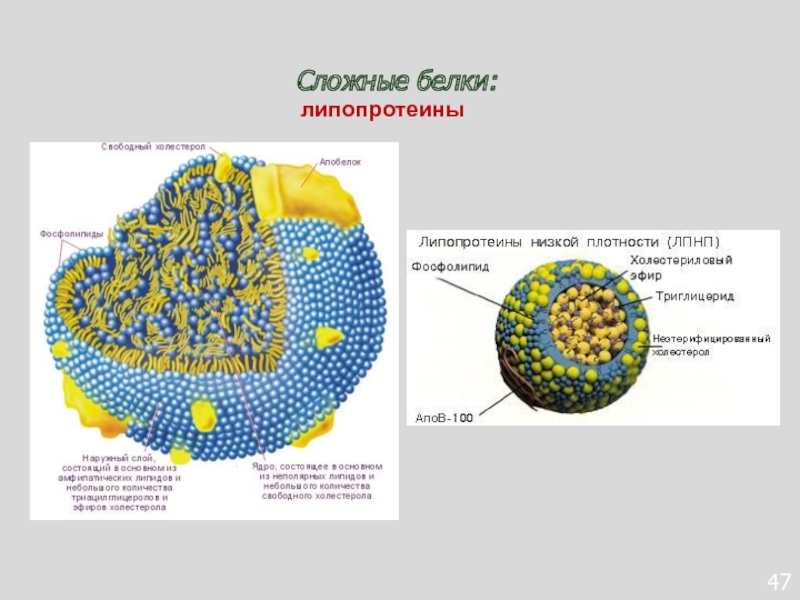
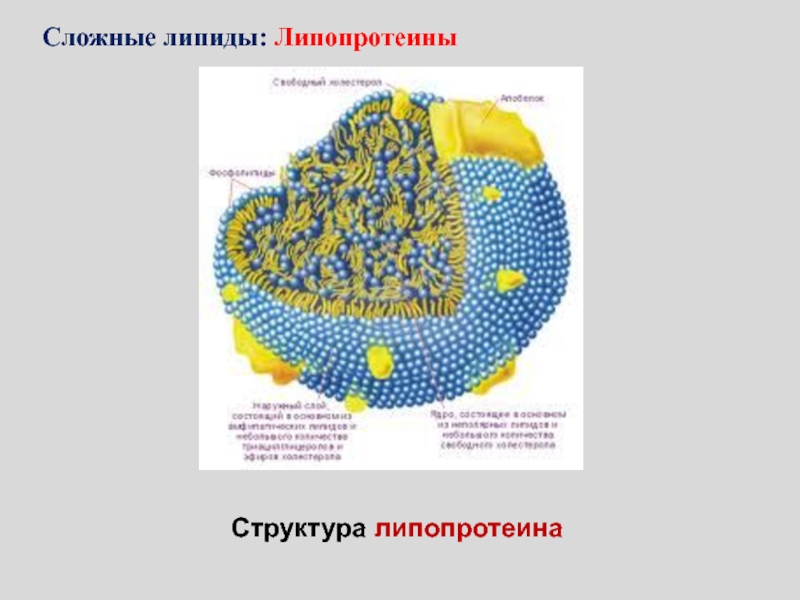
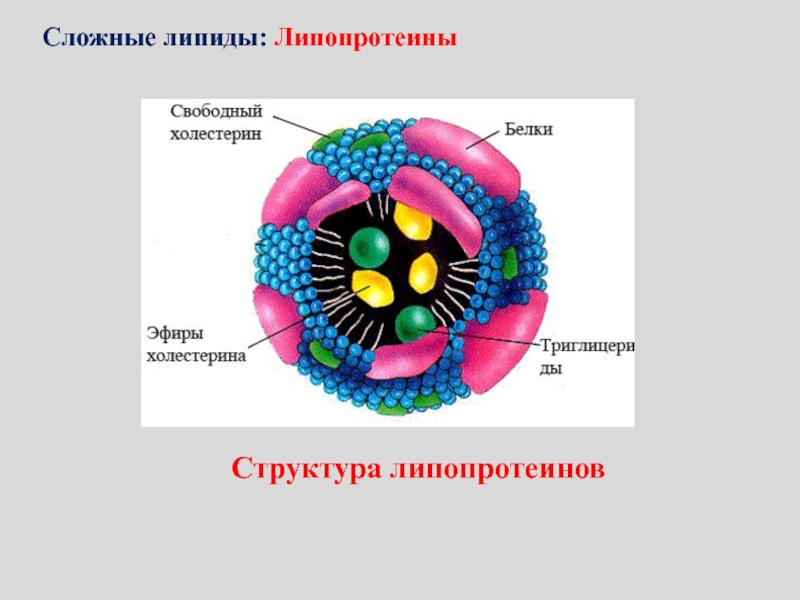
- 125. Структура липопротеинаСложные липиды: Липопротеины
- 126. Структура липопротеинов Сложные липиды: Липопротеины
- 127. Нормальное содержание различных липидов в крови человека
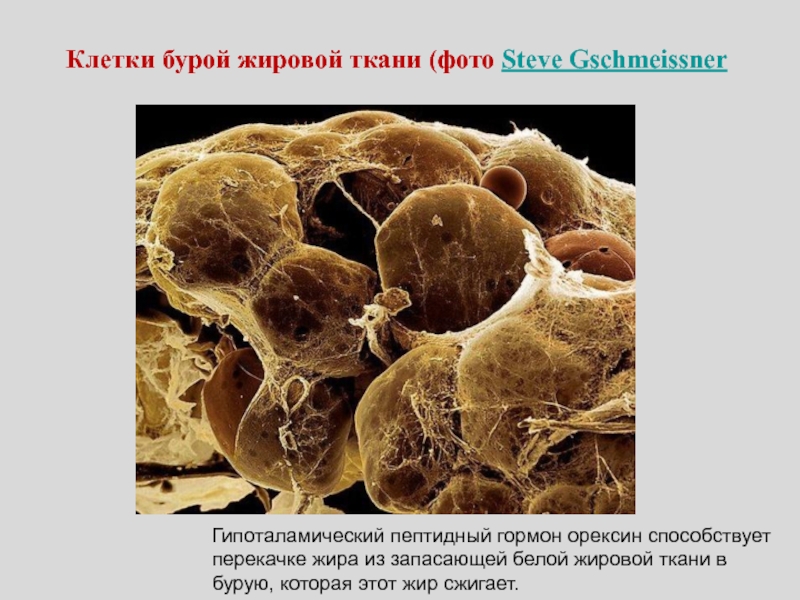
- 128. Клетки бурой жировой ткани (фото Steve GschmeissnerГипоталамический
- 129. Белый жир
- 130. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1УМКД БИОХИМИЯ
Факультет физической культуры и спорта
Направление - 032100 «Физическая
культура»
Слайд 2БИБЛИОГРАФИЧЕСКИЙ СПИСОК
Основной
Биохимия. Учебник для институтов физической культуры./Под ред. В.В.
Меньшикова, Н.И. Волкова. - М.: Физкультура и спорт, 1986.
Биохимия. Краткий
курс с упражнениями и задачами. /Под ред. Северина Е.С., Николаева. - М.: ГЭОТАР-МЕД, 2001. Проскурина И. К. Биохимия : учебное пособие для вузов по спец. 033100 "Физ. культура". Допущено Министерством образования РФ/И. К. Проскурина. - 2003
Волков Н.И. Биохимия мышечной деятельности. - М.: Олимпийский спорт, 2001.
Михайлов С.С. Спортивная биохимия. – М.: Советский спорт, 2006.
Николаев А.Я. Биологическая химия. - М.: Высшая школа, 1989.
Дополнительный
Альбертс Б., Брей Д., Льюис Дж., Рафф М., Робертс К., Уотсон Дж. Молекулярная биология клетки. В 3-х т. 2-е изд.- М.: Мир, 1994
Арансон М.В. Питание для спортсменов. - М.: ФиС. – 2001.
Березов Т.Т., Коровкин Б.Ф. Биологическая химия. - М.: Медицина, 1998.
Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека, тт. 1-2. - М.: Мир, 1993.
Мусил Я., Новакова О., Кунц К. Современная биохимия в схемах. - М.: Мир, 1984.
Пустовалова Л.М. Практикум по биохимии. - Ростов-на-Дону: Феникс, 1999.
Страйер Л. Биохимия, тт. 1-3. М.: Мир, 1985.
Филлипович Ю.Б. Основы биохимии. - М.: Агар, 1999.
Интернет.
Слайд 3ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ Федеральное государственное образовательное учреждение высшего и профессионального
образования
Сибирский федеральный университет
Кафедра биохимии и физиологии человека и животных
Красноярск
2007Слайд 4Содержание:
ЧАСТЬ 1. СТАТИЧЕСКАЯ БИОХИМИЯ
Строение, свойства, биологическая роль углеводов и липидов
Строение, свойства, биологическая роль белков
Строение, свойства, биологическая роль нуклеотидов
Витамины, ферменты
Гормоны,
биологическая роль, классификация, механизм действия3
СТАТИЧЕСКАЯ БИОХИМИЯ
Слайд 5Содержание:
ЧАСТЬ 2. ДИНАМИЧЕСКАЯ БИОХИМИЯ
Переваривание углеводов в пищеварительном тракте. Гликолиз.
Окислительное декарбоксилирование пирувата
Аэробный метаболизм углеводов
Липидный обмен
Белковый
обменИнтеграция клеточного обмена
3
ДИНАМИЧЕСКАЯ БИОХИМИЯ
3
Слайд 6СПОРТИВНАЯ БИОХИМИЯ
Содержание
ЧАСТЬ 3. СПОРТИВНАЯ БИОХИМИЯ
Тема 11. Биохимия мышечного сокращения.
Тема 12.
Энергетическое обеспечение мышечной деятельности.
Тема 13. Биохимические изменения в организме при
работе различного характера. Биохимические изменения при утомлении.Тема 14. Биохимические превращения в период восстановления после мышечной работы.
Тема 15. Закономерности биохимической адаптации под влиянием систематической тренировки.
Тема 16. Биохимический контроль при занятиях физической культурой и спортом.
Тема 17. Биохимические основы силы, быстроты и выносливости.
Тема 18. Биохимическое обоснование методики занятий физической культурой и спортом с лицами разного возраста. Биохимические основы рационального питания при занятиях физической культурой.
Библиографический список.
3
Слайд 7Биохимия – наука о молекулярных основах жизни
Биохимия изучает стуктуру и
функции веществ живого организма, а также особенности их превращений в
различных органах и тканяхСлайд 8ЧАСТЬ 1. СТАТИЧЕСКАЯ БИОХИМИЯ
- Строение, свойства, биологическая роль углеводов, липидов
, белков.
- Строение, свойства, биологическая роль нуклеотидов, витаминов и ферментов
- Гормоны, биологическая роль, классификация, механизм действияСлайд 10Биологические функции углеводов
Энергетическая функция (главный вид клеточного топлива)
Структурная функция (обязательный компонент большинства внутриклеточных структур)
Защитная функция (участие
углеводных компонентов иммуноглобулинов в поддержании иммунитета)Регуляторная
Специфические функции
Слайд 21Глюкоза + Глюкоза = Мальтоза
Глюкоза + Галактоза = Лактоза
Глюкоза +
Фруктоза = Сахароза
Олигосахариды
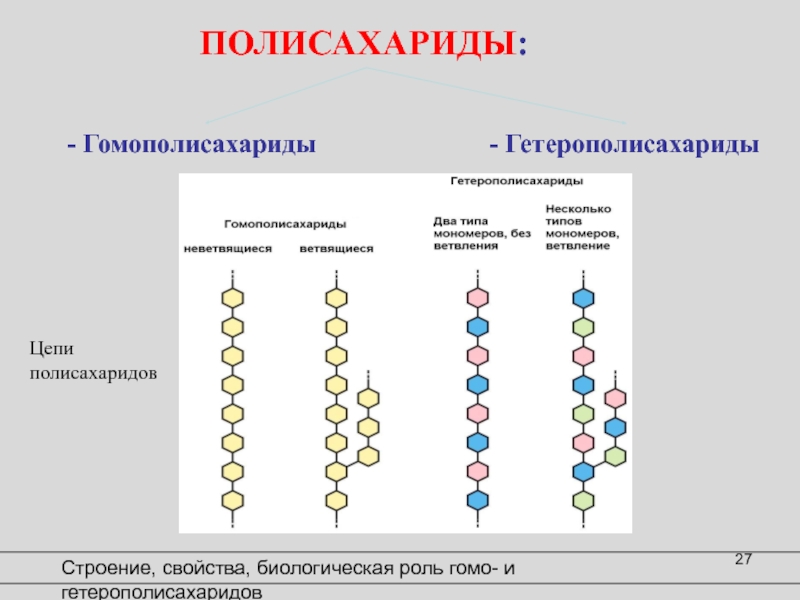
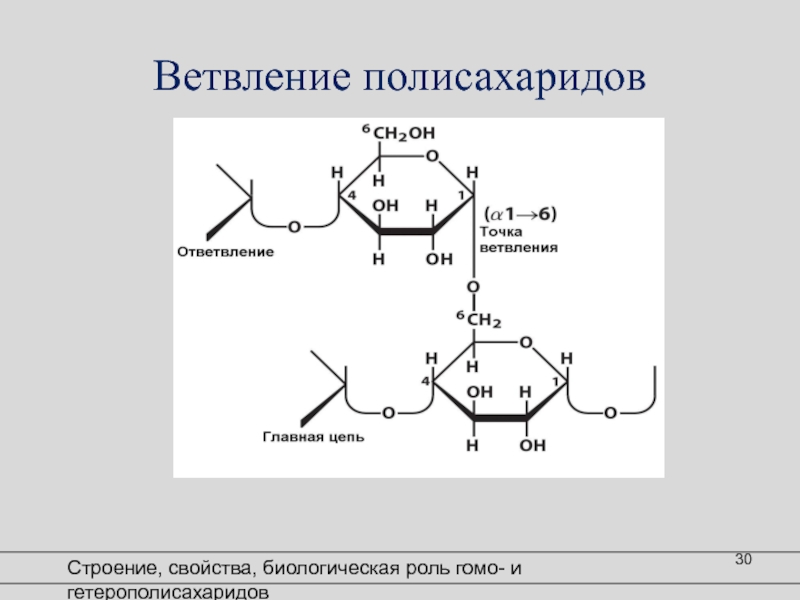
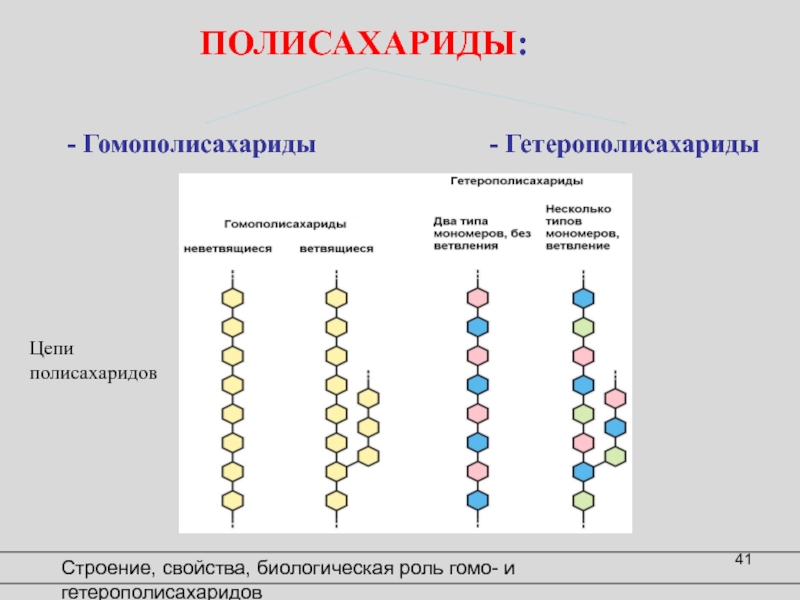
Слайд 27Цепи
полисахаридов
Строение, свойства, биологическая роль гомо- и гетерополисахаридов
ПОЛИСАХАРИДЫ:
- Гомополисахариды
- Гетерополисахариды
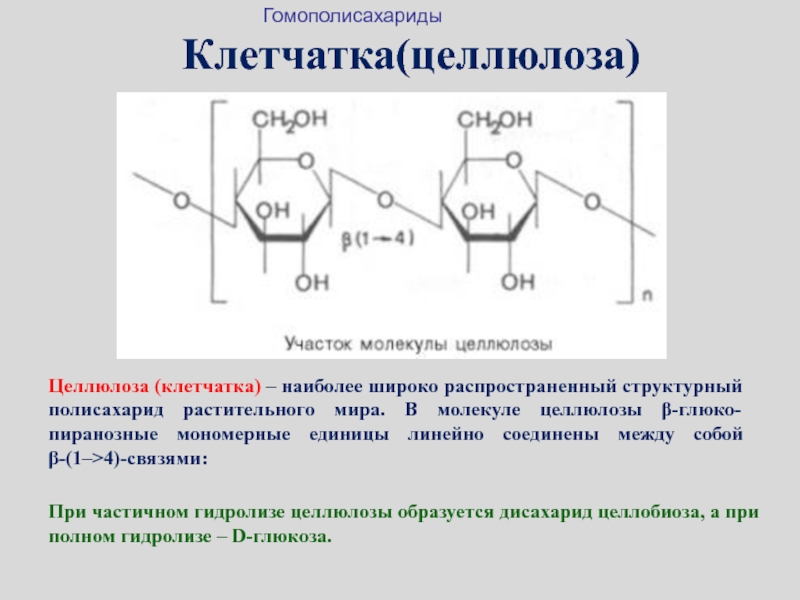
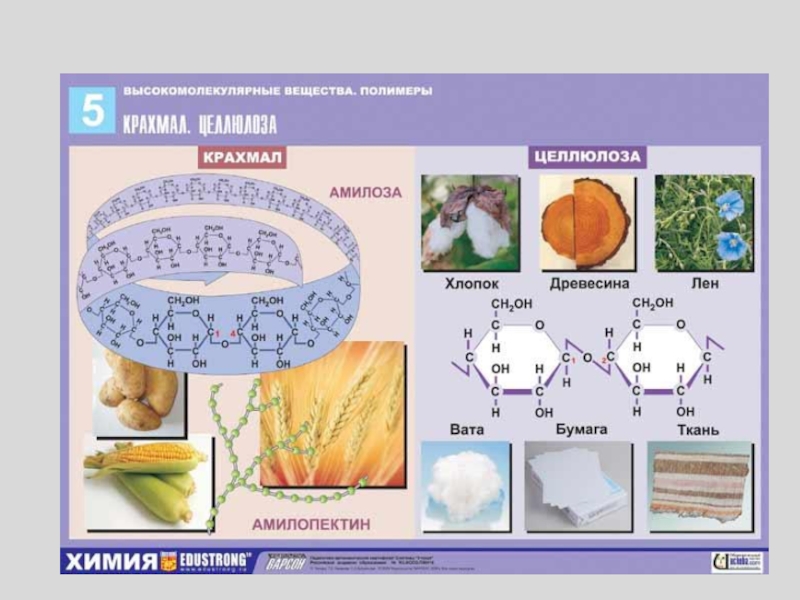
Слайд 33Клетчатка(целлюлоза)
Целлюлоза (клетчатка) – наиболее широко распространенный структурный полисахарид растительного мира.
В молекуле целлюлозы β-глюко-пиранозные мономерные единицы линейно соединены между собой
β-(1–>4)-связями:При частичном гидролизе целлюлозы образуется дисахарид целлобиоза, а при полном гидролизе – D-глюкоза.
Гомополисахариды
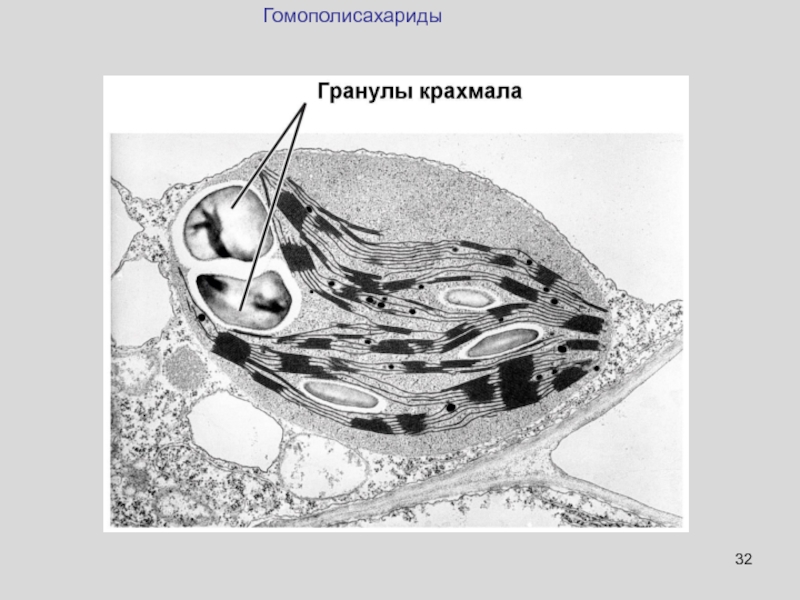
Слайд 38Гликоген
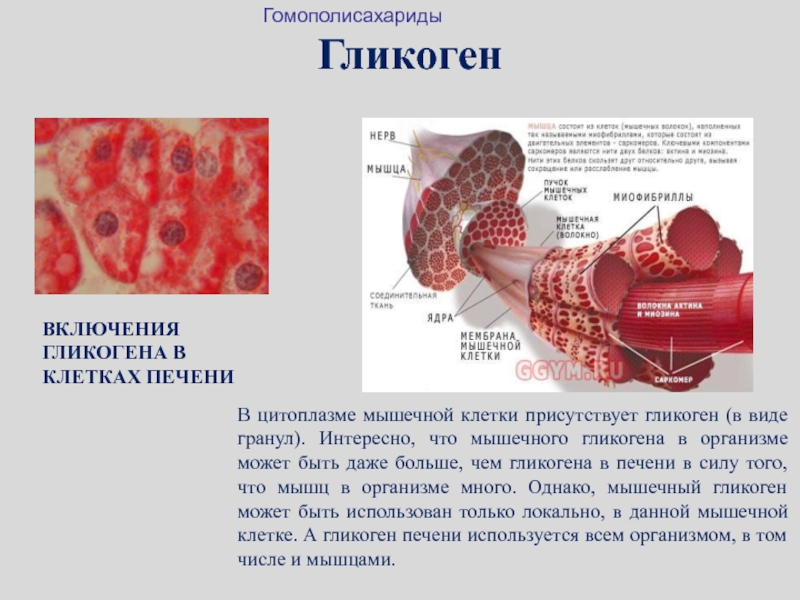
ВКЛЮЧЕНИЯ ГЛИКОГЕНА В КЛЕТКАХ ПЕЧЕНИ
В цитоплазме мышечной клетки присутствует гликоген
(в виде гранул). Интересно, что мышечного гликогена в организме может
быть даже больше, чем гликогена в печени в силу того, что мышц в организме много. Однако, мышечный гликоген может быть использован только локально, в данной мышечной клетке. А гликоген печени используется всем организмом, в том числе и мышцами.Гомополисахариды
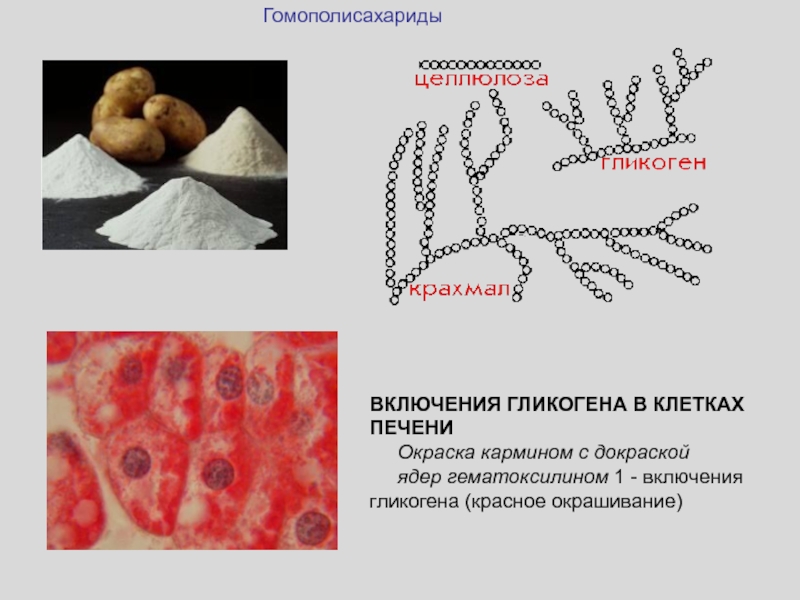
Слайд 39ВКЛЮЧЕНИЯ ГЛИКОГЕНА В КЛЕТКАХ ПЕЧЕНИ Окраска кармином с докраской ядер
гематоксилином 1 - включения гликогена (красное окрашивание)
Гомополисахариды
Слайд 40Хитин (C8H13NO5)n
(фр. chitine, от др.-греч. χιτών: хитон — одежда, кожа, оболочка) — природное
соединение из группы азотсодержащих полисахаридов.
Хитин, гомополимер из N-ацетилглюкозамина, связанного
в положении β(1→4), — основной компонент наружного скелета насекомых и панцыря ракообразных. Кроме того, хитин входит в состав клеточных стенок мицелия грибов.
Гомополисахариды
Слайд 41Цепи
полисахаридов
Строение, свойства, биологическая роль гомо- и гетерополисахаридов
ПОЛИСАХАРИДЫ:
- Гомополисахариды
- Гетерополисахариды
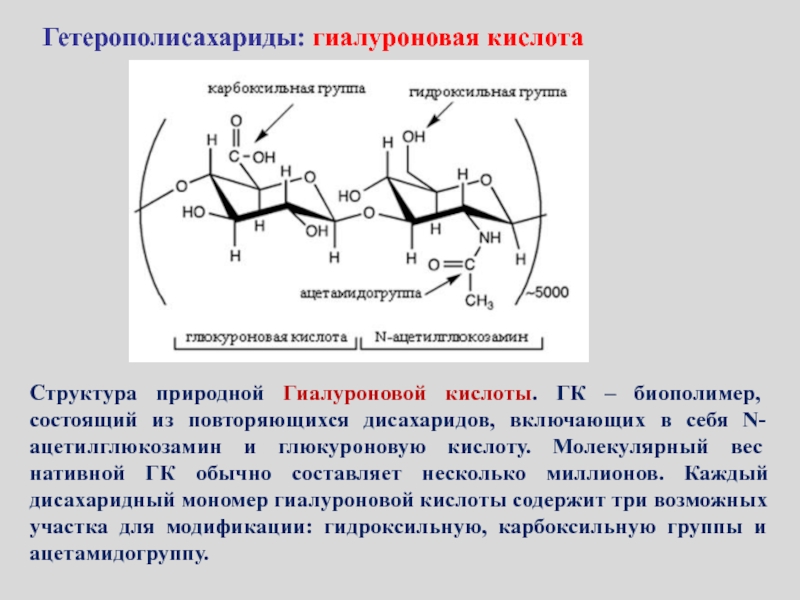
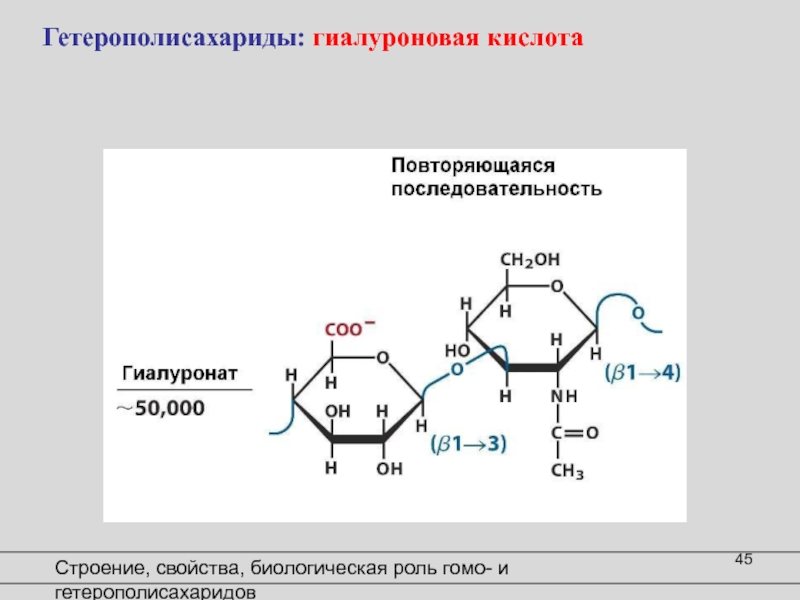
Слайд 42Структура природной Гиалуроновой кислоты. ГК – биополимер, состоящий из повторяющихся
дисахаридов, включающих в себя N-ацетилглюкозамин и глюкуроновую кислоту. Молекулярный вес
нативной ГК обычно составляет несколько миллионов. Каждый дисахаридный мономер гиалуроновой кислоты содержит три возможных участка для модификации: гидроксильную, карбоксильную группы и ацетамидогруппу.Гетерополисахариды: гиалуроновая кислота
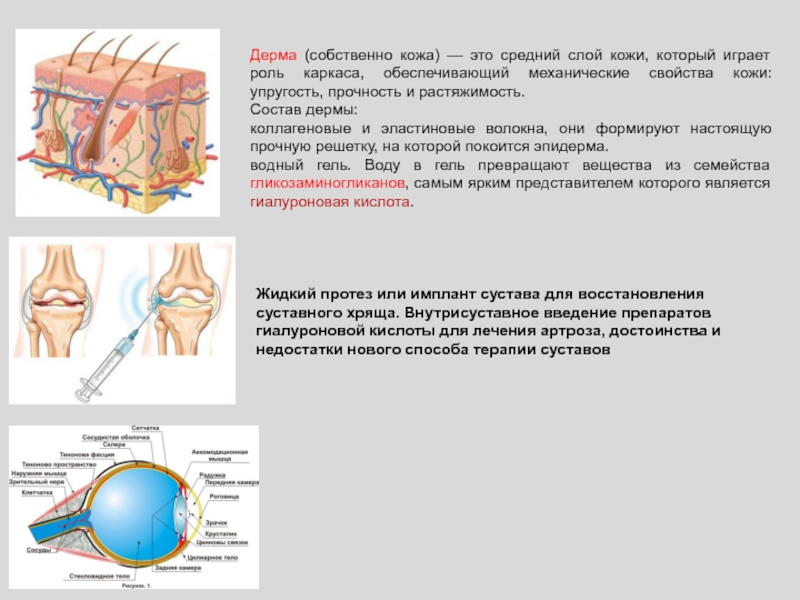
Слайд 43Дерма (собственно кожа) — это средний слой кожи, который играет
роль каркаса, обеспечивающий механические свойства кожи: упругость, прочность и растяжимость.
Состав
дермы:коллагеновые и эластиновые волокна, они формируют настоящую прочную решетку, на которой покоится эпидерма.
водный гель. Воду в гель превращают вещества из семейства гликозаминогликанов, самым ярким представителем которого является гиалуроновая кислота.
Жидкий протез или имплант сустава для восстановления суставного хряща. Внутрисуставное введение препаратов гиалуроновой кислоты для лечения артроза, достоинства и недостатки нового способа терапии суставов
Слайд 44Гиалуроновая кислота – тот редкий тип веществ, молекулы которого одинаковы
для всех живых организмов: и для человека, и для микробов.
В организме она выполняет множество функций, например, поддержание нормальной увлажненности эпидермиса и глубоких слоев кожи. Это своеобразный биологический «цемент», скрепляющий волокна коллагена и его предшественника эластина в коже. В косметике гиалуроновая кислота и ее натриевая соль (гиалуронат натрия) используются в качестве интенсивных поверхностных и глубоких увлажнителей. Чистая гиалуроновая кислота помогает бороться с признаками старения кожи. Наша кожа на 70% состоит из воды, что составляет около 15% всей воды, содержащейся в организме! Количество воды в организме зависит от возраста и наследственной предрасположенности человека. Именно гиалуроновая кислота, как никакое другое вещество, ответственна за сохранение влаги в коже.Слайд 45Строение, свойства, биологическая роль гомо- и гетерополисахаридов
Гетерополисахариды: гиалуроновая кислота
Слайд 46Гепарин представляет собой сульфатированный гликозаминогликан, обычно используемый в качестве антикоагулянта
при проведении диализа или операций, связанных с сердечно-сосудистой деятельностью.
В
клинической практике гепарин известен, как прямой антикоагулянт, то есть, как вещество, препятствующее свёртыванию крови. Применяется для профилактики и терапии тромбоэмболических заболеваний, при операциях на сердце и кровеносных сосудах, для поддержания жидкого состояния крови в аппаратах искусственного кровообращения и гемодиализа, а также для предотвращения свертывания крови при лабораторных исследованиях. Синтезируется в тучных клетках, скопления которых находятся в органах животных, особенно в печени, лёгких, стенках сосудов.Гетерополисахариды: гепарин
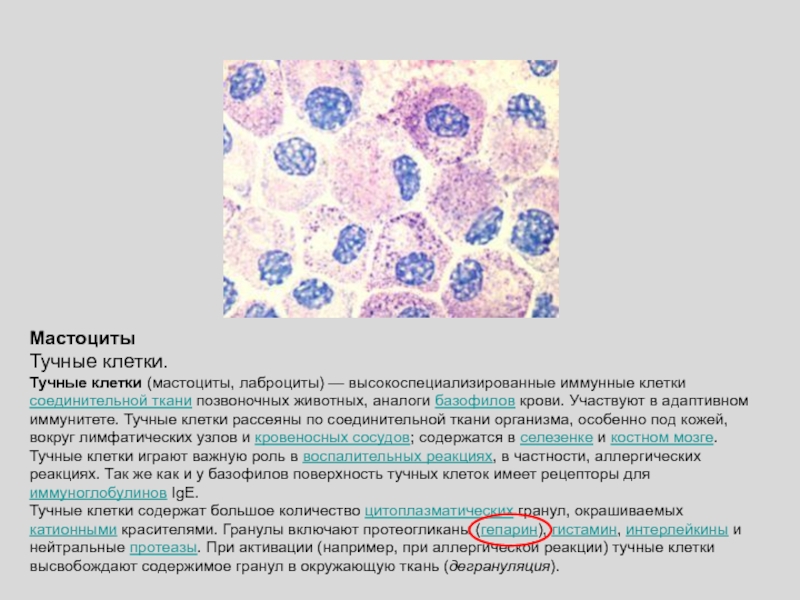
Слайд 47Мастоциты
Тучные клетки.
Тучные клетки (мастоциты, лаброциты) — высокоспециализированные иммунные клетки соединительной
ткани позвоночных животных, аналоги базофилов крови. Участвуют в адаптивном иммунитете.
Тучные клетки рассеяны по соединительной ткани организма, особенно под кожей, вокруг лимфатических узлов и кровеносных сосудов; содержатся в селезенке и костном мозге. Тучные клетки играют важную роль в воспалительных реакциях, в частности, аллергических реакциях. Так же как и у базофилов поверхность тучных клеток имеет рецепторы для иммуноглобулинов IgE.Тучные клетки содержат большое количество цитоплазматических гранул, окрашиваемых катионными красителями. Гранулы включают протеогликаны (гепарин), гистамин, интерлейкины и нейтральные протеазы. При активации (например, при аллергической реакции) тучные клетки высвобождают содержимое гранул в окружающую ткань (дегрануляция).
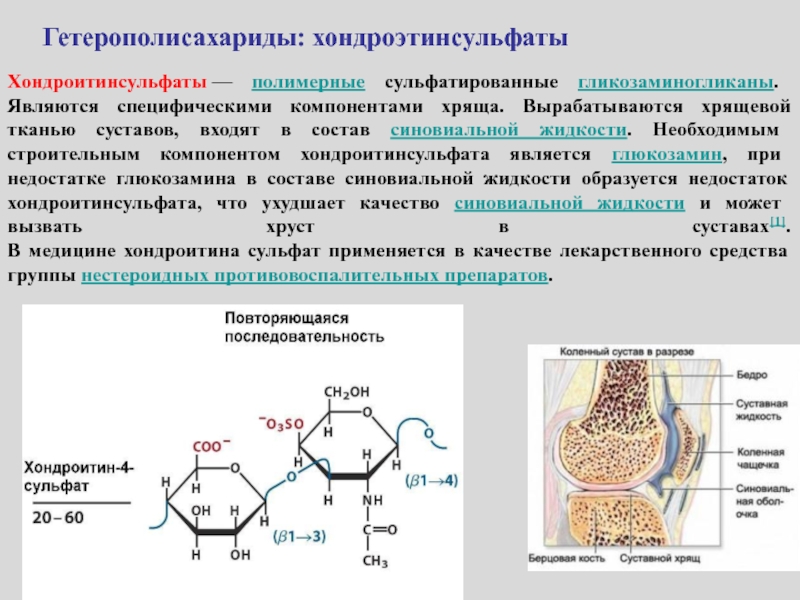
Слайд 48Хондроитинсульфаты — полимерные сульфатированные гликозаминогликаны. Являются специфическими компонентами хряща. Вырабатываются хрящевой
тканью суставов, входят в состав синовиальной жидкости. Необходимым строительным компонентом
хондроитинсульфата является глюкозамин, при недостатке глюкозамина в составе синовиальной жидкости образуется недостаток хондроитинсульфата, что ухудшает качество синовиальной жидкости и может вызвать хруст в суставах[1]. В медицине хондроитина сульфат применяется в качестве лекарственного средства группы нестероидных противовоспалительных препаратов.Гетерополисахариды: хондроэтинсульфаты
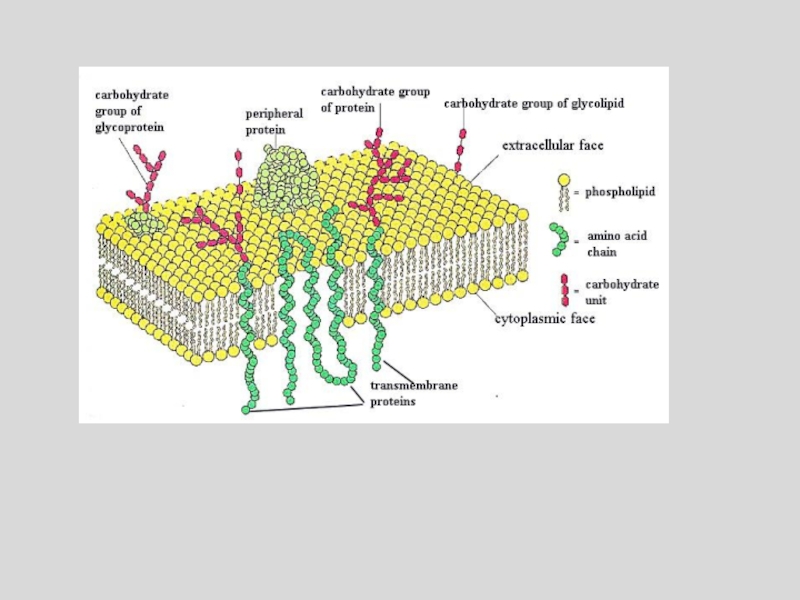
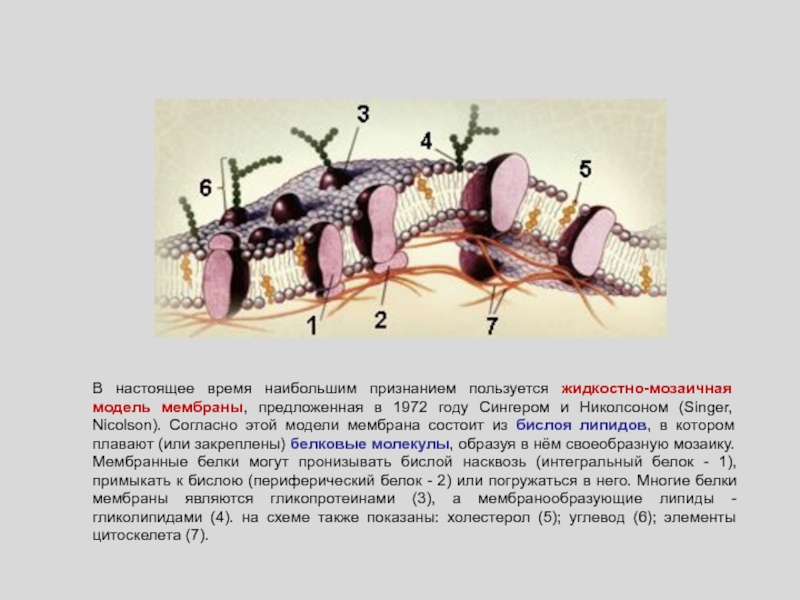
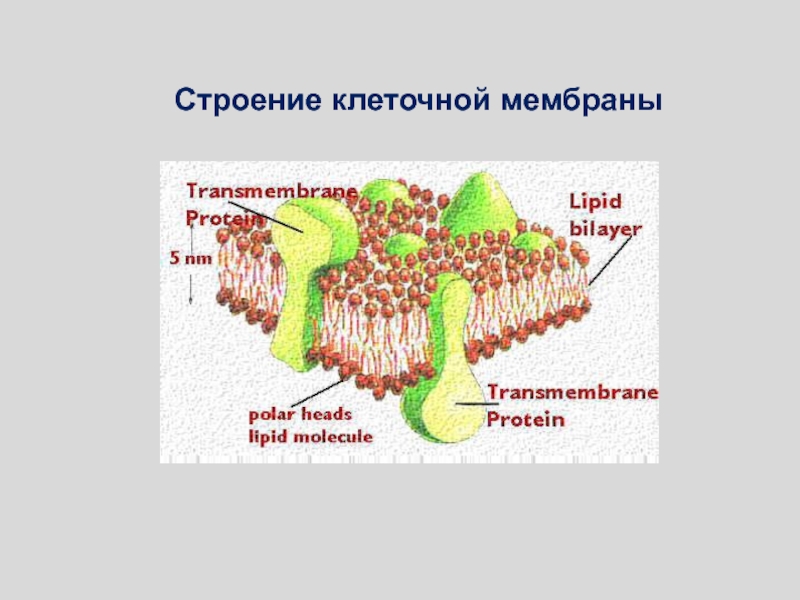
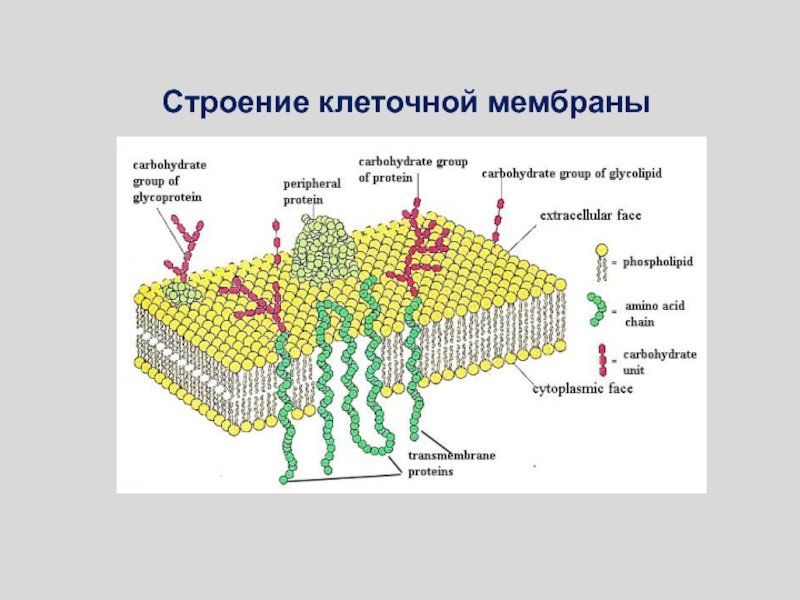
Слайд 56В настоящее время наибольшим признанием пользуется жидкостно-мозаичная модель мембраны, предложенная
в 1972 году Сингером и Николсоном (Singer, Nicolson). Согласно этой
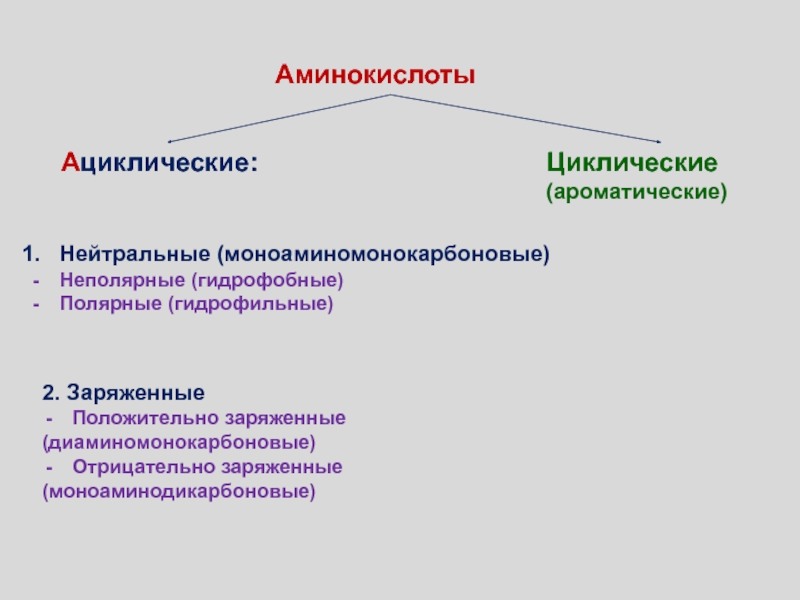
модели мембрана состоит из бислоя липидов, в котором плавают (или закреплены) белковые молекулы, образуя в нём своеобразную мозаику. Мембранные белки могут пронизывать бислой насквозь (интегральный белок - 1), примыкать к бислою (периферический белок - 2) или погружаться в него. Многие белки мембраны являются гликопротеинами (3), а мембранообразующие липиды - гликолипидами (4). на схеме также показаны: холестерол (5); углевод (6); элементы цитоскелета (7).Слайд 66Ациклические:
Циклические
(ароматические)
Аминокислоты
Нейтральные (моноаминомонокарбоновые)
Неполярные (гидрофобные)
Полярные (гидрофильные)
2. Заряженные
Положительно заряженные
(диаминомонокарбоновые)
Отрицательно заряженные
(моноаминодикарбоновые)
Слайд 69Полярные, незаряженные R-группы
Ациклические
Нейтральные (моноаминомонокарбоновые)
Полярные (гидрофильные)
Слайд 74Последовательность аминокислот для каждого белка уникальна и закреплена генетически
Первичная структура
характеризует последовательность аминокислотных остатков в полипептидной цепи, связанных ковалентыми связями
трипептид:
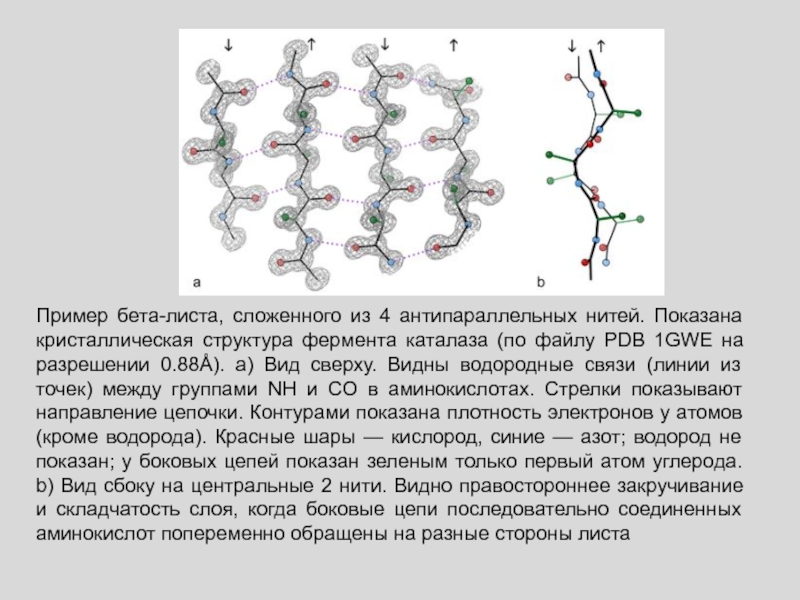
глицилаланиллизинСлайд 76Пример бета-листа, сложенного из 4 антипараллельных нитей. Показана кристаллическая структура
фермента каталаза (по файлу PDB 1GWE на разрешении 0.88Å). a)
Вид сверху. Видны водородные связи (линии из точек) между группами NH и CO в аминокислотах. Стрелки показывают направление цепочки. Контурами показана плотность электронов у атомов (кроме водорода). Красные шары — кислород, синие — азот; водород не показан; у боковых цепей показан зеленым только первый атом углерода. b) Вид сбоку на центральные 2 нити. Видно правостороннее закручивание и складчатость слоя, когда боковые цепи последовательно соединенных аминокислот попеременно обращены на разные стороны листаСлайд 77Связи, стабилизирующие белковую молекулу
Водородная связь
Локализованное электростатическое притяжение
– ОН .
. . . . . . . . . .
ОСЭлектроположительные водородные атомы, соединенные с кислородом или азотом в группах – ОН или – NH, стремятся обобществить электроны с находящимся по соседству с электроотрицательным атомом кислорода, например, с кислородом группы = СО
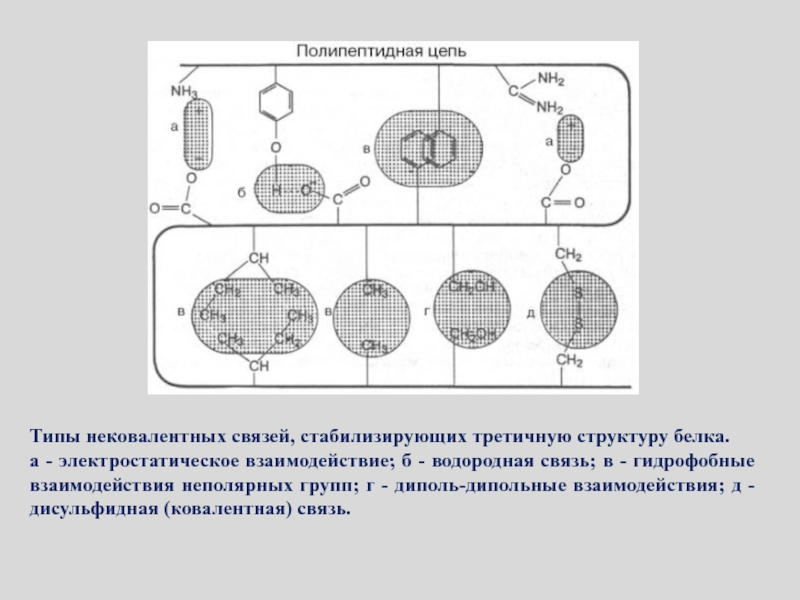
Слайд 82Типы нековалентных связей, стабилизирующих третичную структуру белка.
а - электростатическое взаимодействие;
б - водородная связь; в - гидрофобные взаимодействия неполярных групп;
г - диполь-дипольные взаимодействия; д - дисульфидная (ковалентная) связь.Слайд 83Четвертичная структура белка
Гемоглобин
состоит из четырех субъединиц (двух α-цепей и двух
β-цепей - верхний рисунок),
одна субъединица (средний рисунок),
простетическая группа гемоглобина
(нижний рисунок)Слайд 84Для справки
Диализ — освобождение коллоидных растворов и субстанций высокомолекулярных веществ
от растворённых в них низкомолекулярных соединений при помощи полупроницаемой мембраны.
При диализе молекулы растворенного низкомолекулярного вещества проходят через мембрану, а неспособные диализировать (проходить через мембрану) коллоидные частицы остаются за ней. Простейший диализатор представляет собой мешочек из коллодия (полупроницаемого материала), в котором находится диализируемая жидкость. Мешочек погружают в растворитель (например в воду). Постепенно концентрация диализирующего вещества в диализируемой жидкости и в растворителе становится одинаковой. Меняя растворитель, можно добиться практически полной очистки от нежелательных примесей.Диализ применяют для очистки коллоидных растворов от примесей электролитов и низкомолекулярных неэлектролитов. Диализ применяют в промышленности для очистки различных веществ, например в производстве искусственных волокон, при изготовлении лекарственных веществ.
В медицине диализ – основа работы «искусственной почки»
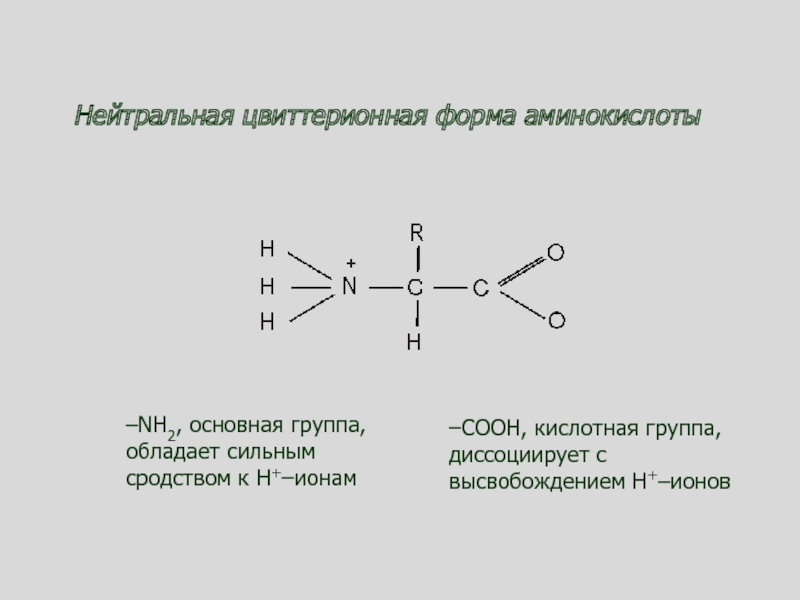
Слайд 85Нейтральная цвиттерионная форма аминокислоты
–NH2, основная группа,
обладает сильным
сродством к Н+–ионам
–СООН, кислотная группа, диссоциирует с высвобождением Н+–ионов
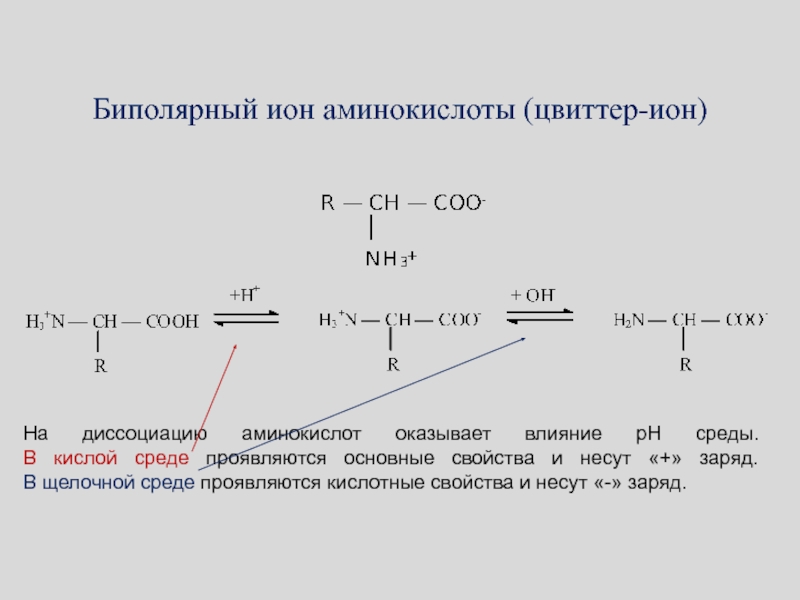
Слайд 86На диссоциацию аминокислот оказывает влияние pH среды. В кислой среде проявляются
основные свойства и несут «+» заряд. В щелочной среде проявляются кислотные
свойства и несут «-» заряд.Биполярный ион аминокислоты (цвиттер-ион)
Слайд 92Строение, свойства, биологическая роль белков
49
СТАТИЧЕСКАЯ БИОХИМИЯ
Сложные белки
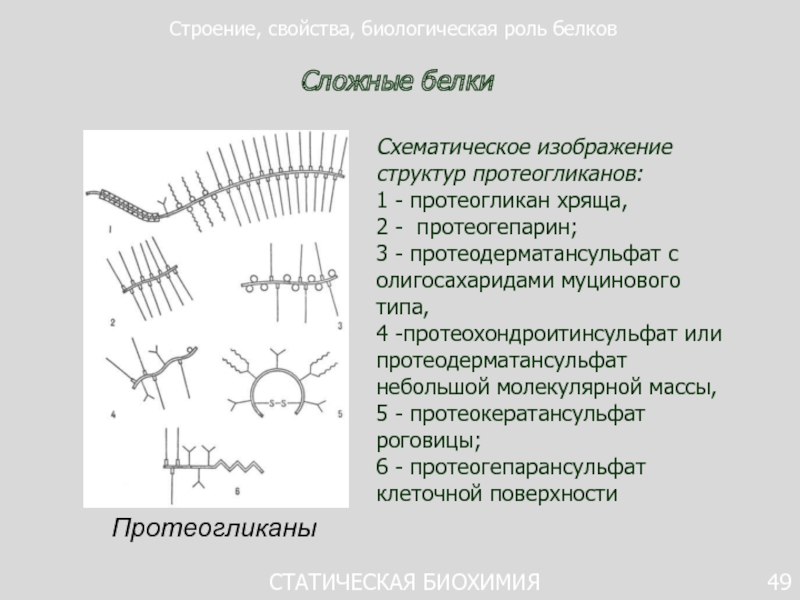
Схематическое изображение структур протеогликанов:
1 - протеогликан хряща,
2 - протеогепарин;
3 - протеодерматансульфат
с олигосахаридами муцинового типа, 4 -протеохондроитинсульфат или протеодерматансульфат небольшой молекулярной массы,
5 - протеокератансульфат роговицы;
6 - протеогепарансульфат клеточной поверхности
Протеогликаны
Слайд 93Строение, свойства, биологическая роль белков
50
СТАТИЧЕСКАЯ БИОХИМИЯ
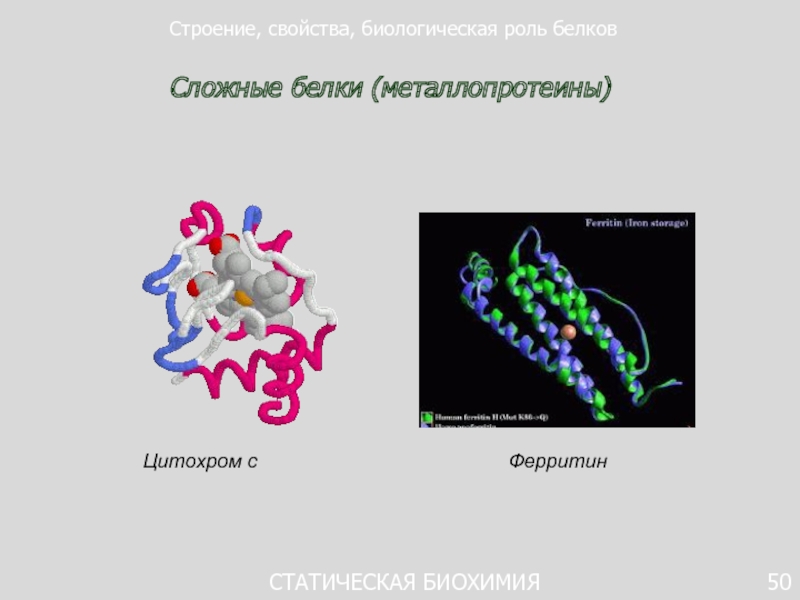
Сложные белки (металлопротеины)
Цитохром с
Ферритин
Слайд 94Строение, свойства, биологическая роль белков
51
СТАТИЧЕСКАЯ БИОХИМИЯ
Сложные белки (нуклеопротеины)
Модель вируса мозаичной
болезни табака,
а - спираль РНК; б - субъединицы белка
Слайд 99ЖИРЫ
Резервный жир
откладывается в жировой ткани
Запасается в организме 7-8 кг
Зависит от
пола, возраста, режима питания и др.
Протоплазматический жир
- является структурным компонентом
протоплазмы клетокВходит в состав всех органов и тканей
-составляет 25% от всех липидов организма
Остаётся на одном уровне в течении всей жизни организма
Слайд 100Биологическая роль липидов
Структурная функция или строительная
Регуляторная
Транспортная
Энергетическая функция
Запасная
Специфические функции
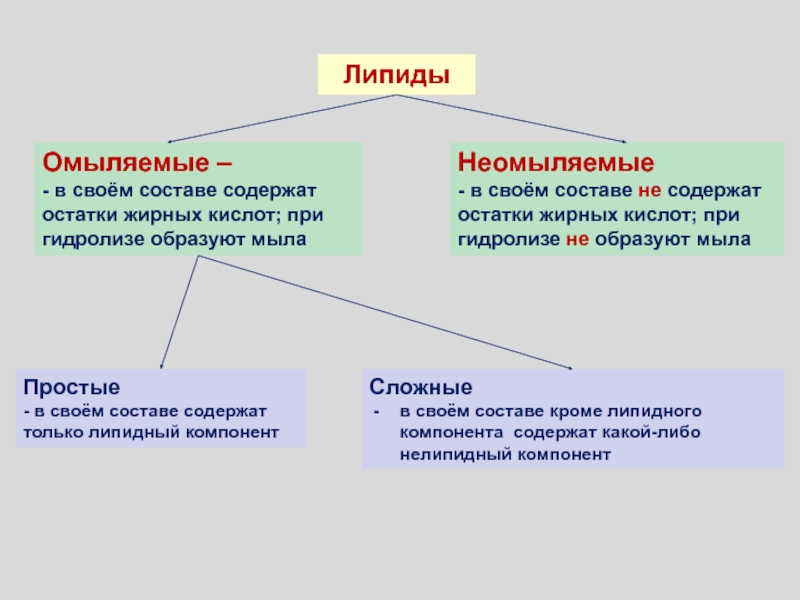
Слайд 104Омыляемые –
- в своём составе содержат остатки жирных кислот;
при гидролизе образуют мыла
Неомыляемые
- в своём составе не содержат остатки
жирных кислот; при гидролизе не образуют мылаЛипиды
Простые
- в своём составе содержат
только липидный компонент
Сложные
в своём составе кроме липидного компонента содержат какой-либо нелипидный компонент
Слайд 105Процесс гидролиза сложных эфиров в щелочной среде до сих пор
называют «омылением».
Например, омыление эфира, образованного глицерином, пальмитиновой и стеариновой
кислотами: Натриевые соли высших карбоновых кислот — основные компоненты твердого мыла, калиевые соли — жидкого мыла.
Омыляемые липиды
Слайд 106В живых организмах происходит ферментативный гидролиз жиров. В кишечнике под
влиянием фермента липазы жиры пищи гидратизуются на глицерин и органические
кислоты, которые всасываются стенками кишечника, и в организме синтезируются новые жиры, свойственные данному организму. Они по лимфатической системе поступают в кровь, а затем в жировую ткань. Отсюда жиры поступают в другие органы и ткани организма, где в процессе обмена веществ в клетках опять гидролиэу-ются и затем постепенно окисляются до оксида углерода и воды с выделеиием энергии, необходимой для жизнедеятельности.Омыляемые липиды
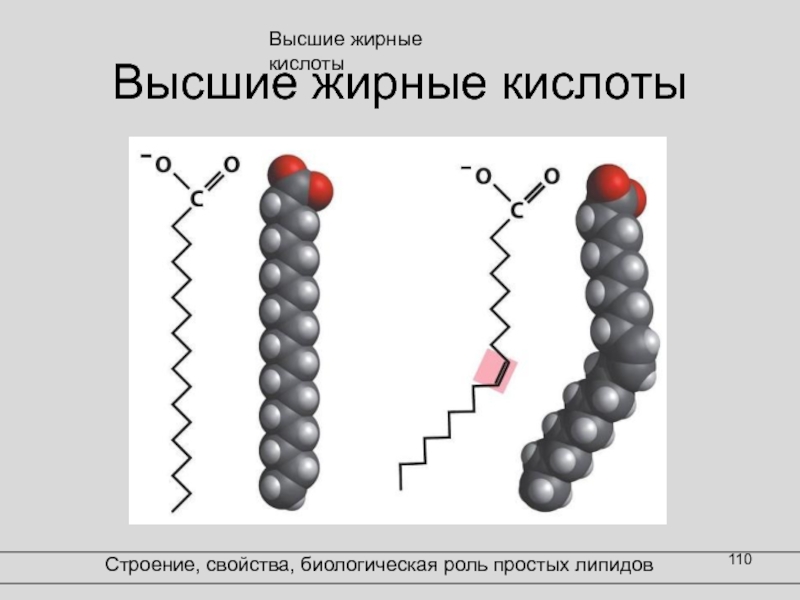
Слайд 110Высшие жирные кислоты
Строение, свойства, биологическая роль простых липидов
Высшие жирные кислоты
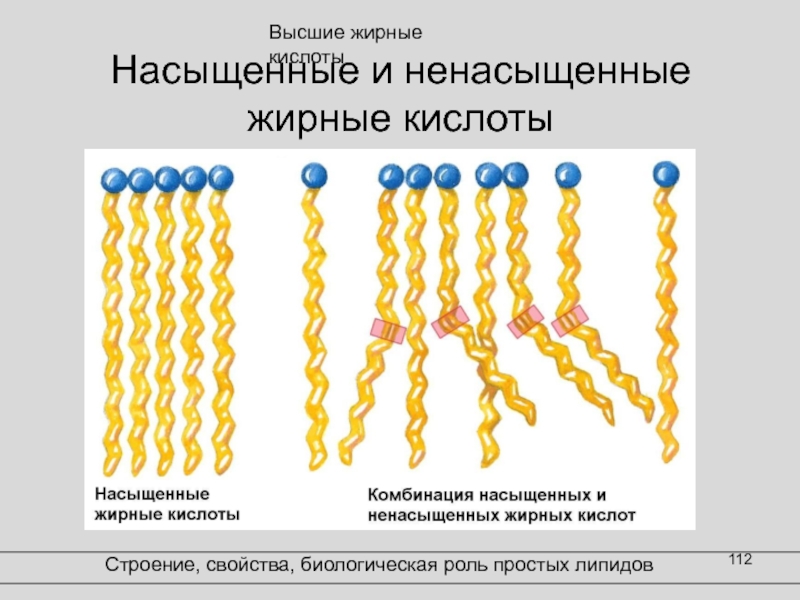
Слайд 112Насыщенные и ненасыщенные жирные кислоты
Строение, свойства, биологическая роль простых липидов
Высшие жирные кислоты
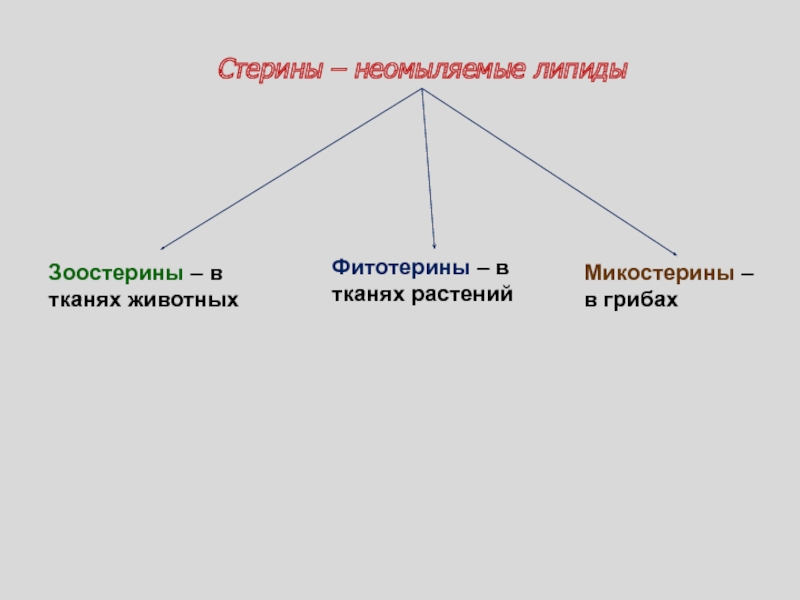
Слайд 117Стерины – неомыляемые липиды
Зоостерины – в тканях животных
Фитотерины – в
тканях растений
Микостерины – в грибах
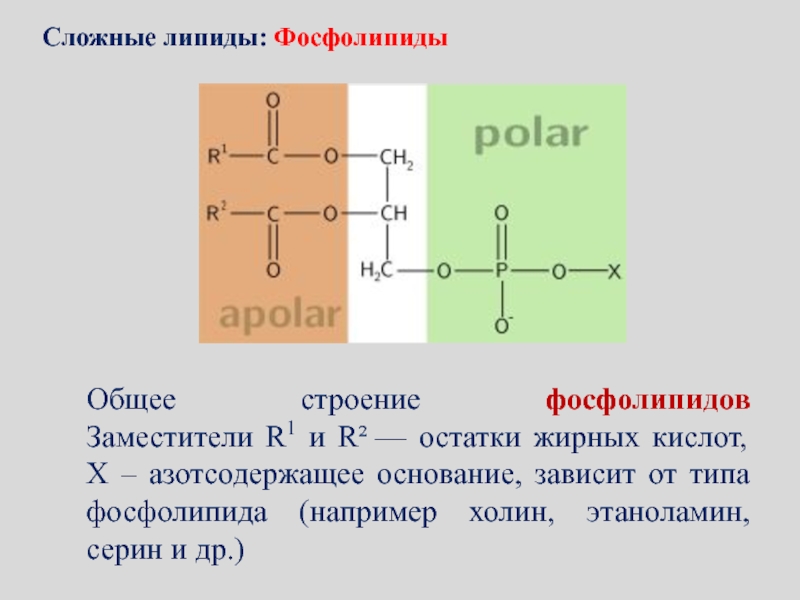
Слайд 120Общее строение фосфолипидов Заместители R1 и R² — остатки жирных кислот, X
– азотсодержащее основание, зависит от типа фосфолипида (например холин, этаноламин,
серин и др.)Сложные липиды: Фосфолипиды
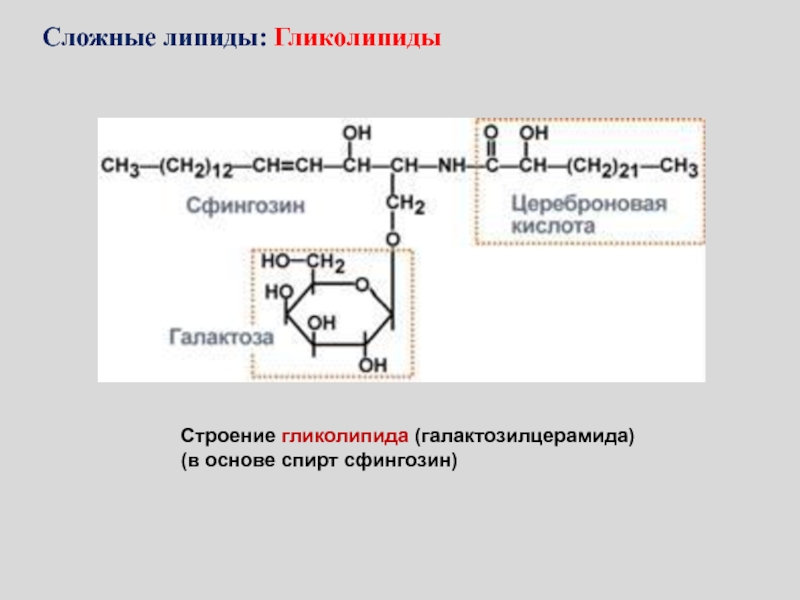
Слайд 123Строение гликолипида (галактозилцерамида)
(в основе спирт сфингозин)
Сложные липиды: Гликолипиды
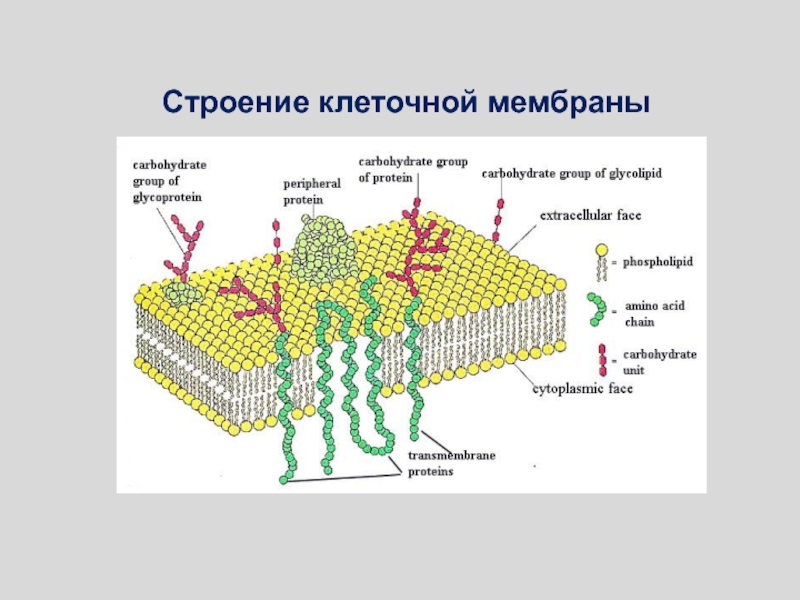
Слайд 124В настоящее время наибольшим признанием пользуется жидкостно-мозаичная модель мембраны, предложенная
в 1972 году Сингером и Николсоном (Singer, Nicolson). Согласно этой
модели мембрана состоит из бислоя липидов, в котором плавают (или закреплены) белковые молекулы, образуя в нём своеобразную мозаику. Мембранные белки могут пронизывать бислой насквозь (интегральный белок - 1), примыкать к бислою (периферический белок - 2) или погружаться в него. Многие белки мембраны являются гликопротеинами (4), а мембранообразующие липиды - гликолипидами (3). на схеме также показаны: холестерол (5); углевод (6); элементы цитоскелета (7).Сложные липиды: Гликолипиды
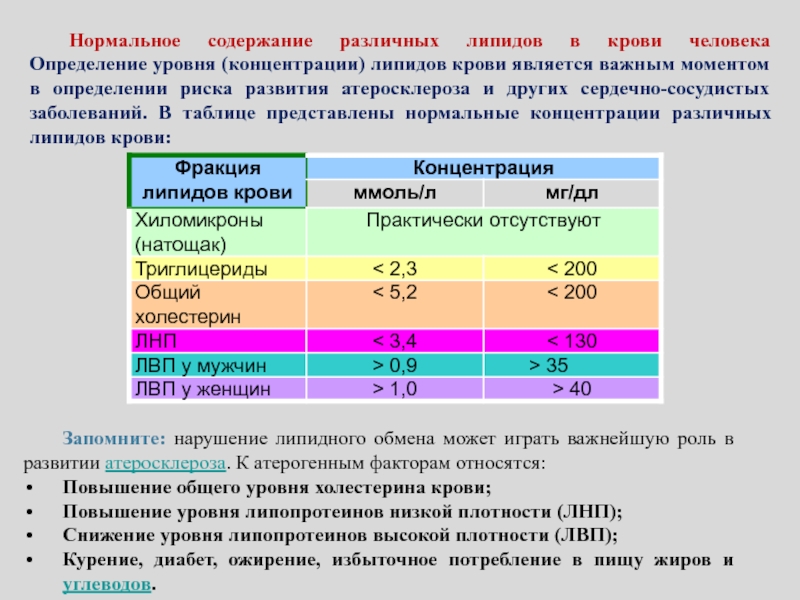
Слайд 127Нормальное содержание различных липидов в крови человека Определение уровня (концентрации) липидов
крови является важным моментом в определении риска развития атеросклероза и
других сердечно-сосудистых заболеваний. В таблице представлены нормальные концентрации различных липидов крови:Запомните: нарушение липидного обмена может играть важнейшую роль в развитии атеросклероза. К атерогенным факторам относятся:
Повышение общего уровня холестерина крови;
Повышение уровня липопротеинов низкой плотности (ЛНП);
Снижение уровня липопротеинов высокой плотности (ЛВП);
Курение, диабет, ожирение, избыточное потребление в пищу жиров и углеводов.