Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Уральский государственный аграрный университет д.х.н., проф. Хонина Татьяна
Содержание
- 1. Уральский государственный аграрный университет д.х.н., проф. Хонина Татьяна
- 2. План лекции 1. Сущность периодического закона. Причина
- 3. 3 п.1. Сущность периодического закона. Причина
- 4. 4
- 5. 5
- 6. Периодическая таблица Д.И. Менделеева6
- 7. 7
- 8. Периодический закон"Свойства простых тел, а также формы
- 9. Периодический закон сегодня:"Свойства химических элементов, а также
- 10. Периодическая система химических элементовПериодическая система химических
- 11. ПериодичностьПериодичность – это повторяемость химических и физических
- 12. 12 п.2. Строение периодической системы химических
- 13. Энергия ионизации Энергия (потенциал) ионизации атома Ei -
- 14. Сродство к электронуСродство атома к электрону Ee
- 15. Электроотрицательность(абсолютная электроотрицательность)Относительная электроотрицательность: Li = 1
- 16. Периодическая таблица Д.И. Менделеева16
- 17. ПериодичностьВертикальная периодичностьзаключается в повторяемости свойств химических элементов
- 18. П.3 Электронные s-,p-,d и f- семейства это
- 19. п.4. Основные типы химической связи
- 20. Ковалентная химическая связь это связь, возникающая между атомами
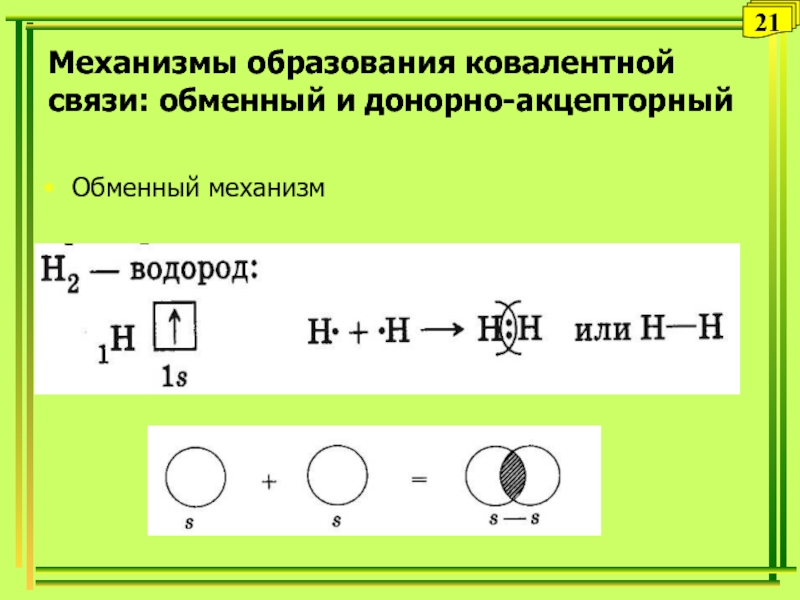
- 21. Обменный механизм21Механизмы образования ковалентной связи: обменный и донорно-акцепторный
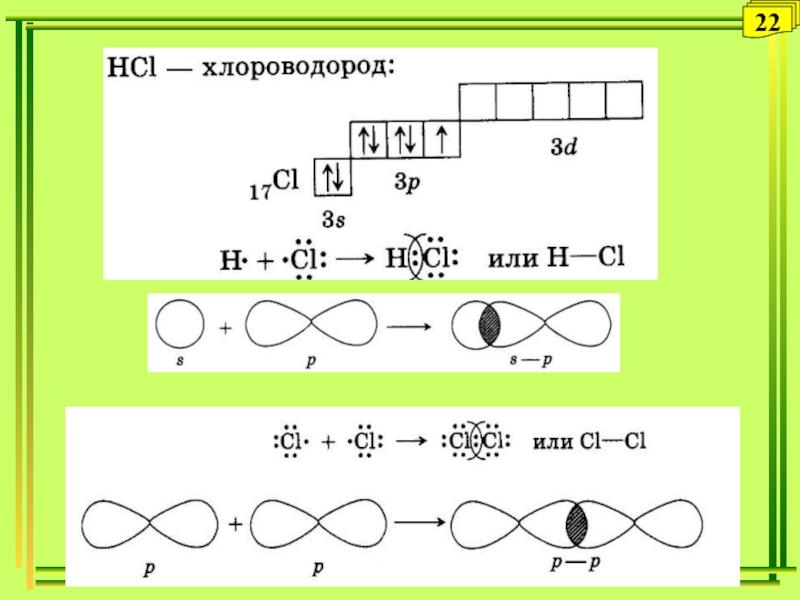
- 22. 22
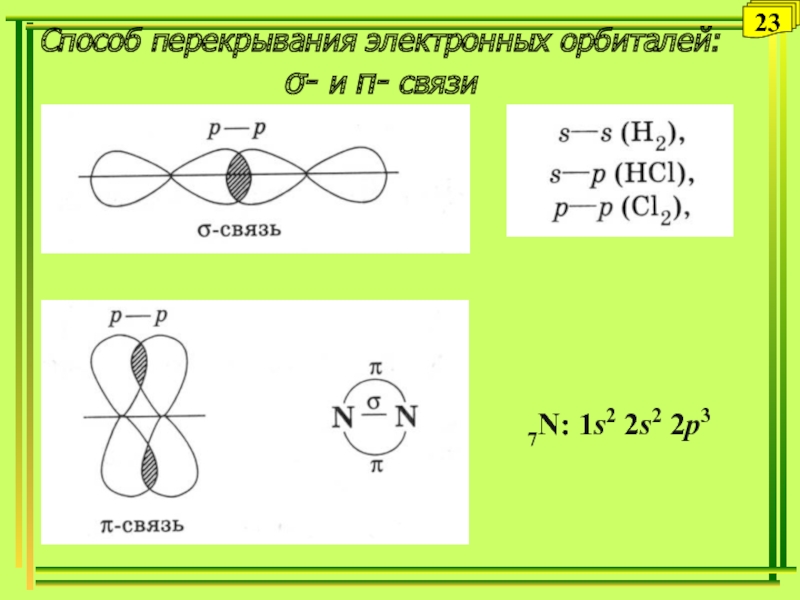
- 23. Способ перекрывания электронных орбиталей: - и - связи237N: 1s2 2s2 2p3
- 24. Полярность ковалентной связистепень смещенности общих электронных пар
- 25. Донорно-акцепторный механизм25Определение валентности:Валентность – способность атома к
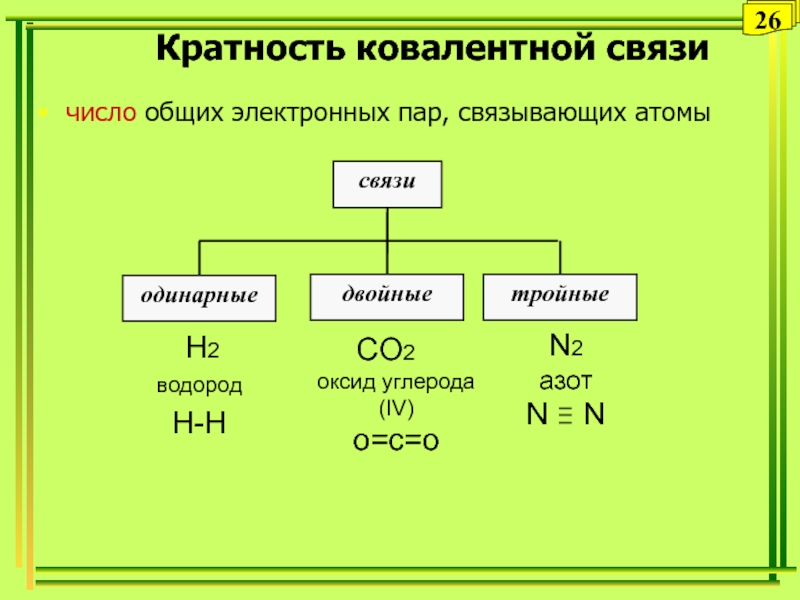
- 26. Кратность ковалентной связичисло общих электронных пар, связывающих атомы 26
- 27. Гибридизация атомных орбиталейГибридизация – это выравнивание (усреднение)
- 28. Примеры гибридизации (sp)4Be: [He]2s24Be*: [He]2s12p1s-АО + p-АО = 2sp-АО 284Be: 1s2 2s2BeF29F: 1s2 2s2 2p5
- 29. Примеры гибридизации (sp2)5B: [He]2s22p15B*: [He]2s12p2s-АО + 2p-АО
- 30. Примеры гибридизации (sp3) 6С: [He]2s22p26С*: [He]2s12p3s-АО + 3p-АО = 4sp3-АО Тетраэдр306С: 1s2 2s2 2p2
- 31. Ионная химическая связьэто связь, образовавшаяся за счет
- 32. Водородная связьХимическая связь между положительно поляризованными атомами
- 33. Металлическая связьсвязь в металлах и сплавах, которую
- 34. 34Вопросы к экзамену по общей и неорганической
- 35. 35Вопросы к экзамену (продолжение)10. Основные законы химии:
- 36. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Уральский государственный
аграрный университет
д.х.н., проф. Хонина Татьяна Григорьевна
Периодический закон
Д.И. Менделеева.
Химическая
связь и ее типы
Слайд 2План лекции
1. Сущность периодического закона. Причина периодической повторяемости химических
свойств и количественных характеристик атомов с увеличением зарядов их ядер.
2.
Строение периодической системы химических элементов Д.И. Менделеева. Характер и причины изменения металлических и неметаллических свойств, радиусов, энергии ионизации, энергии сродства к электрону, электроотрицательности атомов в периодах и группах периодической системы.3. Электронные s-, p-, d- и f – семейства.
4. Основные типы химической связи (ковалентная, ионная, металлическая, водородная), механизм их образования и свойства.
2
Слайд 3
3
п.1. Сущность периодического закона. Причина периодической повторяемости химических
свойств и количественных характеристик атомов с увеличением зарядов их ядер.
Электронная
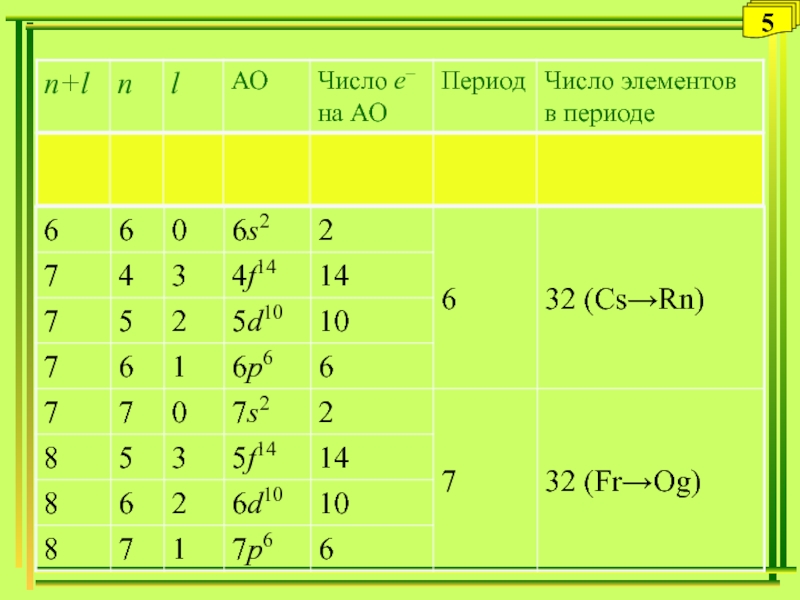
формула (конфигурация) атома – это условная запись, в которой все электроны атома распределены по энергетическим уровням и подуровням1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p
(n+l):
1 2 3 3 4 4 5 5 5 6 6 6 7 7 7 7 8 8 8
Слайд 8Периодический закон
"Свойства простых тел, а также формы и свойства соединений
элементов находятся в периодической зависимости (или, выражаясь алгебраически, образуют периодическую
функцию) от величины атомных весов элементов».МЕНДЕЛЕЕВ Дмитрий Иванович (8.02.1834 - 2.02.1907)
8
Слайд 9Периодический закон сегодня:
"Свойства химических элементов, а также образуемых ими простых
и сложных веществ находятся в периодической зависимости от заряда ядра".
Заряд ядра атома определяет число электронов.
Электроны заселяют атомные орбитали таким образом, что строение внешней электронной оболочки периодически повторяется.
Это выражается в периодическом изменении химических свойств элементов и их соединений.
9
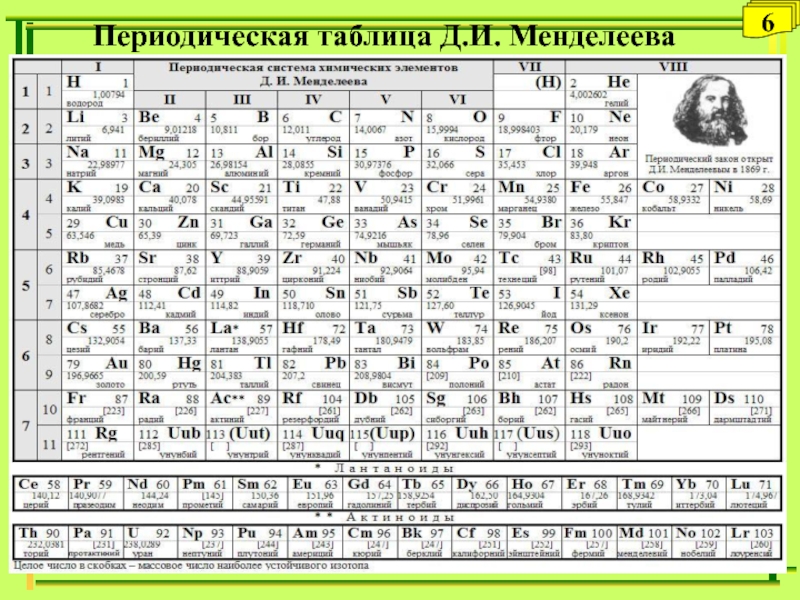
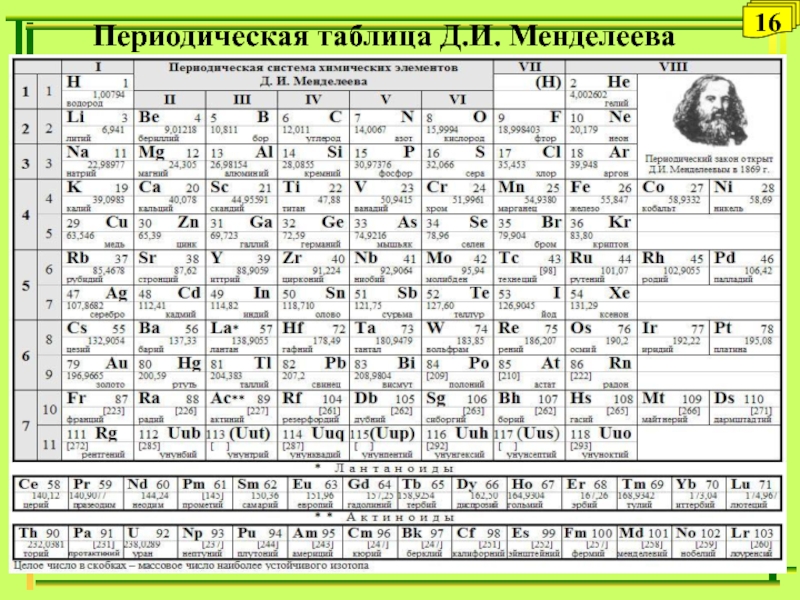
Слайд 10 Периодическая система химических элементов
Периодическая система химических элементов - естественная
классификация химических элементов, являющаяся табличным выражением периодического закона Д.И. Менделеева.
Прообразом Периодической системы химических элементов послужила таблица, составленная Д.И. Менделеевым 1 марта 1869 г.
В 1870 г. Менделеев назвал систему естественной, а в 1871 г. - периодической.
Формы периодической таблицы: короткопериодная, длиннопериодная
10
Слайд 11Периодичность
Периодичность – это повторяемость химических и физических свойств элементов и
их соединений по определенному направлению периодической системы при изменении порядкового
номера элементов.Виды периодичности: вертикальная, горизонтальная.
11
Слайд 12
12
п.2. Строение периодической системы химических элементов Д.И. Менделеева.
Характер и причины изменения металлических и неметаллических свойств, радиусов, энергии
ионизации, энергии сродства к электрону, электроотрицательности атомов в периодах и группах периодической системы.Свойства атомов
энергия ионизации
энергия сродства к электрону
электроотрицательность
атомный и ионный радиус
металлические свойства
неметаллические свойства
Слайд 13Энергия ионизации
Энергия (потенциал) ионизации атома Ei - минимальная энергия, необходимая
для удаления электрона из атома:
Х = Х+ + е−;
Ei Значения Ei (кДж/моль):
H 1312,1
K 418,7 F 1680,8 He 2372
Rb 403,0 Cl 1255,5 Ne 2080
Cs 375,7 Br 1142,6 Ar 1520
13
Слайд 14Сродство к электрону
Сродство атома к электрону Ee – способность атомов
присоединять добавочный электрон и превращаться в отрицательный ион.
Мерой сродства
к электрону служит энергия, выделяющая или поглощающаяся при этом: Х + е− = Х− ; Ee Значения Ee (кДж/моль)
F −345,7
Cl −366,7
Br −341,6
14
Слайд 15Электроотрицательность
(абсолютная электроотрицательность)
Относительная электроотрицательность:
Li = 1
F = 4
Лайнус-Карл ПОЛИНГ
(28.02.1901 – 19.08.1994)
Одна из
самых распространенных – шкала электроотрицательности Оллреда – Рохова 15
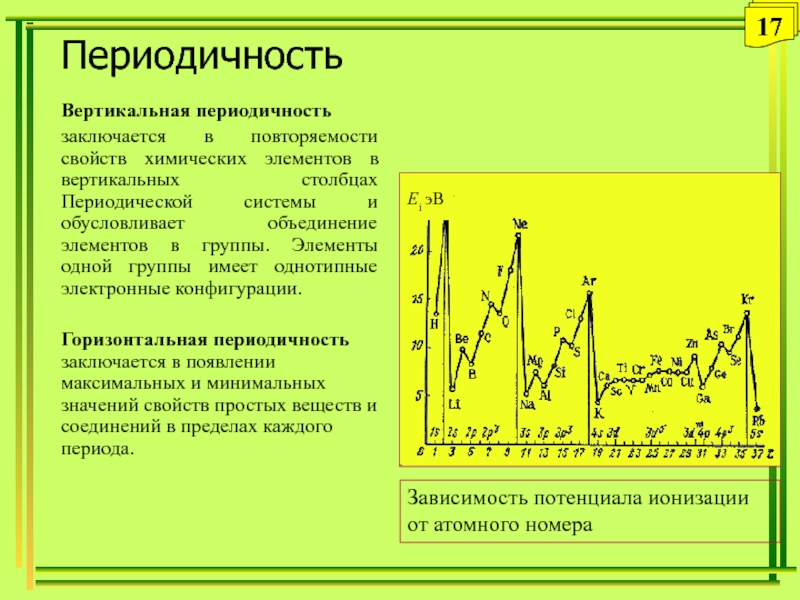
Слайд 17Периодичность
Вертикальная периодичность
заключается в повторяемости свойств химических элементов в вертикальных столбцах
Периодической системы и обусловливает объединение элементов в группы. Элементы одной
группы имеет однотипные электронные конфигурации.Горизонтальная периодичность заключается в появлении максимальных и минимальных значений свойств простых веществ и соединений в пределах каждого периода.
Зависимость потенциала ионизации от атомного номера
17
Слайд 18П.3 Электронные s-,p-,d и f- семейства это связь между положением элемента
в периодической системе и электронным строением его атома; от того,
какой энергетический подуровень заполняется последним, различают 4 электронных семейства: s-, p-, d- и f. S-Элементы – семейство химических элементов, у которых при заполнении электронных подуровней последний электрон заполняет s-подуровень внешнего энергетического уровня. Это главные подгруппы I и II групп. ns1,2; (n=1-7). 14 s-элементов. Р-Элементы – семейство химических элементов, у которых при заполнении электронных подуровней последний электрон заполняет р-подуровень внешнего энергетического уровня. Это элементы главных подгрупп III – VIII групп. ns2nр1-6 . (n=2-7). 36 р-элементов. d-Элементы – заполняется d-подуровень предвнешнего уровня. Это элементы побочных подгрупп; входят в 4-7 периоды. ns2(n-1)d1-10 ; (n=4-7). 40 d-элементов. f- Элементы – заполняется f-подуровень предпредвнешнего уровня (3-ий снаружи). Это элементы 6 и 7 периодов, соответственно, лантаноиды: № 58 (церий) - №71(лютеций) и актиноиды: №90 (торий) - №103 (лоуренсий). ns2(n-2)f1-14; (n=6,7). 28 f- элементов18
Слайд 19 п.4. Основные типы химической связи (ковалентная, ионная, металлическая, водородная),
механизм их образования и свойства. Под химической связью понимают такое взаимодействие
атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы19
Слайд 20Ковалентная химическая связь
это связь, возникающая между атомами за счет образования
общих электронных пар
20
Параметры и свойства ковалентной связи
Энергия связи характеризует
прочность химической связи.Длина связи – расстояние между ядрами атомов, образующих связь.
Насыщаемость. Способность атомов образовывать ограниченное число валентных связей. В соответствии с принципом Паули на перекрываемых орбиталях могут присутствовать не более двух электронов с противоположными спинами.
Направленность. Перекрываемые орбитали должны иметь одинаковую симметрию относительно межъядерной оси (вдоль σ-связей). Совокупность направленных, строго ориентированных в пространстве σ-связей создает структуру химической частицы.
Полярность связи характеризует смещение связующего электронного облака в сторону более ЭО элемента
Образование кратных связей при дополнительном перекрывании атомных орбиталей (-связи).
Гибридизация - выравнивание электронных орбиталей по форме и энергии
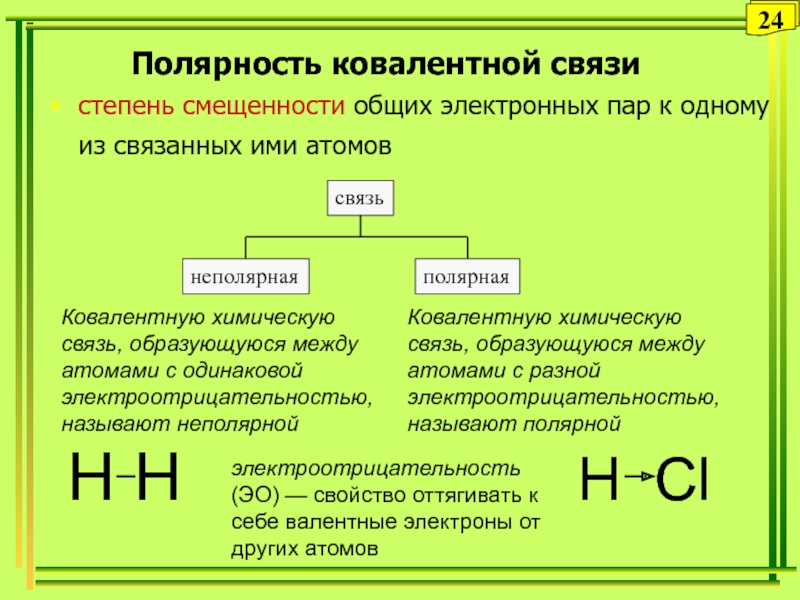
Слайд 24Полярность ковалентной связи
степень смещенности общих электронных пар к одному из
связанных ими атомов
электроотрицательность (ЭО) — свойство оттягивать к себе
валентные электроны от других атомовКовалентную химическую связь, образующуюся между атомами с одинаковой электроотрицательностью, называют неполярной
Ковалентную химическую связь, образующуюся между атомами с разной электроотрицательностью, называют полярной
H H
H Сl
24
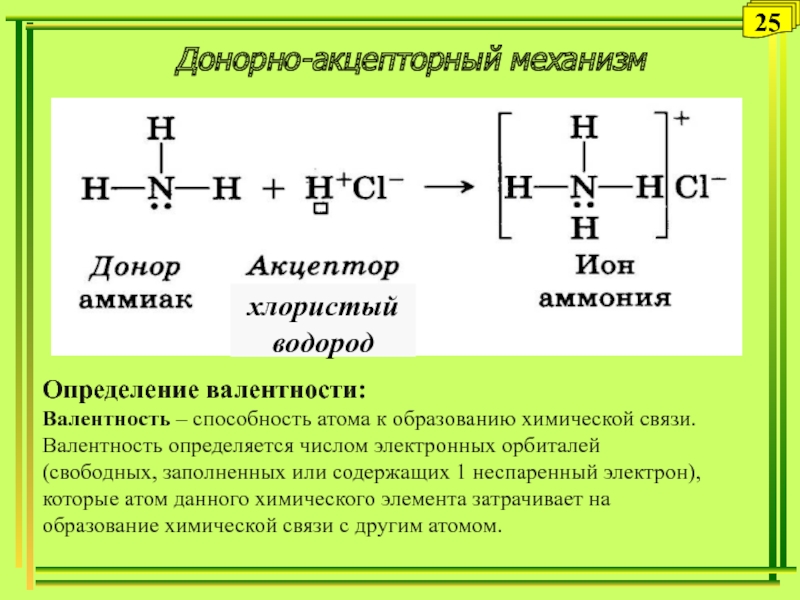
Слайд 25Донорно-акцепторный механизм
25
Определение валентности:
Валентность – способность атома к образованию химической связи.
Валентность определяется числом электронных орбиталей (свободных, заполненных или содержащих 1
неспаренный электрон), которые атом данного химического элемента затрачивает на образование химической связи с другим атомом.Слайд 27Гибридизация атомных орбиталей
Гибридизация – это выравнивание (усреднение) энергетических и геометрических
характеристик атомных орбиталей разных подуровней при образовании химических связей.
В
результате появляются гибридные орбитали, которые ориентируются в пространстве таким образом, чтобы расположенные на них электронные пары (или неспаренные электроны) были максимально удалены друг от друга.27
Слайд 28Примеры гибридизации (sp)
4Be: [He]2s2
4Be*: [He]2s12p1
s-АО + p-АО = 2sp-АО
28
4Be:
1s2 2s2
BeF2
9F: 1s2 2s2 2p5
Слайд 29Примеры гибридизации (sp2)
5B: [He]2s22p1
5B*: [He]2s12p2
s-АО + 2p-АО = 3sp2-АО
Плоский
треугольник
29
5B: 1s2 2s2 2p1
9F: 1s2 2s2 2p5
Слайд 30Примеры гибридизации (sp3)
6С: [He]2s22p2
6С*: [He]2s12p3
s-АО + 3p-АО = 4sp3-АО
Тетраэдр
30
6С: 1s2 2s2 2p2
Слайд 31Ионная химическая связь
это связь, образовавшаяся за счет
электростатического
притяжения
катионов к анионам
31
Кристаллическая решетка хлорида натрия,
состоящая из противоположно заряженных ионов натрия и хлорид-ионовСлайд 32Водородная связь
Химическая связь между положительно поляризованными атомами водорода одной молекулы
(или ее части) и отрицательно поляризованными атомами сильно электроотрицательных элементов,
имеющих неподеленные электронные пары (F, О, N и реже Сl и S) другой молекулы (или ее части)O H…..O H…..O H….
H H H
32
Слайд 33Металлическая связь
связь в металлах и сплавах, которую выполняют относительно свободные
электроны между ионами металлов в металлической кристаллической решетке
о п+М — пе М
Схема образования металлической связи:
.
33
Слайд 3434
Вопросы к экзамену
по общей и неорганической химии
1. Понятия: материя,
вещество. Предмет науки химия
2. Качественная и количественная характеристика состава атомов
3.
Строение электронных оболочек атомов. Квантовые числа. Энергетические уровни и подуровни, атомные электронные орбитали.4. Правила составления электронных формул и схем строения электронных оболочек атомов (принцип минимальной энергии, правила Клечковского, Хунда, принцип Паули)
5. Химические (окислительные, восстановительные) свойства атомов химических элементов и порядок их определения
6. Сущность периодического закона. Причина периодической повторяемости химических свойств и количественных характеристик атомов с увеличение зарядов их ядер
7. Строение периодической системы химических элементов Д.И.Менделеева. Характер и причины изменения металлических и неметаллических свойств, радиусов, энергии ионизации, энергии сродства к электрону, электроотрицательности атомов в периодах и группах периодической системы
8. Основные типы химической связи (ковалентная, ионная, металлическая), механизм их образования и свойства
9. Классы сложных неорганических соединений. Состав, номенклатура, химические свойства и реакции оксидов, кислот, оснований и солей
Слайд 3535
Вопросы к экзамену (продолжение)
10. Основные законы химии: закон сохранения массы
вещества, закон постоянства состава вещества, закон Авогадро и два следствия
из него. Применение этих законов для вычисления состава, массы и объема веществ11. Основы термохимии. Тепловой эффект химической реакции, изменение энтальпии химической реакции. Закон Гесса. Пример расчета изменения энтальпии реакции
12. Понятия скорости гомогенной и гетерогенной реакций. Зависимость скорости химической реакции от концентрации реагирующих веществ, давления, температуры. Закон действия масс, правило Вант-Гоффа.
13. Сущность химического равновесия и условие его наступления. Константа химического равновесия. Определение направления смещение химического равновесия в соответствии с принципом Ле Шателье.
14. Понятие раствор. Типы растворов. Способы выражения состава (концентрации) растворов
15. Теория электролитической диссоциации. Степень и константа диссоциации. Сильные и слабые электролиты
16. Диссоциация воды, ионное произведение воды. Водородный показатель. Шкала рН растворов
17. Реакции ионного обмена, условия их протекания. Порядок составления ионных уравнений
18. Гидролиз солей
19. Сущность окислительно-восстановительных реакций и условие их протекания. Степени окисления атомов и порядок их определения. Составление уравнений окислительно-восстановительных реакции на основе метода электронного баланса
20. Комплексные соединения металлов, их состав и поведение (устойчивость) в растворах. Константа нестойкости комплексных ионов.
21. Химия s,p,d-элементов таблицы Менделеева
22. Химия биогенных элементов. Понятие о микроэлементах.

















![Уральский государственный
аграрный университет
д.х.н., проф. Хонина Татьяна Примеры гибридизации (sp)4Be: [He]2s24Be*: [He]2s12p1s-АО + p-АО = 2sp-АО 284Be: 1s2 2s2BeF29F: 1s2 2s2 2p5 Примеры гибридизации (sp)4Be: [He]2s24Be*: [He]2s12p1s-АО + p-АО = 2sp-АО 284Be: 1s2 2s2BeF29F: 1s2 2s2 2p5](/img/thumbs/5a842c75455bff14c2ac79c14cb140eb-800x.jpg)
![Уральский государственный
аграрный университет
д.х.н., проф. Хонина Татьяна Примеры гибридизации (sp2)5B: [He]2s22p15B*: [He]2s12p2s-АО + 2p-АО = 3sp2-АО Плоский треугольник295B: Примеры гибридизации (sp2)5B: [He]2s22p15B*: [He]2s12p2s-АО + 2p-АО = 3sp2-АО Плоский треугольник295B: 1s2 2s2 2p19F: 1s2 2s2 2p5](/img/thumbs/751f1d15a85076330a59ae6b96305297-800x.jpg)
![Уральский государственный
аграрный университет
д.х.н., проф. Хонина Татьяна Примеры гибридизации (sp3) 6С: [He]2s22p26С*: [He]2s12p3s-АО + 3p-АО = 4sp3-АО Тетраэдр306С: 1s2 2s2 2p2 Примеры гибридизации (sp3) 6С: [He]2s22p26С*: [He]2s12p3s-АО + 3p-АО = 4sp3-АО Тетраэдр306С: 1s2 2s2 2p2](/img/thumbs/592830298a135634e98c97d058ba5941-800x.jpg)
























