Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Урок по химии 11 класс по теме: Строение атома
Содержание
- 1. Урок по химии 11 класс по теме: Строение атома
- 2. Понятие атом Атом (греч. «atomos» – неделимый)
- 3. Атомно-молекулярное учениеВозродил атомистическую теорию английский физик и
- 4. Атом делим!!!Атом делим, как доказали следующие экспериментальные
- 5. Катодные лучи В 1879 году Крукс
- 6. Фотоэффект Русский ученый Столетов открыл явление фотоэффекта
- 7. Рентгеновское излучениеЗначимым стало открытие Рентгеном «Х»-лучей. Эти
- 8. РадиоактивностьБольшой вклад в развитие представлений об элементарных
- 9. ЭлектролизВспомните, что это?Электро́лиз — физико-химический процесс, состоящий в
- 10. Модели строения атомаМодель Томсона – «пудинговая модель»1904 год
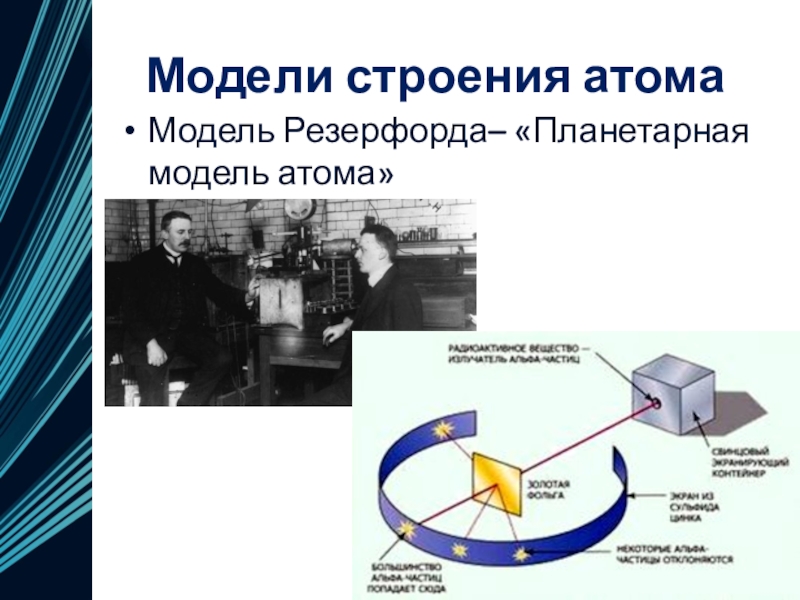
- 11. Модели строения атомаМодель Резерфорда– «Планетарная модель атома»
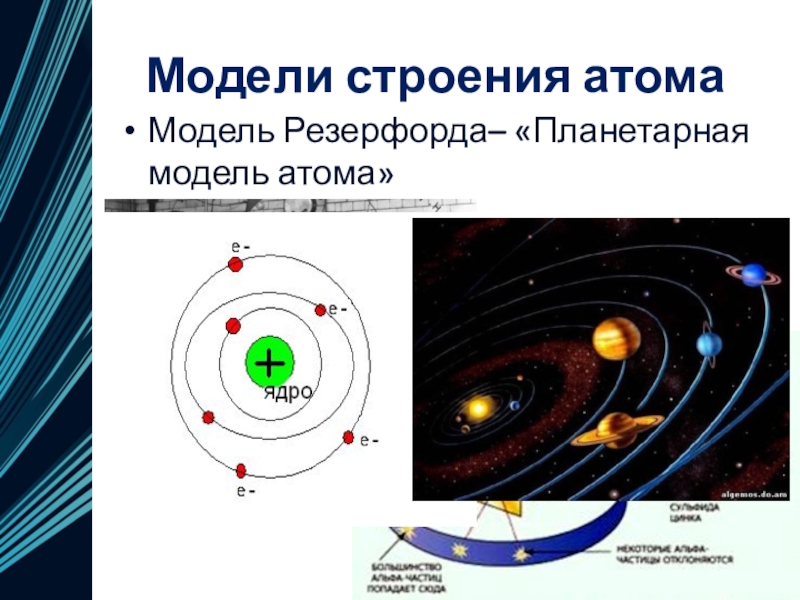
- 12. Модели строения атомаМодель Резерфорда– «Планетарная модель атома»
- 13. Недостатки 1)Резерфорд не смог объяснить устойчивости атома.
- 14. Квантовая модель1913 год Основные
- 15. Протонно-нейтронная модель В 1932 году Иваненко
- 16. Протонно-нейтронная модель Атом – электронейтральная система
- 17. Протонно-нейтронная модель1. Определите число протонов и нейтронов
- 18. Изотопы - Это разновидности атомов одного и
- 19. Электронное облако- - это Пространство вокруг атомного
- 20. РефлексияТема сегодняшнего урока была интересна, все было
- 21. Д/з п.1, в.3,6,7,10
- 22. Источники Габриелян О.С. Химия. 11 класс. Базовый
- 23. Источникиhttps://upload.wikimedia.org/wikipedia/commons/thumb/9/95/X-ray_tube_3.jpg/350px-X-ray_tube_3.jpghttps://upload.wikimedia.org/wikipedia/commons/e/ee/Pierrecurie.jpghttps://upload.wikimedia.org/wikipedia/commons/thumb/3/39/ElectrochemCell.png/250px-ElectrochemCell.pnghttp://www.welsch.com/gallery/bitmap/Rosinenkuchen_nach__Thompson_077.jpghttp://konspekta.net/studopediaorg/baza8/1675971940325.files/image077.pnghttp://nasha-vselennaya.ru/wp-content/uploads/2014/03/article_2148631_133EEE43000005.jpghttp://900igr.net/datas/fizika/Spektr-izluchenija/0015-015-2-natrij.jpghttp://msk.edu.ua/ivk/Fizika/Konspekt/model_yadra_f/3.gifhttps://upload.wikimedia.org/wikipedia/commons/thumb/4/4a/Single_electron_orbitals.jpg/500px-Single_electron_orbitals.jpghttp://i.playground.ru/i/13/77/37/00/pix/image.jpghttp://cs3.livemaster.ru/zhurnalfoto/2/8/7/150215092945.jpeghttp://imagenes.cartelitosface.com/galerias/iconos-estado-de-animo/008.png
- 24. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Урок по химии 11 класс по теме: «Строение атома».
Преподаватель ГБПОУ
ВО ВАТ имени В.П.Чкалова Кузнецова Е.В.
Слайд 2Понятие атом
Атом (греч. «atomos»
– неделимый) ввел Демокрит.
Атомы
выступают в роли первоначала. Они неделимы, различаются по величине, весу,
форме и находятся в вечном движении.(ок. 460 до н. э. — 370 до н. э.)
Слайд 3Атомно-молекулярное учение
Возродил атомистическую теорию английский физик и химик Джон Дальтон.
Атомы одного элемента имеют одинаковые свойства, а разных элементов –
различаются по свойствам. Дальтон ввел важную характеристику атома – атомную массу и для очень многих элементов были установлены ее относительные значения.
«Атом неделим, вечен и неразрушим».
(1766 —1844)
Слайд 4Атом делим!!!
Атом делим, как доказали следующие экспериментальные открытия, сделанные в
науке на рубеже конца 19-начала 20 века.
Слайд 5Катодные лучи
В 1879 году Крукс открыл катодные лучи, представляющие
собой поток электронов в вакуумной трубке, содержащей катод и анод.
Английский физик Джозеф Томпсон назвал частицы катодных лучей электронами.Слайд 6Фотоэффект
Русский ученый Столетов открыл явление фотоэффекта
– испускание металлом
электронов под действием падающего на него света.
Алекса́ндр Григо́рьевич Столе́тов
(1839, - 1896, )
Слайд 7Рентгеновское излучение
Значимым стало открытие Рентгеном «Х»-лучей.
Эти лучи представляют собой
электромагнитное излучение подобное свету с гораздо более высокой частотой, испускаемой
при действии на них катодных лучей.Слайд 8Радиоактивность
Большой вклад в развитие представлений об элементарных частицах внесли
Радиоактивность
– это явление самопроизвольного превращения одного химического элемента в другой,
сопровождаемое испусканием электронов или других частиц и рентгеновского излучения.Мари́я Склодо́вская-Кюри́
(1867- 1934)
Слайд 9Электролиз
Вспомните, что это?
Электро́лиз — физико-химический процесс, состоящий в выделении на электродах составных частей
растворённых веществ или других веществ, являющихся результатом окислительно-восстановительных реакций на электродах,
который возникает при электрического тока через раствор, либо расплав электролитаСлайд 13Недостатки
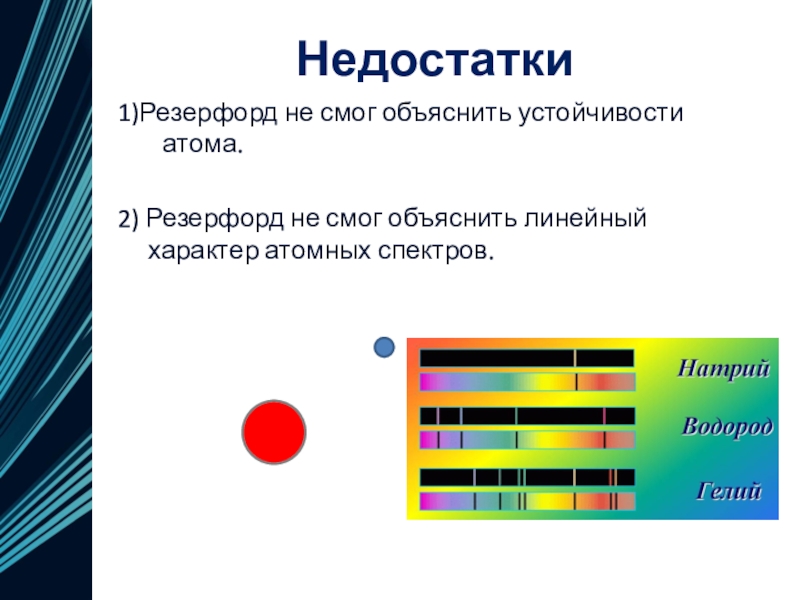
1)Резерфорд не смог объяснить устойчивости атома.
2) Резерфорд не
смог объяснить линейный характер атомных спектров.
Слайд 14Квантовая модель
1913 год
Основные положения он сформулировал
в виде постулатов:
I. Электрон может вращаться вокруг ядра по определенным,
стационарным круговым орбиталям.II. Двигаясь по стационарной орбите, электрон не излучает энергию.
III. Излучение электромагнитной энергии (либо ее поглощение) происходит при переходе электрона с одной стационарной орбиты на другую.
Нильс Хе́нрик
Дави́д Бор
(1885-1962)
Слайд 15 Протонно-нейтронная модель
В 1932 году Иваненко предложил протонно-нейтронную модель
ядра. Эту теорию развил Гейзенберг. Эта модель строения атома существует
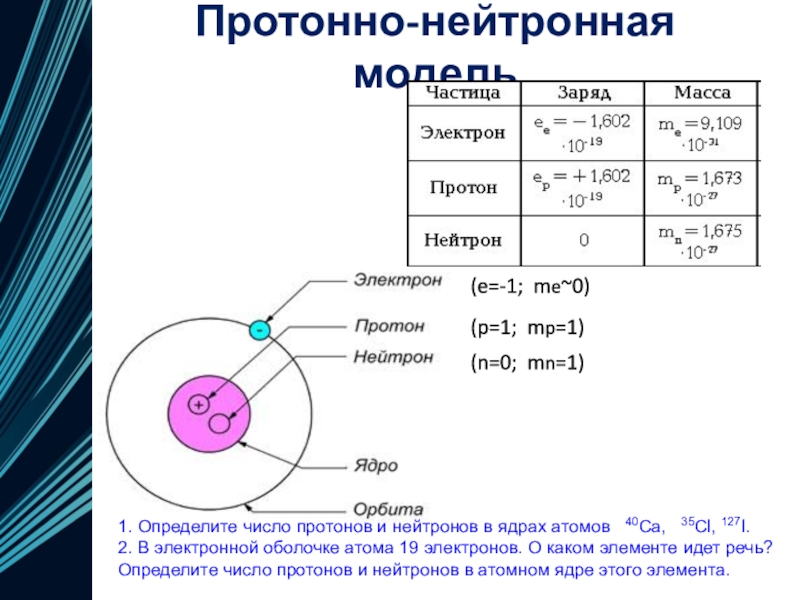
до сих пор, сочетает в себе все предыдущие модели и «исправляет» их недостатки.Слайд 16 Протонно-нейтронная модель
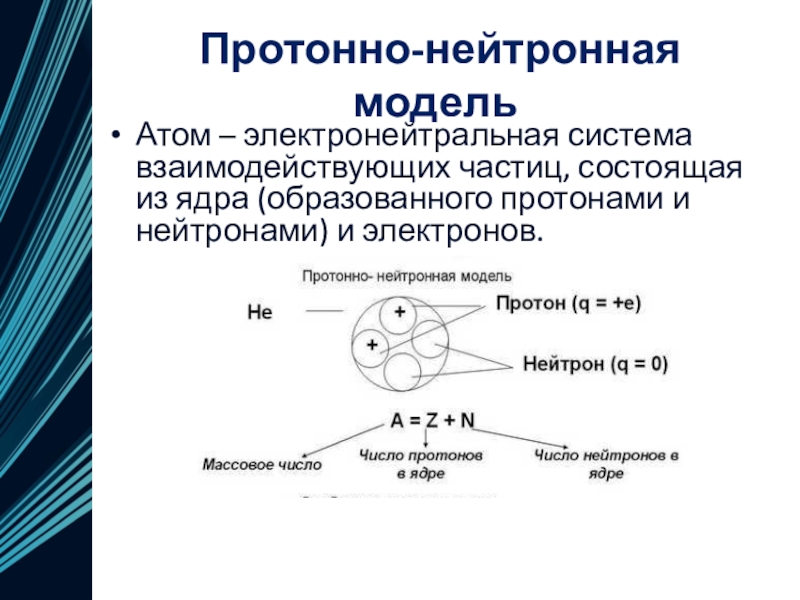
Атом – электронейтральная система взаимодействующих частиц, состоящая
из ядра (образованного протонами и нейтронами) и электронов.
Слайд 17Протонно-нейтронная модель
1. Определите число протонов и нейтронов в ядрах атомов
40Ca, 35Cl, 127I.
2. В электронной оболочке атома 19
электронов. О каком элементе идет речь? Определите число протонов и нейтронов в атомном ядре этого элемента.Слайд 18Изотопы -
Это разновидности атомов одного и того же химического
элемента, имеющие одинаковый заряд атомного ядра(одинаковое число протонов в нем,
но разные массовые числа(разное число протонов)Химический элемент – это вид атомов с одинаковым зарядом ядра, или совокупность изотопов.
Какими величинами характеризуется изотоп?
Почему изотопы одного элемента имеют разные массовые числа?
Почему в периодической системе у химических элементов указаны дробные значения относительной атомной массы?
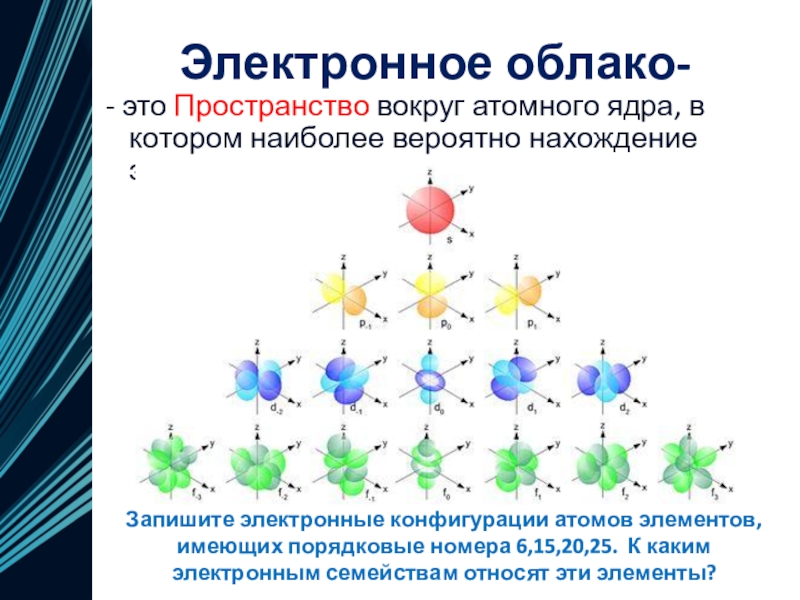
Слайд 19Электронное облако-
- это Пространство вокруг атомного ядра, в
котором наиболее вероятно нахождение электрона.
Запишите электронные конфигурации атомов элементов, имеющих
порядковые номера 6,15,20,25. К каким электронным семействам относят эти элементы?Слайд 20Рефлексия
Тема сегодняшнего урока была интересна, все было понятно -
Мне
было интересно, но не все было понятно
Было неинтересно, ничего не
понятноСлайд 22Источники
Габриелян О.С. Химия. 11 класс. Базовый уровень: учеб. для
общеобразоват. учреждений. – М., 2013.
Габриелян О.С. Настольная книга учителя химии: 11
класс: в 2 ч. / О.С. Габриелян, Г.Г. Лысова, А.Г. Введенская – М., 2004.Шаблон презентации http://lotoskay.ucoz.ru/load/shablony_dlja_prezentacij/khimija/atom/189-1-0-6494
https://upload.wikimedia.org/wikipedia/commons/thumb/5/50/Sir_William_Crookes.jpg/208px-Sir_William_Crookes.jpg
https://upload.wikimedia.org/wikipedia/commons/thumb/b/b6/Jj-thomson2.jpg/267px-Jj-thomson2.jpg
http://joy4mind.com/wp-content/uploads/2013/08/Trubka-Kruksa.jpg
http://people.bath.ac.uk/lg371/index_htm_files/26.png
https://upload.wikimedia.org/wikipedia/commons/thumb/7/71/Roentgen2.jpg/200px-Roentgen2.jpg
https://upload.wikimedia.org/wikipedia/commons/thumb/f/fb/Curie-nobel-portrait-2-600.jpg/250px-Curie-nobel-portrait-2-600.jpg
https://upload.wikimedia.org/wikipedia/commons/thumb/a/a3/Henri_Becquerel.jpg/250px-Henri_Becquerel.jpg