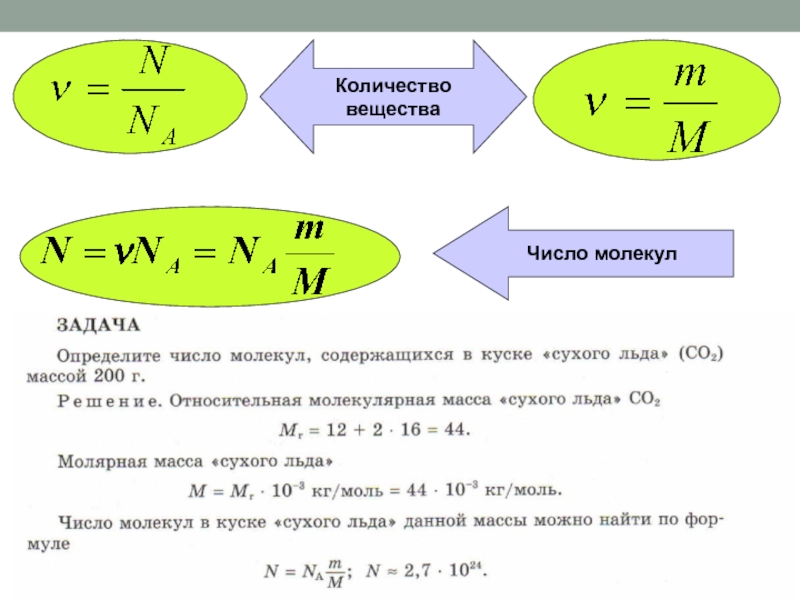
Слайд 1Валентность. Степень окисления. Составление электронных конфигураций Типы химической связи.
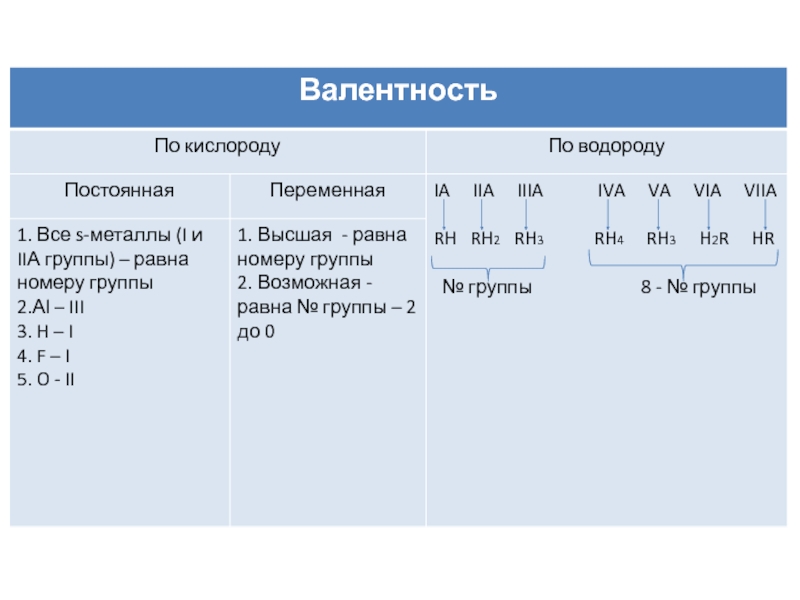
Слайд 4Правило валентности
В большинстве бинарных соединений типа AxBy
произведение валентности элемента А (m) на число его атомов в
молекуле (х) равно произведению валентности элемента В (n) на число его атомов (y):
mx=ny
Пример:
Определить валентность фосфора в соединении Р2О5
Р2О5
Валентность кислорода постоянна и равна II
m*2=2*5
m=5
Фосфор в соединении P2O5 пятивалентен
m II
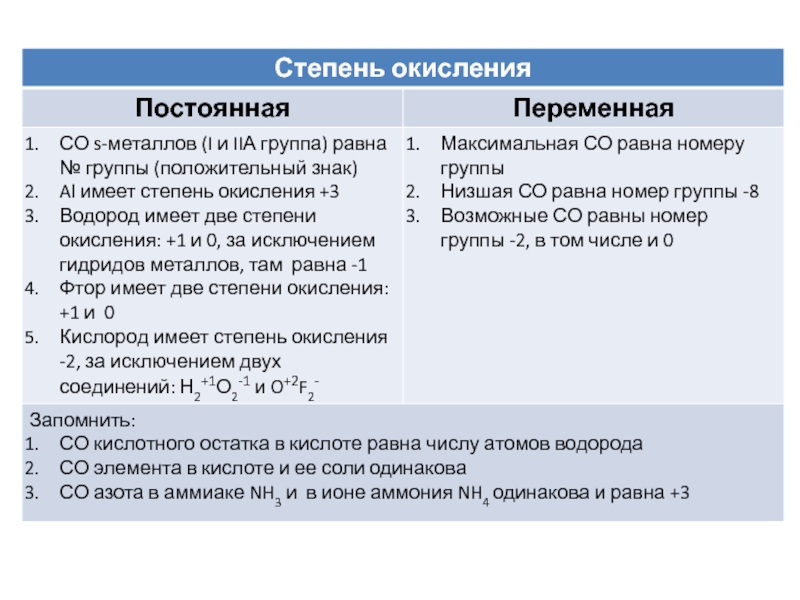
Слайд 7Правило определения степени окисления
Сумма зарядов всех атомов в молекуле равна
нулю.
Примеры:
H Cl O4
1+x+(-2)*4=0
x=+7
Ca (Cl O3)2
2+x*2+(-2)*6=0
x=+10/2=+5
(NH4)2 Cr2 O7
1*2+x*2+(-2)*7=0
x=+12/2=+6
H2 S O4
1*2+x+(-2)*4=0
x=+6
H Cl
O3
1+x+(-2)*3=0
x=+5
H2 P2 O7
1*2+x*2+(-2)*7=0
x=+12/2=+6
+8 -8
+12 -12
+8 -8
+6 -6
+14 -14
+14 -14
Слайд 8Квантовые числа
n – главное квантовое число. Характеризует энергию электрона на
энергетическом уровне.
Определяет:
Число энергетических уровней (n= №
периода)
Максимальное число электронов на энергетическом уровне по формуле 2n2
Число энергетических подуровней на энергетическом уровне
Слайд 9Квантовые числа
2. l – побочное квантовое число. Характеризует энергию электрона
на энергетическом подуровне и форму электронного облака.
Численно равно n-1
Слайд 10Квантовые числа
3. ml – магнитное квантовое число. Определяет ориентацию электронного
облака и число электронных орбиталей на подуровне
Численно равно –l; 0;
l
Слайд 11Квантовые числа
4. ms - спиновое квантовое число.
Определяет направление вращения электрона
вокруг собственной оси.
Слайд 12Правила для определения расположения электрона в атоме
Принцип Паули(принцип запрета)
В атоме
не может быть двух электронов с одинаковым набором всех четырех
квантовых чисел. Поэтому на одной орбитали не может быть больше двух электронов.
Максимальное число электронов на подуровне:
s p d f
2 6 10 14
Слайд 132. Правило Гунда
Электроны располагаются таким образом, чтобы суммарный спин был
максимальным
Правила для определения расположения электрона в атоме
Слайд 143. Правило Клечковского
Электроны заполняю энергетические подуровни в порядке увеличения их
энергии
4s 3d
Правила
для определения расположения электрона в атоме
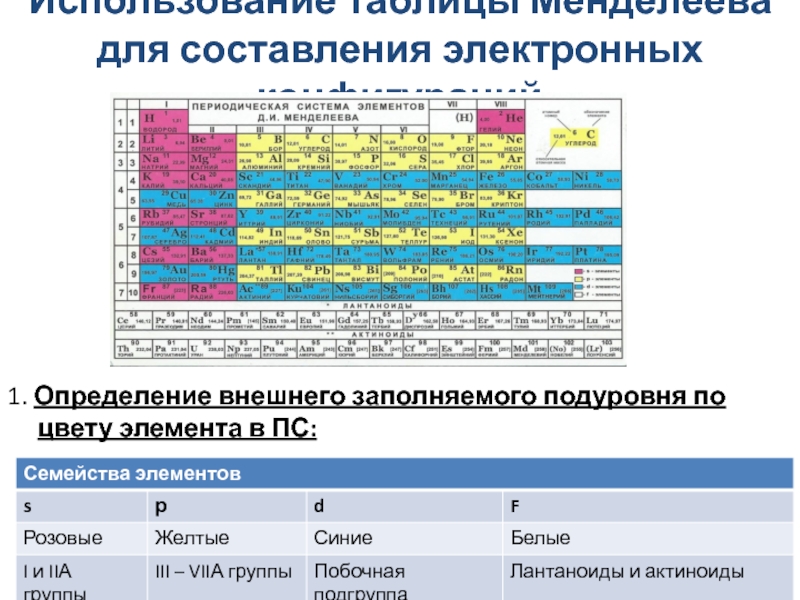
Слайд 15Использование таблицы Менделеева для составления электронных конфигураций
1. Определение внешнего заполняемого
подуровня по цвету элемента в ПС:
Слайд 16Использование таблицы Менделеева для составления электронных конфигураций
2. Определение номера внешнего
заполняемого подуровня
Для s-элементов и p-элементов равен номеру периода
Для d –элементов
равен номер периода - 1
Для f-элементов равен номер периода - 2
Слайд 173. Определение числа электронов на внешнем уровне.
Оно равно номеру
группы.
Использование таблицы Менделеева для составления электронных конфигураций
Слайд 18Составление электронных конфигураций
Запомнить:
У некоторых элементов происходит «провал» электрона
с более высокого энергетического уровня на более низкий для уменьшения
энергии. Характерно для d-элементов.
Слайд 19Химическая связь
Химическая связь – силы взаимодействия, которые соединяют атомы в
молекулы, ионы или кристаллы.
В образовании хим. связей участвуют валентные электроны:
Неспаренные
валентные электроны (s, p –внешнего уровня, d – внешнего и предвнешнего уровня)
Неподеленная пара валентных электронов, находящаяся на внешнем уровне
Вакантные орбитали
Типы химической связи:
Ионная
Ковалентная
Водородная
Металлическая
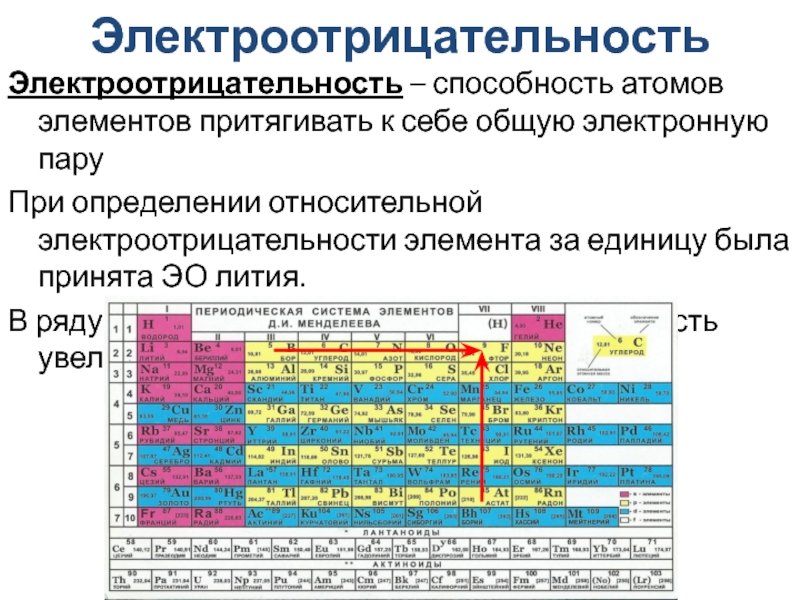
Слайд 20Электроотрицательность
Электроотрицательность – способность атомов элементов притягивать к себе общую электронную
пару
При определении относительной электроотрицательности элемента за единицу была принята ЭО
лития.
В ряду Si, H, Br, N, Cl, O, F электроотрицательность увеличивается.
Слайд 21Ионная связь
Ионная связь – это связь между противоположно заряженными ионами.
Механизм образования: электростатическое притяжение анионов и катионов.
ΔЭО > 1,7 (2)
Случаи
возникновения и.х.св.:
Между типичным металлом (I и II A-группы) и типичным неметаллом (O,H,Cl,F,S,N)
В веществах сложного состава:
Катионы Анионы
NH4+ OH-, анионы
кислородсодержащих
кислот
Механизм образования:
Ионы приобретают устойчивую электронную конфигурацию соответствующего инертного газа.
Слайд 22Примеры образования ионной связи
Слайд 23Характеристика веществ с ионной связью
Ионная кристаллическая решетка
Твердые, прочные, нелетучие
В твердом
состоянии не проводят электрический ток
Хорошо растворимы в полярных растворителях, поэтому
их растворы и расплавы хорошо проводят электрический ток
Слайд 24Ковалентная связь
Ковалентная связь – химическая связь, возникающая в результате образования
общих электронных пар при перекрывании электронных облаков с антипараллельными спинами.
ΔЭО
>= 0
ΔЭО < 1,7 (2)
Слайд 25Механизм образования
Обменный
В случае ковалентной неполярной и полярной связи
Донорно-акцепторный
В случае ковалентной
полярной связи
Слайд 26Характеристика веществ с ковалентной связью
Образуют молекулярную кристаллическую решетку
Обладают малой твердостью,
низкой температурой кипения и плавления, проводят электрический ток, нерастворимы или
малорастворимы в полярных растворителях
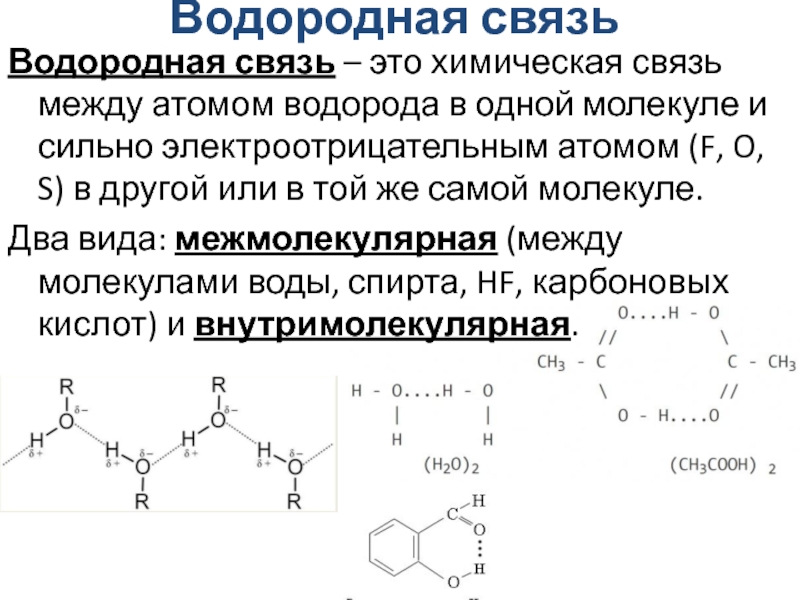
Слайд 27Водородная связь
Водородная связь – это химическая связь между атомом водорода
в одной молекуле и сильно электроотрицательным атомом (F, O, S)
в другой или в той же самой молекуле.
Два вида: межмолекулярная (между молекулами воды, спирта, HF, карбоновых кислот) и внутримолекулярная.
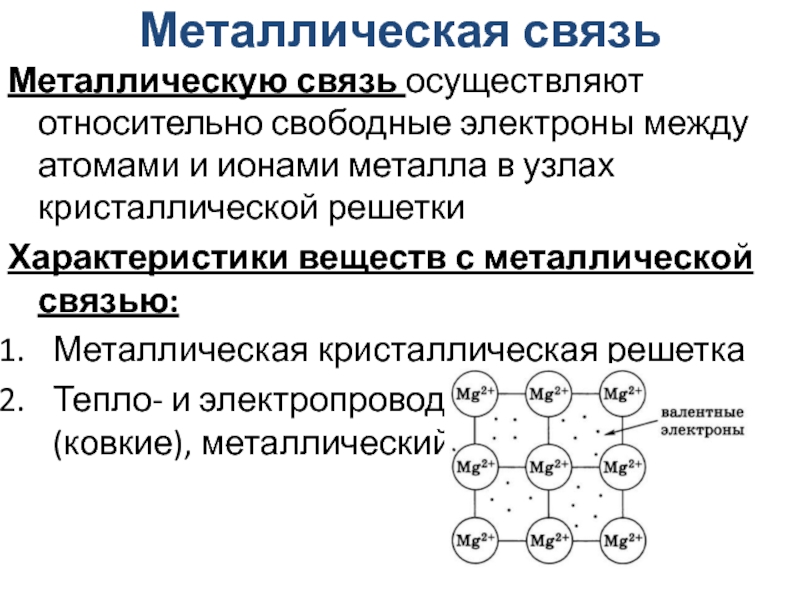
Слайд 28Металлическая связь
Металлическую связь осуществляют относительно свободные электроны между атомами и
ионами металла в узлах кристаллической решетки
Характеристики веществ с металлической связью:
Металлическая
кристаллическая решетка
Тепло- и электропроводны, пластичны (ковкие), металлический блеск.































![АВТОМАТИЗАЦИЯ ЗВУКА [ Л ]
В СЛОВАХ](/img/tmb/6/598195/9904114927fd66f267234b3a5c44ea6c-800x.jpg)