Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
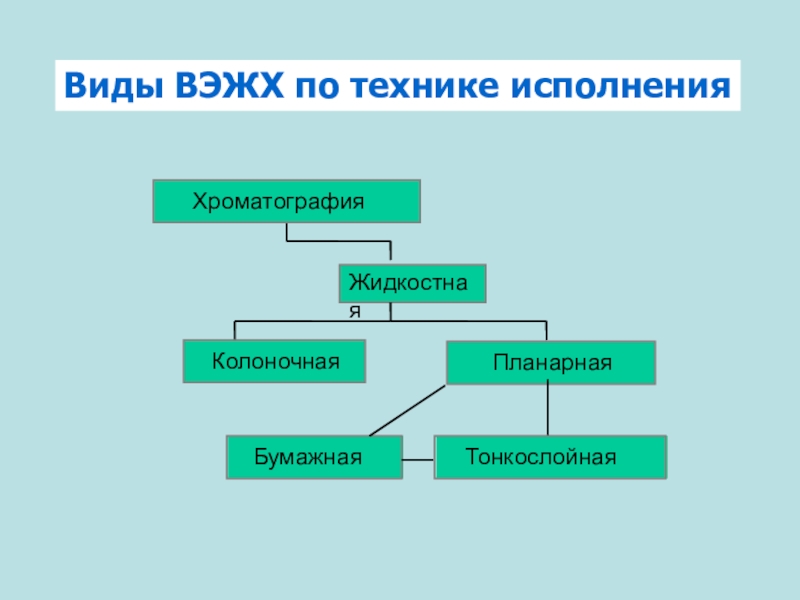
Виды ВЭЖХ по технике
Содержание
- 1. Виды ВЭЖХ по технике
- 2. Планарная (тонкослойная) хроматография
- 3. Разделение веществ происходит на открытом слое сорбента
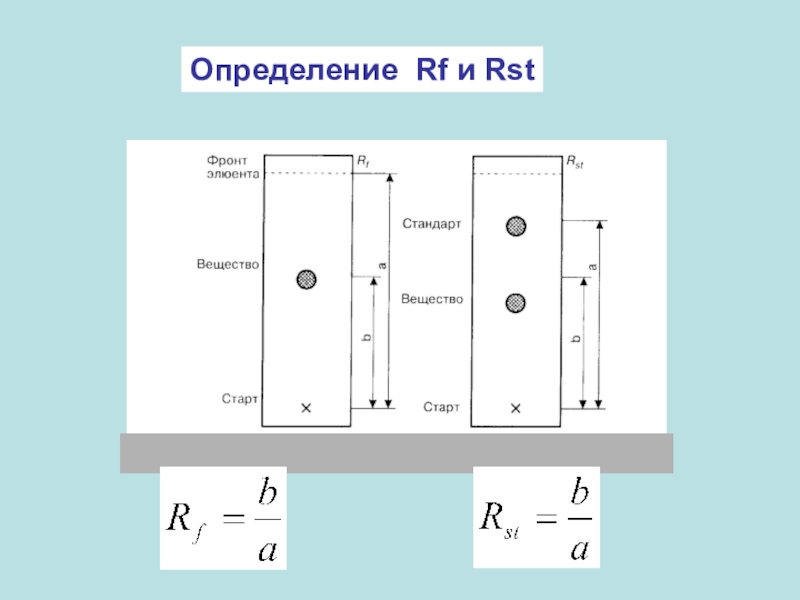
- 4. Определение Rf и Rst
- 5. Rf зависит от: «Активности» и качества сорбента
- 6. Достоинства планарной хроматографии
- 7. - единственный хроматографический метод, который позволяет проводить
- 8. обладает высокой селективностью, которую легко варьировать, подбирая
- 9. Недостатки планарной хроматографии
- 10. ограниченная разделяющая способность из-за сравнительно небольшой длины
- 11. Области применения плоскостной хроматографии
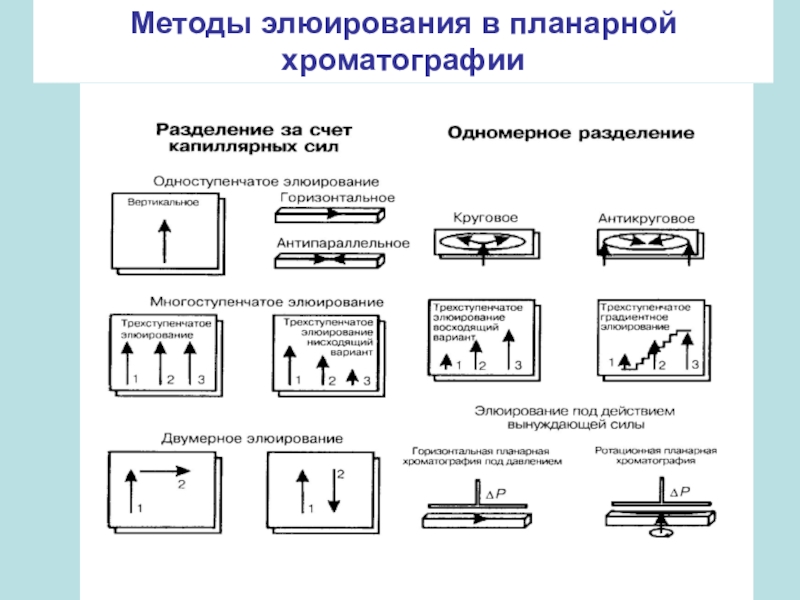
- 12. Методы элюирования в планарной хроматографии
- 13. Слайд 13
- 14. Слайд 14
- 15. Слайд 15
- 16. Круговая хроматографияПодача элюентаНанесение пробыЗоны разделяемых компонентовЕмкость с элюентомПластинкаПодача элюента
- 17. При нанесении пробы необходимо: легкое удаление растворителя
- 18. Слайд 18
- 19. Слайд 19
- 20. Слайд 20
- 21. Слайд 21
- 22. Слайд 22
- 23. Подложки: стекло, алюминевая фольга, полимерные пленкиСвязующие вещества
- 24. образуют химически и физически стабильные слои;
- 25. Предварительная подготовка слоя сорбента- промыть пластинку активировать
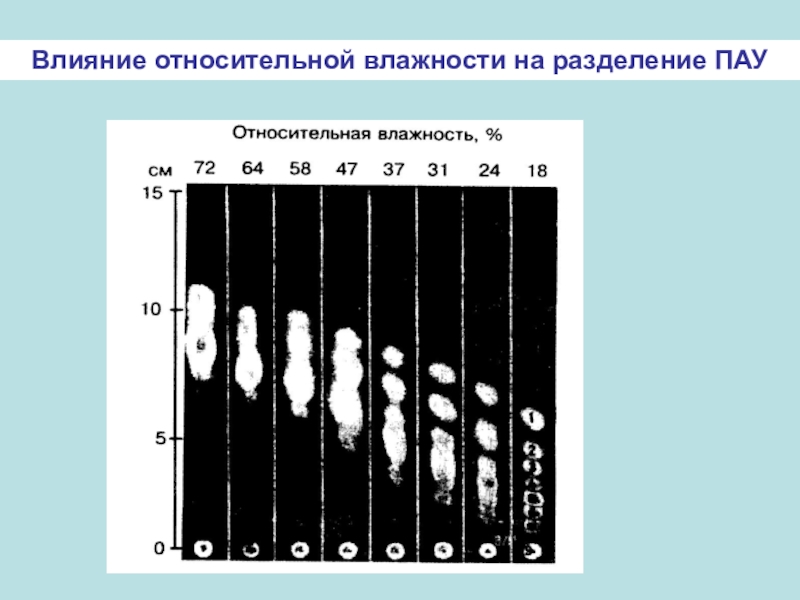
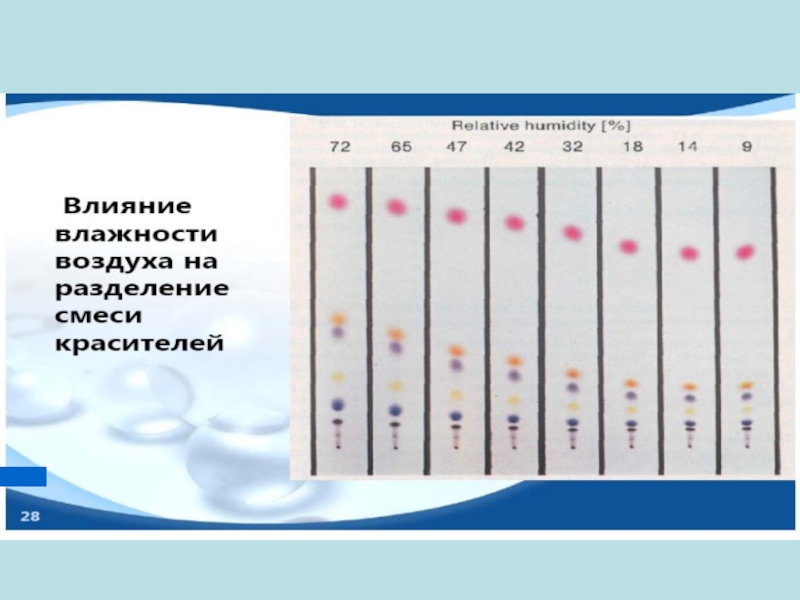
- 26. Влияние относительной влажности на разделение ПАУ
- 27. Слайд 27
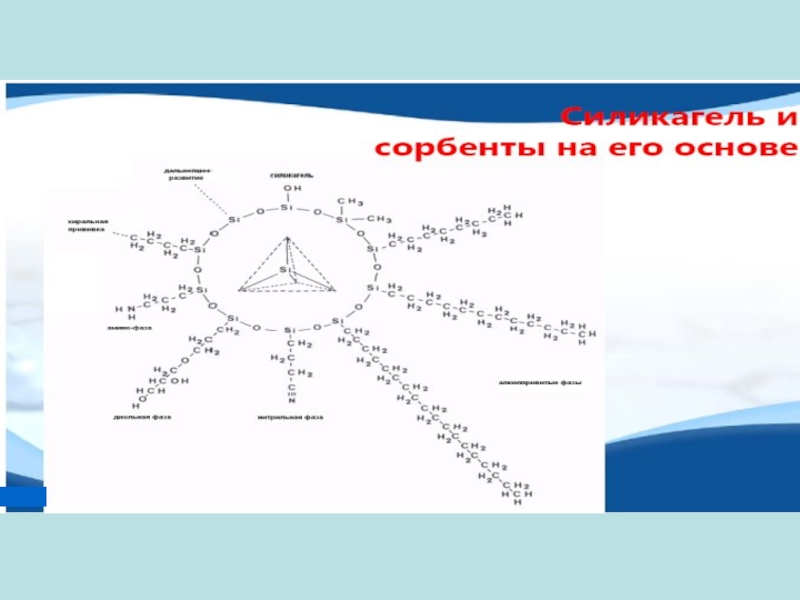
- 28. Основные типы сорбентов в ТСХ
- 29. Силикагель - полярный адсорбент, содержит активные силанольные
- 30. Слайд 30
- 31. Алифатические углеодороды Неполярный Простые эфиры Сложные эфиры Карбонильные
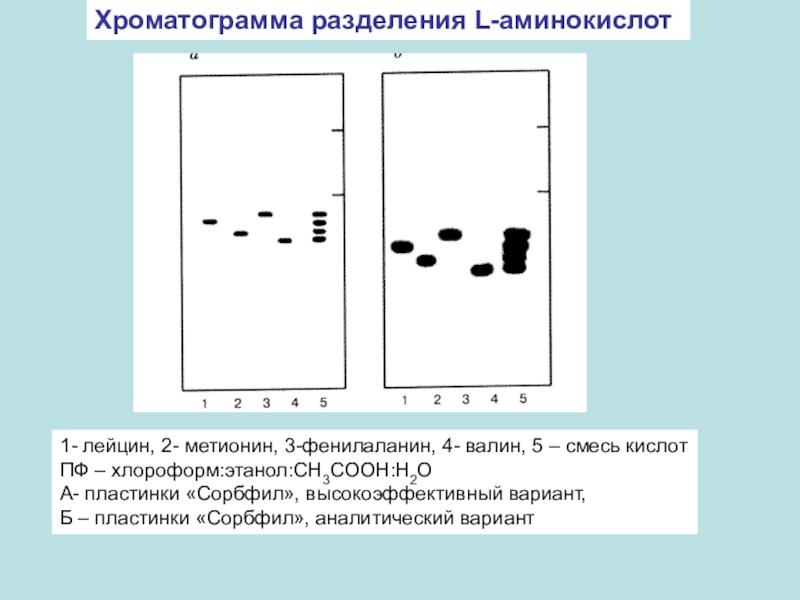
- 32. Хроматограмма разделения L-аминокислот 1- лейцин, 2- метионин,
- 33. Некоторые характеристики ТСХ- и ВЭТСХ пластинок
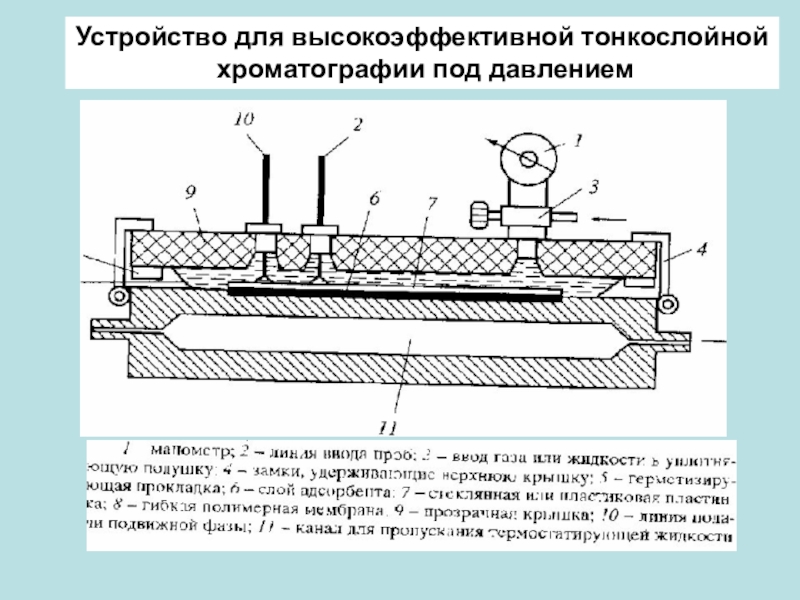
- 34. Устройство для высокоэффективной тонкослойной хроматографии под давлением
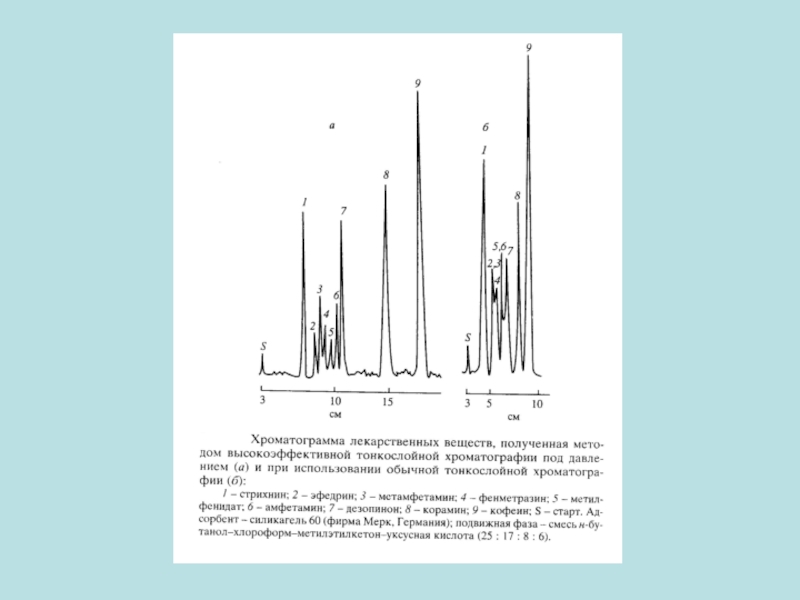
- 35. Слайд 35
- 36. Выбор подвижной фазы
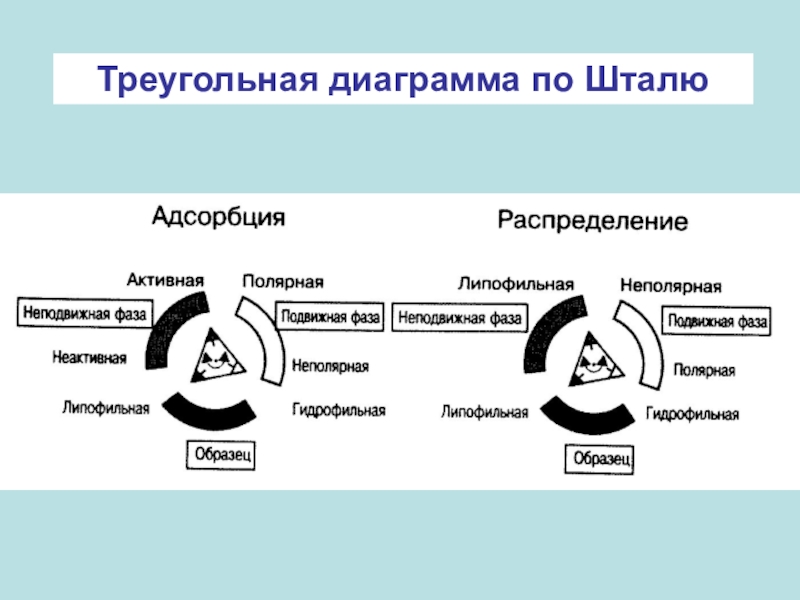
- 37. Треугольная диаграмма по Шталю
- 38. Методы подбора и оптимизациисостава подвижной фазы
- 39. Стандартные системы для адсорбционной ПХ:Хлороформ – метанолХлороформ
- 40. Стандартные системы для распределительной ПХ:Хлороформ – метанол
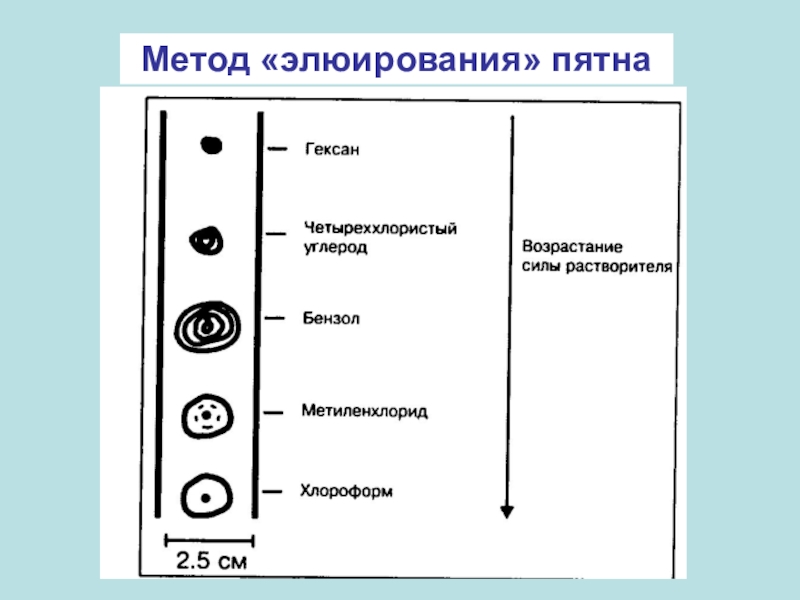
- 41. Метод «элюирования» пятна
- 42. Схема подбора ПФ фирмы «Camag»
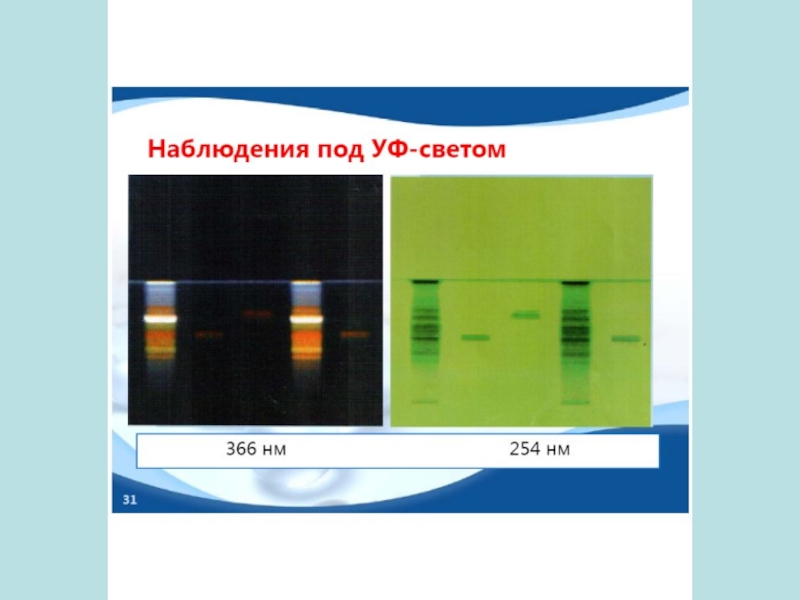
- 43. Идентификация компонентов - физическими методами, основанными на поглощении
- 44. Слайд 44
- 45. Слайд 45
- 46. Количественный анализ в тонкослойной хроматографии
- 47. Определение с удалением хроматографической зоны с пластинки
- 48. Слайд 48
- 49. Слайд 49
- 50. Использование метода денситометрииСканирование хроматограмм в видимом и
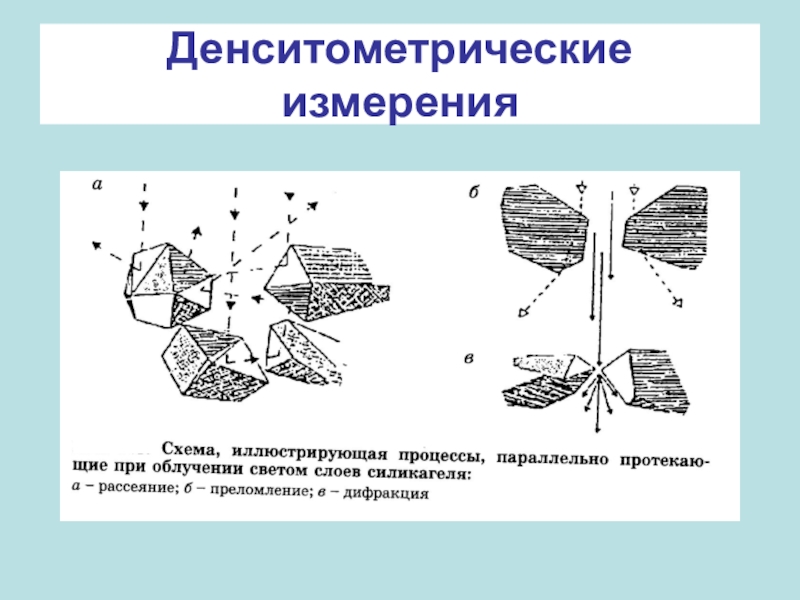
- 51. Денситометрические измерения
- 52. Денситометрические измерения
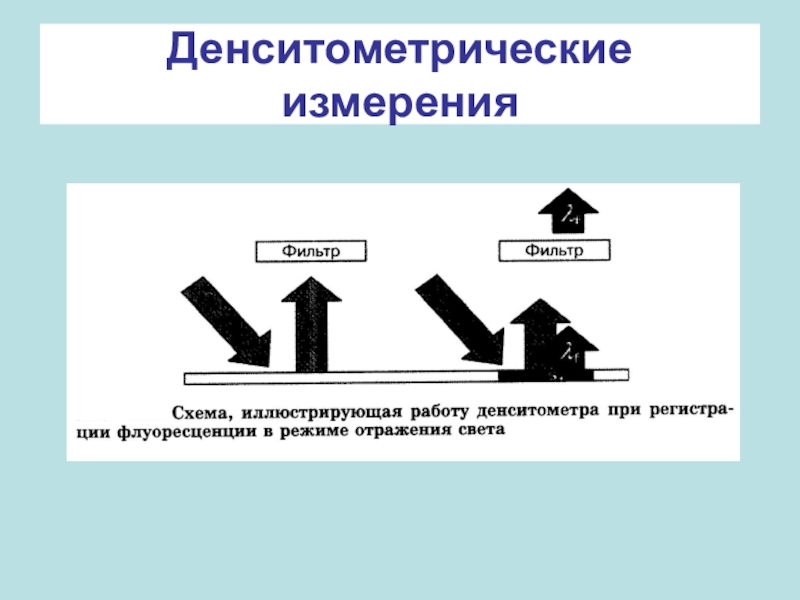
- 53. Денситометрические измерения
- 54. Использование метода видеоденситометрии Введение изображения хроматограммы в
- 55. Слайд 55
- 56. Вид пространственного распределения яркости в области пятнаАi,j
- 57. обработку пятна в видеоденситометрии проводят по двум
- 58. Слайд 58
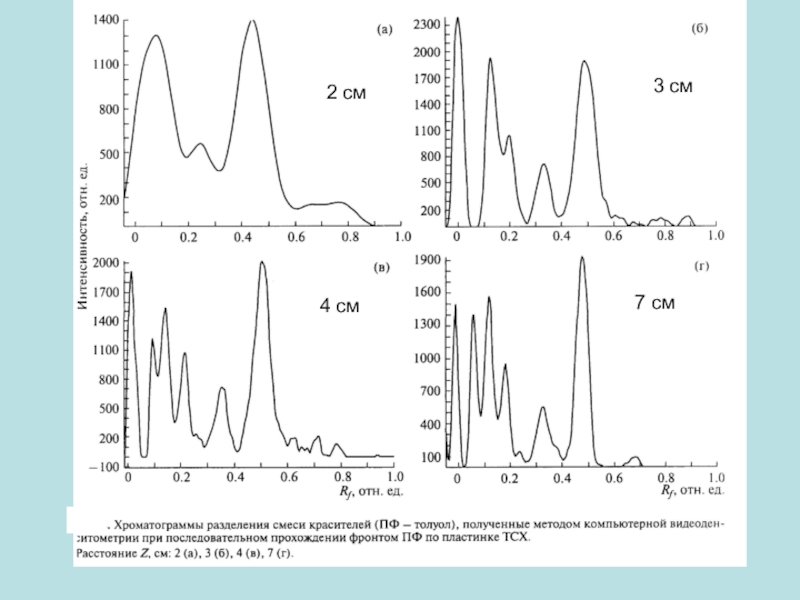
- 59. 2 см3 см4 см7 см
- 60. Примеры определений
- 61. Денситограмма ТСХ-хроматограммы питьевой воды с добавкой гербицидов
- 62. Разделение тетрациклиновых антибиотиковСорбент – силикагель RP-18W;ПФ: 0,5
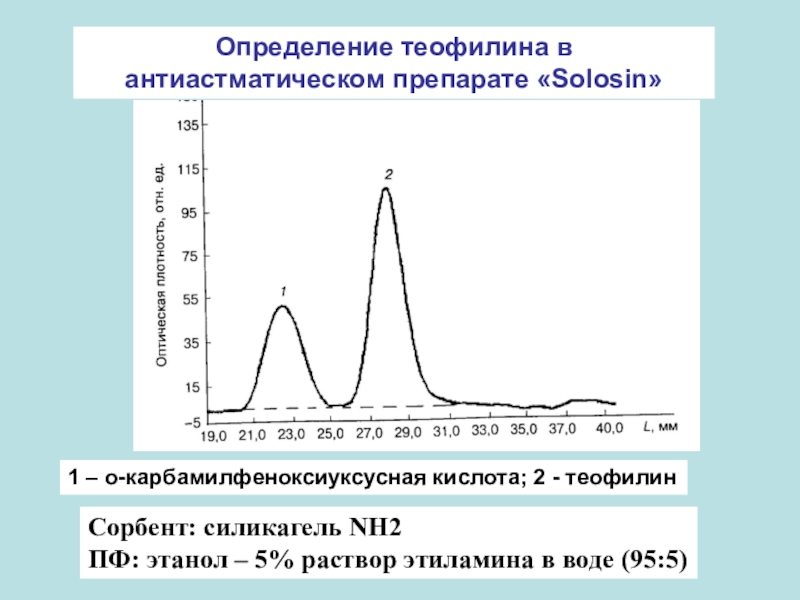
- 63. Определение теофилина в антиастматическом препарате «Solosin»Сорбент: силикагель
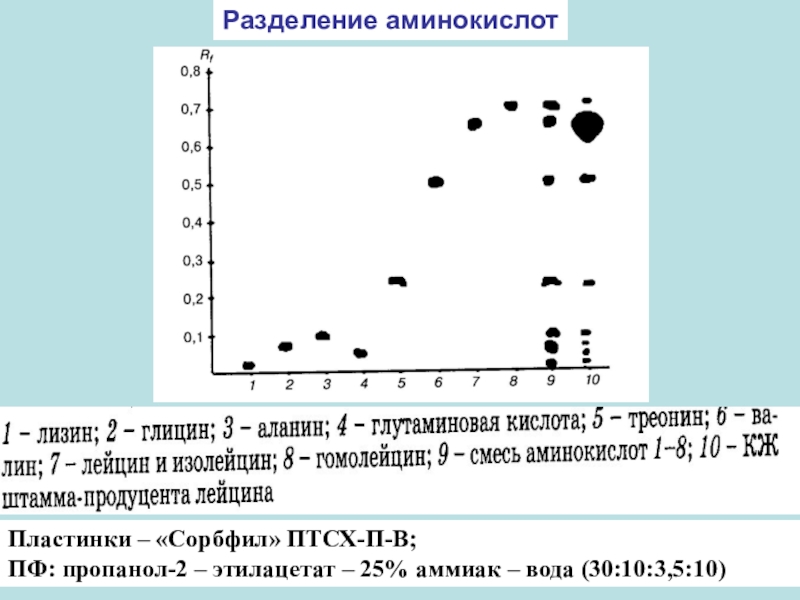
- 64. Разделение аминокислотПластинки – «Сорбфил» ПТСХ-П-В;ПФ: пропанол-2 – этилацетат – 25% аммиак – вода (30:10:3,5:10)
- 65. Слайд 65
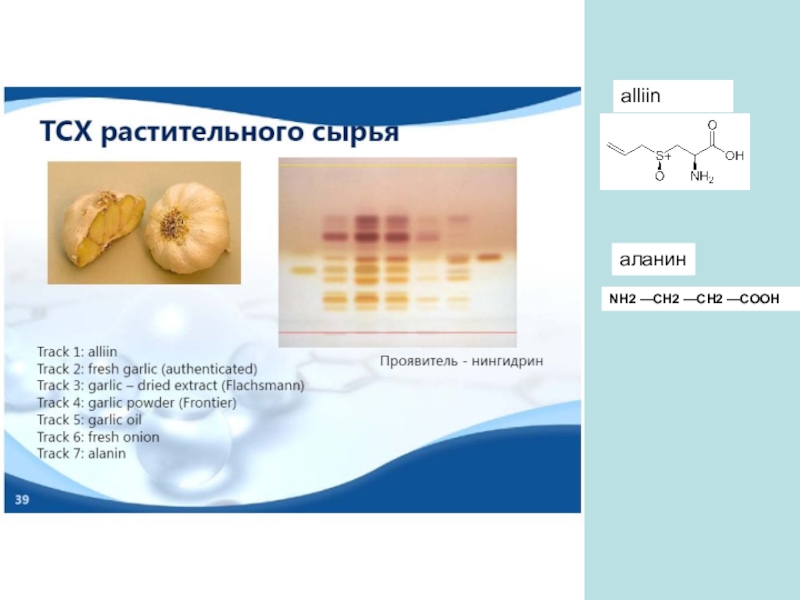
- 66. alliinNH2 —CH2 —CH2 —COOH аланин
- 67. Хроматограммы красящих композиций некоторых популярных тонов коммерческих
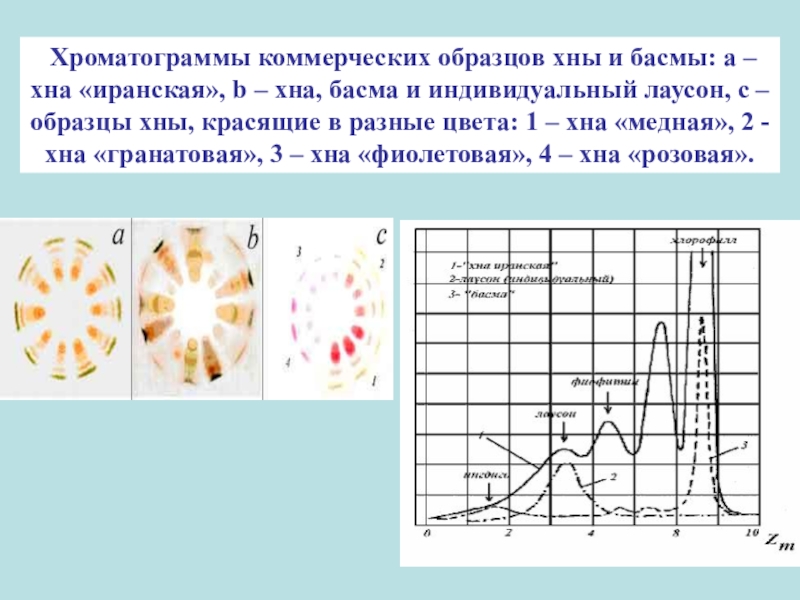
- 68. Хроматограммы коммерческих образцов хны и басмы:
- 69. Благодарю за внимание
- 70. Скачать презентанцию
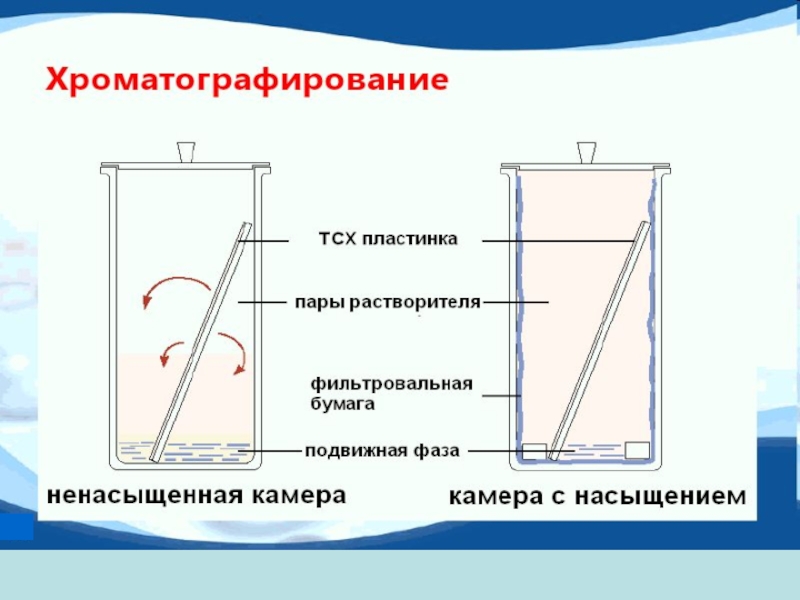
Планарная (тонкослойная) хроматография
Слайды и текст этой презентации
Слайд 3Разделение веществ происходит на открытом слое сорбента
Хроматографический процесс обеспечивается
передвижением подвижной фазы (элюента) посредством капиллярных сил
Слайд 5Rf зависит от:
«Активности» и качества сорбента
Природы и качества
растворителей
Толщины слоя сорбента
Количества нанесенного вещества
Способа работы
Слайд 7 - единственный хроматографический метод, который позволяет проводить полный анализ неизвестной
смеси, т.к можно проверить, не осталось ли на старте неэлюированных
компонентов;- по производительности, по крайней мере, на порядок, превосходит газовую и высокоэффективную жидкостную хроматографию;
- используется более простое и дешевое оборудование;
Слайд 8обладает высокой селективностью, которую легко варьировать, подбирая состав подвижной фазы;
- нет ограничений как в ВЭЖХ на выбор растворителей;
-
дает возможность одновременного разделения нескольких образцов в условиях однократного или многократного элюирования (при различных условиях);- возможность детектировать соединения с высокой чувствительностью и селективностью, которые легко варьировать, подбором проявляющего реагента;
Слайд 10ограниченная разделяющая способность из-за сравнительно небольшой длины разделяющей зоны (3-10
см);
чувствительность ниже, чем в случае ВЭЖХ;
зависимость от окружающей среды: относительная
влажность, температура, а также наличие загрязняющих веществ в воздухе;- трудности в работе с образцами, имеющими высокую летучесть, а также с веществами, чувствительными к кислороду воздуха или свету.
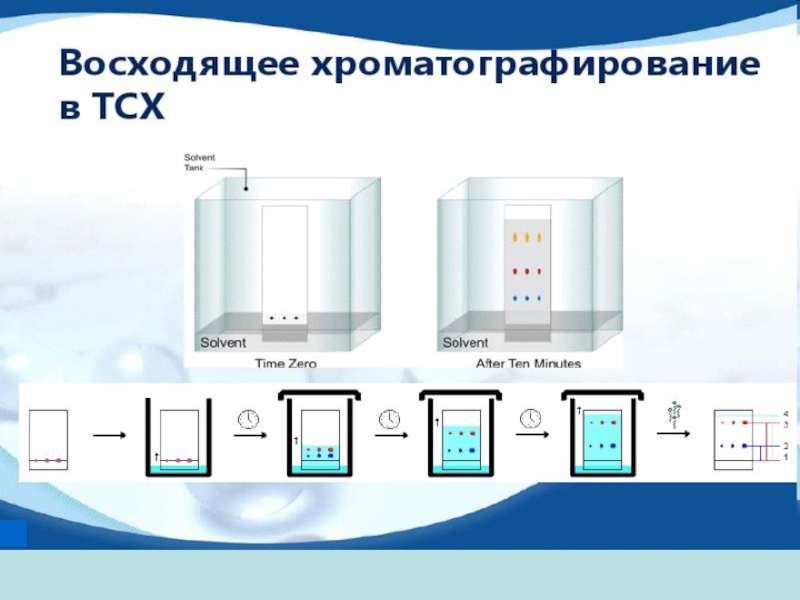
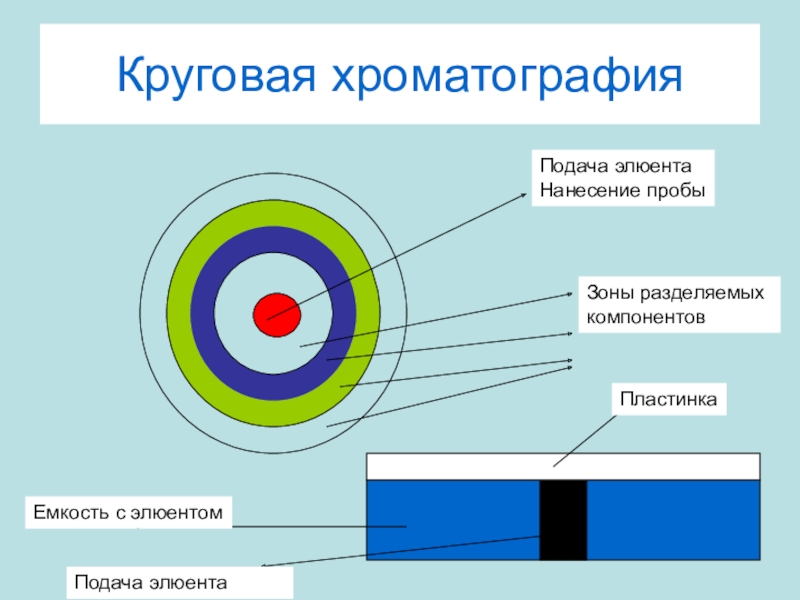
Слайд 16Круговая хроматография
Подача элюента
Нанесение пробы
Зоны разделяемых
компонентов
Емкость с элюентом
Пластинка
Подача элюента
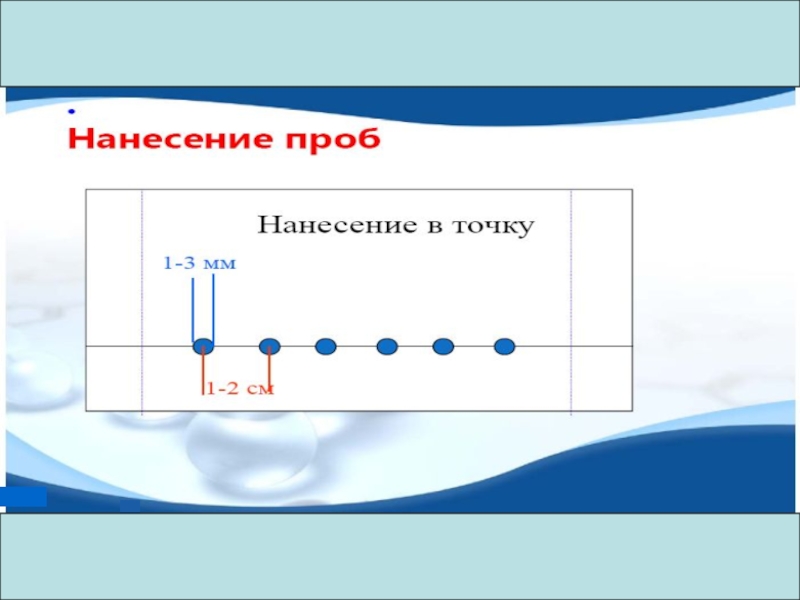
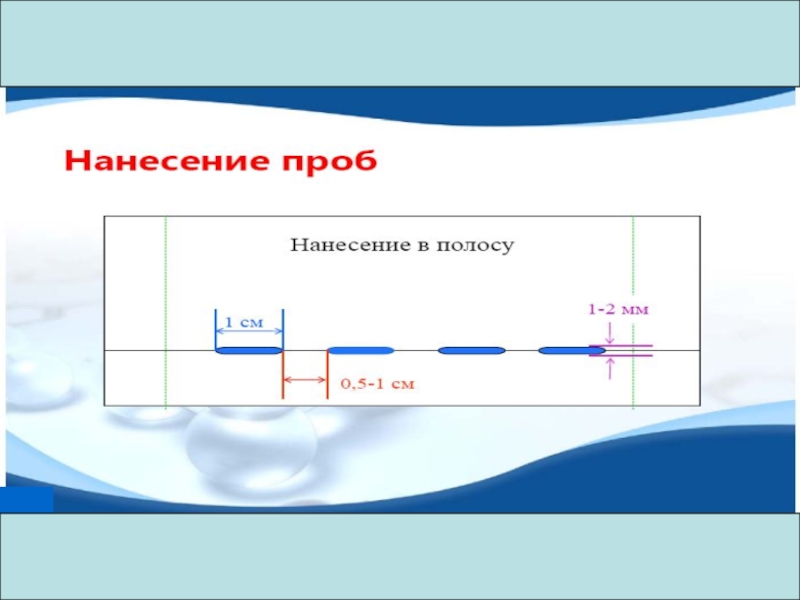
Слайд 17При нанесении пробы необходимо:
легкое удаление растворителя со стартовой
зоны;
растворимость анализируемых веществ должна быть не менее 0,01 г/мл;
растворитель не должен иметь высокую полярность, иначе зона на старте может быть размыта.Слайд 23Подложки: стекло, алюминевая фольга, полимерные пленки
Связующие вещества : гипс (5-10%),
силиказоль, силикаты щелочных металлов, полиакриламид, полиакриловый эфир, крахмал
Флуоресцентный индикатор: смесь
силикатов цинка и магния и смесь сульфидов цинка и кадмия; вольфраматы щелочноземельных элементовСлайд 24 образуют химически и физически стабильные слои;
не образуют ковалентных
связей с разделяемыми
веществами;
не растворяются
в подвижной фазе или перемещаются вместе с ней по пластинке;не содержат компонентов, мешающих разделению или детектированию
не имеют собственной окраски;
не набухают и не сжимаются под действием подвижной фазы.
Требования к сорбентам в ТСХ
Слайд 25Предварительная подготовка слоя сорбента
- промыть пластинку
активировать пластинку
активироавнную пластинку
хранить в вакуум-эксикаторе
при нанесении пробы рабочую область платинки
предохранять покровной стеклянной пластинкойСлайд 29Силикагель - полярный адсорбент, содержит активные силанольные и силоксановые группы.
Применяют для разделения соединений различной полярности.
Оксид алюминия - полярный
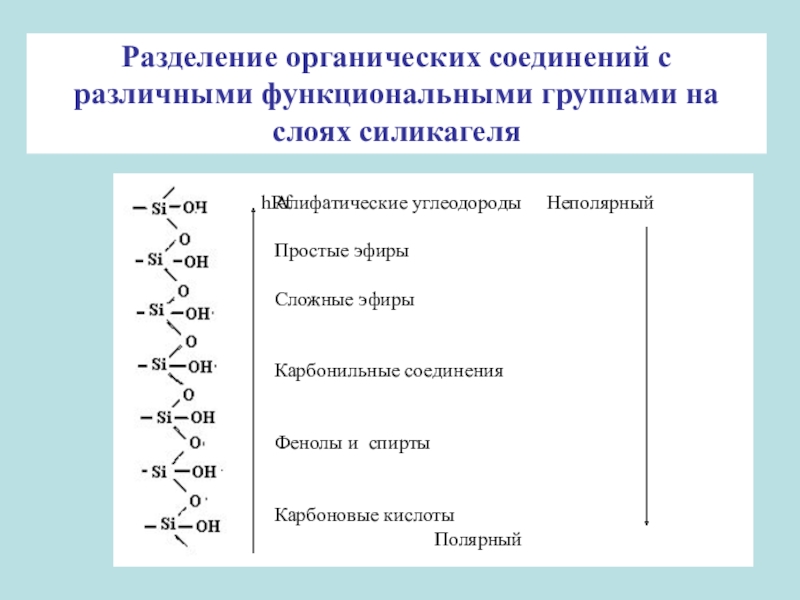
адсорбент с гетерогенной поверхностью, содержит активные ОН-группы, заметно выражены протоноакцепторные свойства. Применяют для разделения ароматических углеводородов, алкалоидов, хлоруглеводородов, стероидовСлайд 31 Алифатические углеодороды Неполярный
Простые эфиры
Сложные эфиры
Карбонильные соединения
Фенолы и спирты
Карбоновые
кислоты
Полярный
hRf
Разделение органических соединений с различными функциональными
группами на слоях силикагеляСлайд 32Хроматограмма разделения L-аминокислот
1- лейцин, 2- метионин, 3-фенилаланин, 4- валин,
5 – смесь кислот
ПФ – хлороформ:этанол:CH3COOH:H2O
А- пластинки «Сорбфил», высокоэффективный вариант,
Б
– пластинки «Сорбфил», аналитический вариантСлайд 39Стандартные системы для адсорбционной ПХ:
Хлороформ – метанол
Хлороформ – ацетон
Диэтиловый эфир
– толуол
Диэтиловый эфир – гексан – уксусная кислота
Этилацетат – метанол
Этилацетат
- толуолСлайд 40Стандартные системы для распределительной ПХ:
Хлороформ – метанол – вода
Хлороформ –
метанол – вода – уксусная кислота
Хлороформ – метанол – вода
– водный аммиакБутанол-1 – уксусная кислота – вода
Бутанол-1 – пиридин – вода
Этилацетат – муравьиная кислота – вода
Слайд 43Идентификация компонентов
- физическими методами, основанными на поглощении света и флуоресценции
химическими методами
с «универсальными реагентами»
с реагентами, которые избирательно
реагируют с определенными функциональными группами исследуемых соединений. Слайд 47Определение с удалением хроматографической зоны с пластинки
Проводят двояко:
переносом
хроматографической зоны вместе с сорбентом
экстрагированием хроматографической зоны со слоя
сорбентаОпределение определяемых соединений непосредственно на пластинке
Метод визуального сравнения размеров площадей пятен и их окраски с соответствующими параметрами пятен стандартных образцов
Слайд 50Использование метода денситометрии
Сканирование хроматограмм в видимом и УФ-свете с помощью
«хроматографических спектрофотометров» – денситометров.
Измеряется:
поглощение света веществом на хроматограмме в
режиме пропускания или отражения; флуоресценция и ее гашение.
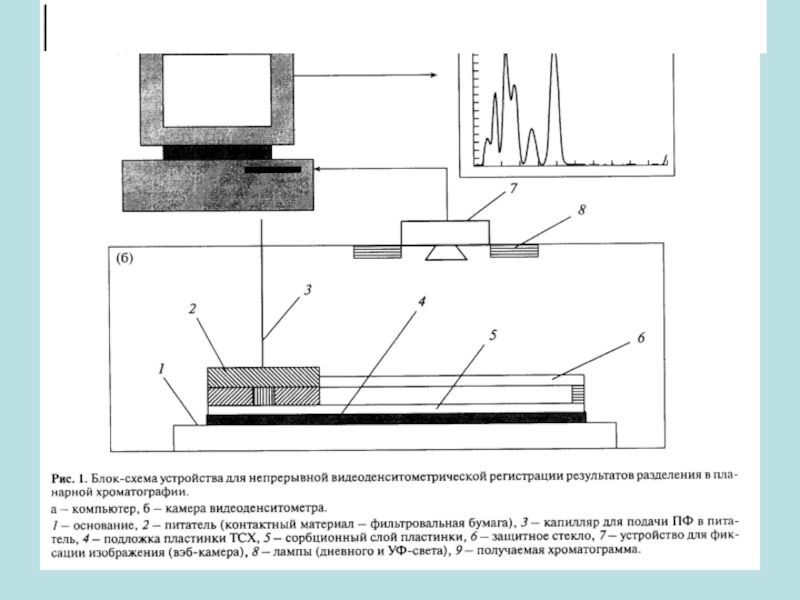
Слайд 54Использование метода видеоденситометрии
Введение изображения хроматограммы в компьютер с помощью
видеокамеры или цифровой камеры;
сравнением интенсивностей пятен стандартных соединений и исследуемых
образцов.Использование денситометрии с планшетным сканером.
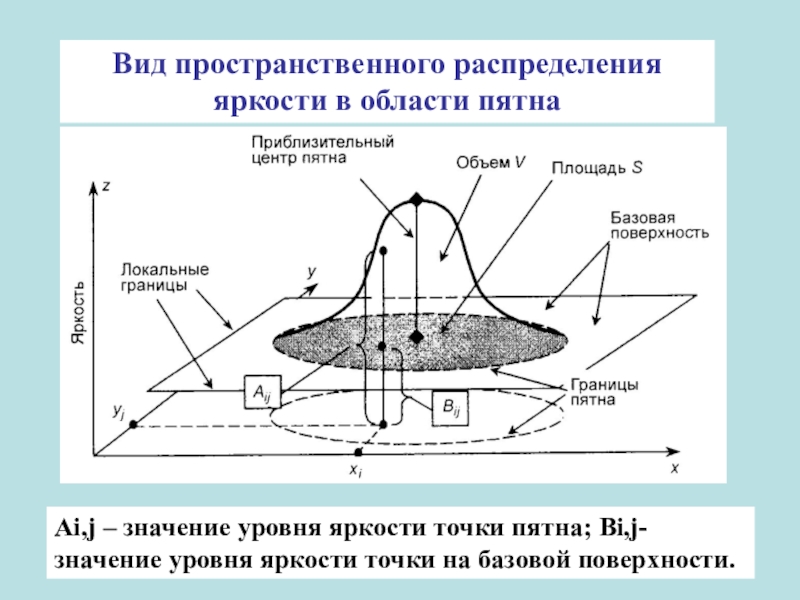
Слайд 56Вид пространственного распределения яркости в области пятна
Аi,j – значение уровня
яркости точки пятна; Вi,j- значение уровня яркости точки на базовой
поверхности.Слайд 57 обработку пятна в видеоденситометрии проводят по двум характеристикам:
площади пятна;
его «объему» в пространстве;
в качестве третьей координаты используют
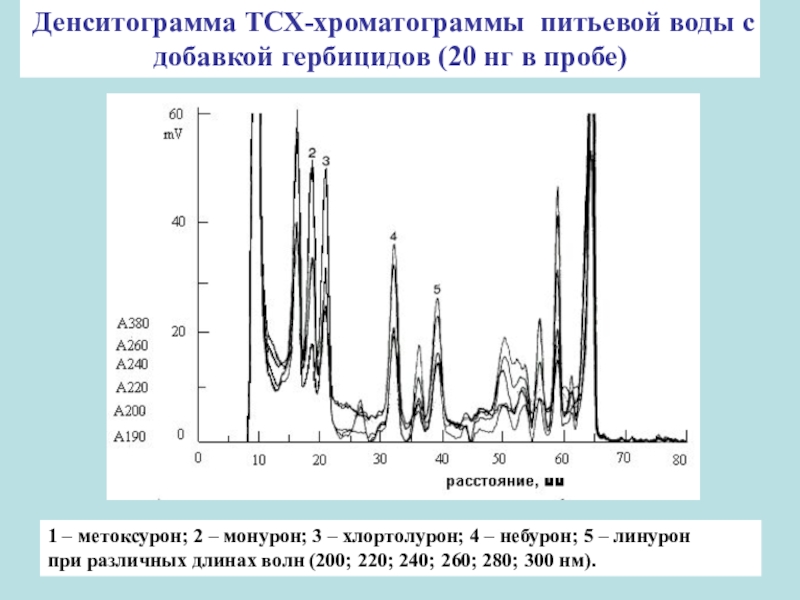
яркость (интенсивность окраски пятна)Слайд 61Денситограмма ТСХ-хроматограммы питьевой воды с добавкой гербицидов (20 нг в
пробе)
1 – метоксурон; 2 – монурон; 3 – хлортолурон; 4
– небурон; 5 – линурон при различных длинах волн (200; 220; 240; 260; 280; 300 нм).
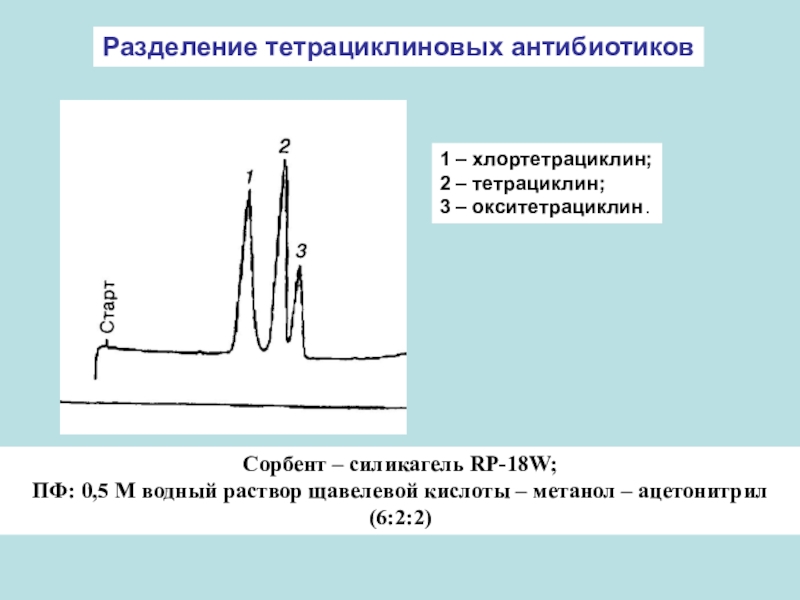
Слайд 62Разделение тетрациклиновых антибиотиков
Сорбент – силикагель RP-18W;
ПФ: 0,5 М водный раствор
щавелевой кислоты – метанол – ацетонитрил (6:2:2)
1 – хлортетрациклин;
2 –
тетрациклин;3 – окситетрациклин.