Слайд 1Возможности ПЦР-анализа
в диагностике пневмоний, гриппа и ОРЗ
Слайд 2Пневмонии
Заболеваемость пневмониями в развитых странах составляет 3,6 - 16 на
1000 человек
Пневмонии занимают 4 – 5-е место в структуре
причин смерти после сердечно-сосудистой патологии, онкологических заболеваний, цереброваскулярной патологии и хронических обструктивных заболеваний легких
Среди инфекционных болезней – 1-е место
Заболеваемость в возрастной группе старше 60 лет: 20 - 44 на 1000 населения в год. Летальность от пневмоний у данной категории больных - 10 – 33%
Высокая летальность от пневмонии среди новорожденных и маленьких детей и достигает 25% у детей младше 5 лет
Уровень смертности детей до 1 года в нашей стране в 2 – 4 раза выше (25,1 на 1000 населения), чем в других экономически развитых странах
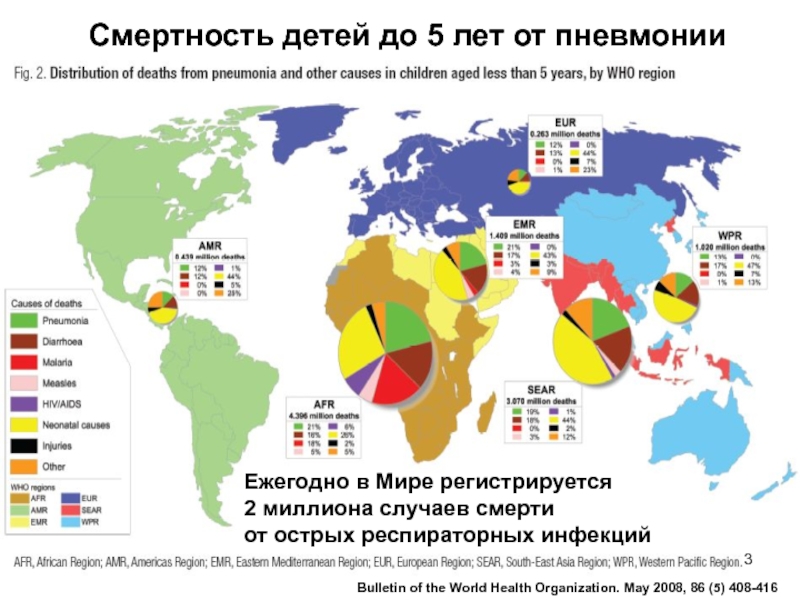
Слайд 3Смертность детей до 5 лет от пневмонии
Bulletin of the World
Health Organization. May 2008, 86 (5) 408-416
Ежегодно в Мире регистрируется
2 миллиона случаев смерти от острых респираторных инфекций
Слайд 4Пневмонии у взрослых
Обзор данных литературы
Слайд 5Причины неудач в установлении этиологии пневмоний
Отсутствие микробного исследования
Неправильный сбор материала
Возбудитель
неизвестен
Предшествующее лечение антибиотиками (до взятия материала)
Неопределенное клиническое значение выделенного
возбудителя
Использование неадекватного метода лечения
Слайд 6Классификации пневмоний
По характеру приобретения:
внебольничная пневмония (ВП)
нозокомиальная (внутрибольничная) пневмония
Классификация ВП, учитывающая
состояние иммунологической реактивности организма пациента:
- типичная ВП (у пациентов с
отсутствием выраженных нарушений иммунитета)
- ВП у пациентов с выраженными нарушениями иммунитета (СПИД, онкогематологические заболевания и др.)
Слайд 7Возбудители пневмонии у детей
Врожденные
Внебольничные
Слайд 8Этиологическая структура пневмоний
февраль - апрель 2006г Хабаровск (дети n=27, аспираты
из трахеи)
Пневмококк – 26%
вирусная этиология – 45%
вирусно-бактериальные ассоциации
– 18%
Не уточнённая этиология – 11%
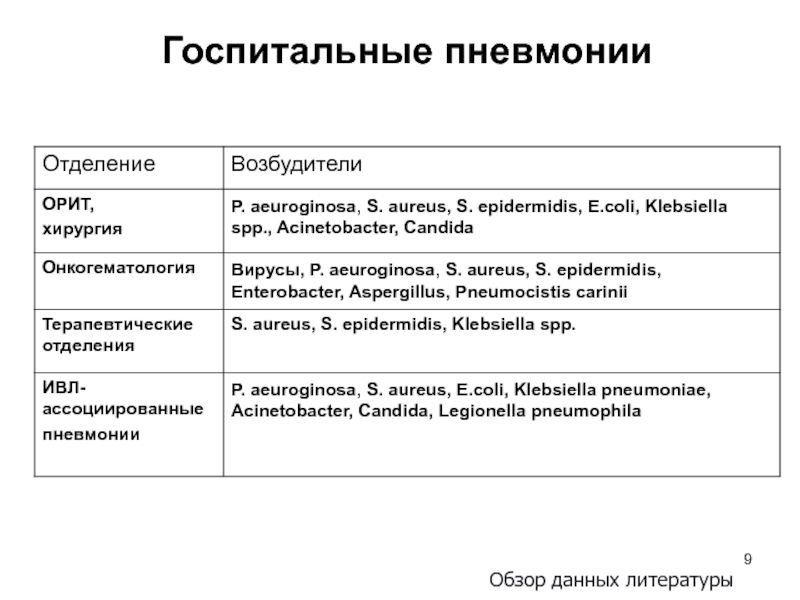
Слайд 9Госпитальные пневмонии
Обзор данных литературы
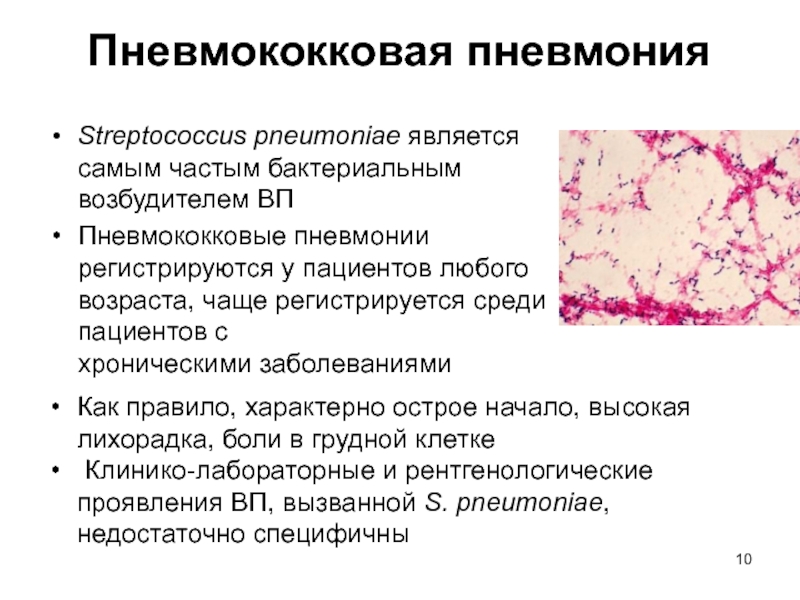
Слайд 10Пневмококковая пневмония
Streptococcus pneumoniae является самым частым бактериальным возбудителем ВП
Пневмококковые пневмонии
регистрируются у пациентов любого возраста, чаще регистрируется среди пациентов с
хроническими заболеваниями
Как правило, характерно острое начало, высокая лихорадка, боли в грудной клетке
Клинико-лабораторные и рентгенологические проявления ВП, вызванной S. pneumoniae, недостаточно специфичны
Слайд 11Культуральный метод в диагностике пневмококковой пневмонии
Материал для исследования: мокрота, венозная
кровь, инвазивные респираторные образцы, плевральная жидкость
Необходимость оценки качества доставленного образца
Критерии
пригодности мокроты для бактериологического исследования: ˃25 сегментоядерных лейкоцитов и не более 10 эпителиальных клеток в п/з
Обнаружение грамположительных кокков (чаще - ланцетовидные диплококки) d=0,5 - 1,25 мкм, не имеющих спор и жгутиков
Слайд 12Культуральный метод в диагностике пневмококковой пневмонии
Чаще используют питательные среды:
обогащенные дефибринированной
кровью животных (5 %)
обогащенные дефибринированной кровью человека
шоколадный агар
Инкубация в
атмосфере с повышенным
содержанием СO2 (S. pneumoniae - факультативный анаэроб)
Вероятность выделения увеличивается при использовании селективных сред, ингибирующих рост сапрофитных и грамотрицательных микроорганизмов (колистин, гентамицин)
Ключевой тест дифференциации пневмококков от других α-гемолитических стрептококков - чувствительность к оптохину
Информативность культурального исследования зависит от соблюдения общепринятых правил их сбора, хранения и транспортирования
Слайд 13Иммунохроматографический тест
Выявление пневмококкового клеточного полисахаридного антигена в моче
Возможность использования «у
постели больного»
Пневмококковый экспресс-тест демонстрирует приемлемую чувствительность (50 - 80 %)
и достаточно высокую специфичность (> 90 %)
Возможность получения ложноположительных результатов при пневмококковом носительстве
Слайд 14ПЦР в диагностике пневмококковой пневмонии
В качестве мишеней для амплификации используются
гены, кодирующие факторы патогенности:
- аутолизин (lytA)
пневмококковый поверхностный антиген
(psaA)
пневмолизин (ply)
пневмококковый поверхностный протеин А (PspA)
марганец-зависимая супероксид-дисмутаза (sodA)
поверхностный пенициллин-связывающий белок 2b (Pbp2b)
Spn9802 и Spn9828
Данные методы пока не получили распространения в клинической практике
Возможность использования мультиплексной ПЦР
Слайд 15Пневмония, вызванная
Mycoplasma pneumoniae
Периодичность эпидемий с интервалами от 3 до
7 лет
Распространению инфекции способствует частота и длительность контактов среди
лиц, пребывающих в закрытых и полузакрытых коллективах
Только в 3 - 10 % случаев микоплазменной инфекции рентгенологически диагностируется пневмония
Диагностика микоплазменной пневмонии только на основании клинических или рентгенологических данных невозможна - не имеет патогномонических черт
Необходимость лабораторной этиологической диагностики
Слайд 16Диагностика микоплазменной пневмонии
обнаружение ДНК М. pneumoniae методом полимеразной цепной реакции (ПЦР)
выявление
антигена микоплазм в реакции прямой иммунофлуоресценции (РИФ)
серологические исследования по обнаружению
специфических антител класса IgM и IgG к M. pneumoniae в сыворотках крови методом иммуноферментного анализа (ИФА)
Культуральный метод не рекомендован
Слайд 17Диагностика пневмонии, вызванной Chlamydophila pneumoniae
С. pneumoniae - патогенная для человека грамотрицательная
бактерия с облигатным внутриклеточным типом паразитирования
Вызывает пневмонии различной тяжести, длительно
протекающие бронхиты, фарингиты, синуситы
Пневмония, вызванная С. рneumoniae, обычно имеет благоприятное течение
Микст-инфекция осложняет течение заболевания и увеличивает риск летального исхода
Частота заболеваемости хламидийной пневмонией выше у детей школьного возраста
Эпидемические вспышки происходят каждые 4 - 10 лет
Ни один из известных в настоящее время методов диагностики хламидийной пневмонии не обеспечивает 100 %-ю надежность выявления возбудителя
Слайд 18Культуральный метод:
Длительность и трудоемкость процесса
Низкая чувствительность
Доступность только специализированным лабораториям
Но
в случае выделения жизнеспособного возбудителя диагноз может быть поставлен с
наибольшей достоверностью без необходимости применения подтверждающих тестов
При персистентной инфекции возбудитель переходит в некультивируемое состояние
Серологический метод:
применяют для ретроспективной диагностики и ретроспективного анализа природы эпидемических вспышек
Для обнаружения специфических IgM-, и IgG-антител используют метод иммуноферментного анализа (ИФА) или реакцию иммунофлюоресценции (РИФ)
Слайд 19ПЦР-диагностика
Chlamydophila pneumoniae
Наиболее специфичный и чувствительный метод выявления возбудителя
Но метод не
дает возможность дифференцировать острую и хроническую инфекцию
Рекомендован биологический материал, полученный
из нижних дыхательных путей
Слайд 20Проблемы диагностики инфекций, вызванных Chlamydophila pneumoniae
Infection · 2003 ·
31 No. 6
S.M. Schmidt et al. C. pneumoniae Carriage
and Infection in Hospitalized Children
Доказано носительство у доноров (459) в лейкоцитах крови: Elisa – 47,7% Иммуно-флуоресцентная микроскопия – 24,6 % Культуральные исследования с ПИФ – 24,8 %
Наблюдается носительство в респираторном тракте: у взрослых без симптомов ОРЗ (1–2%) у детей без симптомов ОРЗ (4–6%)
BMC Infectious Diseases 2006, 6:23
Слайд 21
Род Legionella включает 49 видов
Для 22 видов доказана роль в
инфекционной патологии человека
Более 90% легионеллезов - L.pneumophila (16 серогрупп):
-80% -
1 серогруппа
-5-10 % - 4 и 6 серогруппы
Другие виды, наиболее часто вызывающие заболевания людей:
L.micdadei, L.longbeachae, L.dumofii, L.bozemanii
(при нарушениях иммунитета, после трансплантации,
при получении иммуносупрессивной терапии)
Болезнь легионеров
Слайд 22Основные источники легионеллезной инфекции:
Система водоснабжения;
Системы генерирующие аэрозоль:
1. централизованные системы кондиционирования воздуха
2.
бассейны, ванны с циркулирующей под давлением водой (типа джакузи)
3. другие (увлажнители воздуха, фонтаны;
любое оборудование, распыляющее водный
аэрозоль)
Слайд 23Эпидемии легионеллеза
(70-е годы ХХ века)
Слайд 24Клинические формы
Болезнь легионеров (пневмония)
2–6% от общего числа пневмоний
10–15% от атипичных пневмоний
Инкубационный период – 2-10 дней
Лихорадка, боли в груди, острая дыхательная недостаточность, малопродуктивный кашель, головная боль
Смертность – 6- 15%
лихорадка Понтиак (гриппоподобное заболевание)
1-2 дневное повышение температуры, сухой кашель, катаральные явления в носоглотке, головные и мышечные боли
летальные исходы не зарегистрированы
носительство и персистенция легионелл в организме человека не отмечают
Слайд 251986 году создана Европейская экспертная рабочая группа 37 стран
Подтверждение болезни легионеров
выделение культуры микроорганизма (из образцов респираторного тракта, лёгких или крови)
или
обнаружение в моче фильтрующегося антигена
или
подъём в 4 раза титра антител специфичных для Legionella pneumophila I серогруппы
! В случае получения положительного результата методом ПЦР диагноз считать предположительно установленным
Слайд 27Диагностика
Выделение культуры возбудителя:
- мокрота – чувствительность - 10-80%,
специфичность – 100%
- биоптаты– 90-99%, специфичность – 100%
- кровь– 10-30%,
специфичность – 100%
2. Определение уровня антител:
- чувствительность 75%, специфичность 95-99%
3. Определение растворимого антигена в моче:
- чувствительность 90-99%, специфичность 99-100%
4. Прямая иммунофлюоресценция:
- мокрота – чувствительность - 25-75%, специфичность – 95-99%
- биоптаты– 80-90%, специфичность – 99%
5. ПЦР:
- чувствительность – 85%, специфичность – 99%
Тартаковский И.С., 2000 г. P. Edelsten, 1994. T. Harrison 1998
Diederen B. M. W. J Med Microb 2006, 55:639–642
Слайд 28Преимущества ПЦР-анализа
Быстрота (от 5 до 8 часов)
Специфичность (зависит от мишени,
характеристик тест-сиcтемы и способа детекции)
Большая чувствительность по сравнению с бактериологическим
анализом
Возможность быстрой идентификации L.pneumophila с обнаружением всех серогрупп (зависит от характеристик т/c)
Слайд 29Легионеллез - область применения ПЦР-анализа
Мониторинг объектов окружающей среды
с последующим бактериологическим исследованием положительных образцов с высокой нагрузкой ДНК
Исследование объектов окружающей среды (быстрое расследование источника вспышки)
Подтверждение случаев смертельного исхода от пневмонии невыясненной этиологии
Диагностика пневмоний у лиц со сниженным иммунным статусом (L.pneumophila различных серогрупп)
Идентификация культур, подозрительных на L.pneumophila
Молекулярно-эпидемиологическое расследование (ПЦР+секвенирование ДНК)
Слайд 30Диагностика пневмоцистоза
Возбудитель - Pneumocystis jiroveci
Пневмоцисты тропны исключительно к легочной ткани
Группами
риска в отношении инфицированности Pneumocystis jiroveci являются:
- дети недоношенные, ослабленные новорожденные
и дети раннего возраста с гипогаммаглобулинемией, гипотрофией и рахитом
больные лейкозом, онкологические больные, реципиенты органов, получающие иммунодепрессанты
больные туберкулезом, цитомегалией и другими инфекциями
- ВИЧ-инфицированные
Слайд 31Диагностика пневмоцистоза
Паразитологический метод (импрегнация метенамин-серебряным нитратом по Гомори, окраска толуидиновым
синим, гематоксилином и эозином, по Грамму и раствором Шиффа, методом
Романовского-Гимза)
Иммунологический метод (иммунофлюоресцентный метод (РИФ) для выявления цист и трофозоитов, выявление специфических антител классов IgG и IgM (ИФА))
ПЦР-диагностика
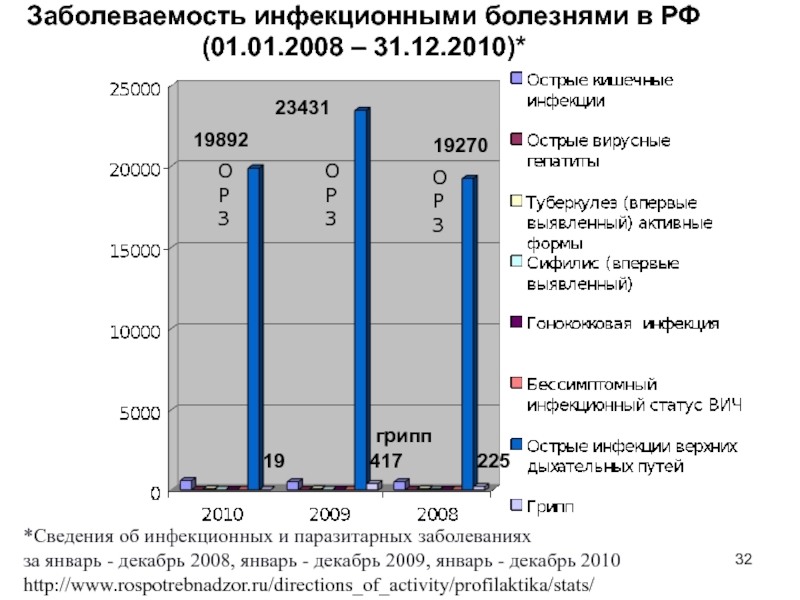
Слайд 32Заболеваемость инфекционными болезнями в РФ (01.01.2008 – 31.12.2010)*
*Сведения об инфекционных
и паразитарных заболеваниях
за январь - декабрь 2008, январь -
декабрь 2009, январь - декабрь 2010 http://www.rospotrebnadzor.ru/directions_of_activity/profilaktika/stats/
ОРЗ
ОРЗ
19270
23431
225
417
19892
ОРЗ
19
грипп
Слайд 33Регистрируемые в РФ формы ОРЗ и потенциальные возбудители
Грипп
Острые инфекции
верхних
дыхательных путей множественной
или неуточненной локализации
Острые инфекции нижних
дыхательных путей
ОРВИ ( 90-97 % ОРЗ)
Paramyxoviridae
Respirovirus – Parainfluenza virus 1,3
Rubulavirus – Parainfluenza virus 2,4
Pneumovirus – RS virus
Metapneumovirus
Picornaviridae
Rhinovirus, Enterovirus, Parechovirus
Adenoviridae
Coronaviridae
Reoviridae
Herpesviridae – Human herpesvirus 3
Parvoviridae – Human bocavirus
Условно-патогенные бактерии
Mycoplasma pneumoniae
Chlamydophila pneumoniae
Legionella pneumophila
Influenza virus (A, B, C)
Регистрируемые в РФ формы ОРЗ
Потенциальные возбудители
Слайд 34Методы диагностики ОРВИ,
применяемые на территории РФ
Реакции прямой /
непрямой
иммунофлуоресценции
(наиболее широко применяемый метод как в условиях стационаров, так и в службе Госсанэпиднадзора)
2. Вирусологические исследования ~ 3%*
*доклад ФЦГиЭ
«Основные направления деятельности вирусологических лабораторий»
Получение культуры возможно для:
Influenza A and B viruses, RSV, parainfluenza virus types 1, 2, 3, metapneumovirus, adenovirus
Слайд 35Современное состояние
этиологической диагностики ОРЗ
В амбулаторной практике этиология ОРЗ верхних дыхательных путей и нижних дыхательных путей не уточняется
При госпитализации этиологию удается уточнить в 15 - 30 % случаев
Слайд 36Проблемы этиологической диагностики ОРЗ
Трудоемкость культуральной диагностики ОРВИ
Низкая специфичность
и чувствительность ПИФ
Бессимптомное носительство условно-патогенных бактерий в носо/ротоглотке
Нестабильность
Str. pneumoniae (аутолиз) при хранении и транспортировке клинического материала
Конкуренция в бактериальных ассоциациях при культивировании мокроты
Плохая высеваемость бактерий из крови
Низкая специфичность ИФА для диагностики ОРЗ, вызванных Mycoplasma pneumoniae
Слайд 37Условия успешного проведения лабораторной
диагностики
тип клинического материала, адекватный нозологии
сроки отбора материала в соответствии
с этапом инфекционного процесса – наибольшая вероятность обнаружения возбудителя
отбор материала до антибактериальной терапии
1. Использование информативного клинического материала:
Высокое качество клинического материала
(техника получения материала, репрезентативная мокрота)
3. Обеспечение сохранности клинического материала
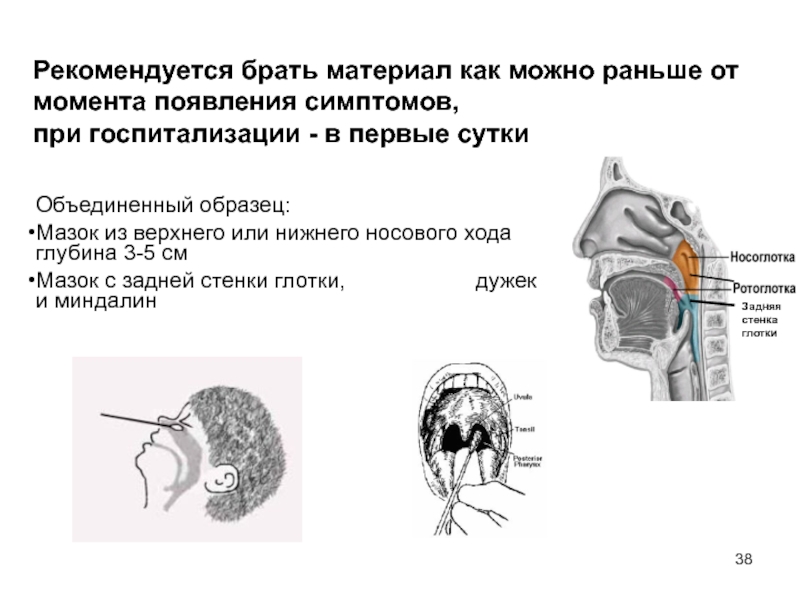
Слайд 38Рекомендуется брать материал как можно раньше от момента появления симптомов,
при госпитализации - в первые сутки
Объединенный образец:
Мазок из верхнего или нижнего носового хода глубина 3-5 см
Мазок с задней стенки глотки, дужек и миндалин
Слайд 39Зонды для взятия мазков из верхних дыхательных путей
Не использовать
зонды на деревянной основе
Не использовать зонды
с хлопковыми тампонами
Назофарингеальный велюр-тампон на пластиковом аппликаторе (503CS01, COPAN, Италия)
Педиатрический назофарингеальный велюр-тампон на пластиковом аппликаторе (516CS01, COPAN, Италия)
Зонд-тампон ПС+Виск,
1шт/уп. индивидуальная упаковка,
Стерильный, ИЛС Кат. № 300202
10 см
Зонды для мазков из ротоглотки
Полистирол + вискоза
Слайд 40Как правильно держать зонды
Правильно
НЕ правильно
возможна травматизация пациента !
Слайд 41Мазки берут сухими стерильными зондами с вискозными тампонами
Зонд с тампоном
вводят легким движением по наружной стенке полости носа на глубину
2-3 см до нижней носовой раковины
Затем зонд слегка опускают книзу, вводят в нижний носовой ход под нижнюю носовую раковину до носоглотки, и удаляют вдоль наружной стенки полости носа, производя вращательные движения
Рабочую часть зонда с тампоном помещают в стерильную одноразовую пробирку с 500 мкл стерильного 0,9 % раствора натрия хлорида, раствора фосфатного буфера или коммерческой транспортной среды
Конец зонда отламывают с расчетом, чтобы он позволил плотно закрыть крышку пробирки
Пробирку с раствором и рабочей частью зонда закрывают
Мазки из носоглотки
Слайд 42Мазки берут сухими стерильными зондами с вискозными тампонами вращательными движениями
с поверхности небных дужек, миндалин и задней стенки ротоглотки
Рабочую часть
зонда с тампоном помещают в стерильную одноразовую пробирку с 500 мкл стерильного 0,9 % раствора натрия хлорида, раствора фосфатного буфера или коммерческой транспортной среды
Конец зонда отламывают с расчетом, чтобы он позволил плотно закрыть крышку пробирки
Пробирку с раствором и рабочей частью зонда закрывают
Мазки из ротоглотки
При сборе мазков рекомендуется совмещать мазки из полости носа и ротоглотки в одной пробирке и исследовать как один образец
Слайд 43Хранение и транспортирование образцов
Предобработка материала (в лаборатории):
мокрота и аспираты
из трахеи для снижения вязкости обрабатываются препаратом муколизин (по инструкции
к препарату)
для мазков предобработка не требуется - пробирку с зондами перемешать на вортексе, не открывая крышек, кратковременно ЦФ и отобрать нужный объем для исследования
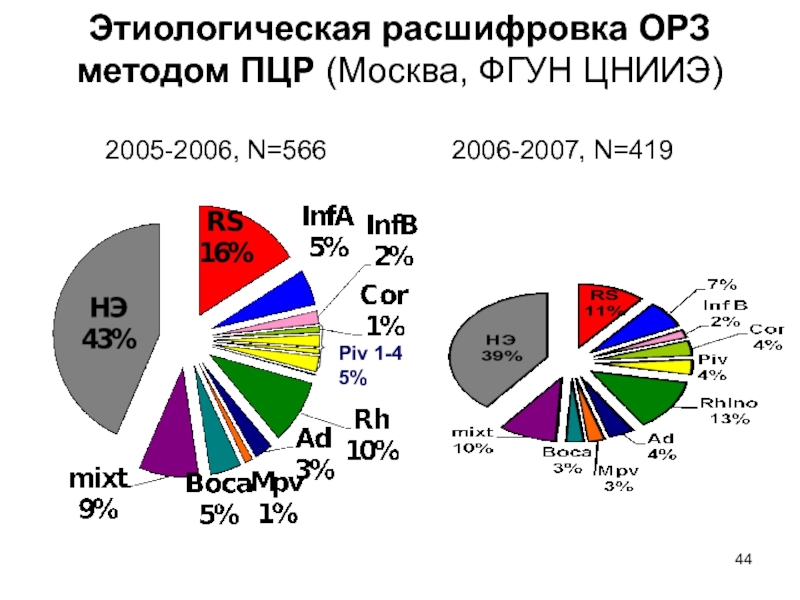
Слайд 44Этиологическая расшифровка ОРЗ
методом ПЦР (Москва, ФГУН ЦНИИЭ)
2005-2006, N=566
2006-2007,
N=419
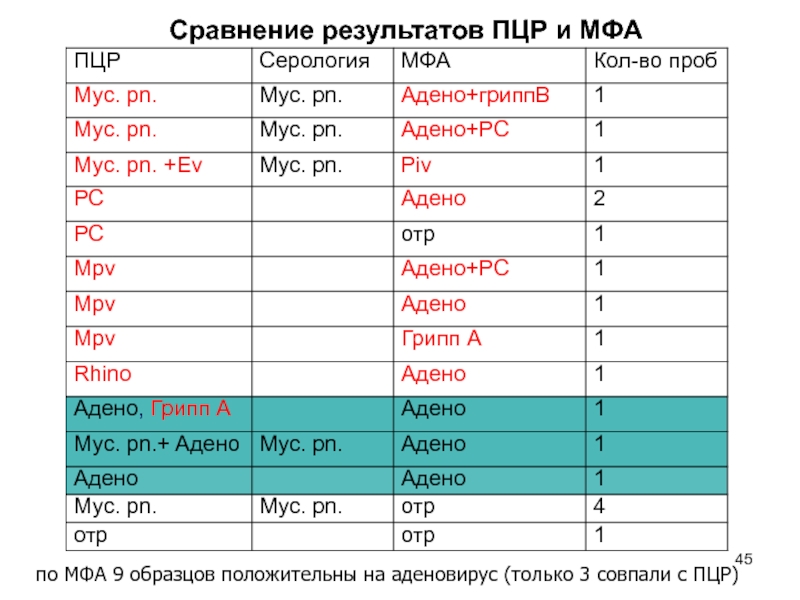
Слайд 45Сравнение результатов ПЦР и МФА
по МФА 9 образцов положительны
на аденовирус (только 3 совпали с ПЦР)
Слайд 46Высокоэффективна для этиологической диагностики ОРЗ спорадического и вспышечного характера
Использование ПЦР
позволит уточнить долю типичных бактериальных возбудителей в этиологической структуре пневмоний
и изучать роль вирусных агентов и вирусно-бактериальных ассоциаций в патогенезе ОРЗ
Внедрение ПЦР позволит избежать часто необоснованного применения антибиотиков при ОРВИ, и своевременно назначать специфическую терапию при инфицировании бактериальными возбудителями ОРЗ
Перспективы изучения этиологии хронических заболеваний дыхательных путей (бронхиальной астмы, ХОБ, ХОБЛ)
Возможности ПЦР - диагностики
Слайд 47ПЦР тест-системы, производимые в ЦНИИЭ АмплиСенс®
«Influenza virus А/В» -
вирусы гриппа А и В
«Influenza virus А/H1-swine»
«Influenza virus A-тип»
«Influenza virus A H5N1»
«hRSV» - респираторно-синцитиальный вирус
«Adenovirus» - Аденовирусы (ЭФ)
«PIV-FRT» - вирусы парагриппа c типированием
«Mycoplasma pneumoniae» (ЭФ)
«Mycoplasma pneumoniae/Chlamydophila pneumoniae»
«Legionella pneumophila»
«ОРВИ-скрин-FL»
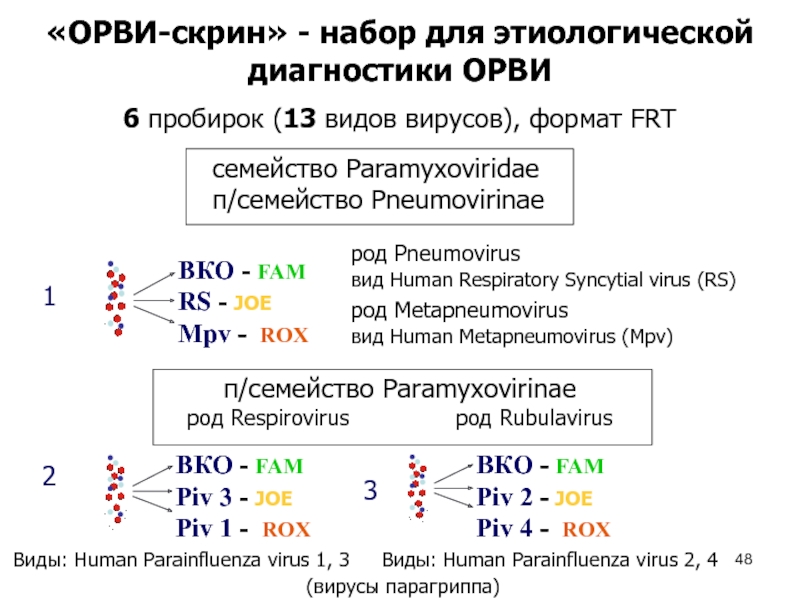
Слайд 48«ОРВИ-скрин» - набор для этиологической диагностики ОРВИ
1
2
3
6 пробирок
(13 видов вирусов), формат FRT
семейство Paramyxoviridae
п/семейство Pneumovirinae
род Metapneumovirus
вид Human
Metapneumovirus (Mpv)
род Pneumovirus
вид Human Respiratory Syncytial virus (RS)
п/семейство Paramyxovirinae
род Respirovirus род Rubulavirus
Виды: Human Parainfluenza virus 1, 3
Виды: Human Parainfluenza virus 2, 4
(вирусы парагриппа)
Слайд 49ВКО - FAM
E 229 / NL 63 - JOE
OC 43
/ HKU 1- ROX
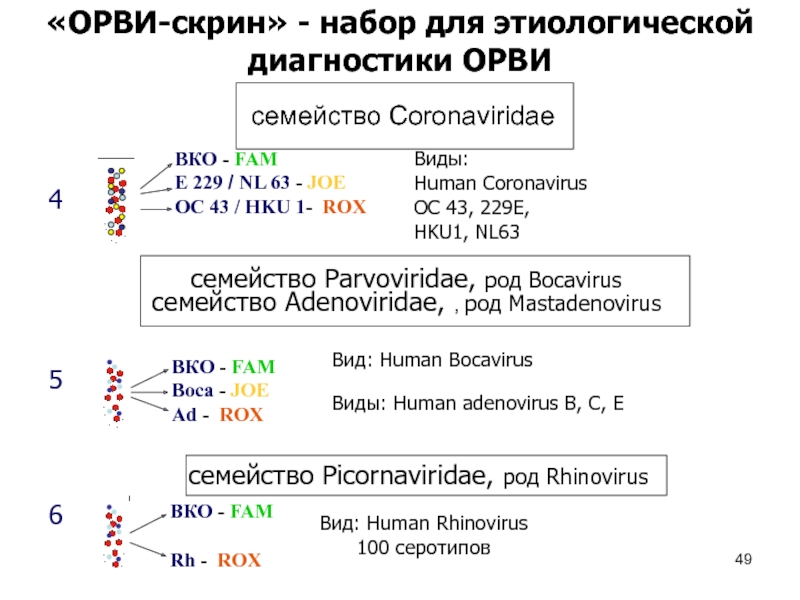
«ОРВИ-скрин» - набор для этиологической
диагностики ОРВИ
4
5
6
семейство Parvoviridae, род Bocavirus семейство Adenoviridae, , род Mastadenovirus
семейство Coronaviridae
Human Coronavirus
OC 43, 229E,
HKU1, NL63
Виды:
семейство Picornaviridae, род Rhinovirus
Вид: Human Rhinovirus
100 серотипов
Вид: Human Bocavirus
Виды: Human adenovirus B, C, E
Слайд 50Характеристика основных возбудителей ОРЗ
Слайд 51Респираторно-синцитиальный вирус
семейство Paramyxoviridae
п/семейство Pneumovirinae
род Pneumovirus
вид Human respiratory syncytial virus
(HRSV)
Геном – o.ц. РНК отрицательной полярности; оболочка – есть
Поражает как
ВДП, так и НДП вызывает значительную деструкцию эпителия
На HRSV приходится 64 млн случаев ОРЗ в год в мире
Уровень летальности в мире от HRSV-инфекции составляет 160 тыс в год
HRSV-инфекция – причина госпитализации 19% детей до 5 лет с ОРЗ НДП В Европейских странах (причина бронхиолитов до 85% и пневмонии до 20% )
Причина 20% гриппо-подобных болезней у взрослых от 15 до 45 лет
Иммунитет – нестойкий
Доказана значимость, как причины развития бронхиальной астмы
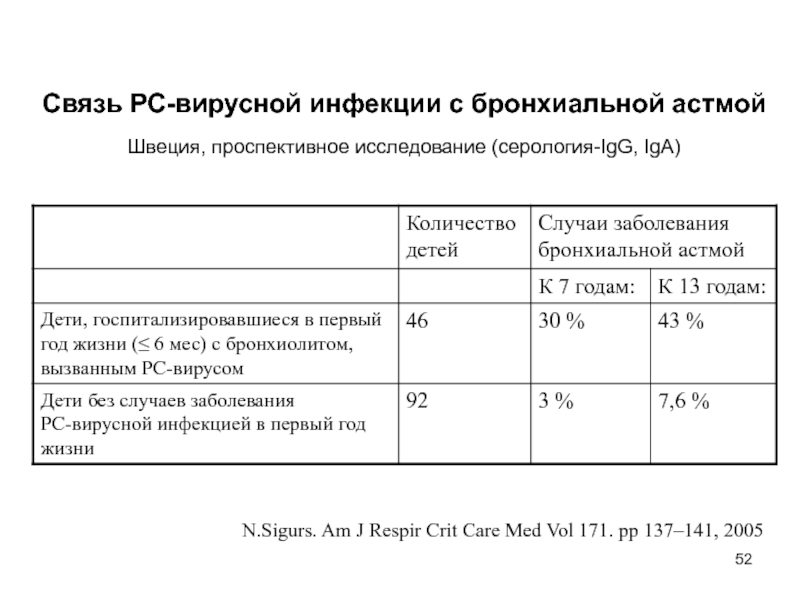
Слайд 52N.Sigurs. Am J Respir Crit Care Med Vol 171. pp
137–141, 2005
Связь РС-вирусной инфекции с бронхиальной астмой
Швеция, проспективное исследование (серология-IgG,
IgA)
Слайд 53Метапневмовирус
семейство Paramyxoviridae п/семейство Pneumovirinae
род metapneumovirus
вид Human metapneumovirus (HMPV)
Выделен в 2001
г. из назофарингиальных аспиратов детей с ОРЗ
Клиника HMPV-инфекции сходна с
HRSV (заболевания НДП у детей)
К 5 годам практически все дети имеют антитела к вирусу
Часто выявляется вместе с другими вирусами
Инкубация 3-5 дней
Противовирусные средства не известны
Основные клинические проявления — ринит, бронхиолит, круп
Слайд 54семейство Paramyxoviridae
п/семейство Paramyxovirinae
род Respirovirus
виды Human Parainfluenza virus 1,3 (HPIV-1,3)
род
Rubulavirus
виды Human Parainfluenza virus 2,4 (HPIV-2,4)
Вирусы парагриппа
Геном – o.ц. РНК
отрицательной полярности; оболочка – есть
Поражает как ВДП, так и НДП вызывает значительную деструкцию эпителия
HPIV-инфекция является второй по частоте причиной госпитализации детей и пожилых людей после HRSV
Почти все дети к 2 годам хотя бы один раз переболевают HPIV-инфекцией
В США на HPIV-инфекцию приходится 64% случаев крупов и 22% случаев заболевания нижних дыхательных путей
HPIV-1-4 (круп и бронхо-обструкция), HPIV-3 (пневмонии и бронхиолиты)
Инкубация — 2-6 дней, иммунитет не стойкий, повторные инфекции — не редкость
Противовирусные средства не известны
Слайд 55семейство Picornaviridae
род Rhinovirus
виды Human Rhinovirus (HRV)
более 100 серотипов, выделяют
генотипы А, В, С
Риновирусы
Более 100 серотипов, относящихся к пикорнавирусам, заражение
от человека к человеку, часто через загрязненные вирусом руки
Геном – o.ц. РНК положительной полярности
Оболочки – нет
Отличие от Энтеровирусов – кислото-неустойчивость
Поражает преимущественно ВДП, не вызывает деструкции эпителия, но доказана возможность репликации в бронхиолах
HRV второй по частоте случаев ОРЗ после PC у детей и первый -у взрослых
У детей вызывают обструкцию дыхательных путей, бронхиты, бронхиолиты, пневмонию, синуситы, отиты; у взрослых – заболевания верхних дыхательных путей
Дискутируется значимость, как причины обострений бронхиальной астмы
Длительность выделения вируса – до 3-х недель
Иммунитет – серотип-специфичный IgA, нестойкий
Слайд 56Бокавирус человека
семейство Parvoviridae
п/сем Parvovirinae
род Bocavirus
вид human Bocavirus (HBoV)
Открыт
в 2005 году
Зарегистрирована высокая распространенность
(6 годам все дети имеют антитела к бокавирусу человека)
Доказательcтво инфекционности:
- зарегистрировано выявление ДНК возбудителя в назофарингеальных мазках и в крови с одновременным повышением титра антител > 10 раз у пациентов
с ОРЗ нижних отделов респираторного тракта
Вирусная ДНК обнаруживается также в фекалиях, сыворотке, моче
Endo R., Ishiguro N., Kikuta H. et al. J. Clin. Microbiol., 2007
Геном – о.ц. ДНК
Оболочки – нет
Слайд 57семейство Adenoviridae
род Mastadenovirus
виды Human adenovirus А-F (HAdVA, ..F, G)
Аденовирусы
ДНК-вирусы,
имеют более 50 серотипов, составляющие 6 видов (A-F)
С ОРЗ ассоциированы
аденовирусы B, C и E
Геном – д.ц. ДНК
Оболочки – нет
Очень стабилен в окружающей среде
Поражает преимущественно ВДП, не вызывает деструкции эпителия (четвертый по частоте у детей)
Может вызывать крупы, бронхиты, пневмонии
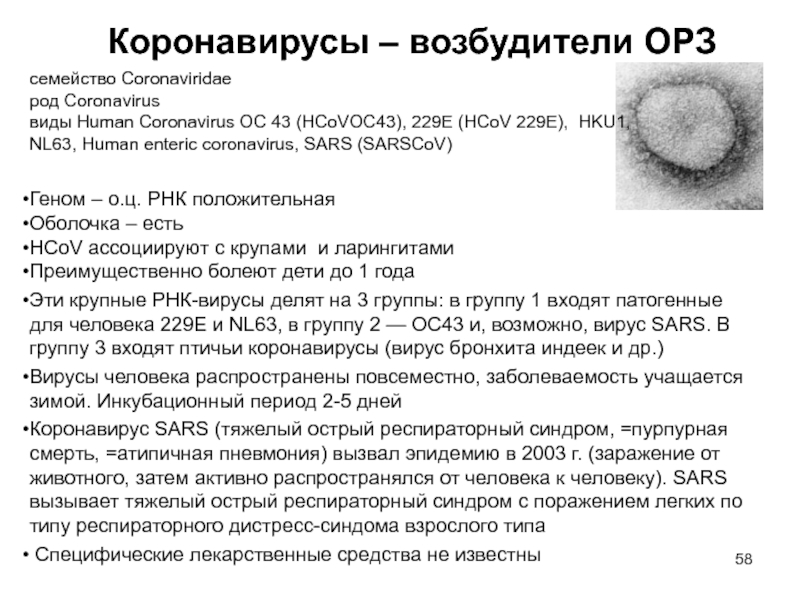
Слайд 58Коронавирусы – возбудители ОРЗ
семейство Coronaviridae
род Coronavirus
виды Human Coronavirus OC
43 (HCoVOC43), 229E (HCoV 229E), HKU1, NL63, Human enteric coronavirus,
SARS (SARSCoV)
Геном – о.ц. РНК положительная
Оболочка – есть
HCoV ассоциируют с крупами и ларингитами
Преимущественно болеют дети до 1 года
Эти крупные РНК-вирусы делят на 3 группы: в группу 1 входят патогенные для человека 229Е и NL63, в группу 2 — ОС43 и, возможно, вирус SARS. В группу 3 входят птичьи коронавирусы (вирус бронхита индеек и др.)
Вирусы человека распространены повсеместно, заболеваемость учащается зимой. Инкубационный период 2-5 дней
Коронавирус SARS (тяжелый острый респираторный синдром, =пурпурная смерть, =атипичная пневмония) вызвал эпидемию в 2003 г. (заражение от животного, затем активно распространялся от человека к человеку). SARS вызывает тяжелый острый респираторный синдром с поражением легких по типу респираторного дистресс-синдома взрослого типа
Специфические лекарственные средства не известны
Слайд 59SARS/ТОРС: хронология событий
осень 2002г – Китай, провинция Guandong -
регистрация случаев «атипичных пневмоний» с высокой летальностью
21 февраля 2003г
– Гон Конг - регистрация завозного случая у гражданина Китая и развитие заболевания у 18 контактировавших с ним лиц
март 2003г – распространение заболевания в 13 стран мира. Общее количество заболевших 1622, погибших – 58
10 августа 2003г – Итоги: 8422 заболевших и 916 (11%) погибших пациентов в 32 странах мира
Слайд 60Циветты – источник вируса ТОРС для человека
(SARS-CoV)
Циветты, енотовидные собаки, барсуки:
США, Канада, Европа, Китай, Индия, Япония
Слайд 61Лабораторная диагностика ТОРС в РФ
РТ-ПЦР РНК вируса SARS-CoV (
ИФА IgM и IgG (≥2 недели)
специфичность - 95%
IgM в
ИФА сохраняется более 4 недель
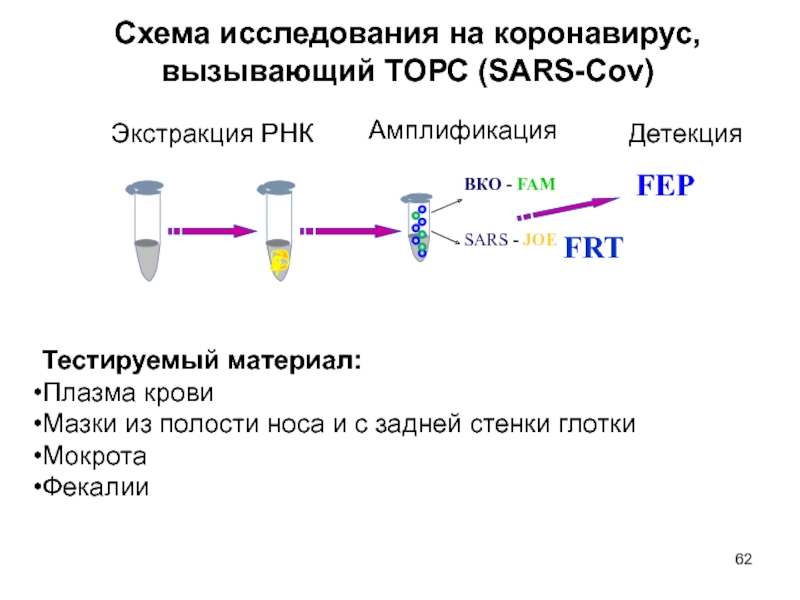
Слайд 62ВКО - FAM
SARS - JOE
FEP
Экстракция РНК
Амплификация
Детекция
Тестируемый материал:
Плазма крови
Мазки из полости носа и с задней стенки
глотки
Мокрота
Фекалии
FRT
Схема исследования на коронавирус, вызывающий ТОРС (SARS-Cov)
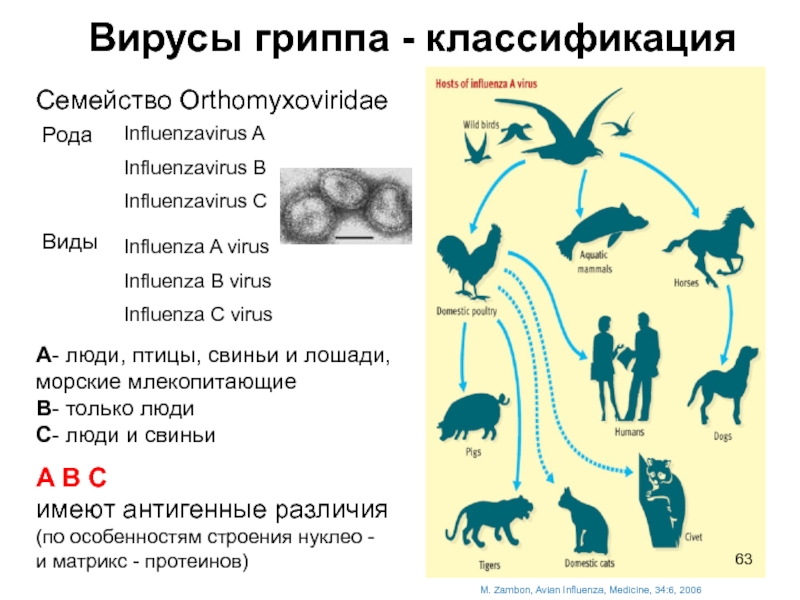
Слайд 63Вирусы гриппа - классификация
M. Zambon, Avian Influenza, Medicine, 34:6, 2006
Слайд 64Грипп A
Вызывает эпидемии и пандемии, ежегодно в мире:
600 млн
случаев заболеваний,
150 - 200тыс случаев госпитализаций,
250-500тыс
летальных исходов,
Субтипы гриппа A отличающиеся по сочетанию двух поверхностных гликопротеинов:
Гемагглютинин (HA) = 16 типов
Нейраминидаза (NA) = 9 типов
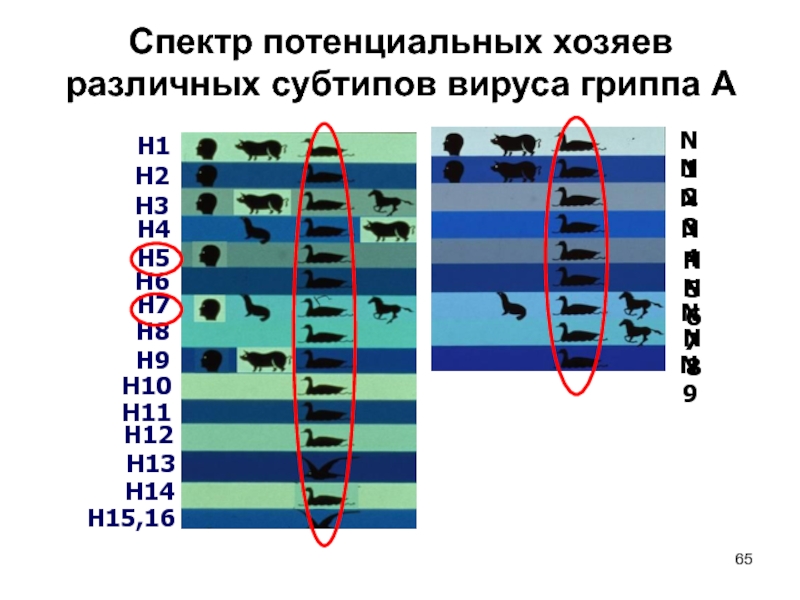
Все субтипы вируса А циркулируют среди диких птиц
Сезонный грипп: только субтипы H1N1, H3N2 циркулируют среди людей в настоящее время
Слайд 65Спектр потенциальных хозяев различных субтипов вируса гриппа A
Слайд 66Мутационный процесс вируса гриппа А
Антигенный дрейф
(Незначительные изменения HA/NA)
Точечные мутации
во время
репликации, подтип остается тем же
Следствия:
Постоянные изменения антигенных свойств
Ежегодные эпидемии
Необходимость ежегодного обновления вакцин
Антигенный шифт
(Значительные изменения HA/NA)
Генетическая реассортация
или
Адаптация вируса гриппа птиц или других животных к организму человека
Следствия:
Появляется новый субтип
Опасность пандемии
Слайд 67Пандемии гриппа в ХХ веке и в ХХI веке….
H1N1
H2N2
H3N2
1918: “Испанка”
40-50
млн погибших
1957: “Азиатский грипп”
1-4 млн погибших
1968: “Гонконгский грипп”
> 1 млн
погибших
H1N1swl
2009: “Свиной грипп”
~ 18 тыс. лабораторно подтвержденных случаев летального исхода (ВОЗ)
Обнаружение и типирование вирусов гриппа - контроль появления новых субтипов с потенциальной пандемической опасностью
Своевременное применение этиотропной терапии гриппа
Слайд 68Вирус гриппа A/H5N1
Вирус может присутствовать у инфицированной птицы во всех
органах и частях
Выживание в фекалиях:
35 дней при 4°C/6 дней
при 37°C
Выживание в птичниках:
Несколько недель
Только тщательная термическая обработка позволяет инактивировать вирус
Замораживание/охлаждение неадекватны
Яйца инфицированной птицы могут быть контаминированы как изнутри так и снаружи скорлупы (кипячение не менее 10 минут)
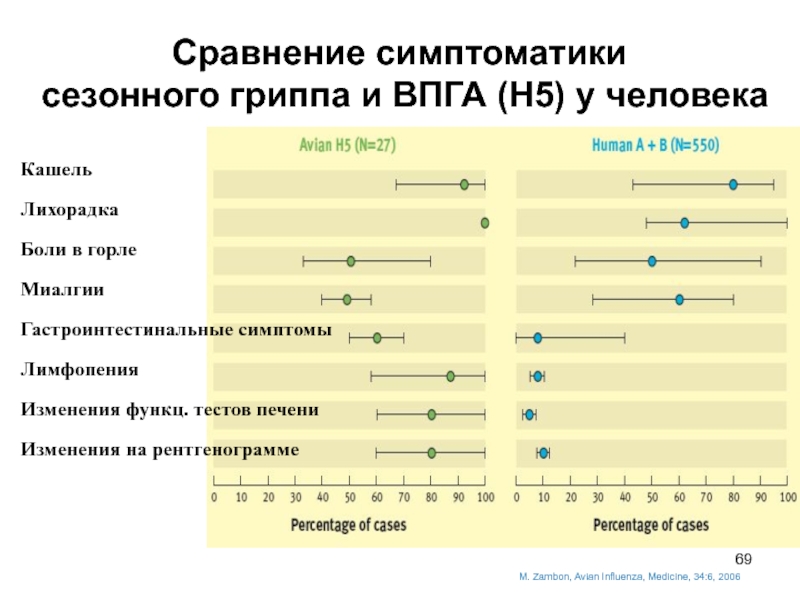
Слайд 69M. Zambon, Avian Influenza, Medicine, 34:6, 2006
Сравнение симптоматики
сезонного гриппа и ВПГА (Н5) у человека
Кашель
Лихорадка
Боли в горле
Миалгии
Гастроинтестинальные симптомы
Лимфопения
Изменения функц. тестов печени
Изменения на рентгенограмме
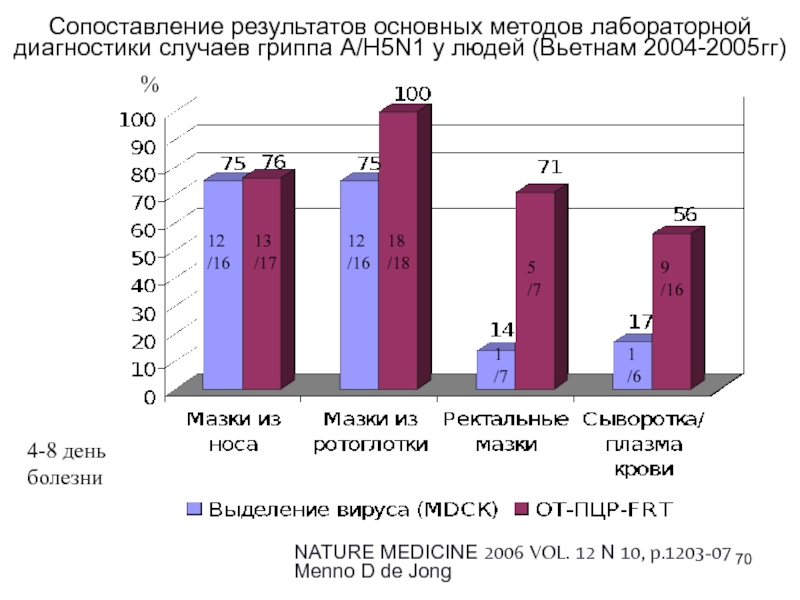
Слайд 70Сопоставление результатов основных методов лабораторной диагностики случаев гриппа А/Н5N1 у
людей (Вьетнам 2004-2005гг)
NATURE MEDICINE 2006 VOL. 12 N 10, p.1203-07
Menno D de Jong
4-8 день
болезни
%
Слайд 71Пандемия гриппа 2009г (A/H1N1)
С 18 марта в Федеральном округе Мехико
в рамках эпиднадзора стали регистрироваться случаи выявления схожей с гриппом
болезни (СсГБ или ГПЗ).
В апреле число случаев заболевания устойчиво росло, на 23 апреля в Мехико было зарегистрировано более 854 случаев пневмонии, 59 из которых закончились смертельным исходом. 24 апреля 2009 г. Правительство США сообщило о семи подтвержденных случаях заболевания людей свиным гриппом A/H1N1 в США (в Калифорнии и Техасе) и девяти подозреваемых случаях заболевания.
В Мексике 18 случаев были лабораторно подтверждены как свиной грипп A/H1N1, 12 из них были генетически идентичны с вирусами свиного гриппа A/H1N1 из Калифорнии.
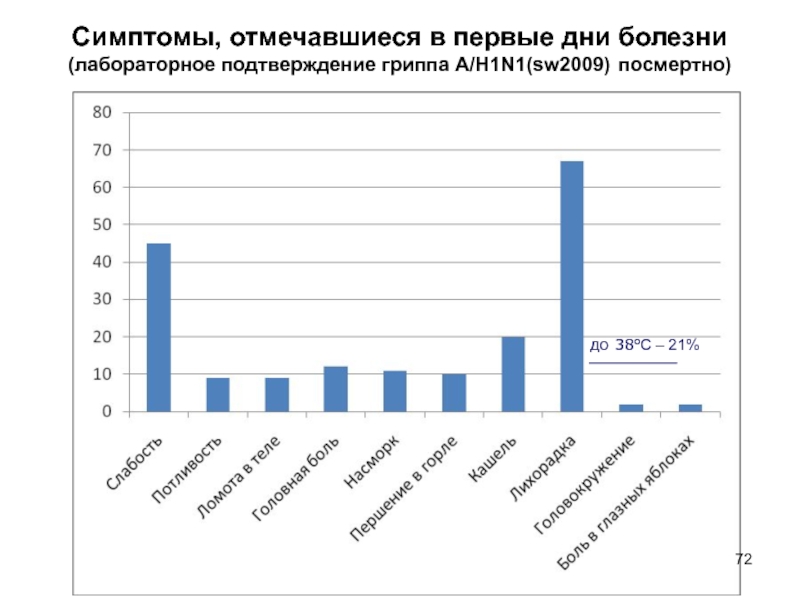
Слайд 72Симптомы, отмечавшиеся в первые дни болезни (лабораторное подтверждение гриппа A/H1N1(sw2009)
посмертно)
до 38ºС – 21%
Слайд 7303.05.09
26.05.09
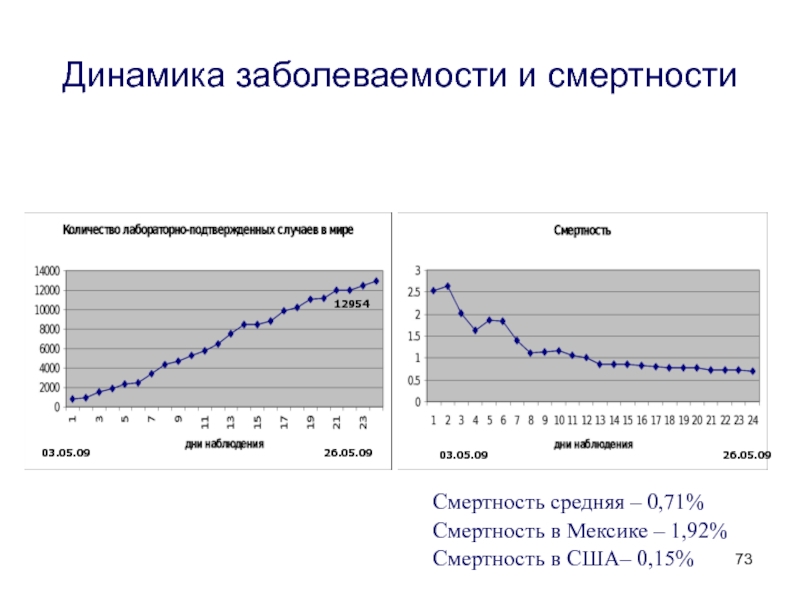
12954
Динамика заболеваемости и смертности
03.05.09
26.05.09
Смертность средняя – 0,71%
Смертность в Мексике –
1,92%
Смертность в США– 0,15%
Слайд 74Лабораторная диагностика: рекомендации Центра по контролю и профилактике заболеваний CDC
США
ПЦР с использованием валидированных протоколов
Изоляция вируса в культуре MDCK или
на куриных эмбрионах с последующим секвенированием генома (окончательная идентификация)
Не рекомендуются быстрые тесты по обнаружению антигенов гриппа А: иммунофлуоресценция, иммунохроматография, в связи с низкой чувствительностью (от 40 до 60%) и отсутствием специфичности определения «свиного» штамма
Слайд 75ПЦР - диагностика гриппа
наборы для ПЦР-FRT/FEP (ФГУН ЦНИИЭ)
«Influenza virus
A/B»
Типирование вирусов гриппа
«Influenza virus A-тип-FL»
«Influenza virus A H5/N1»
H5 - FAM
N1 - JOE
семейство Orthomyxoviridae
«Influenza virus A/H1-swine»
ВКО - FAM
Н1-swine - JOE
Слайд 76Алгоритм проведения ПЦР-анализа (Грипп)
Экстракция НК (50-100 мкл)
«Рибо-преп», 20-40 мин
«Рибо-сорб», 40-60
мин
Реакция ОТ (37ºС)
ПЦР-FEP-детекция
2-2,5 ч
15-30 мин
2-2,5 ч
45-60 мин
ПЦР-FRT
(качественный анализ)
Наличие эпидпоказаний для
тестирования на пандемический грипп
РНК-10 мкл - кДНК (20 мкл)
Разведение 1:2 (40 мкл)
«Influenza virus A/B»
Influenza virus A -
Influenza virus A +
«Influenza virus A/H1-swine»
Influenza virus A/H1-swine +
Influenza virus A/H1-swine -
«Influenza virus A - тип»
Influenza virus A/H1N1 +
Или Influenza virus A/H3N2 +
Influenza virus A/H1N1 -
И Influenza virus A/H3N2 -
Неизвестный субтип!
Требуется изучение в референс-центрах
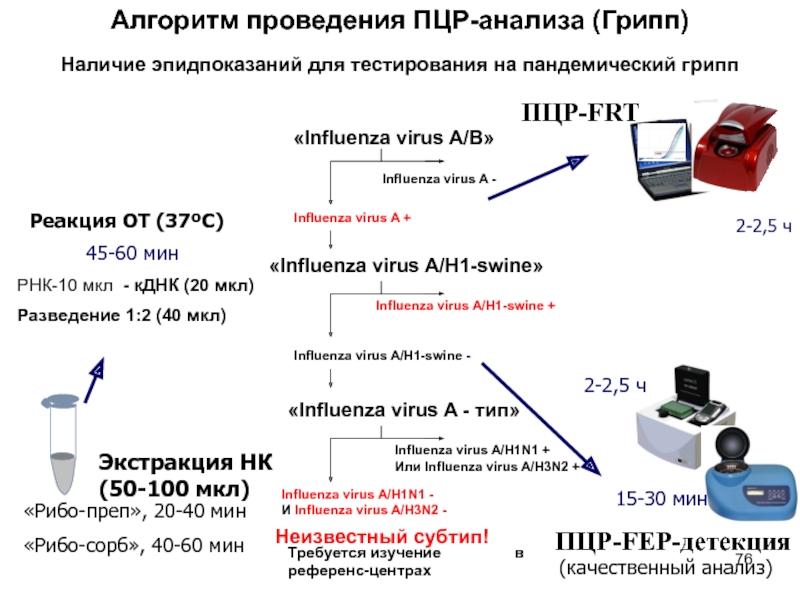
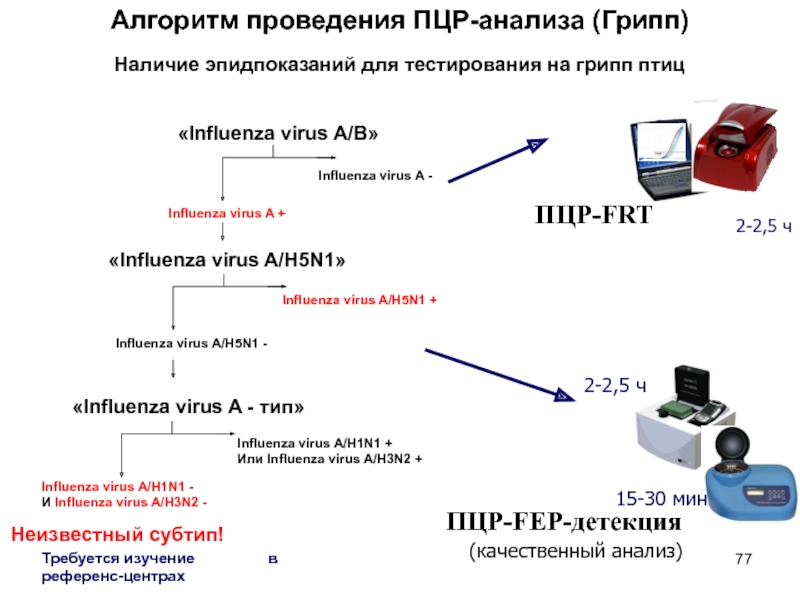
Слайд 77Алгоритм проведения ПЦР-анализа (Грипп)
ПЦР-FEP-детекция
2-2,5 ч
15-30 мин
2-2,5 ч
ПЦР-FRT
(качественный анализ)
Наличие эпидпоказаний для
тестирования на грипп птиц
«Influenza virus A/B»
Influenza virus A -
Influenza virus
A +
«Influenza virus A/H5N1»
Influenza virus A/H5N1 +
Influenza virus A/H5N1 -
«Influenza virus A - тип»
Influenza virus A/H1N1 +
Или Influenza virus A/H3N2 +
Influenza virus A/H1N1 -
И Influenza virus A/H3N2 -
Неизвестный субтип!
Требуется изучение в референс-центрах
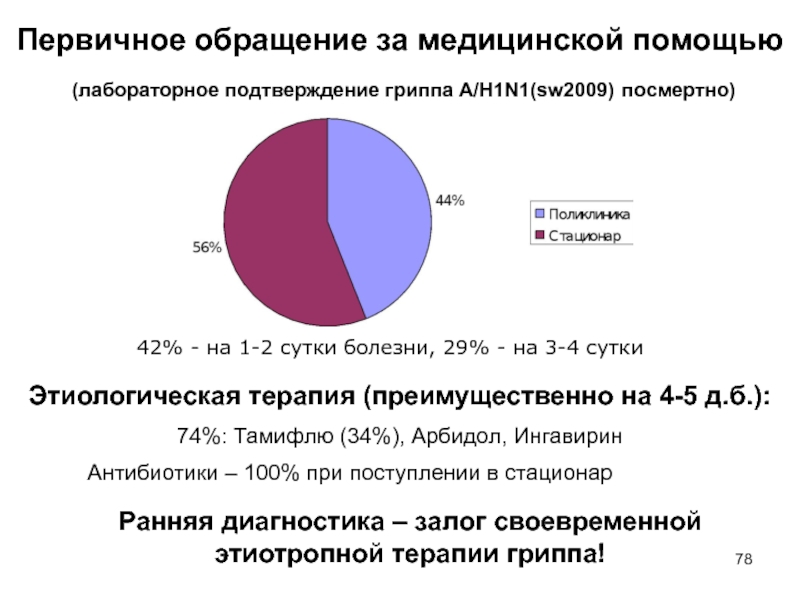
Слайд 78Первичное обращение за медицинской помощью
(лабораторное подтверждение гриппа A/H1N1(sw2009) посмертно)
42%
- на 1-2 сутки болезни, 29% - на 3-4 сутки
Этиологическая
терапия (преимущественно на 4-5 д.б.):
74%: Тамифлю (34%), Арбидол, Ингавирин
Антибиотики – 100% при поступлении в стационар
Ранняя диагностика – залог своевременной
этиотропной терапии гриппа!