Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Взаимодействие в двухкомпонентных системах Фазовые диаграммы двухкомпонентных
Содержание
- 1. Взаимодействие в двухкомпонентных системах Фазовые диаграммы двухкомпонентных
- 2. Фрагмент P-T-x фазовой диаграммы бинарной системы. Существование пара и жидкости и область сосуществования этих фаз
- 3. Взаимодействие в двухкомпонентных системахПримитивные виды взаимодействия: без промежуточных фаз
- 4. Взаимодействие в двухкомпонентных системахПримитивные виды взаимодействия: без
- 5. А если смешение не является полным, то
- 6. Взаимная растворимость в системе “вода – фенол”
- 7. Взаимная растворимость в системе “вода – фенол”
- 8. Вариант примитивного взаимодействия двух компонентов:Область гомогенности жидкого
- 9. Вариант примитивного взаимодействия: полное смешение в жидкой
- 10. … добавим и другие сечения при различных температурах, < 0С:сосуществующий раствор становится всё более концентрированным
- 11. …соединим границы области существования жидкой фазы линией
- 12. … жидкость L (раствор сахара в воде)
- 13. …пусть имеется состав двух компонентов, который попадает
- 14. Для ответа на поставленный вопрос проведем горизонтальную
- 15. Что будет происходить с некоторым составом жидкой
- 16. Как вычислить координаты эвтектической точки?Решаем совместно уравнение
- 17. Уравнение Шрёдера – Ле-Шателье описывает линию ликвидуса…
- 18. А как быть с концентрированными растворами?
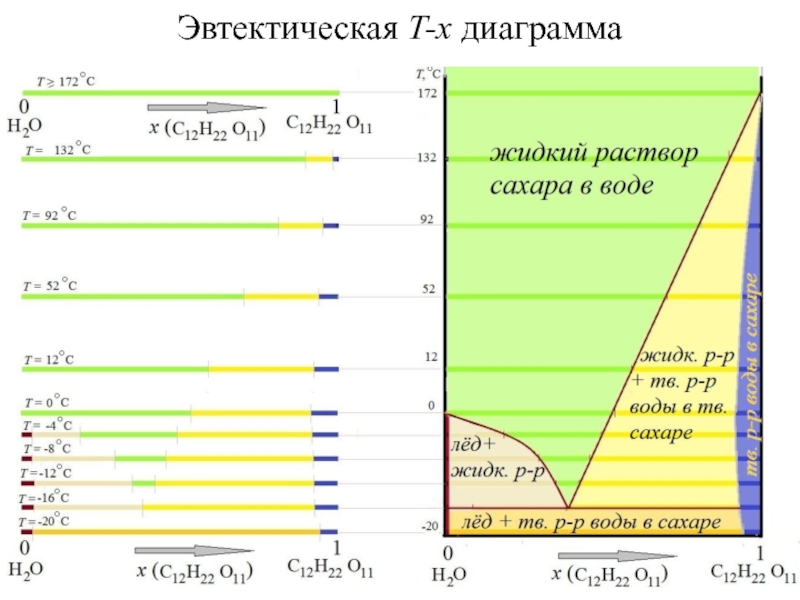
- 19. Эвтектическая T-x диаграмма
- 20. Эвтектическая T-x диаграммадругой пример: вода – мочевинаH2O
- 21. Слайд 21
- 22. Слайд 22
- 23. Особые примеры структур эвтектических сплавов Спиральная
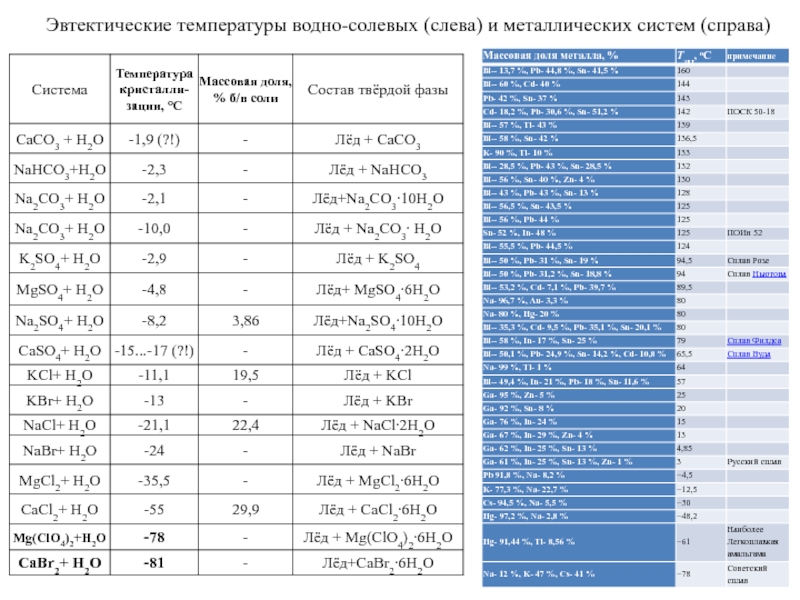
- 24. Эвтектические температуры водно-солевых (слева) и металлических систем (справа)
- 25. В пустыне есть свои удивительные объекты...В нашем
- 26. Пример эвтектической T-x диаграммы (Cd-Zn) с ретроградным
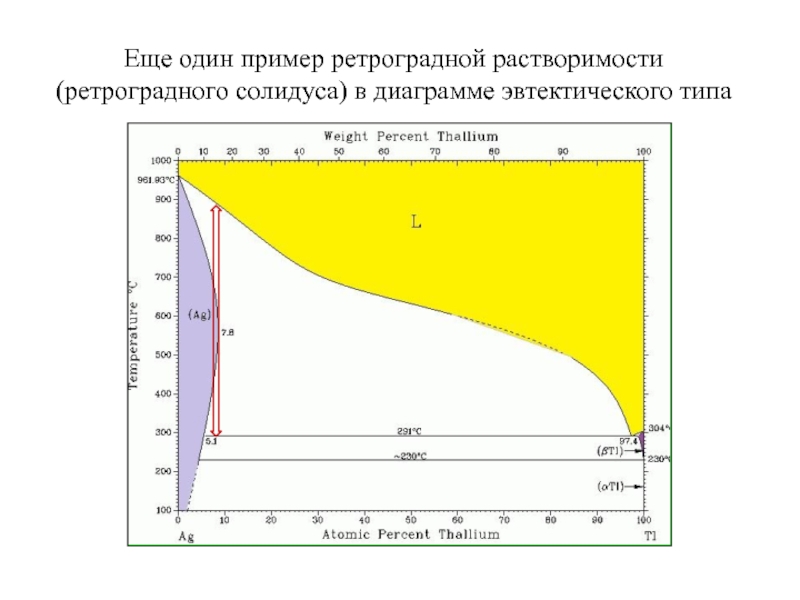
- 27. Еще один пример ретроградной растворимости (ретроградного солидуса) в диаграмме эвтектического типа
- 28. Другие примитивные типы взаимодействия...Михал Карч, примитивист («мало знаний»)
- 29. Один из наиболее примитивных типов взаимодействия: монотектический
- 30. Один из наиболее примитивных типов взаимодействия: монотектический тип (более примитивный, чем эвтектический)
- 31. Один из наиболее примитивных типов взаимодействия: монотектический тип. Еще пример. (более примитивный, чем эвтектический)
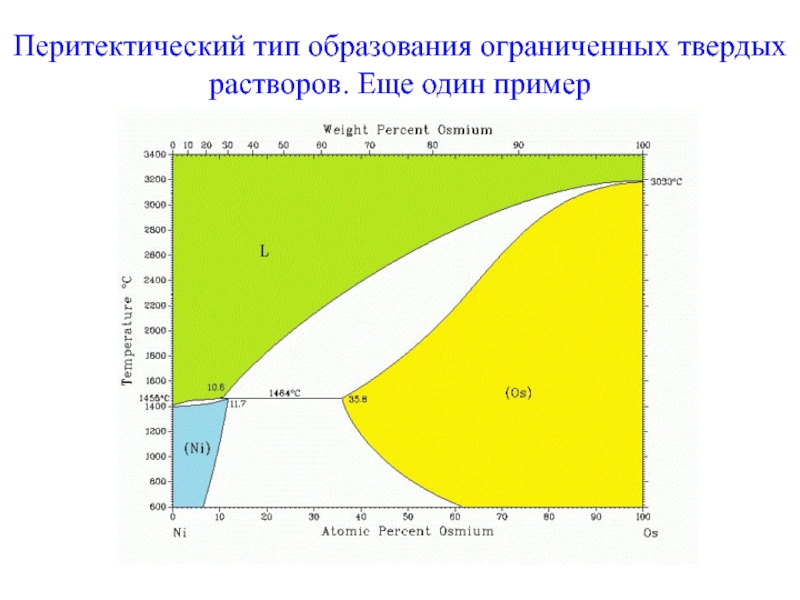
- 32. “Несколько менее примитивный” тип взаимодействия:перитектический тип образования ограниченных твердых растворов
- 33. Перитектический тип образования ограниченных твердых растворов. Еще пример. (На полиморфизм железа пока не обращать внимания)
- 34. Перитектический тип образования ограниченных твердых растворов. Еще один пример
- 35. Перитектический тип образования ограниченных твердых растворов. Еще один пример
- 36. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Взаимодействие в двухкомпонентных системах
Примитивные виды взаимодействия: без промежуточных фаз
Слайд 4Взаимодействие в двухкомпонентных системах
Примитивные виды взаимодействия: без промежуточных фаз
Компоненты: A,
B. Должны быть переменные: P, T, xA, xB
Но можно обойтись
набором трёх (а не четырех) переменных: P, T, xB, т.к. xB = 1 – xAДолжна быть трехмерная диаграмма с осями P, T, xB.
Зафиксируем первые две переменные: P = const, T=const.
Пространство состояний в этом случае представлено числовым отрезком. Если происходит полное смешивание A и B при P = const, T=const, то весь этот числовой отрезок [0, 1] и представляет собой P, T – фиксированную области гомогенности. A B
0 xB→ 1
Слайд 5А если смешение не является полным, то на фазовой диаграмме
(и на P, T – фиксированном сечении этой диаграммы) появляются
“пустые” области, лишенные физического смысла.Взаимная растворимость в системе “вода – фенол” при различных фиксированных температурах. Давление в системе также фиксировано и равно 1 атм.
Слайд 6Взаимная растворимость в системе “вода – фенол” при различных фиксированных
температурах. Давление в системе также фиксировано и равно 1 атм
...
а теперь поместим все концентрационные отрезки на ось температур...... и соединим границы областей гомогенности, полученные при разных температурах плавными линиями..
Получаем T-x сечение бинарной диаграммы
“вода – фенол”
для P = 1 атм
Слайд 7Взаимная растворимость в системе “вода – фенол” при различных фиксированных
температурах. Давление в системе также фиксировано и равно 1 атм
T-x
сечение системы “H2O-C6H5OH”... а теперь пометим область существования (область гомогенности) жидкой фазы (осуществим заливку зеленым цветом).
Полузаконный приём: P можно жестко и не фиксировать. Не слишком большие (десятки атм) варьирования давления мало сказываются на состоянии конденсированных (ж. и тв.) фаз! Именно только такие фазы и рассматриваем далее. Тогда правило фаз можно условно записывать как
Ф + С = K +1
и говорить о T-x диаграмме системы.
P = 1 атм
Слайд 8Вариант примитивного взаимодействия двух компонентов:
Область гомогенности
жидкого раствора сахара
в воде
(разб. раствор)
Построим изобарно – изотермическое сечение в системе “сахароза –
вода” при температуре 0С в области существования жидкого раствора (при низких концентрациях сахара).полное смешение в жидкой фазе...
... и полное расслоение в твердых фазах
Слайд 9Вариант примитивного взаимодействия: полное смешение в жидкой фазе и полное
расслоение в твердой фазе (продолжение)
Область гомогенности
жидкого раствора сахара
в
воде (разб. раствор)Добавим изобарно – изотермическое сечение в системе в системе “сахар – вода” при температуре, немного меньше 0 С: появляется область расслоения за счет кристаллизации льда
Область расслоения:
сосуществуют лёд и ж. раствор; любой состав в этой области расслаивается как показано красными стрелками
Слайд 10… добавим и другие сечения при различных температурах, < 0С:
сосуществующий
раствор становится всё более концентрированным
Слайд 12… жидкость L (раствор сахара в воде) существует в области,
которая выделена зеленой заливкой
Линия, которая отделяет область существования жидкой
фазы от области расслоения (в которой появляется твёрдая фаза) называется линией ликвидусаСлайд 13…пусть имеется состав двух компонентов, который попадает в область расслоения
(красная точка)
Какие фазы и какого состава появятся при попытке приготовить
фазу состава, отвечающего данной точке (b) в условиях равновесия?b
Слайд 14Для ответа на поставленный вопрос проведем горизонтальную линию (коноду)
Конода пересекает
границы существования областей каждой из фаз в определенных точках (точки
a и c). Эти точки и будут отвечать составам сосуществующих фаз. Отношения количеств фаз определяется исходя из “правила рычага”:(nS/nL) = (ab/bc)-1
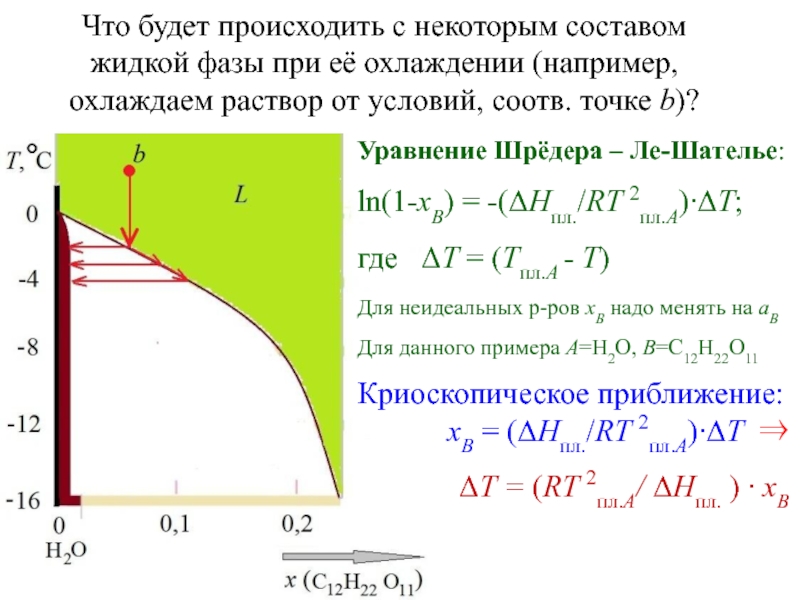
Слайд 15Что будет происходить с некоторым составом жидкой фазы при её
охлаждении (например, охлаждаем раствор от условий, соотв. точке b)?
Уравнение
Шрёдера – Ле-Шателье:ln(1-xB) = -(DHпл./RT 2пл.А)∙DT;
где DT = (Tпл.А - T)
Для неидеальных р-ров xB надо менять на aB
Для данного примера A=H2O, B=C12H22O11
Криоскопическое приближение:
xB = (DHпл./RT 2пл.А)∙DT
DT = (RT 2пл.А/ DHпл. ) ∙ xB
Слайд 16Как вычислить координаты эвтектической точки?
Решаем совместно уравнение Шредера – Ле-Шателье
для обеих ветвей ликвидуса
ln(1-xB) = -(DHпл.A/RT 2пл.А)∙(T пл.А - T)
ln(xB)
= -(DHпл.B/RT 2пл.B)∙(T пл.B - T)с неизвестными T и xB (для реального раствора – с переменными T и aB)
P.S. Еще некоторые важные моменты – применение правила фаз, построение кривых нагревания/охлаждения и некоторые др. – см. конспекты лекций (разбирается на доске с мелом).
Слайд 17Уравнение Шрёдера – Ле-Шателье описывает линию ликвидуса… или (что то
же самое) отвечает на вопрос: “Какой температуре соответствует первичная кристаллизация
раствора”? Кристаллизуется растворитель!Слайд 23Особые примеры структур эвтектических сплавов
Спиральная эвтектика системы Zn-MgZn2.
Примеры этой и других гетероструктур эвтектических сплавов см. на рис.
справа.Микроструктура эвтектик. По работе Тарана и Мазура, 1978.
а - Sb+Zn4Sb3, ув.х200; б - Sb + Cu2Sb, ув. х 400; в - Fe+Fe3C, ув. х 400; г - Fe+C, ув. х 150; д - Fe+W6C, ув.х 250; е - Fe+MoC, ув. х 500; ж - Zn+MgZn2, ув. х1000; з - Al+FeAlSi, ув. х 500; и- Pb + Sb, ув. x 200.
Слайд 25В пустыне есть свои удивительные объекты...
В нашем случае (диаграммы эвтектического
типа) такой объект – ФД с ретроградным солидусом...
Слайд 26Пример эвтектической T-x диаграммы (Cd-Zn) с ретроградным солидусом (ограничивает область
гомогенности тв. р-ра на основе Zn)
! На линии ликвидуса (со
стороны ретроградной растворимости) часто встречается перегиб, близкий по температуре максимальной растворимости примеси в твердой фазеКажущийся парадокс: для диаграмм такого типа возможны такие диапазоны температур и составов, в которых увеличение температуры приводит к кристаллизации, а уменьшение T – к плавлению (см. следующий слайд – область, выделенную стрелками ).