Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ядерный реактор. Получение радиоактивных изотопов и их применение
Содержание
- 1. Ядерный реактор. Получение радиоактивных изотопов и их применение
- 2. ОпределениеИзото́пы (от др.-греч. ισος — «равный», «одинаковый», и
- 3. Открытие изотоповПервое доказательство того, что вещества, имеющие
- 4. Изотопы в природеСчитается, что изотопный состав большинства
- 5. Получение радиоактивных изотопов.Получают радиоактивные изотопы в атомных
- 6. Применение в биологии и медицине Одним из
- 7. Применение в промышленностиОдним из примеров может служить
- 8. Изотопы в сельском хозяйстве Все более широкое
- 9. Изотопы в археологии Интересное применение для определения
- 10. Радиоактивные изотопы — источники излученийРадиоактивные изотопы широко
- 11. Прибор для обнаружения ядра искусственно полученного трансуранового элемента – менделевия 101 Md
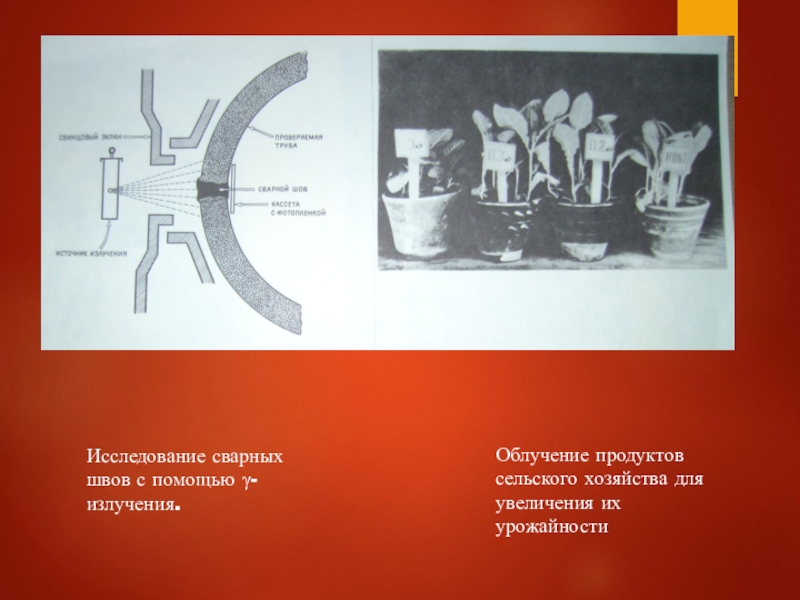
- 12. Исследование сварных швов с помощью γ-излучения. Облучение продуктов сельского хозяйства для увеличения их урожайности
- 13. Распределение в листьях помидора радиоактивного фосфора, внесенного в удобренияПерчаточный бокс для работы с радиоактивными веществами
- 14. Гамма-терапевтический аппарат.Исследование щитовидной железы с помощью радиоактивного йода
- 15. Скачать презентанцию
ОпределениеИзото́пы (от др.-греч. ισος — «равный», «одинаковый», и τόπος — «место») — разновидности атомов (и ядер) какого-либо химического элемента, которые имеют одинаковый атомный номер, но при этом разные массовые числа. Название связано с тем,
Слайды и текст этой презентации
Слайд 2Определение
Изото́пы (от др.-греч. ισος — «равный», «одинаковый», и τόπος — «место») — разновидности
Слайд 3Открытие изотопов
Первое доказательство того, что вещества, имеющие одинаковое химическое поведение,
могут иметь различные физические свойства, было получено при исследовании радиоактивных
превращений атомов тяжёлых элементов. В 1906—1907 годах выяснилось, что продукт радиоактивного распада урана — ионий и продукт радиоактивного распада тория — радиоторий имеют те же химические свойства, что и торий, но отличаются от него атомной массой и характеристиками радиоактивного распада. Было обнаружено позднее, что у всех трёх продуктов одинаковы оптические и рентгеновские спектры. Такие вещества, идентичные по химическим свойствам, но различные по массе атомов и некоторым физическим свойствам, по предложению английского учёного Содди с 1910 г. стали называть изотопами.Слайд 4Изотопы в природе
Считается, что изотопный состав большинства элементов на Земле
одинаков во всех материалах. Некоторые физические процессы в природе приводят
к нарушению изотопного состава элементов (природное фракционирование изотопов, характерное для лёгких элементов, а также изотопные сдвиги при распаде природных долгоживущих изотопов). Постепенное накопление в минералах ядер — продуктов распада некоторых долгоживущих нуклидов используется в ядерной геохронологии. Особое значение имеют процессы образования изотопов углерода в верхних слоях атмосферы под воздействием космического излучения. Эти изотопы распределяются в атмосфере и гидросфере планеты, вовлекаются в оборот углерода живыми существами (животными и растениями). Изучение распределения изотопов углерода лежит в основе радиоуглеродного анализа.Слайд 5Получение радиоактивных изотопов.
Получают радиоактивные изотопы в атомных реакторах и на
ускорителях элементарных частиц. В настоящее время производством изотопов занята большая
отрасль промышленности.Слайд 6Применение в биологии и медицине
Одним из наиболее выдающихся исследований,
проведенных с помощью меченых атомов, явилось исследование обмена веществ в
организмах. Было доказано, что за сравнительно небольшое время организм подвергается почти полному обновлению. Слагающие его атомы заменяются новыми.Лишь железо, как показали опыты по изотопному исследованию крови, является исключением из этого правила. Железо входит в состав гемоглобина красных кровяных шариков. При введении в пищу радиоактивных атомов железа было обнаружено, что они почти не поступают в кровь. Только в том случае, когда запасы железа в организме иссякают, железо начинает усваиваться организмом.
Если не существует достаточно долго живущих радиоактивных изотопов, как, например, у кислорода и азота, меняют изотопный состав стабильных элементов. Так, добавлением к кислороду избытка изотопа было установлено, что свободный кислород, выделяюнщйся при фотосинтезе, первоначально входил в состав воды, а не углекислого газа.
Слайд 7Применение в промышленности
Одним из примеров может служить способ контроля износа
поршневых колец в двигателях внутреннего сгорания. Облучая поршневое кольцо нейтронами,
вызывают в нем ядерные реакции и делают его радиоактивным. При работе двигателя частички материала кольца попадают в смазочное масло. Исследуя уровень радиоактивности масла после определенного времени работы двигателя, определяют износ кольца.Радиоактивные изотопы позволяют судить о диффузии металлов, процессах в доменных печах и т. д. Мощное -излучение радиоактивных препаратов используют для исследования внутренней структуры металлических отливок с целью обнаружения в них дефектов.
Слайд 8Изотопы в сельском хозяйстве
Все более широкое применение получают радиоактивные
изотопы в сельском хозяйстве. Облучение семян растений (хлопчатника, капусты, редиса
и др.) небольшими дозами -лучей от радиоактивных препаратов приводит к заметному повышению урожайности.Большие дозы радиации вызывают мутации у растений и микроорганизмов, что в отдельных случаях приводит к появлению мутантов с новыми ценными свойствами (радиоселекция). Так выведены ценные сорта пшеницы, фасоли и других культур, а также получены высокопродуктивные микроорганизмы, применяемые в производстве антибиотиков. Гамма-излучение радиоактивных изотопов используется также для борьбы с вредными насекомыми и для консервации пищевых продуктов.