Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Зависимость свойств химических элементов от положения в ПСХЭ
Содержание
- 1. Зависимость свойств химических элементов от положения в ПСХЭ
- 2. Слайд 2
- 3. Слайд 3
- 4. Апериодические закономерности изменения свойств атомов ХЭ от
- 5. Периодическая зависимость свойств атомов ХЭ от их
- 6. - радиус, - прочность связи внешних
- 7. 1. Радиус атома: - в группе сверху
- 8. 2. Прочность связи внешних электронов с ядром:
- 9. 3. Способность отдавать электроны (металлические свойства):в группе
- 10. 4. Способность принимать электроны (неметаллические свойства): в
- 11. Выбери из изученных свойств те, рост которых соответствует направлению стрелок (см. следующий слайд)
- 12. Слайд 12
- 13. Скачать презентанцию
Апериодические закономерности изменения свойств атомов ХЭ от их положения в ПСХЭ:Заряд ядра (в периоде↑ (растет) слева направо, в группе↑ сверху вниз) 2) Число е (в периоде↑ слева направо, в группе↑ сверху
Слайды и текст этой презентации
Слайд 1Зависимость свойств химических элементов от положения в ПСХЭ
(периодической системе химических
элементов)
Слайд 4Апериодические закономерности изменения свойств атомов ХЭ от их положения в
ПСХЭ:
Заряд ядра
(в периоде↑ (растет) слева направо, в группе↑ сверху
вниз) 2) Число е
(в периоде↑ слева направо, в группе↑ сверху вниз)
3) Число уровней
(в периоде не изменяется , в группе↑ )
4) Масса атома
(в периоде↑ слева направо, в группе↑)
Слайд 5Периодическая зависимость свойств атомов ХЭ от их положения в ПСХЭ:
Число
валентных электронов
(в периоде РАСТЁТ слева направо,
а в группе
не изменяется)Слайд 6- радиус, - прочность связи внешних электронов с ядром пропорциональна силе Это
основные свойства атома
при оценке химических свойств (металлических/неметаллических - для
ХЭ и простых веществ, образуемых ими; кислотно/основных – для некоторых соединений этих ХЭ)
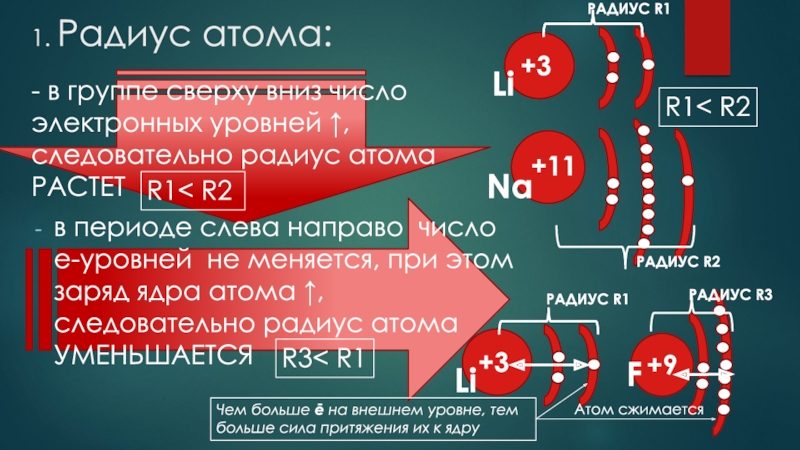
Слайд 71. Радиус атома:
- в группе сверху вниз число электронных
уровней ↑, следовательно радиус атома РАСТЕТ
в периоде слева направо число
е-уровней не меняется, при этом заряд ядра атома ↑, следовательно радиус атома УМЕНЬШАЕТСЯ +3
+9
+3
+11
РАДИУС R2
+3
РАДИУС R1
РАДИУС R1
РАДИУС R3
Li
Li
Na
F
Чем больше ē на внешнем уровне, тем больше сила притяжения их к ядру
Атом сжимается
R3< R1
R1< R2
R1< R2
Слайд 82. Прочность связи внешних электронов с ядром:
в группе сверху вниз
радиус атома ↑, следовательно прочность связи внешних е с ядром
УМЕНЬШАЕТСЯ;в периоде слева направо радиус ↓, при этом заряд ядра ↑, значит прочность связи внешних е с ядром РАСТЕТ.
Слайд 93. Способность отдавать электроны (металлические свойства):
в группе вниз – прочность
связи внешних е с ядром ↓, следовательно металлические свойства(способность отдавать
электроны) УСИЛИВАЮТСЯ;В периоде слева направо прочность внешних е с ядром ↑, следовательно металлические свойства ОСЛВБЕВАЮТ.