Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Альдегиды
Содержание
- 1. Альдегиды
- 2. Цели урока:Познакомиться с классом альдегидов, его свойствами. Выяснить области применения альдегидов.Развивать умственные способности студентов.
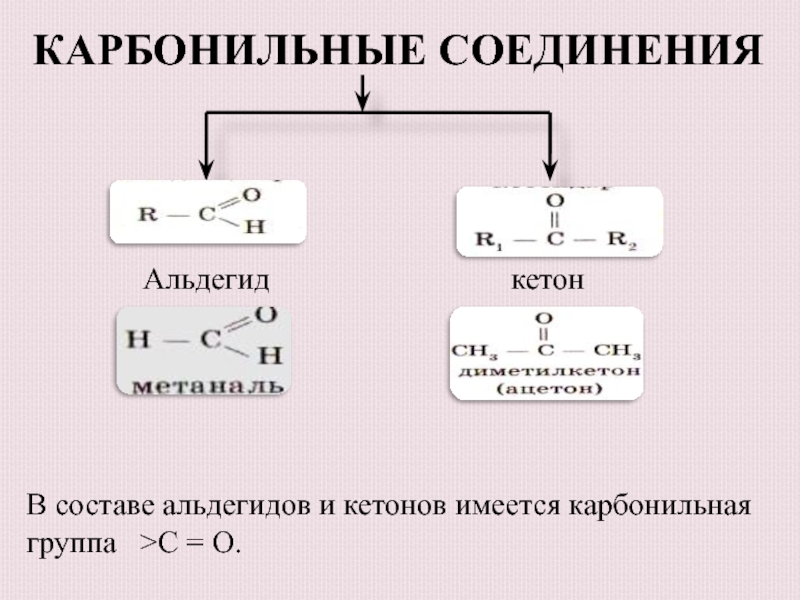
- 3. КАРБОНИЛЬные соединения
- 4. Альдегиды – это производные углеводородов, в молекулах
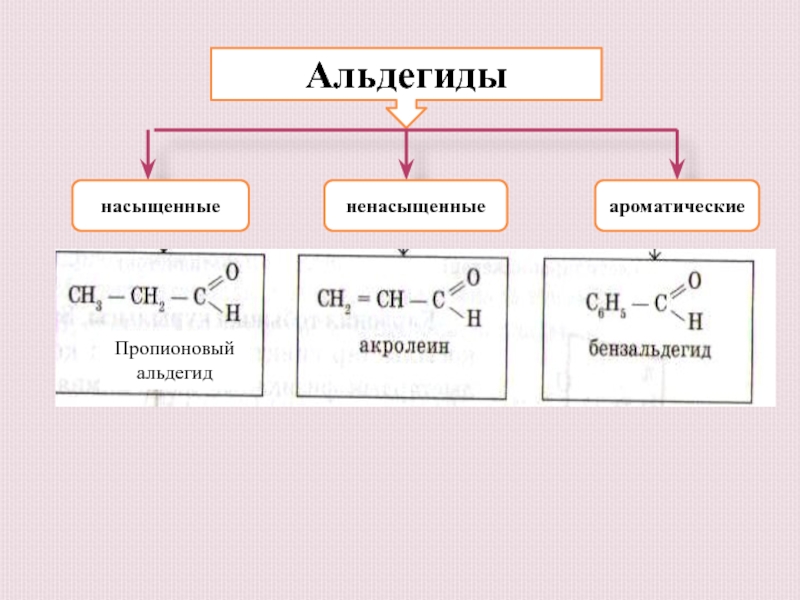
- 5. Альдегиды насыщенныененасыщенныеароматическиеПропионовый альдегид
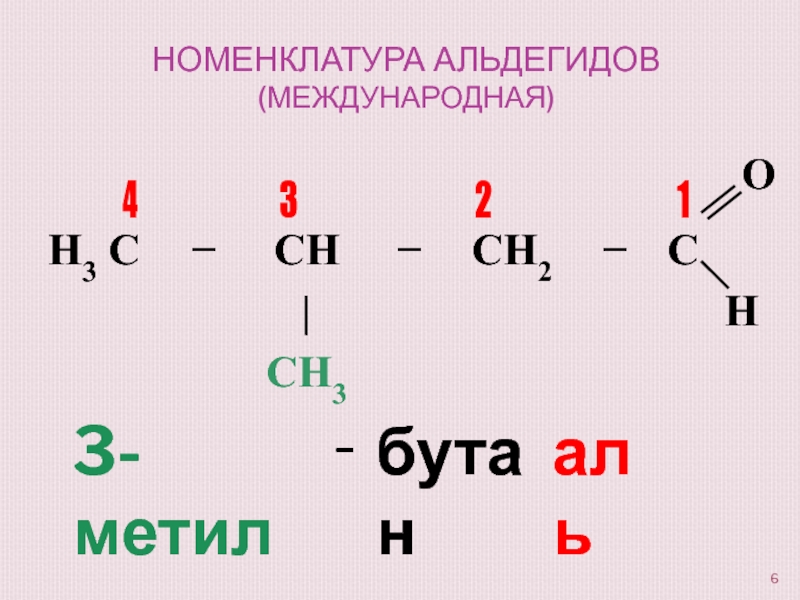
- 6. Номенклатура альдегидов (международная)14323-метил-бутаналь
- 7. Как составить формулу альдегида по названию?3-метил-пентанальС -
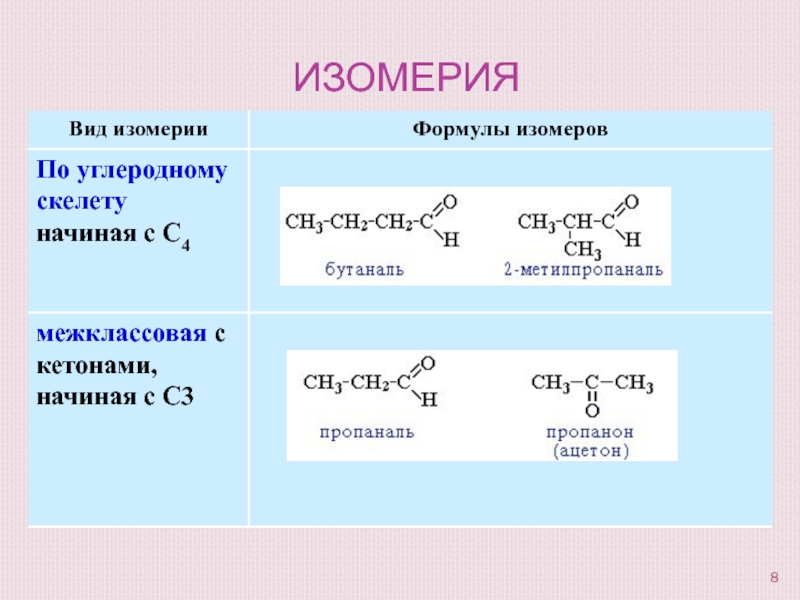
- 8. Изомерия
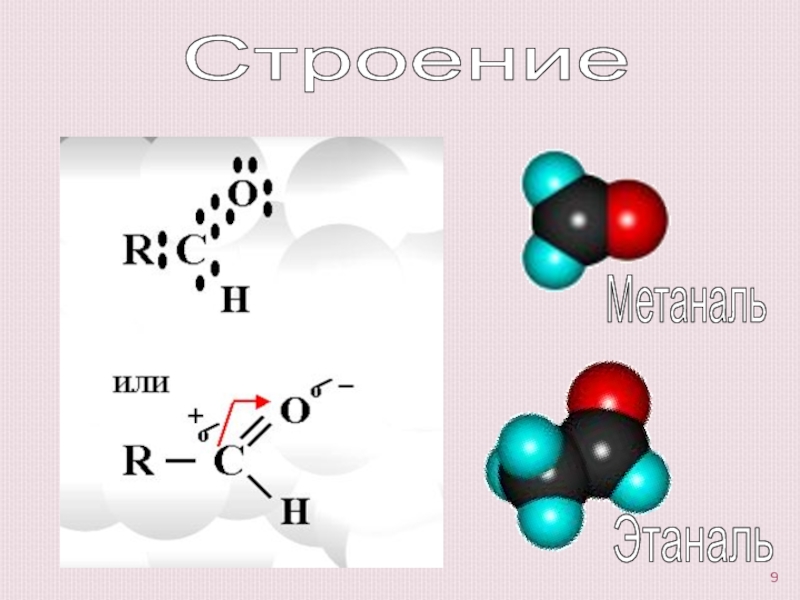
- 9. СтроениеЭтанальМетаналь
- 10. Атом углерода в карбонильной группы находится в
- 11. Способы получения альдегидов: 1.В промышленности альдегиды получают
- 12. Способы получения альдегидов: 2. При окислении первичных
- 13. Способы получения альдегидов: 3. Альдегиды получают по
- 14. Способы получения альдегидов: 4. Альдегиды можно получить гидролизом дигалогенопроизводных алканов:
- 15. ФИЗИЧЕСКИЕ СВОЙСТВА. Муравьиный альдегид – газ с
- 16. Химические свойства. Реакции присоединения.1. Присоединение водорода к
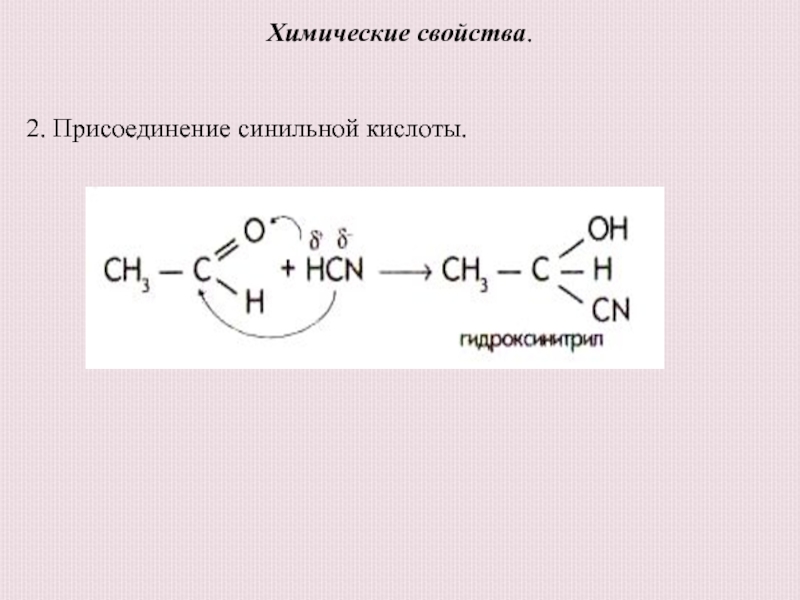
- 17. Химические свойства. 2. Присоединение синильной кислоты.
- 18. Химические свойства. 3. Реакции окисления. При окислении
- 19. Химические свойства. 4. Качественной реакцией на определение
- 20. Химические свойства. Реакция замещения 5. Галоген замещает атом водорода в радикале углеводорода:
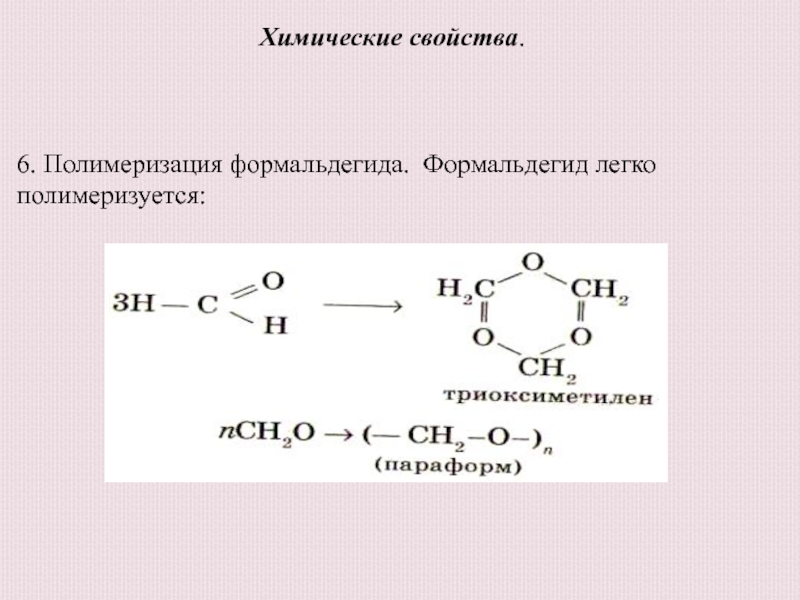
- 21. Химические свойства. 6. Полимеризация формальдегида. Формальдегид легко полимеризуется:
- 22. Химические свойства. 7. Реакция поликонденсации (взаимодействие формальдегида
- 23. Химические свойства. Уравнение можно представить в следующим
- 24. Фенолформальдегид-ные смолыУксусная кислотаЭтилацетатФормалин Применение альдегидовПарфюмерияПолимерные материалыПроизводство веществЗагрязнители
- 25. Широко применяется 40%-ный водный раствор формальдегида —
- 26. Закрепление материалаНапишите уравнение реакций позволяющих осуществить следующие
- 27. Закрепление материалаСоставьте формулы альдегидов:3 – этилгексаналь3, 3
- 28. Скачать презентанцию
Цели урока:Познакомиться с классом альдегидов, его свойствами. Выяснить области применения альдегидов.Развивать умственные способности студентов.
Слайды и текст этой презентации
Слайд 2
Цели урока:
Познакомиться с классом альдегидов, его свойствами.
Выяснить области применения
альдегидов.
Слайд 3КАРБОНИЛЬные соединения
Альдегид
кетонВ составе альдегидов и кетонов имеется карбонильная группа >С = О.
Слайд 4
Альдегиды – это производные углеводородов, в молекулах которых атом водорода
замещен альдегидной группой
Общая формула альдегидов
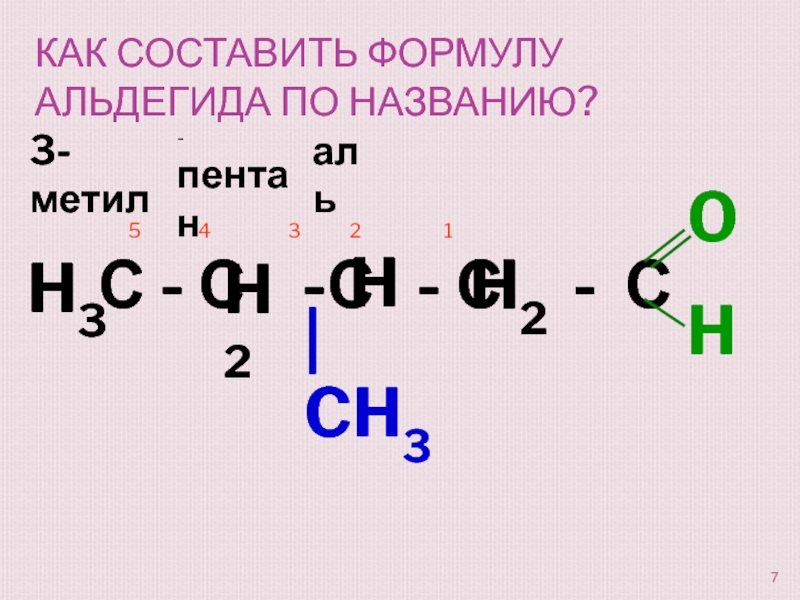
Слайд 7Как составить формулу альдегида по названию?
3-метил
-пентан
аль
С - С -С
- С - С
5
4 3 2 1O
H
|
CH3
H3
H2
H
H2
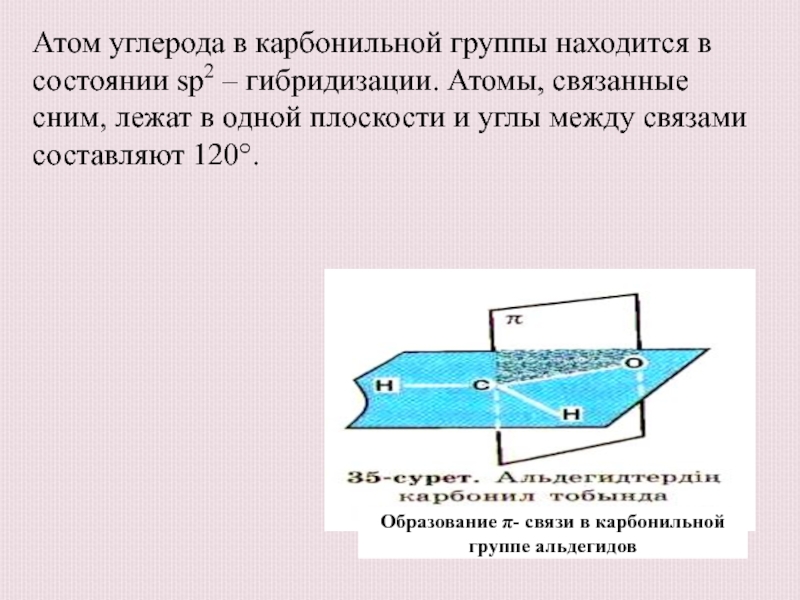
Слайд 10Атом углерода в карбонильной группы находится в состоянии sp2 –
гибридизации. Атомы, связанные сним, лежат в одной плоскости и углы
между связами составляют 120°.Образование π- связи в карбонильной группе альдегидов
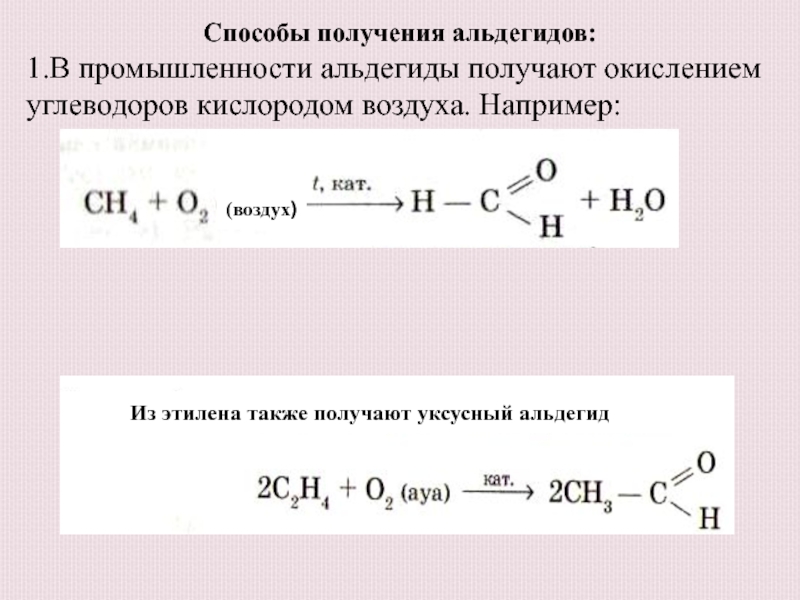
Слайд 11Способы получения альдегидов:
1.В промышленности альдегиды получают окислением углеводоров кислородом
воздуха. Например:
(воздух)
Из этилена также получают уксусный альдегид
Слайд 12Способы получения альдегидов:
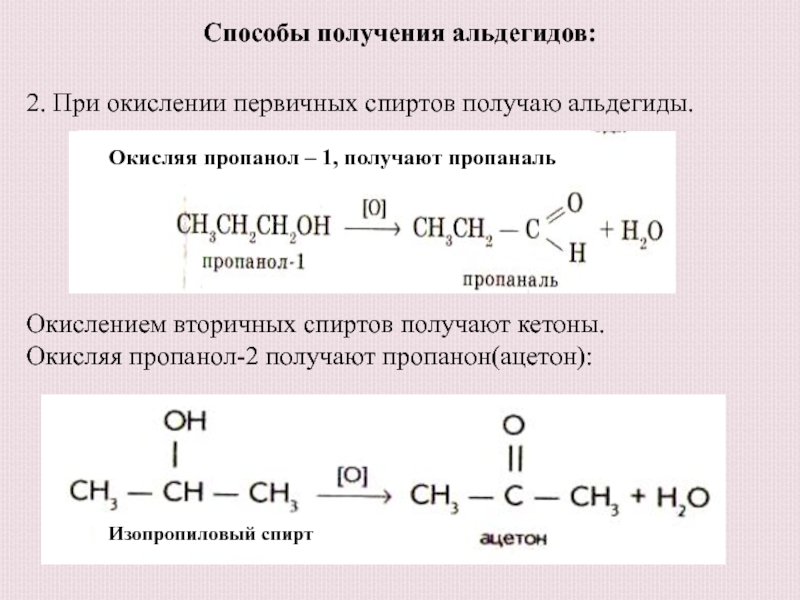
2. При окислении первичных спиртов получаю альдегиды.
Окислением
вторичных спиртов получают кетоны.
Окисляя пропанол-2 получают пропанон(ацетон):
Окисляя пропанол – 1,
получают пропаналь:Изопропиловый спирт
Слайд 13Способы получения альдегидов:
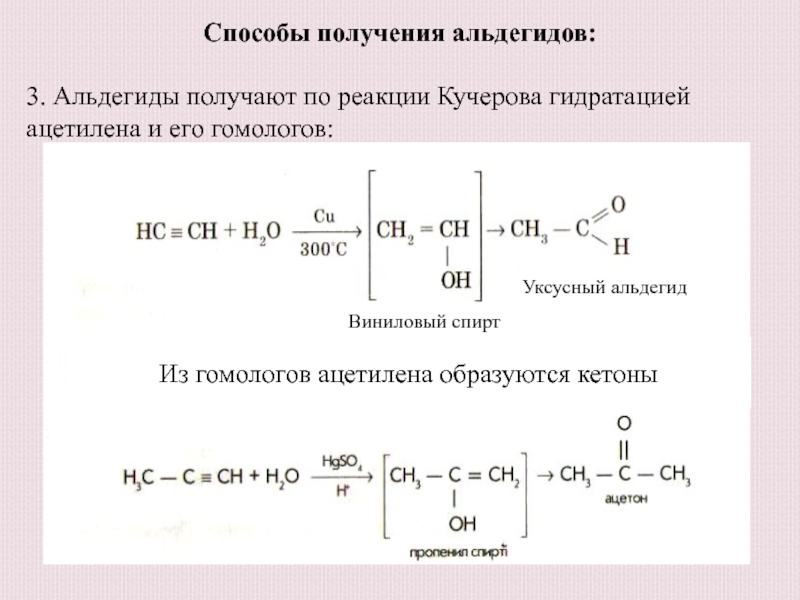
3. Альдегиды получают по реакции Кучерова гидратацией
ацетилена и его гомологов:
Виниловый спирт
Уксусный альдегид
Из гомологов ацетилена образуются кетоны
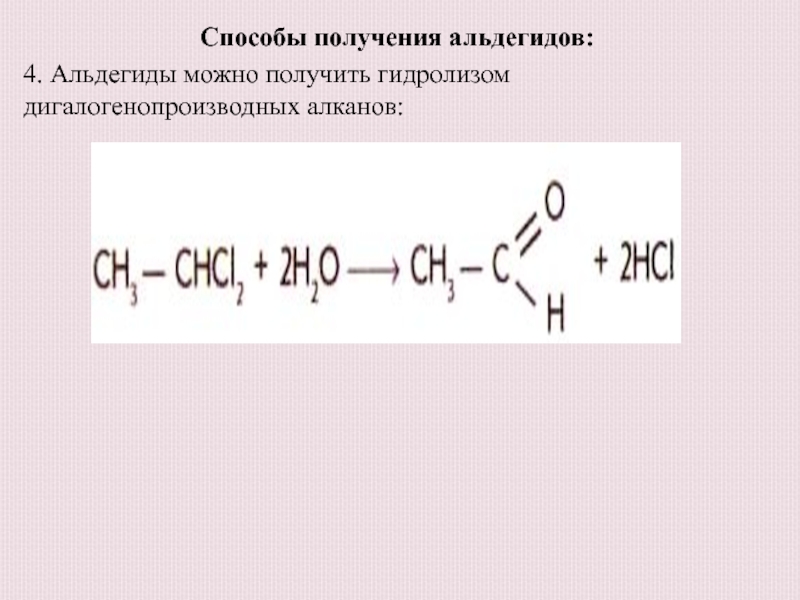
Слайд 14Способы получения альдегидов:
4. Альдегиды можно получить гидролизом дигалогенопроизводных алканов:
Слайд 15
ФИЗИЧЕСКИЕ СВОЙСТВА.
Муравьиный альдегид – газ с резким удушливливым запахом.
Начиная с уксусного альдегида и следующие представители – жидкости, высшие
члены гомологического ряда – твердые вещества. Первые представители гомологического ряда хорошо растворяются в воде. Все альдегиды хорошо растворяются в органических растворителях.Слайд 16Химические свойства.
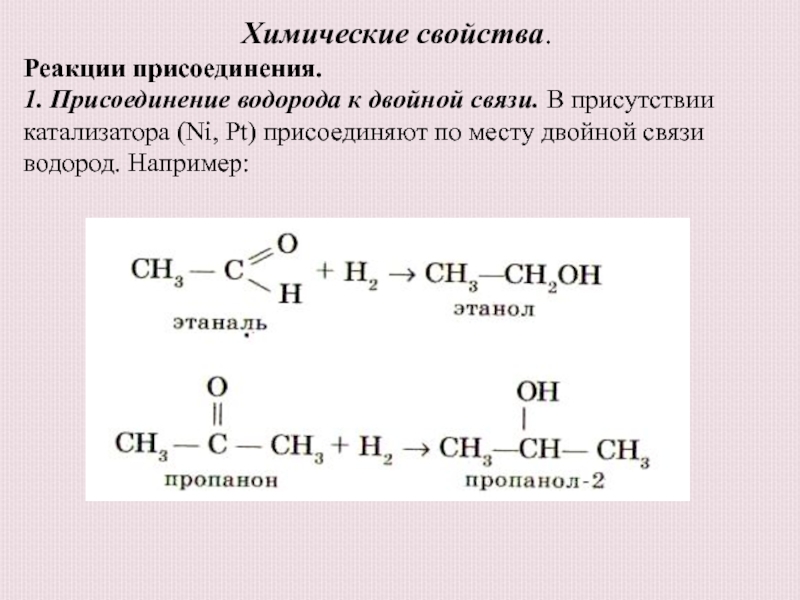
Реакции присоединения.
1. Присоединение водорода к двойной связи. В
присутствии катализатора (Ni, Pt) присоединяют по месту двойной связи водород.
Например:Слайд 18Химические свойства.
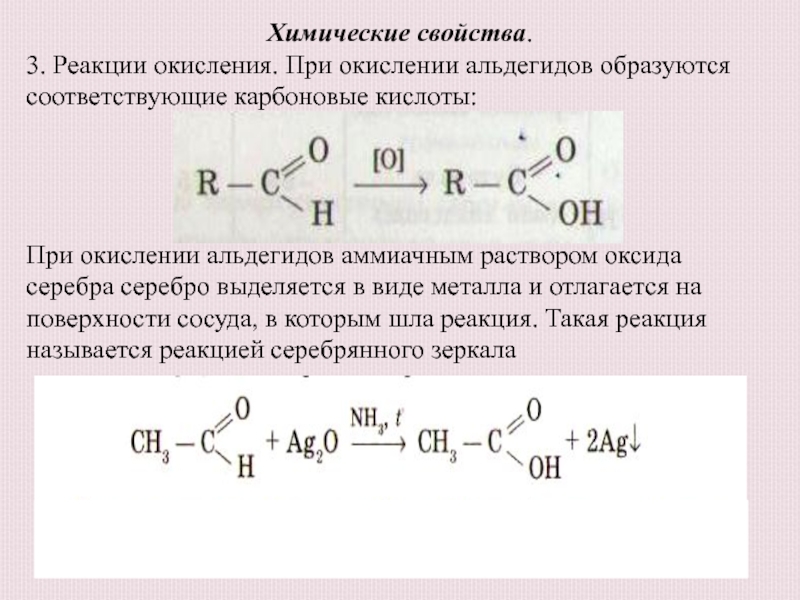
3. Реакции окисления. При окислении альдегидов образуются соответствующие
карбоновые кислоты:
При окислении альдегидов аммиачным раствором оксида серебра серебро выделяется
в виде металла и отлагается на поверхности сосуда, в которым шла реакция. Такая реакция называется реакцией серебрянного зеркалаСлайд 19
Химические свойства.
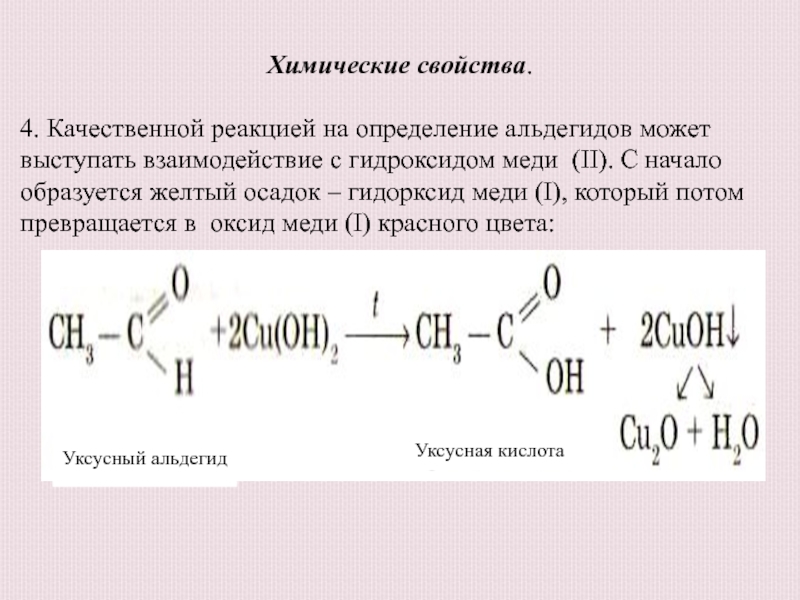
4. Качественной реакцией на определение альдегидов может выступать
взаимодействие с гидроксидом меди (ІІ). С начало образуется желтый осадок
– гидорксид меди (І), который потом превращается в оксид меди (І) красного цвета:Уксусный альдегид
Уксусная кислота
Слайд 20Химические свойства.
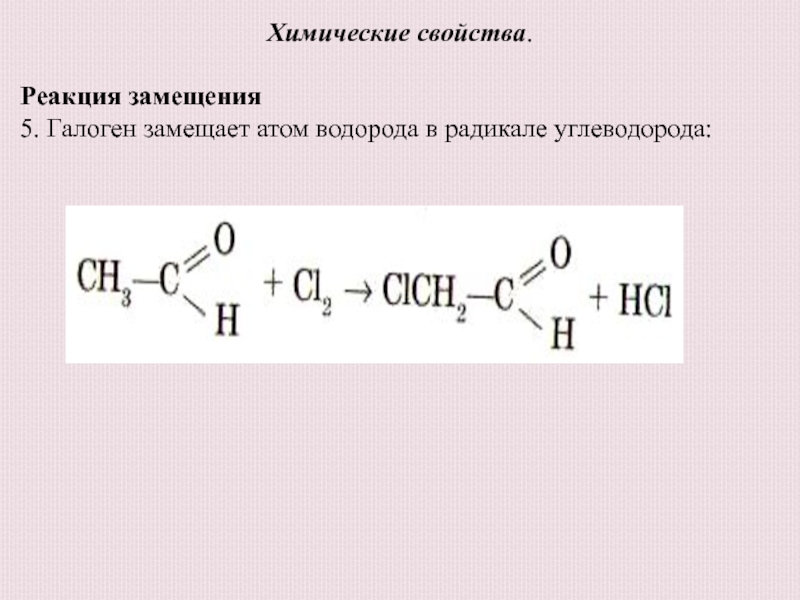
Реакция замещения
5. Галоген замещает атом водорода в
радикале углеводорода:
Слайд 22
Химические свойства.
7. Реакция поликонденсации (взаимодействие формальдегида с фенолом). Формальдегид,
легко взаимодействуя с фенолом, образует высокомолекулярные соединения – фенолформальдегидные смолы.
Если в результате реакции наряду с полимером образуется низкомолекулярное соединение, то такая реакция называется реакцией поликонденсацией.
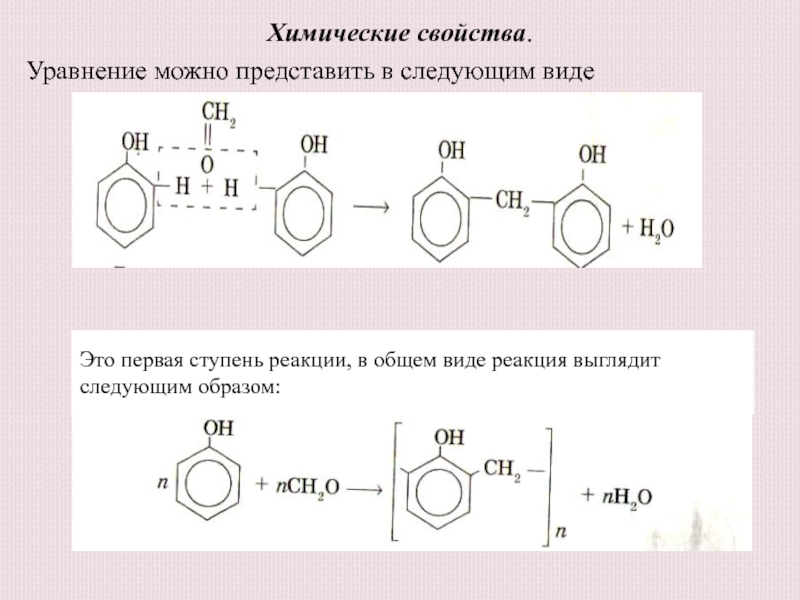
Слайд 23Химические свойства.
Уравнение можно представить в следующим виде
Это первая
ступень реакции, в общем виде реакция выглядит следующим образом:
Слайд 24Фенолформальдегид-ные смолы
Уксусная кислота
Этилацетат
Формалин
Применение альдегидов
Парфюмерия
Полимерные материалы
Производство веществ
Загрязнители атмосферы
Альдегид анисовый, обепин
– жидкость с приятным запахом мимозы
Альдегид дециловый, деканаль – при
разбавлении появляются нотки запаха апельсиновой коркиСлайд 25Широко применяется 40%-ный водный раствор формальдегида — формалин. Его использование
связано со способностью свертывать белок. Так, например, в кожевенном производстве
в результате дубильного действия формалина кожа твердеет и не подвергается гниению. На том же свойстве основано применение формалина для хранения биологических препаратов. Формалин используется для дезинфекции и протравливания семян.Слайд 26Закрепление материала
Напишите уравнение реакций позволяющих осуществить следующие превращения:
ацетилен →
ацетальдегид → этанол → этилен → ацетилен.
Слайд 27Закрепление материала
Составьте формулы альдегидов:
3 – этилгексаналь
3, 3 – диметилбутаналь
2,4,5 –
трихлоргексаналь
2, 5 – диметил 4 – этилоктаналь
3 – этилгексаналь
3, 3
– диметилбутаналь2,4,5 – трихлоргексаналь
2, 5 – диметил 4 – этилоктаналь