Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Урок химии 10 класс "Кислородсодержащие органические соединения"
Содержание
- 1. Урок химии 10 класс "Кислородсодержащие органические соединения"
- 2. О чем поговорим сегодня?Тема: Кислородсодержащие органические соединения
- 3. Какое слово здесь зашифровано? Кислота
- 4. Что мы можем узнать с вами сегодня? Чему научиться?Карбоновые кислоты
- 5. В каком порядке мы будем изучать тему?Свойства
- 6. Карбоновые кислоты – это производные УВ, содержащие
- 7. Общая формула карбоновых кислот :
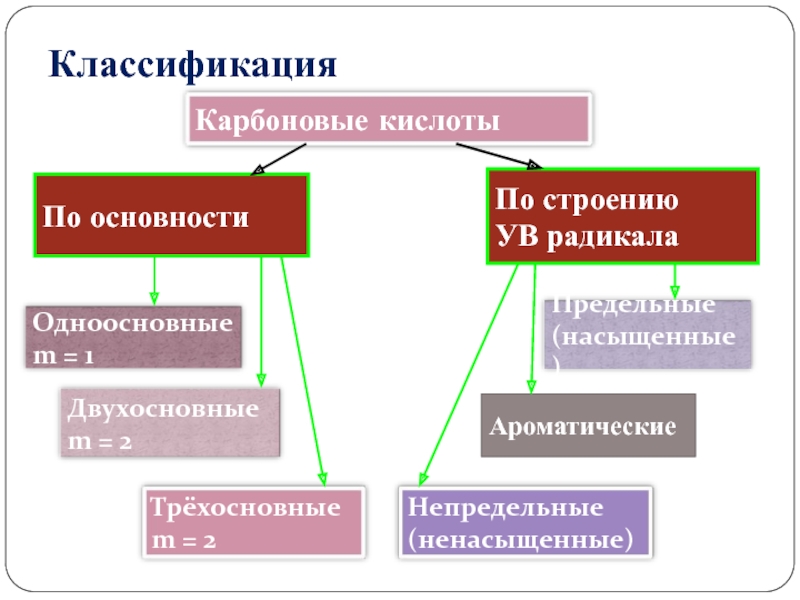
- 8. По основности По строению УВ радикалаАроматическиеКлассификация
- 9. Некоторые представители карбоновых кислот
- 10. Номенклатура и изомерияПо международной заместительной номенклатуре название
- 11. Свойства карбоновых кислот1. Карбоновые кислоты диссоциируют в
- 12. 2. Карбоновые кислоты реагируют с активными металлами
- 13. 3. Кислоты реагируют с основными оксидами:
- 14. 4. Кислоты реагируют с основаниями:
- 15. 5. Кислоты реагируют с аммиаком на холоду
- 16. 6. Карбоновые кислоты реагируют с солями более слабых и летучих кислот:
- 17. 7. Кислоты RCOOH реагируют со спиртами R'OH
- 18. 8. Кислоты реагируют с хлоридами фосфора РСl3,
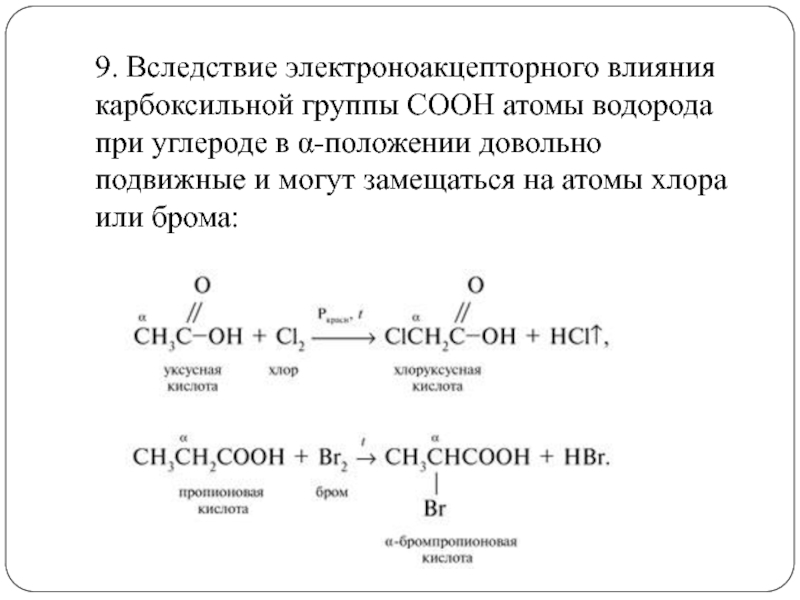
- 19. 9. Вследствие электроноакцепторного влияния карбоксильной группы СООН
- 20. Слайд 20
- 21. Муравьиная кислота НСООН по химическим свойствам несколько
- 22. Из-за наличия в молекуле Н–СООН альдегидного протона
- 23. О чем мы планировали узнать? А что
- 24. Среди карбоновых кислот Известных "лиц" невпроворот. В кислотах - группы карбоксильные, Но все кислоты здесь - несильные.
- 25. Спасибо всемКто сегодня работал!
- 26. Скачать презентанцию
О чем поговорим сегодня?Тема: Кислородсодержащие органические соединения
Слайды и текст этой презентации
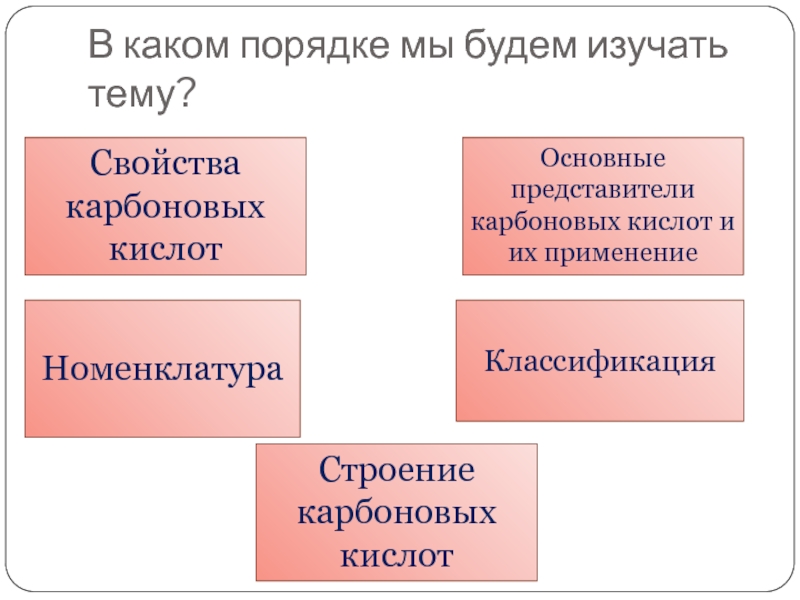
Слайд 5В каком порядке мы будем изучать тему?
Свойства карбоновых кислот
Основные представители
карбоновых кислот и их применение
Номенклатура
Классификация
Строение карбоновых кислот
Слайд 6Карбоновые кислоты – это производные УВ, содержащие функциональную карбоксильную группу
-СООН
или
Карбоновые кислоты – это органические вещества, молекулы которых содержат одну или несколько карбоксильных групп, соединённых с УВ радикалом или водородным атомом.
Слайд 7Общая формула карбоновых кислот :
∕∕ О
R (-C − ОН )m,
где m – число карбоксильных групп, определяющее основность кислоты
Слайд 10Номенклатура и изомерия
По международной заместительной номенклатуре название кислоты производят от
названия соответствующего (с тем же числом атомов углерода) углеводорода с
добавлением окончания -овая и слова кислота.Нумерацию цепи всегда начинают с атома углерода карбоксильной группы, поэтому в названиях положение группы -СООН не указывают.
Например:
5 4 3 2 1 О
СН3-СН2-СН-СН2-С 3-метилпентановая кислота
СН3 ОН
Слайд 11Свойства карбоновых кислот
1. Карбоновые кислоты диссоциируют в водном растворе с
отщеплением протонов Н+, обусловливающих кислую среду раствора
Водные растворы карбоновых кислот
изменяют окраску индикаторов и являются электролитами. По сравнению с сильными минеральными кислотами (H2SO4, HNO3, HCl) – это слабые кислоты.Слайд 122. Карбоновые кислоты реагируют с активными металлами (примерно от Li
до Fe в ряду напряжений металлов), выделяя водород:
Слайд 155. Кислоты реагируют с аммиаком на холоду с образованием солей
аммония:
Соли аммония карбоновых кислот термически неустойчивые соединения, при нагревании они
отщепляют воду и превращаются в амиды кислот:При нагревании амидов с водоотнимающими средствами (например, с пентаоксидом фосфора Р2О5) образуются нитрилы карбоновых кислот:
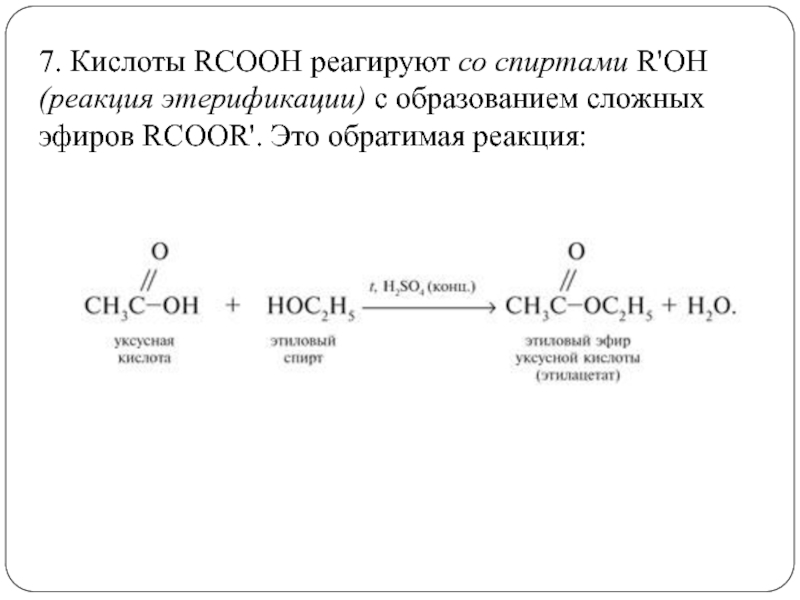
Слайд 177. Кислоты RCOOH реагируют со спиртами R'OH (реакция этерификации) с
образованием сложных эфиров RCOOR'. Это обратимая реакция:
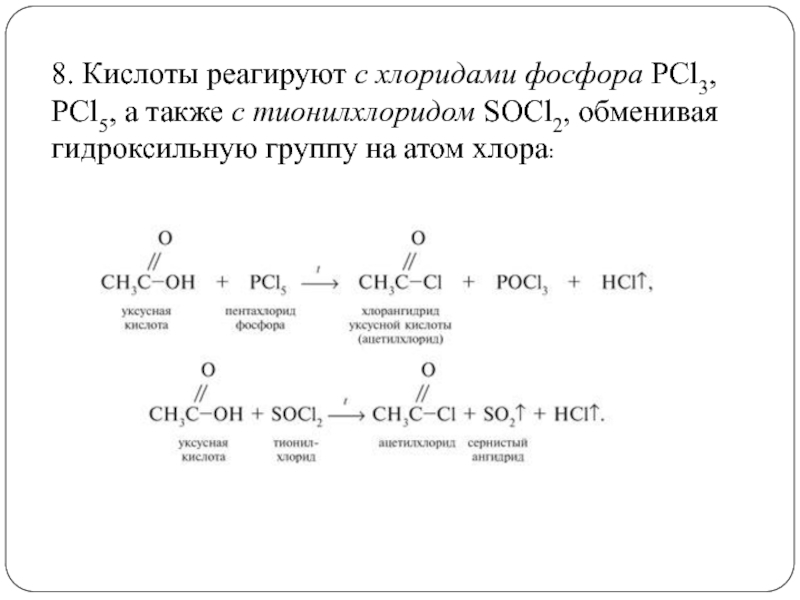
Слайд 188. Кислоты реагируют с хлоридами фосфора РСl3, РСl5, а также
с тионилхлоридом SOCl2, обменивая гидроксильную группу на атом хлора:
Слайд 199. Вследствие электроноакцепторного влияния карбоксильной группы СООН атомы водорода при
углероде в α-положении довольно подвижные и могут замещаться на атомы
хлора или брома:Слайд 21Муравьиная кислота НСООН по химическим свойствам несколько отличается от других
карбоновых кислот. Так, для нее неизвестны хлорангидрид и ангидрид. В
присутствии водоотнимающих средств (PCl5, SOCl2, H2SO4 (конц.)) муравьиная кислота отщепляет воду с выделением оксида углерода(II):Слайд 22Из-за наличия в молекуле Н–СООН альдегидного протона муравьиная кислота легко
окисляется, в частности дает реакцию «серебряного зеркала»:
Слайд 23О чем мы планировали узнать?
А что узнали?
Сенквейн на тему урока
1
строка- одно слово- название стихотворения, тема, обычно существительное;
2 строка- два прилагательных,
раскрывающих тему синквейна;3 строка- три глагола, описывающих действия по теме синквейна;
4 строка- фраза, предложение, цитата или крылатое выражение, выражающее свое отношение к теме;
5 строка- слово-резюме, дающее новую интерпретацию темы.