Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Алкандарды? ??рылысы
Содержание
- 1. Алкандарды? ??рылысы
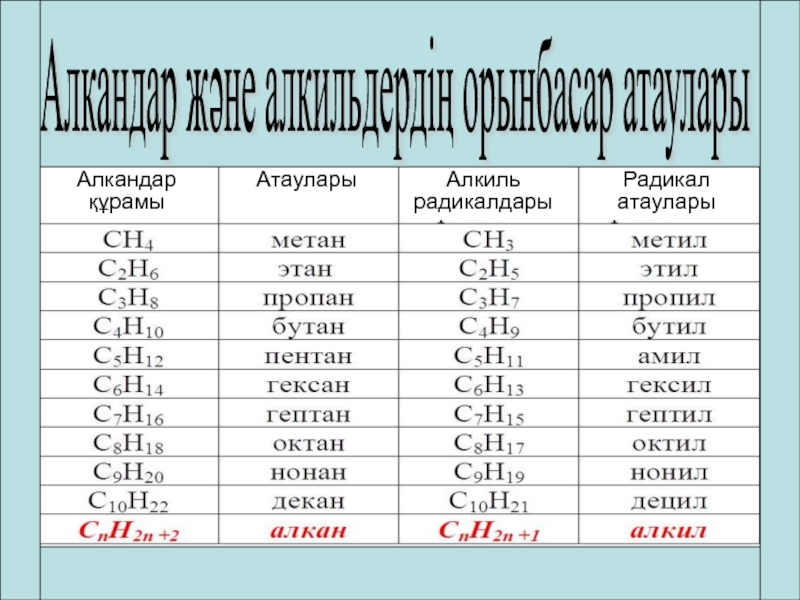
- 2. Алкандар құрамыАтауларыАлкиль радикалдарыРадикал атаулары Алкандар және алкильдердің орынбасар атаулары
- 3. Метан (лат. Methanum) - Газ түріндегі көмірсутек СН4, метанды немесе парафинді көмірсутектері тізбегінің алғашқы мүшесі.
- 4. 1. Алкандарды лабораторияда қанықпаған көмірсутектерді Ni, Pt,
- 5. 3. Алкандарды көмірді гидрлеп алуға да болады.
- 6. Алкендер — молекула құрамында бір қос байланысы
- 7. Алкендер химиялық белсенді болғандықтан табиғатта өте сирек
- 8. 1. Гидрленуі (сутектің қосылуы). Алкендер сутекті қосып
- 9. 3. Галогенсутпектперді қосу. Алкендерге галогенсутектердің қосылуы оңай
- 10. 4. Гидраттану. Алкендер қос байланыс бойынша су
- 11. 7. Қатаң жағдайларда тотықтырғанда (күкірт қышқылы, перманганат
- 12. Назарларыңызға рахмет!
- 13. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Алкандар — молекула құрамындағы көміртек атомдары өзара тек дара σ-байланыстар
арқылы байланысқан жалпы формуласы CnH2n+2 болатын алифатты қаныққан көмірсутектер.
қарапайым алкан — метанның құырылымыСлайд 2Алкандар құрамы
Атаулары
Алкиль радикалдары
Радикал атаулары
Алкандар және алкильдердің орынбасар
атаулары
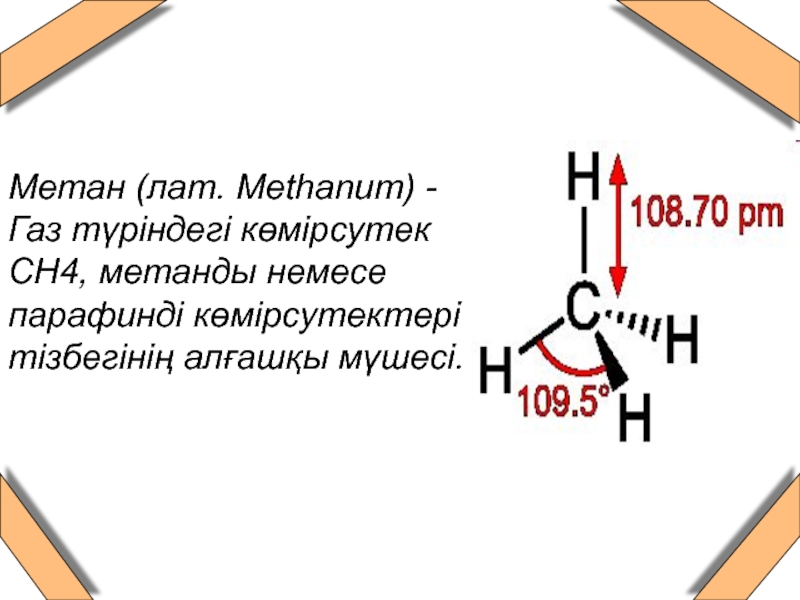
Слайд 3 Метан (лат. Methanum) - Газ түріндегі көмірсутек СН4, метанды немесе
парафинді көмірсутектері тізбегінің алғашқы мүшесі.
Слайд 41. Алкандарды лабораторияда қанықпаған көмірсутектерді Ni, Pt, Pd өршіткілері қатысында
гидрлеп алады: H2C = CH2 + H2 → H3C - CH3 2.
Вюрц реакциясы бойынша, алкандардың галогентуындыларына металл натриймен әсер етіп алады: 2СН3СІ + 2Na → С2Н6 + 2NaCI Егер Вюрц реакциясын әр түрлі алкандардың галогентуындыларының қатысында жүргізсе, алкандардың қоспасы түзіледі. Мысалы, йодметан мен йодэтанның қатысуында Вюрц реакциясы нәтижесінде этан, пропан және бутанның қоспасы түзілуі мүмкін: 2СН3І + 2Na → СН3 - СН3 + 2Nal СН3І + 2Nа + С2H5I → CH3 - С2Н5 + 2Nal 2С2Н5I + 2Na → С2Н5 — С2Н5 + 2Nal
Алкандарды синтездеп алудың бірнеше жолдары бар.
Слайд 53. Алкандарды көмірді гидрлеп алуға да болады. Жай заттардан алкандарды
синтездеу реакциясының теориялық тұрғыдан маңызы зор. Бұл реакция жай заттардың
(бейорганикалық) органикалық қосылыстарға өту мүмкіндігін көрсетеді. Реакция 500°С температура шамасында, өршіткі (темір оксидтері) қатысында жүреді: nC+(n+1)H2 → CnH2n+2 Немесе метанды синтездеу реакциясы Ni катализаторы қатысында жүреді: С + 2Н2 → СН4 + 75 кДж 4. Алкандарды синтездеу мақсатында катализатор қатысында (Co, Ni) көміртек (II) оксиді мен сутектің қоспасын (синтез-газды) да пайдаланады: nCO +(2n+1) H2 → CnH2n+2 + nH2O 5. Метанды лабораторияда натрий ацетаты (сірке қышқылының тұзы) мен натрий гидроксидін балқытып алады: CH3COONa + NaOH → CH4 + Na2CO3
Слайд 6Алкендер — молекула құрамында бір қос байланысы бар, жалпы формуласы
СnН2n болатын қанықпаған көмірсутектер. Алкендердің ең қарапайым өкілі — құрамында екі
көміртек атомы бар — этилен С2Н4Алкендер
Этилен, Этен, CH2=CH2 – органикалық қосылыс. Э. эфир иісті, түссіз газ, балқу t –169,5 °С, қайнау t –103,8 °С, суда нашар, эфирде жақсы ериді.
Слайд 7Алкендер химиялық белсенді болғандықтан табиғатта өте сирек кездеседі. Алкендердің газ
тәрізді мүшелерін мұнайға серік газдардан немесе мұнай өңдегенде және көмірді
кокстегенде бөлінетін газдардан алады. Алкендерді алкандардан және олардың туындыларынан да өндіреді. 1. Алкандарды крекингілеу. Өнеркәсіпте алкандарды 700°С-қа дейін қыздырғанда, алкендер түзіледі: С8Н18 → С4Н10 + С4Н8 2. Алкандарды дегидрлеу. Өнеркәсіпте алкендерді жоғары температурада сутек бөле отырып, сәйкес алкандарды айырып алады. Мысалы, этаннан этилен алуды қарастырайық: H3C — СН3 → CH2 = CH2 + H2 Сутек бөліне журетін айырылу реакциялары дегидрлену деп аталады. Лабораторияда алкендерді бірнеше жолмен алуға болады: 3. Спирттерді дегидраттау. Өршіткі ретінде концентрлі күкірт қышқылы, фосфор қышқылы, алюминий оксиді сияқты су сорғыш заттар қолданылады. Су бөліне жүретін айырылу реакциялары дегидратациялану деп аталады. 4. Галогеналкандарды дегидрогалогендеу. Галогеналкандарға сілтілердің спирттегі ерітінділерімен әсер еткенде алкен түзіліп, галогенсутектер бөлінеді.
Слайд 81. Гидрленуі (сутектің қосылуы). Алкендер сутекті қосып алып, сәйкес алкандарға
айналады. Реакция металл катализаторлар Ni, Pt, Pd қатысында жүреді. Мысалы,
пропенге сутек косылғанда, пропан түзіледі: CH3—CH = CH2 + H — H → CH3 — CH2 — CH3 Немесе осы реакцияны ықшамдап жазсақ: C3H6 + H2 → C3H8 Сутек қосыла журетін реакцияларды гидрлену реакциясы деп атайды.
2. Галогенденуі (галогендердің қосылуы). Алкендер галогендермен әрекеттескенде, реакция қос байланыс бойынша жүріп, нәтижесінде, алкандардың дигалогентуындылары түзіледі. Реакция алкенді галогеннің ерітіндісімен кәдімгі температурада әрекеттестіргенде жүреді. Алкендерді бромды сумен (бромның судағы ерітіндісі) әрекеттестіргенде, ерітіндідегі бромның қызыл қоңыр түсі жойылып, түссіз дибромалкандар (СnН2nВг2) түзіледі:
Н2С = СН2 + Вг2 → ВгН2С - СН2Вr
Қосылу реакциялары
Қанықпаған көмірсутектерге қосылу реакциялары тән. Еселі — қанықпаған (қос) байланысы бойынша алкендер қосылу реакцияларына жеңіл түседі.
Слайд 93. Галогенсутпектперді қосу. Алкендерге галогенсутектердің қосылуы оңай жүріп, нәтижесінде, галогеналкандар
түзіледі: H2C = CH2 + Н - Сl → H3C -
СН2Сl Қосылу реакцияларының жылдамдығы, галогенсутек қышқылының күші өсуіне байланысты артады: HF < HCl < НВг < HI Галогенсутектердің симметриялы емес алкендерге қосылу реакциялары В. В. Марковников ережесі бойынша жүреді. Галогенсутектің сутек атомы сутек көп көміртек атомына, ал галоген сутек аз көміртпек атомына қосылады: H2С = СН3 - СН + Н - Вг → Н3C - СНВг - CH3 sp2-гибридтенген көміртек атомының электртерістігі sp3- гибридтенген көміртек атомына қарағанда жоғары. Сондықтан пропен молекуласындағы дара байланыстың электрон тығыздығы ортаңгы sp2-гибридтенген көміртек атомына қарай ығысады. Соның әсерінен қозғалғыш π-байланыстың электрондары шеткі көміртек атомына қарай ауысады, яғни [δ2-] < [δ1-] Галогенсутек молекуласы полюсті Нδ+ — Xδ- болатынын білесіңдер. Теріс заряды көбірек көміртек атомына реагенттің оң зарядты бөлігі (галогенсутектегі сутек атомы) келіп қосылады. Ал қалған бөлігі қос байланыс жанындағы екінші көміртек атомына қосылады.
Слайд 104. Гидраттану. Алкендер қос байланыс бойынша су молекуласын қосып алып,
сәйкес спирттер түзеді: H2C=CH2 + H - OH —>H3C - CH2OH Бұл
реакцияның өнеркәсіптік маңызы зор. Пропен молекуласына судың қосылуы Марковников ережесі бойынша жүріп, пропанол-1 емес, пропанол-2 түзіледі: СH3—СH =CH2 + H - OH —> H3C - CHOH-CH3 5. Этиленді полимерлеп, полиэтилен алады. Тотығу реакциялары. Алкендер алкандармен салыстырғанда оңай тотығады. 6. Алкендердің қалыпты жағдайда тотығуы. Этиленді калий перманганатының ерітіндісі арқылы өткізсе, оның күлгін түсі жойылып кетеді. Бұл перманганаттың этиленді тотықтыратындығын көрсетеді. Реакция нәтижесінде екіатомды спирт — этиленгликоль түзіледі.
Слайд 117. Қатаң жағдайларда тотықтырғанда (күкірт қышқылы, перманганат немесе хром қоспасы
катысында) алкен молекуласының қос байланысы үзіліп, оттекті органикалық қосылыстар түзіледі: HC3
- CH=CH - CH3 + /O/ → 2CH3 - COOH 8. Алкендердің жануы. Сапалық құрамы алкандардай — көміртек пен сутектен тұратын болғандықтан, алкендер де жанады. Бірақ алкендер алкандарға қарағанда шала жануға (CO немесе күйе түзе) бейім болады. Оттек жеткілікті болғанда, алкендердің толық жануы нәтижесінде су мен көміртек (IV) оксиді түзіледі. Мысалы, этилен ауада жаркырап, жылу бөле жанады: С2Н4 + 3О2 <->2СО2 + 2Н2О + Q