Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Амины
Содержание
- 1. Амины
- 2. Ами́ны — органические соединения, являющиеся производными аммиака,
- 3. По числу замещённых атомов водорода различают соответственно
- 4. Номенклатура К названию органических остатков, связанных с
- 5. Химические свойства Амины, являясь производными аммиака,
- 6. Алкиламины являются сильными основаниями, ариламины
- 7. -Первичные и вторичные амины взаимодействуют с азотистой
- 8. -конденсация первичных аминов с альдегидами и кетонами
- 9. Получение -Восстановлением азотсодержащих соединений: нитросоединений (реакция
- 10. Вредное воздействие Амины являются очень токсичными
- 11. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Ами́ны — органические соединения, являющиеся производными аммиака, в молекуле которого
один, два или три атома водорода замещены на углеводородные радикалы.
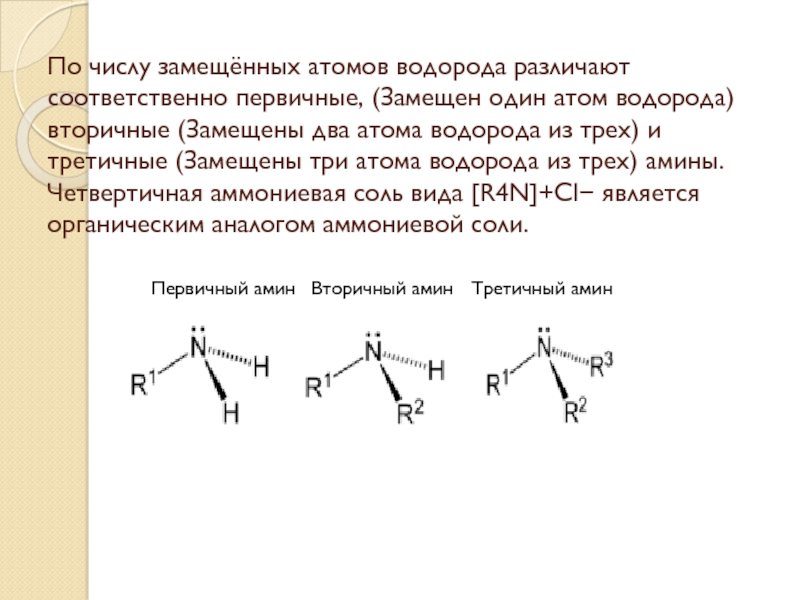
Слайд 3По числу замещённых атомов водорода различают соответственно первичные, (Замещен один
атом водорода) вторичные (Замещены два атома водорода из трех) и
третичные (Замещены три атома водорода из трех) амины. Четвертичная аммониевая соль вида [R4N]+Cl− является органическим аналогом аммониевой соли.Первичный амин Вторичный амин Третичный амин
Слайд 4Номенклатура К названию органических остатков, связанных с азотом, добавляют слово «амин»,
при этом группы упоминают в алфавитном порядке: CH3NHC3Н7 — метилпропиламин,
CH3N(С6Н5)2 — метилдифениламин. Для высших аминов название составляется, взяв за основу углеводород, прибавлением приставки «амино», «диамино», «триамино», указывая числовой индекс атома углерода:2-аминопентан
Для некоторых аминов используются тривиальные названия: С6Н5NH2 — анилин (систематическое название — фениламин).
Слайд 5Химические свойства Амины, являясь производными аммиака, имеют сходное с ним строение
и проявляют подобные ему свойства. Для них также характерно образование
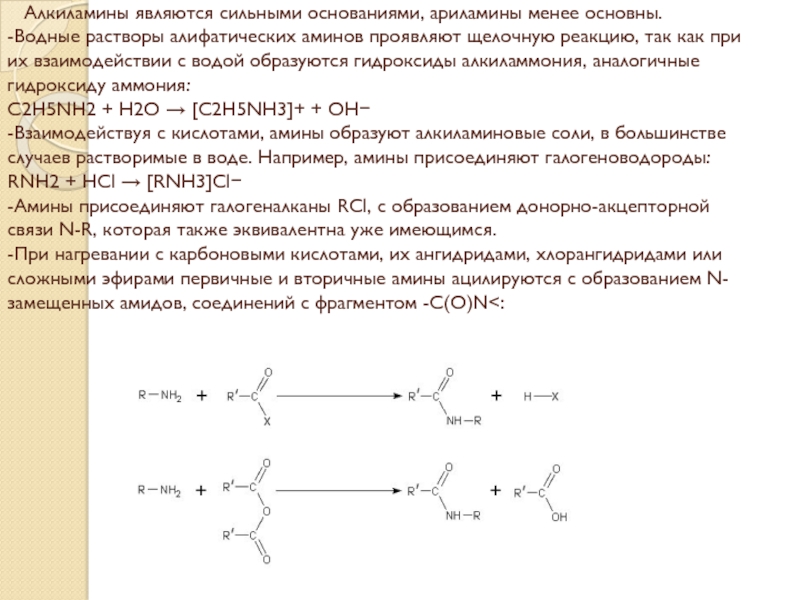
донорно-акцепторной связи. Азот предоставляет неподеленную электронную пару, исполняя роль донора. В качестве акцептора электоронов может выступать, например, протон Н+, образуя ион R3NH+. Возникшая ковалентная связь N-H полностью эквивалентна остальным связям N-H в амине.Слайд 6 Алкиламины являются сильными основаниями, ариламины менее основны. -Водные растворы
алифатических аминов проявляют щелочную реакцию, так как при их взаимодействии
с водой образуются гидроксиды алкиламмония, аналогичные гидроксиду аммония: C2H5NH2 + H2O → [C2H5NH3]+ + OH− -Взаимодействуя с кислотами, амины образуют алкиламиновые соли, в большинстве случаев растворимые в воде. Например, амины присоединяют галогеноводороды: RNH2 + HCl → [RNH3]Cl− -Амины присоединяют галогеналканы RCl, с образованием донорно-акцепторной связи N-R, которая также эквивалентна уже имеющимся. -При нагревании с карбоновыми кислотами, их ангидридами, хлорангидридами или сложными эфирами первичные и вторичные амины ацилируются с образованием N-замещенных амидов, соединений с фрагментом -С(О)N<:Слайд 7-Первичные и вторичные амины взаимодействуют с азотистой кислотой различным образом.
При помощи азотистой кислоты первичные, вторичные и третичные амины отличают
друг от друга. Из первичных аминов образуются первичные спирты: C2H5NH2 + HNO2 → C2H5OH + N2 +H2O При этом выделяется газ (азот). Это признак того, что в колбе первичный амин. Вторичные амины образуют с азотистой кислотой желтые, трудно растворимые нитрозамины — соединения, содержащие фрагмент >N-N=O: (C2H5)2NH + HNO2 → (C2H5)2N-N=O + H2O Вторичные амины сложно не узнать, по лаборатории распространяется характерный запах нитрозодиметиламина. Третичные амины при обычной температуре в азотистой кислоте просто растворяются.Слайд 8-конденсация первичных аминов с альдегидами и кетонами приводит к образованию
иминов или так называемых оснований Шиффа — соединений, содержащих фрагмент
-N=C<:-При горении амин выделяет кроме воды и углекислого газа ещё и азот.