Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Атом
Содержание
- 1. Атом
- 2. Периодический закон Д .И Менделеева и его
- 3. Атом (др.-греч. ἄτομος — неделимый) 1. Атом
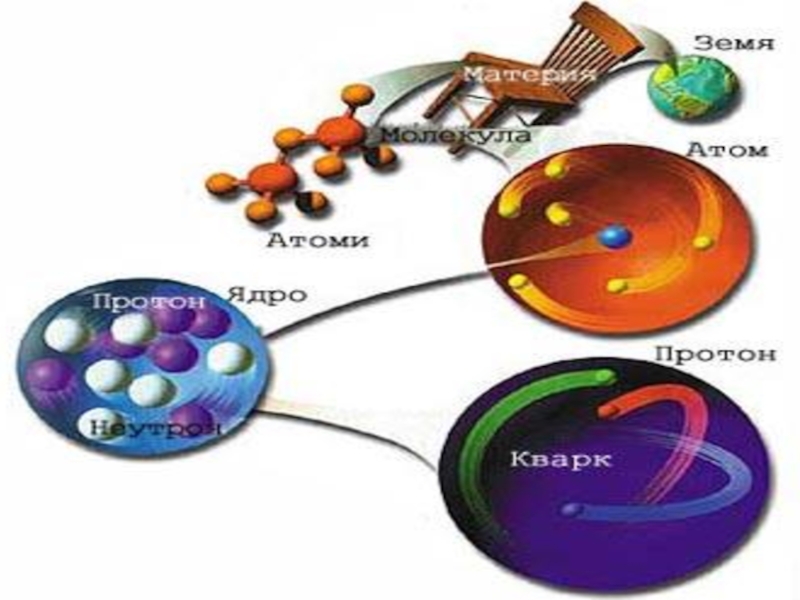
- 4. Структура атома
- 5. В 1911 г. английский ученый Э. Резерфорд
- 6. Резерфорд предположил, что атом устроен подобно
- 7. На основании опытов Резерфорда было установлено: Протон
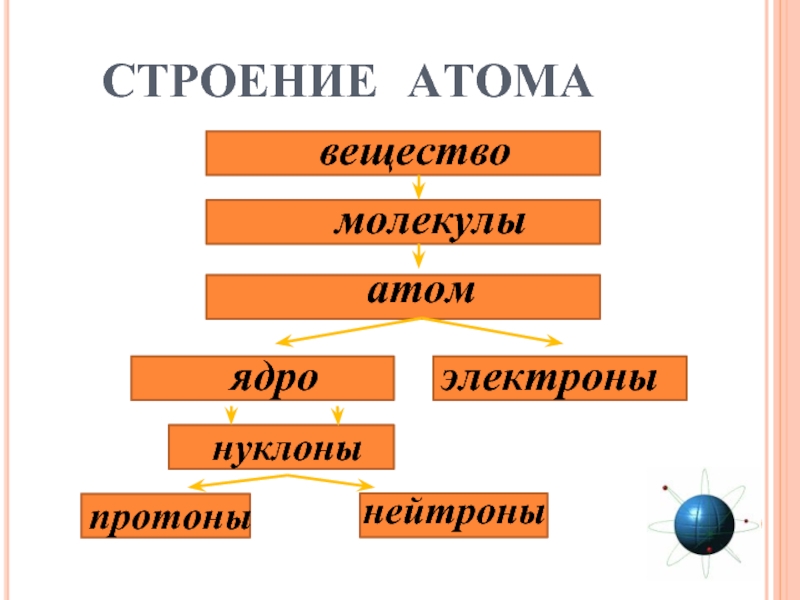
- 8. СТРОЕНИЕ АТОМА веществомолекулыатомнуклоны
- 9. Слайд 9
- 10. Строение атома на примере О+8О
- 11. У кислорода порядковый номер равен 8 ,поэтому
- 12. 5 формул строения атома1)Определение числа протонов,
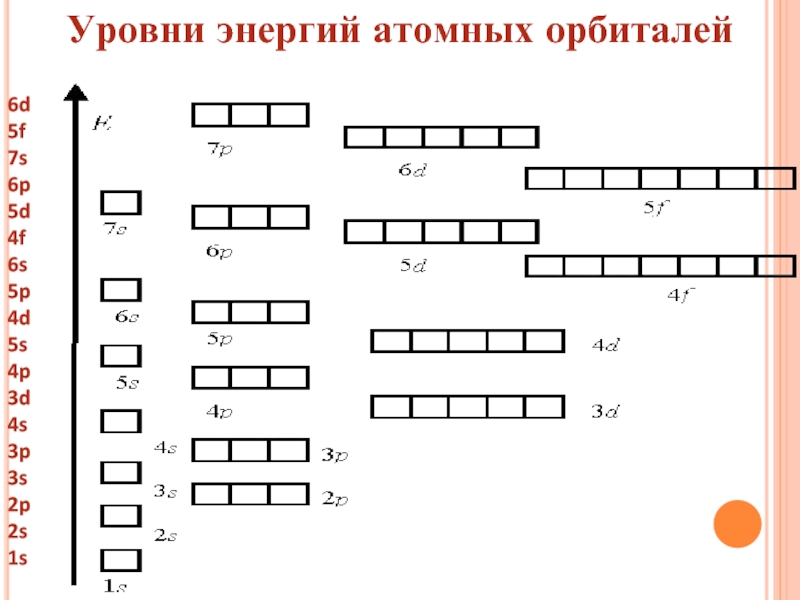
- 13. 6d5f7s6p5d4f6s5p4d5s4p3d4s3p3s2p2s1sУровни энергий атомных орбиталей
- 14. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Атом (др.-греч. ἄτομος — неделимый)
1. Атом – микрочастица, имеющая форму
шара.
2. Атом состоит из ядра и электронов.
3. Ядро имеет очень
маленький размер(r (атома) / r (ядра) = 100000).
4. Ядро имеет положительный заряд.
5. Атом – электронейтрален, так как число протонов и электронов одинаково.
6. Электроны обладают отрицательным зарядом и движутся вокруг ядра.
Слайд 5В 1911 г. английский ученый
Э. Резерфорд
доказал ,что в
центре атома
имеется положительно
заряженное ядро.
Слайд 6 Резерфорд предположил, что атом устроен подобно планетарной системе.
Суть
модели строения атома по Резерфорду заключается в следующем: в центре
атома находится положительно заряженное ядро, в котором сосредоточена вся масса, вокруг ядра по круговым орбитам на больших расстояниях вращаются электроны (как планеты вокруг Солнца).Заряд ядра совпадает с номером химического элемента в таблице Менделеева.
Планетарная модель строения атома
Слайд 7
На основании опытов Резерфорда было установлено:
Протон
Нейтрон
P+
n0 «Нуклеус» (латинское nucleus) – ядро.
Масса атома сосредоточена в ядре. Поэтому эта модель называется - нуклеарная.
Атом
Ядро Электронная оболочка
Состоит из нуклонов Состоит из электронов (ē)
Слайд 10Строение атома на примере О
+8О (
1)Число протонов и электронов равны порядковому номеру элемента
2)Что бы найти
число нейтронов, нужно из молекулярной массы элемента вычестьмассу протонов или электронов.
Слайд 11У кислорода порядковый номер
равен 8 ,поэтому число электронов
и
протонов равны 8,а молекулярная
масса кислорода равна 16,
поэтому чтобы найти
число нейтроновнадо из 16
(молекулярной массы кислорода)
вычесть заряд ядра
(или число протонов или число элетронов)
Слайд 12 5 формул строения атома
1)Определение числа протонов, электронов и нейтронов
у елемента
2)Распределение электронов по энергетическим уровням
3)Электронная формула элемента
4)Ячеечное строения элемента
5)Графическое
изображение электронов, находящихсяна внешнем энергетическом уровне