Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Азотная кислота по химии
Содержание
- 1. Азотная кислота по химии
- 2. Слайд 2
- 3. План урока: 1. Проверка Д/З
- 4. Пора проверить знания!!!
- 5. Проверка результатов Задание № 1 Запишите
- 6. Задание № 2 Расположите соединения азота в
- 7. Задание № 3 Составьте уравнения реакций по
- 8. Слайд 8
- 9. Азотная кислота HNO3 I. Физические свойства
- 10. I. Физические свойства азотной кислоты Агрегатное состояние
- 11. II. Характеристика HNO3По основности:
- 12. III. Химические свойства HNO3Свойства HNO3 как электролитаДиссоциация:
- 13. III. Химические свойства HNO3
- 14. IV. Применение азотной кислоты
- 15. Вопросы на закрепление I. Характерные свойства чистой
- 16. Вопросы на закреплениеII. Назовите вещества, с которыми
- 17. ПОРА ПОДВЕСТИ
- 18. Домашнее задание:Выучить § 27;Проанализировать записи в
- 19. Благодарим всех за внимание!
- 20. Скачать презентанцию
Тема: «Азотная кислота»
Слайды и текст этой презентации
Слайд 2
Тема: «Азотная кислота» Цель урока: Рассмотреть свойства азотной кислоты и области ее применения
Слайд 3План урока: 1. Проверка Д/З (письменная работа); 2. Изучение нового материала; 3.
Закрепление;
4. Подведение итогов;
5. Домашнее задание, его инструктаж.
Слайд 5 Проверка результатов Задание № 1 Запишите формулу соединения азота и его название
на основании физических свойств
I вариант: Бесцветный газ, плохо растворим
в воде, легко соединяется с кислородом воздуха, образуя бурый газ.NO – оксид азота (II)
II вариант: Бесцветный газ с характерным резким запахом, хорошо растворим в воде, легче воздуха.
NH3 - аммиак
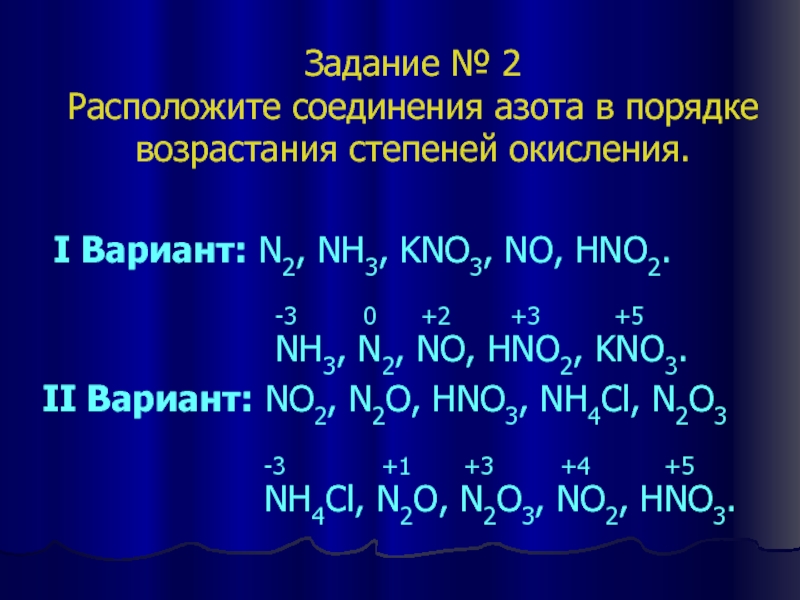
Слайд 6Задание № 2
Расположите соединения азота в порядке возрастания степеней окисления.
I Вариант: N2, NH3, KNO3, NO, HNO2.
-3 0 +2 +3 +5NH3, N2, NO, HNO2, KNO3.
II Вариант: NO2, N2O, HNO3, NH4Cl, N2O3
-3 +1 +3 +4 +5
NH4Cl, N2O, N2O3, NO2, HNO3.
Слайд 7Задание № 3
Составьте уравнения реакций по схеме. Назовите вещество Х.
I
вариант: N2 → X → NH4Cl
X –
NH3 (аммиак)1. N2 + 3H2=2NH3
2. NH3 + HCl = NH4Cl
II Вариант: NO2 → X → NH4NO3
X – HNO3 (азотная кислота)
1.4NO2+2H2O+O2=4HNO3
2. HNO3 + NH3=NH4NO3
Слайд 9Азотная кислота
HNO3
I. Физические свойства азотной кислоты;
II. Характеристика
кислоты;
III. Химические свойства ;
IV. Применение азотной кислоты.
Слайд 10I. Физические свойства
азотной кислоты
Агрегатное состояние – жидкость;
Цвет –
отсутствует;
Запах – едкий, кислотный;
Растворимость в воде – хорошая;
«Дымит» на
воздухе;«Особые приметы»:
при хранении на свету разлагается, приобретая желтоватый оттенок:
4HNO3=4NO2↑ + O2↑ + 2H2O
Слайд 11II. Характеристика HNO3
По основности:
одноосновная
2. По содержанию «О»:
кислородсодержащая
3. По растворимости в воде:
растворимая
4. По стабильности:
нестабильная
5. По летучести:
летучая
6. По степени диссоциации:
сильная
Слайд 12III. Химические свойства HNO3
Свойства HNO3 как электролита
Диссоциация: HNO3 = H+
+ NO3 -
Взаимодействует
А) с оксидами металлов:
CuO + 2HNO3
= Cu(NO3)2 + H2OCuO + 2H+ = Cu2+ + H2O
Б) с основаниями:
Cu(OH)2 + 2HNO3 = Cu(NO3)2 + 2H2O
Cu(OH)2 + 2H+ = Cu2+ + 2H2O
В) с солями:
Na2CO3 + 2HNO3 = 2NaNO3 + CO2↑ + H2O
CO32- + 2H+ = CO2 + H2O
Слайд 13III. Химические свойства HNO3
2. Окислительные
свойства
Взаимодействует с металлами:
K Ca Na Mg
Al Zn Cr Fe Pb H2 Cu Hg Ag AuМе + HNO3 → Me(NO3)n + H2O + NxOy
Cu + 4HNO3(конц) = Cu(NO3)2 + 2H2O + 2NO2↑
3Cu + 8HNO3(разб) = 3Cu(NO3)2 + 4H2O + 2NO↑
Me + HNO3 = Me(NO3)2 + H2↑
Слайд 15Вопросы на закрепление
I. Характерные свойства чистой HNO3:
Твердое агрегатное состояние;
Хорошая
растворимость в воде;
Отсутствие запаха;
Желтый цвет;
Разлагается на свету с выделением азота;
«Дымит»
на воздухе.Слайд 16Вопросы на закрепление
II. Назовите вещества, с которыми может реагировать азотная
кислота как электролит:
SO2 H2 ZnO Ca(OH)2 HCl
Na2SiO3 AgIII. Азотную кислоту применяют для определения примесей в золотых изделиях. Объясните, чем в ряде случаев обуславливается появление бурого газа и голубого раствора при обработке золота кислотой?
Слайд 17 ПОРА ПОДВЕСТИ ИТОГ!
Что
я узнал о свойствах азотной кислоты?
Где применяется азотная кислота?