Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Электролитическая диссоциация
Содержание
- 1. Электролитическая диссоциация
- 2. Электролитическая диссоциация — процесс распада электролита на
- 3. Слайд 3
- 4. Слайд 4
- 5. 2) II Положение: под действием электрического
- 6. Механизм электролитической диссоциации ионных веществ При растворении
- 7. Механизм электролитической диссоциации полярных веществ Аналогично диссоциируют
- 8. Электролиты и неэлектролиты Электролиты и
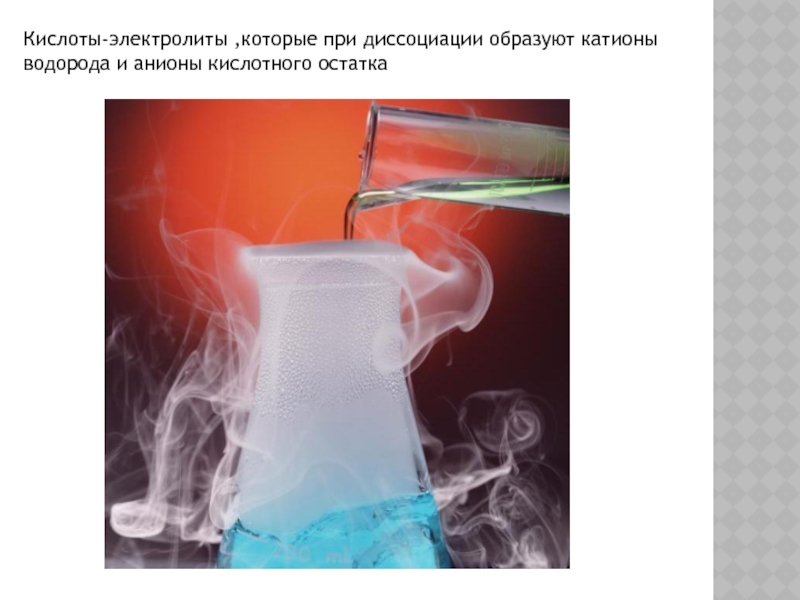
- 9. Кислоты-электролиты ,которые при диссоциации образуют катионы водорода и анионы кислотного остатка
- 10. Основания-электролиты , которые при диссоциации образуют катионы металлов и гидроксид-анионоы
- 11. Соли-электролиты , которые при диссоциации образуют катионы металла и анионы кислотных остатков
- 12. Мини-тест (6 вопросов)1 Электролиты, образующие при электролитической
- 13. Скачать презентанцию
Электролитическая диссоциация — процесс распада электролита на ионы при растворении его в полярном растворителе или при плавлении.
Слайды и текст этой презентации
Слайд 1ЭЛЕКТРОЛИТИЧЕСКАЯДИССОЦИАЦИЯ
Мельситова Татьяна Васильевна
Учитель химии СОМШ № 44
г. Владикавказ
Слайд 2Электролитическая диссоциация — процесс распада электролита на ионы при растворении
его в полярном растворителе или при плавлении.
Слайд 5 2) II Положение: под действием электрического тока положительно заряженные
ионы двигаются к катоду, а отрицательно заряженные к аноду.
3)
причиной диссоциации электролита в водных растворах является его гидратация, то есть взаимодействие электролита с молекулами воды и разрыв химической в нем.4) Электролитическая диссоциация – процесс обратимый для слабых электролитов.
HNO2 <—> H+ + NO2-
5) Не все электролиты в одинаковой мере диссоциируют на ионы.
факторы влияющие на степень диссоциации.
•природа электролита;
•температура;
•концентрация вещества.
Слайд 6Механизм электролитической диссоциации ионных веществ
При растворении соединений с ионными
связями (например, NaCl) процесс гидратации начинается с ориентации диполей воды
вокруг всех выступов и граней кристаллов соли.Ориентируясь вокруг ионов кристаллической решетки, молекулы воды образуют с ними либо водородные, либо донорно-акцепторные связи. При этом процессе выделяется большое количество энергии, которая называется энергией гидратации.
Энергия гидратации, величина которой сравнима с энергией кристаллической решетки, идет на разрушение кристаллической решетки. При этом гидратированные ионы слой за слоем переходят в растворитель и, перемешиваясь с его молекулами, образуют раствор.
Слайд 7Механизм электролитической диссоциации полярных веществ
Аналогично диссоциируют и вещества, молекулы
которых образованы по типу полярной ковалентной связи (полярные молекулы). Вокруг
каждой полярной молекулы вещества (например, HCl), определенным образом ориентируются диполи воды. В результате взаимодействия с диполями воды полярная молекула еще больше поляризуется и превращается в ионную, далее уже легко образуются свободные гидратированные ионы.Слайд 8Электролиты и неэлектролиты
Электролиты и неэлектролиты
Электролитическая диссоциация веществ, идущая
с образованием свободных ионов объясняет электрическую проводимость растворов.
Процесс электролитической диссоциации
принято записывать в виде схемы, не раскрывая его механизма и опуская растворитель (H2O), хотя он является основным участником.CaCl2 « Ca2+ + 2Cl-
KAl(SO4)2 « K+ + Al3+ + 2SO42-
HNO3 « H+ + NO3-
Ba(OH)2 « Ba2+ + 2OH-
Слайд 9Кислоты-электролиты ,которые при диссоциации образуют катионы водорода и анионы кислотного
остатка
Слайд 10Основания-электролиты , которые при диссоциации образуют катионы металлов и гидроксид-анионоы
Слайд 11Соли-электролиты , которые при диссоциации образуют катионы металла и анионы
кислотных остатков
Слайд 12Мини-тест (6 вопросов)
1 Электролиты, образующие при электролитической диссоциации в качестве
катионов только катионы водорода, называются:
а) основаниями (щелочами);
б) кислыми солями;
в) кислотами;г) основными оксидами.
2. Выделите вещество, при электролитической диссоциации которого образуется карбонат-ион:
а)K2SiO3;
б)Ca(NO3) ;
в)Na2CO3.
3. Определите формулы веществ, образующих при электролитической диссоциации гидроксид-ионы:
а)H2SO4;
б)KOH;
в)CH3COOH.
4. Выберите правильную запись уравнения диссоциации азотной кислоты.
а)HNO3>H+ + NO3-;
б)HNO3>H- + 3NO+;
в)HNO3>H- + NO3+;
г)HNO3>H+ + NO3+.
5. Укажите вещество, диссоциирующее в воде по схеме
Me2R3-2Me3++3R2-, где Me – металл, R – кислотный остаток.
а) силикат калия;
б) сульфат хрома(III);
в) нитрат железа(III);
г) оксид хрома(III).