Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химические уравнения
Содержание
- 1. Химические уравнения
- 2. Химические уравнения -Это условная запись химической
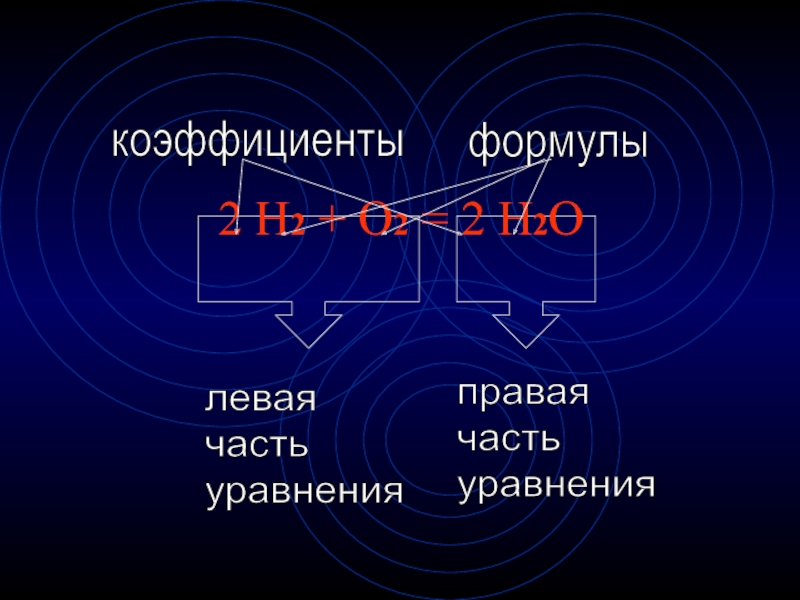
- 3. 2 H2
- 4. Химическая реакция происходит согласно ЗАКОНУ СОХРАНЕНИЯ
- 5. Закон сохранения массы вещества ( М.В. Ломоносов
- 6. NaOH + HCl = NaCl + H2O
- 7. По уравнению можно определить тип химической реакции
- 8. Основные типы химических реакцийсоединенияразложениязамещенияобмена
- 9. Реакции соединения Несколько
- 10. Реакции разложенияЯвляются обратными реакциям соединенияИз одного сложного
- 11. Реакции замещенияЭто реакции между простым и сложным
- 12. Реакции обменаЭто реакции, при которых два сложных
- 13. Составьте уравнения химических реакций:Горение угляВзаимодействие цинка с
- 14. Составьте уравнения химических реакций по схемам, определите
- 15. Расставьте коэффициенты в предложенных схемах уравнений, определите
- 16. Скачать презентанцию
Химические уравнения -Это условная запись химической реакции с помощью химических формул, коэффициентов и математических знаков
Слайды и текст этой презентации
Слайд 5Закон сохранения массы вещества
( М.В. Ломоносов – 1756 г.)
Масса веществ,
вступивших в химическую реакцию,
равна массе веществ, получившихся в ее
результате.Слайд 9Реакции соединения
Несколько простых или сложных
веществ соединяются в одно, более сложное
Zn + S = ZnSCaO + CO2 = CaCO3
Na2O + H2O = 2 NaOH
4Al + 3O2 = 2 Al2O3
Левая часть уравнения – несколько веществ,
правая часть – только одно сложное!
Слайд 10Реакции разложения
Являются обратными реакциям соединения
Из одного сложного вещества получаются несколько
других веществ
CaCO3 = CaO + CO22 KMnO4 = K2MnO4 + MnO2 + O2
2 Fe(OH)3 = Fe2O3 + 3 H2O
В левой части уравнения – одно сложное вещество, в правой – несколько различных.
Слайд 11Реакции замещения
Это реакции между простым и сложным веществами, в которых
атомы простого вещества замещают атомы одного из элементов в сложном
веществе.Mg + 2 HCl = MgCl2 + H2
3 CuSO4 + 2 Al = Al2(SO4)3 +3 Cu
Левая часть уравнения – простое и сложное вещества, правая – новое простое и новое сложное
Слайд 12Реакции обмена
Это реакции, при которых два сложных вещества обмениваются своими
составными частями
CuSO4 + 2 NaOH = Cu(OH)2 +
Na2SO4AgNO3 + HCl = HNO3 + AgCl
Слайд 13Составьте уравнения химических реакций:
Горение угля
Взаимодействие цинка с соляной кислотой
Разложение воды
электрическим током
Прокаливание карбоната кальция
Взаимодействие оксида меди (II) с серной кислотой
Слайд 14Составьте уравнения химических реакций по схемам, определите тип реакций:
Cu(OH)2
Na2O + H2O
Zn + S
P + O2
P2O5 + H2O
Слайд 15Расставьте коэффициенты в предложенных схемах уравнений, определите тип реакций:
Al +
O2 Al2O3
Fe2O3 +H2O
Fe(OH)3K + H3PO4 K3PO4 + H2
NaOH + H2SO4 Na2SO4 + H2O
KMnO4 K2MnO4 + MnO2 + O2