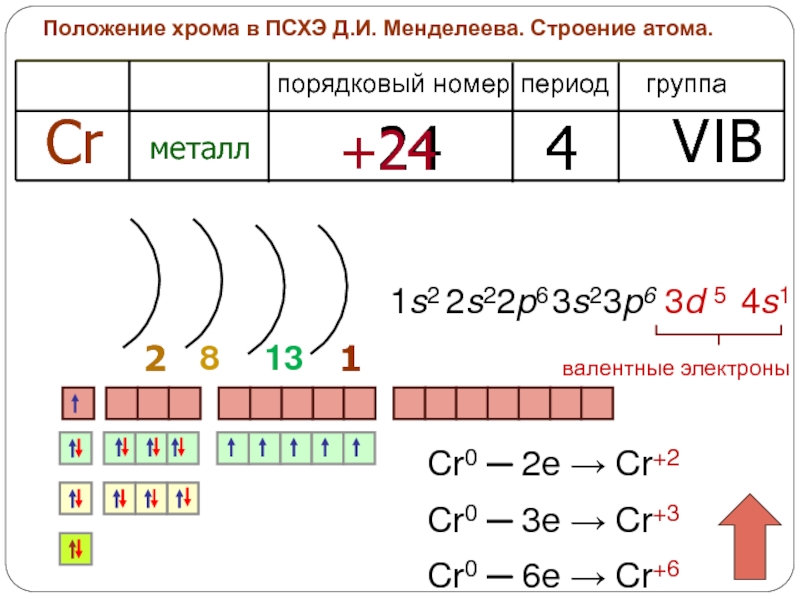
периодической системе
химических элементов Д.И.Менделеева
2. Строение атома.
III.Хром – простое вещество
3.
Нахождение в природе1. Состав. Физические свойства.
2. Получение.
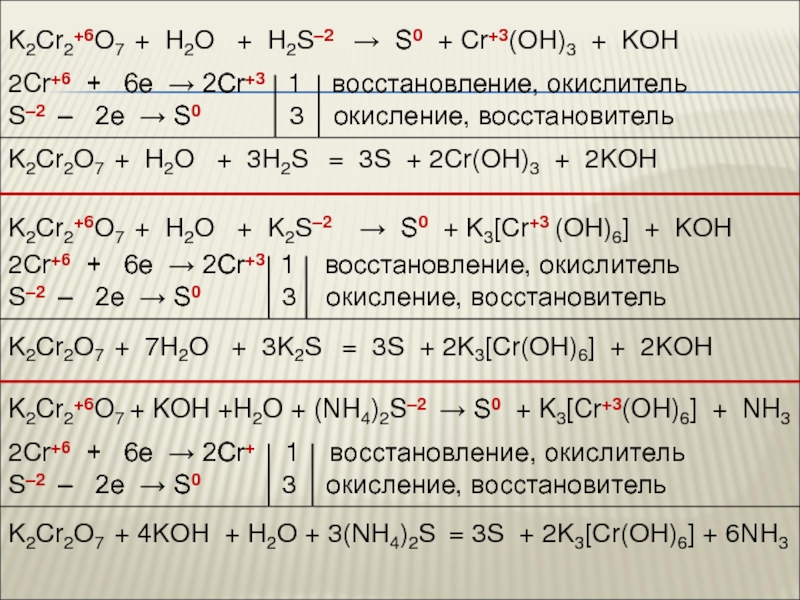
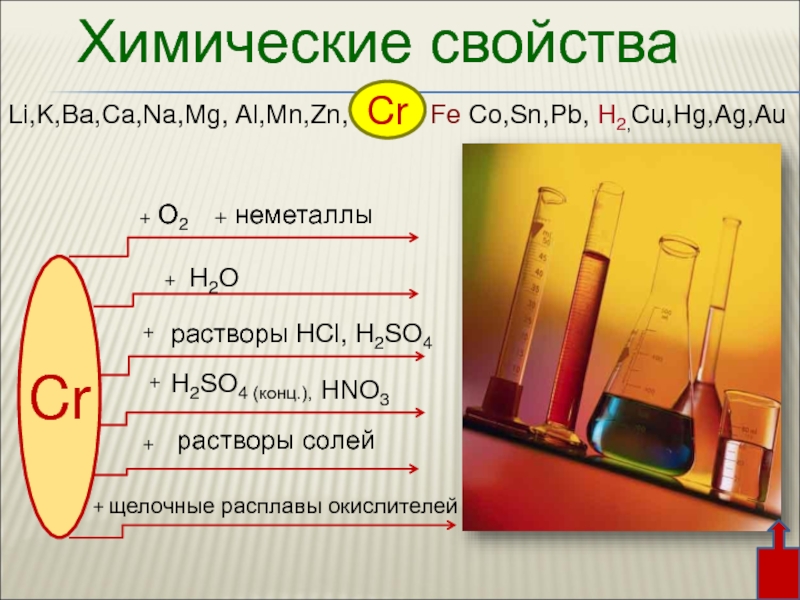
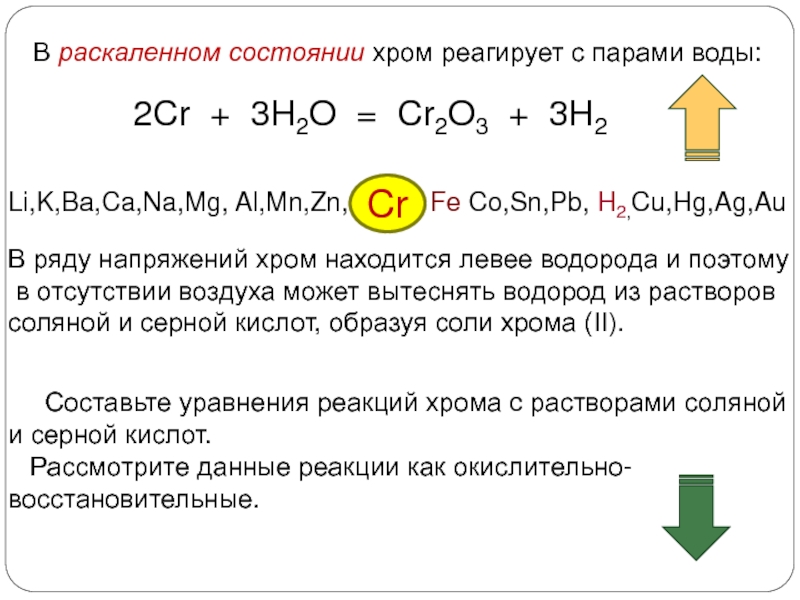
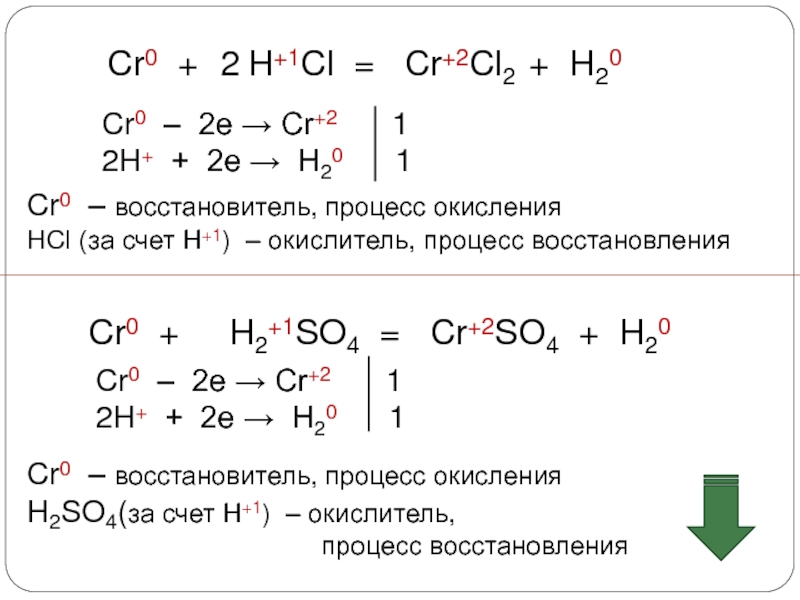
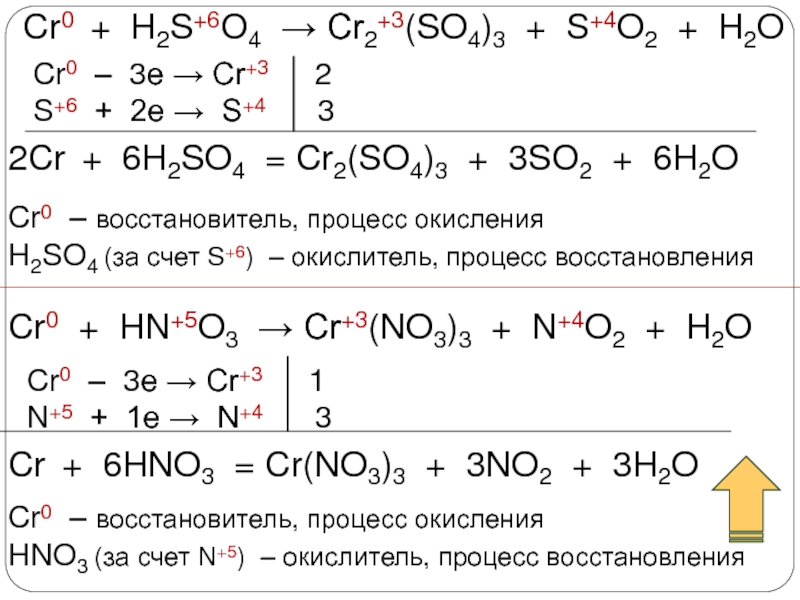
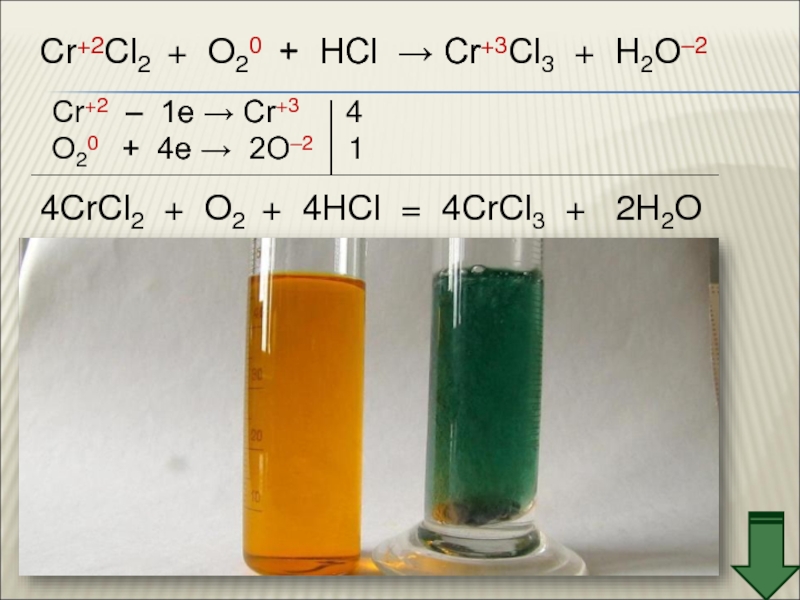
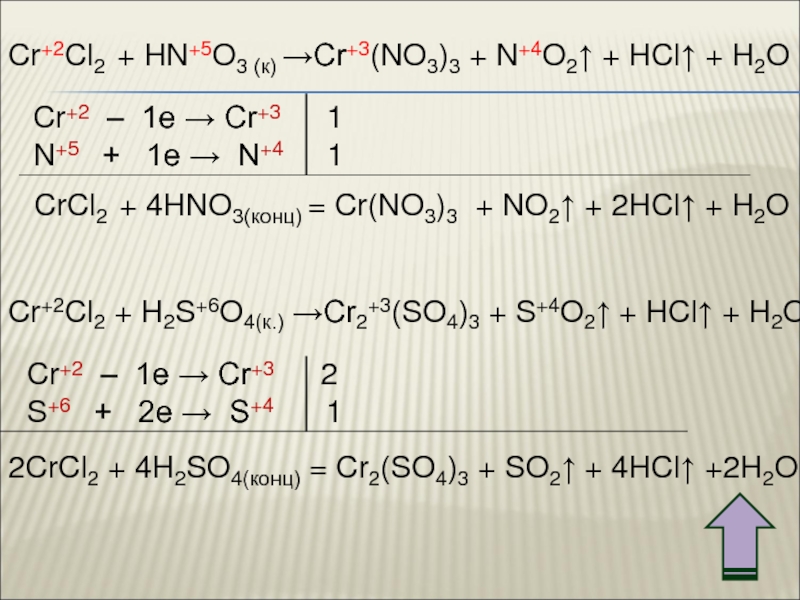
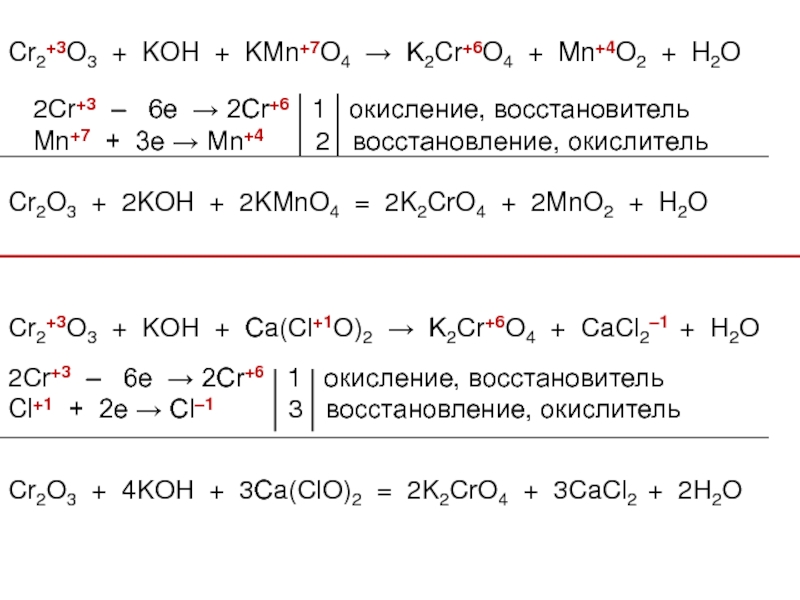
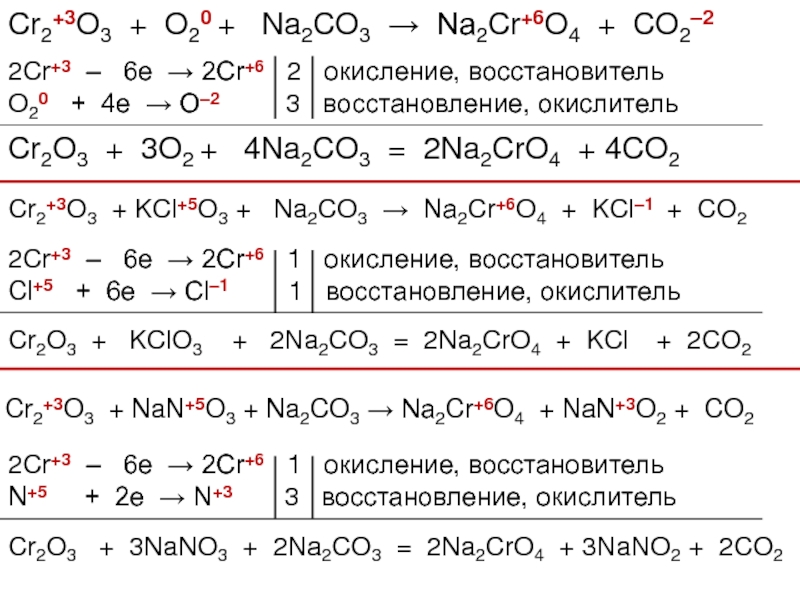
3. Химические свойства
4. Биологическая роль и физиологическое действие.
5. Применение
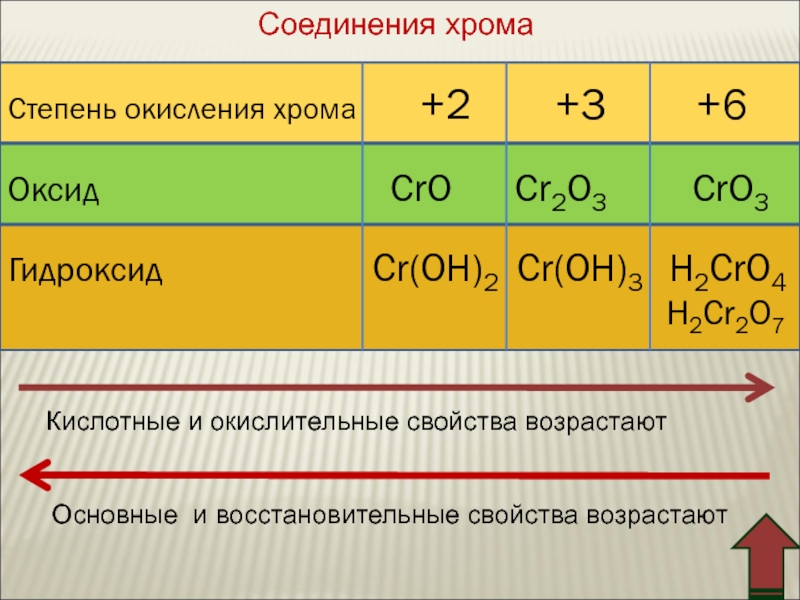
IV. Соединения хрома







































![Хром Cr(OH)3 + 3NaOH = Na3[Cr(OH)6]Cr(OH)3 + 3Na+ + 3OH– = 3Na+ Cr(OH)3 + 3NaOH = Na3[Cr(OH)6]Cr(OH)3 + 3Na+ + 3OH– = 3Na+ + [Cr(OH)6]3–Cr(OH)3 + 3OH– = [Cr(OH)6]3–2Cr(OH)3](/img/thumbs/55a1c9243a97b960e3044a50137c0501-800x.jpg)



![Хром K3[Cr+3(OH)6] + Br20 + KOH → K2Cr+6O4 + KBr– + H2O K3[Cr+3(OH)6] + Br20 + KOH → K2Cr+6O4 + KBr– + H2O Cr+3 – 3e → Cr+6](/img/thumbs/a950b46d2dc35240a1540ea92dcabf6c-800x.jpg)
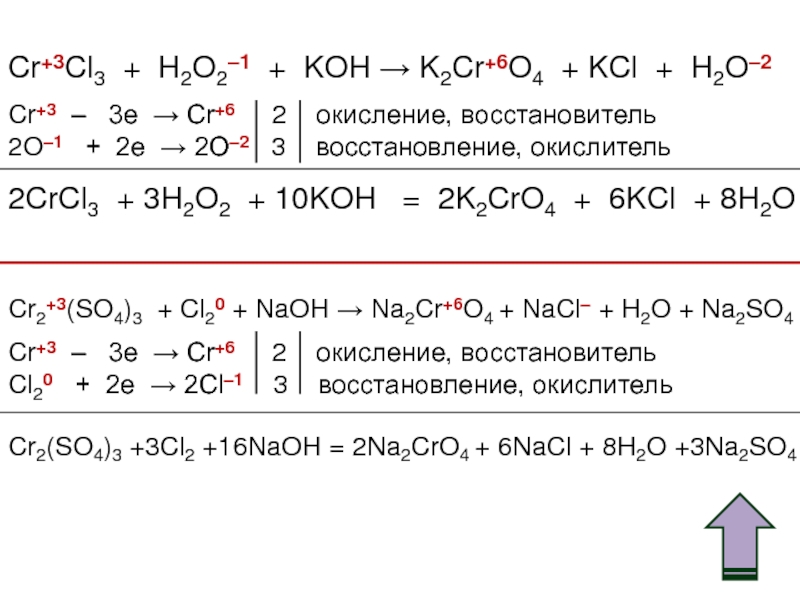






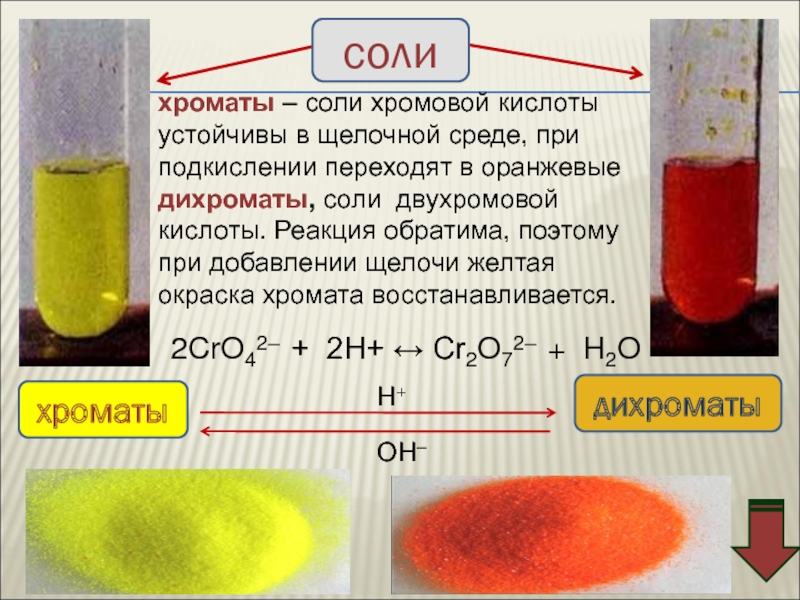



![Хром Соединения хрома (VI) – сильные окислители Cr2O72–Cr3+Cr(OH)3[Cr(OH)6]3–H+H2OOH–Cr2O72– + 14H+ + Соединения хрома (VI) – сильные окислители Cr2O72–Cr3+Cr(OH)3[Cr(OH)6]3–H+H2OOH–Cr2O72– + 14H+ + 6e → 2Cr3+ + 7H2OCr2O72–](/img/thumbs/296380fe3b362cc33a5e6284440e20b3-800x.jpg)