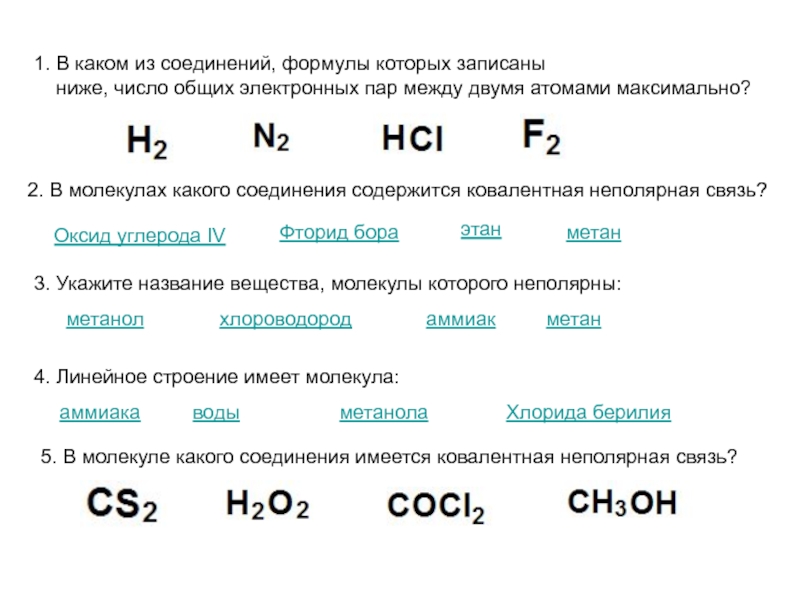
ниже, число общих электронных пар между двумя атомами максимально?
2.
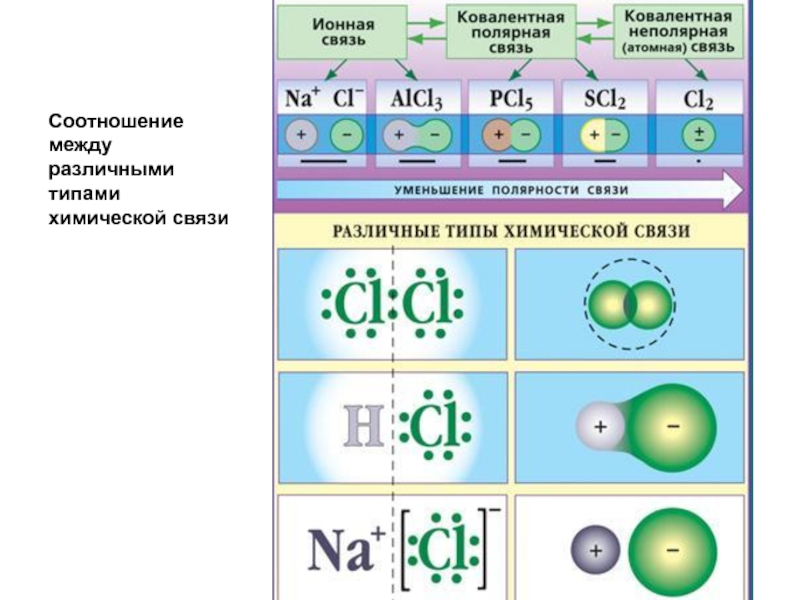
В молекулах какого соединения содержится ковалентная неполярная связь? Оксид углерода IV
Фторид бора
этан
метан
3. Укажите название вещества, молекулы которого неполярны:
метанол
хлороводород
аммиак
метан
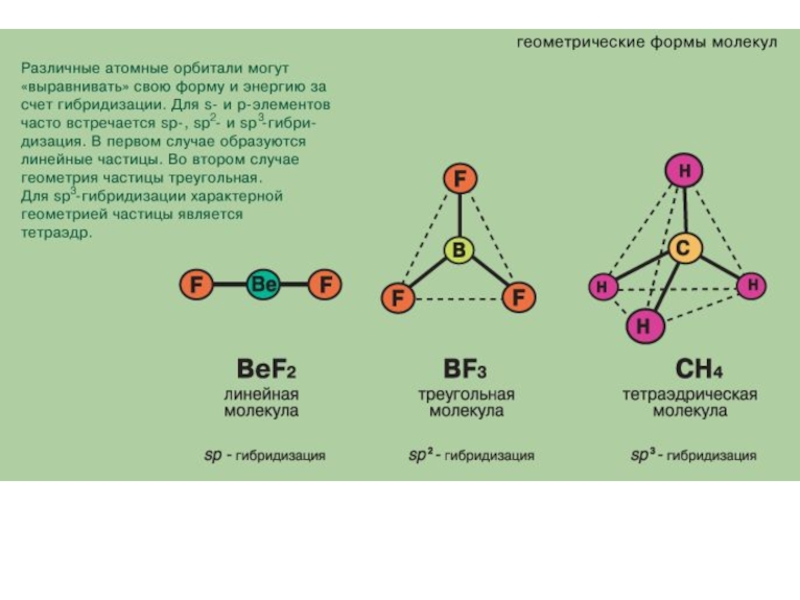
4. Линейное строение имеет молекула:
аммиака
воды
метанола
Хлорида берилия
5. В молекуле какого соединения имеется ковалентная неполярная связь?