Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Использование инновационных технологий при объяснении темы: "Окислительно-восстановительные реакции"
Содержание
- 1. Использование инновационных технологий при объяснении темы: "Окислительно-восстановительные реакции"
- 2. Цель работы:Методическая разработка темы “Окислительно-восстановительные реакции” с использованием инновационных технологий.
- 3. Окислительно-восстановительные реакцииэто процессы, в результате которых происходит
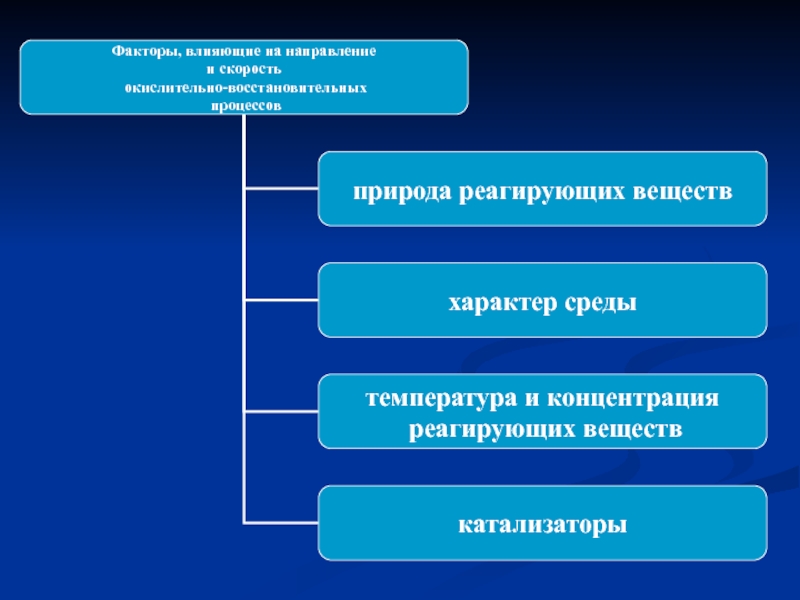
- 4. Слайд 4
- 5. Слайд 5
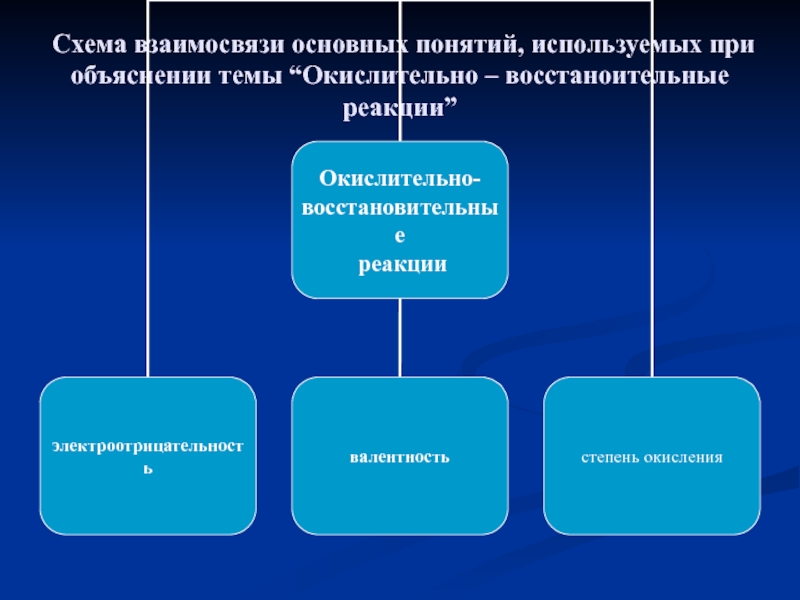
- 6. Схема взаимосвязи основных понятий, используемых при объяснении темы “Окислительно – восстаноительные реакции”
- 7. Инновация – нововведение, новация, новизна, введение новизны.
- 8. Схема перегруппировки учащихся
- 9. 111133331133222244442244123412341234123412341234
- 10. Слайд 10
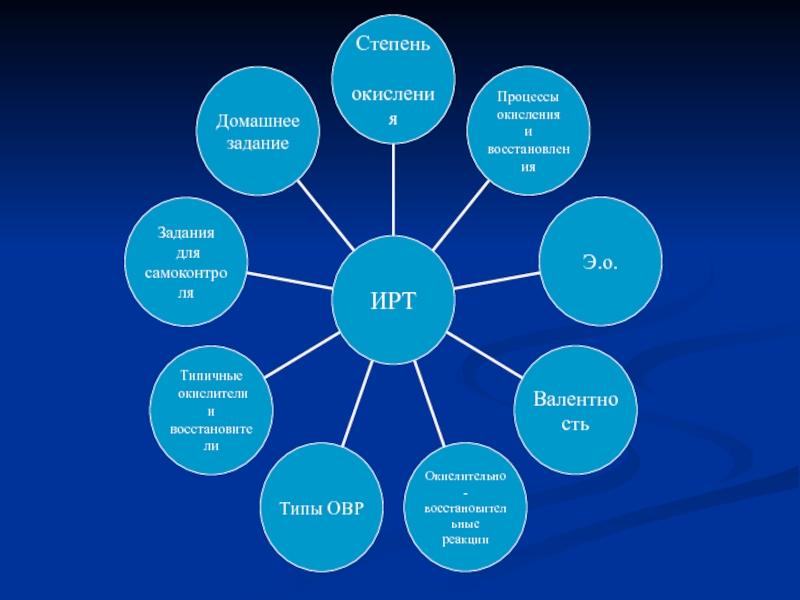
- 11. Интерактивная рабочая тетрадь(фрагмент I )Определите степень окисления
- 12. Интерактивная рабочая тетрадь(фрагмент II )Степень окисления –
- 13. Проведённая работа:Подготовлена методическая разработка проведения занятия по
- 14. Слайд 14
- 15. Слайд 15
- 16. Слайд 16
- 17. ВЫВОДЫ: Работа с ИРТ не настолько формализована,
- 18. Работа по усовершенствованию данного вопроса продолжается.
- 19. Спасибо за внимание!
- 20. Скачать презентанцию
Цель работы:Методическая разработка темы “Окислительно-восстановительные реакции” с использованием инновационных технологий.
Слайды и текст этой презентации
Слайд 2Цель работы:
Методическая разработка темы “Окислительно-восстановительные реакции” с использованием инновационных технологий.
Слайд 3Окислительно-восстановительные реакции
это процессы, в результате которых происходит переход или смещение
валентных электронов от атомов с меньшей электроотрицательностью к атомам с
большей электроотрицательностью. Примеры:H2 + Cl2 = 2HCl
Cl2 + H2O = HClO + HCl
2KClO3 = 2KCL + 3O2
Слайд 6Схема взаимосвязи основных понятий, используемых при объяснении темы “Окислительно –
восстаноительные реакции”
Слайд 7Инновация – нововведение, новация, новизна, введение новизны. Инновационные технологии в обучении
– это введение нового содержания, новых методов, приёмов, средств в
обучении.Слайд 11Интерактивная рабочая тетрадь(фрагмент I )
Определите степень окисления марганца, хрома в
следующих соединениях: K2MnO4, KMnO4, K2CrO4, K2Cr2O7.
Дана схема уравнения реакции: K2SO3+H2SO4+KMnO4=K2SO4
+ MnSO4 + … составьте уравнения ОВР и укажите возможный “пропущенный” продукт реакции.Валентность – это число общих связей в молекуле. Определите валентность элементов по формулам: HgO, K2S, B2O3, ZnO, MnO2, NiO, Cu2O, SnO2.
Даны уравнения реакций: Zn + Cl2 = ZnCl2 , Zn + 2HCl = ZnCl2 + H2. Проставьте над знаками соответствующих химических элементов степени окисления и покажите переход электронов.
Составьте уравнение ОВР, используя метод полуреакций: MnO2 + KClO3 + KOH = …... Чему равна сумма коэффициентов уравнения реакции? а) 14, б) 16, в) 11, г) 17.
Слайд 12Интерактивная рабочая тетрадь(фрагмент II )
Степень окисления – это ......................................
Порассуждайте, в
чём сходство и отличие понятия “степени окисления” с понятием ”валентность”.................................................................................................................................................
Определите
типы ОВР: а) H2S+ 8HNO3 = H2SO4 +8NO2 + 4H2O (….); б) 2H2S + H2SO3 = 3S + 3H2O (….); в) 2Pb(NO3)2 = 2PbO + 4NO2 + O2 (….)Укажите восстановитель и окислитель в реакциях: a) 2Al + 6HCl = 2AlCl3 + H2(….); б) 2H2S + H2SO3 = 3S + 3H2O (….); в) 8HI + H2SO4 = 4I2 + H2S + 4H2O (….); г) 2KClO3 = 2KCL + 3O2 (….)
Слайд 13Проведённая работа:
Подготовлена методическая разработка проведения занятия по теме: ” Окислительно-восстановительные
реакции”, с использованием инновационных технологий, рассчитанного в соответствии с календарно-тематическим
планированием по химии для 8 классов на 3 часа по 1 часу;Для занятий разработана, в соответствии с учебной программой для общеобразовательных школ, интерактивная рабочая тетрадь(ИРТ)по данной теме.
Слайд 17ВЫВОДЫ:
Работа с ИРТ не настолько формализована, как с компьютерной
программой.
ИРТ по мере необходимости создаёт условия самоконтроля, что даёт новые
возможности для развития критического мышления и творческой интеграции идей и возможности учащихся. Использованные интерактивные приёмы и средства обучения повышают уровень знаний учащихся, облегчают восприятие изучаемого материала, способствуют развитию самоконтроля учащихся.