Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Кислотные оксиды
Содержание
- 1. Кислотные оксиды
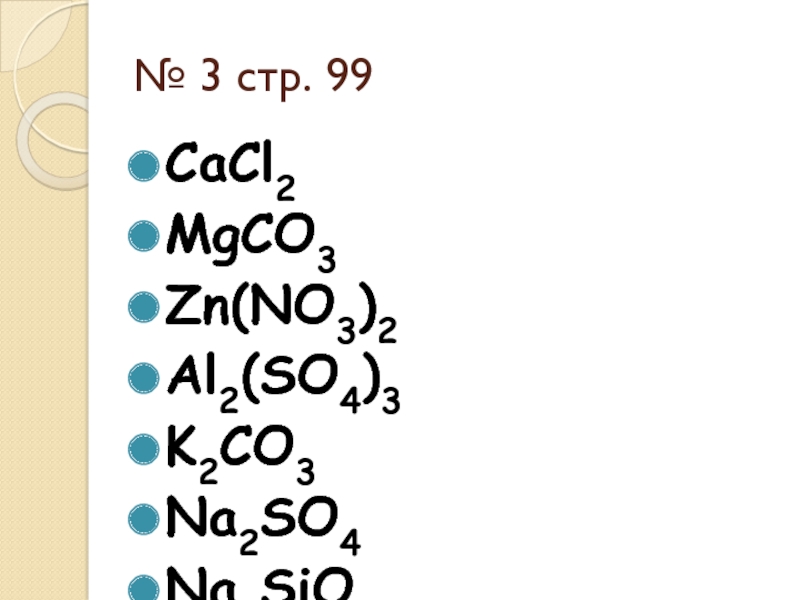
- 2. № 3 стр. 99CaCl2 MgCO3Zn(NO3)2 Al2(SO4)3K2CO3 Na2SO4 Na2SiO3 AgCl MgSO3 Al2S3
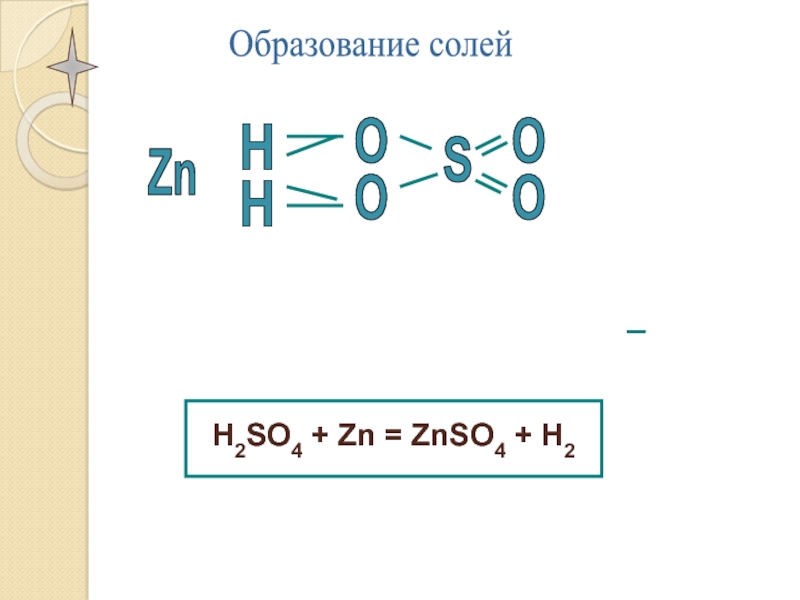
- 3. HHOOSOOОбразование солейZn
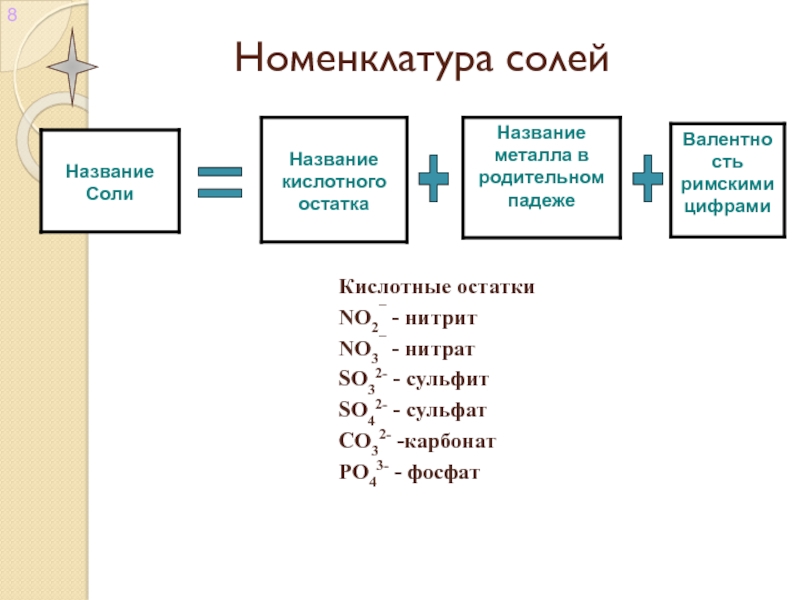
- 4. Номенклатура солей++=
- 5. Составить формулу сульфата алюминия:Al2SO43( )IIIII
- 6. Кислотные оксиды – это оксиды, которым соответствуют
- 7. При взаимодействии кислотных оксидов (ангидридов) с водой
- 8. Задание: § 29 № 3-6 Стр. 103 самое важное в главе 3
- 9. Скачать презентанцию
№ 3 стр. 99CaCl2 MgCO3Zn(NO3)2 Al2(SO4)3K2CO3 Na2SO4 Na2SiO3 AgCl MgSO3 Al2S3
Слайды и текст этой презентации
Слайд 6Кислотные оксиды – это оксиды, которым соответствуют кислоты.
Ангидрид – обезвоженная
кислота
H2SO3 SO2 + H2O
H2CO3 CO2 + H2O
Слайд 7При взаимодействии кислотных оксидов (ангидридов) с водой образуются кислоты
N2O3 +
H2O HNO2
N2O5 + H2O HNO3
P2O5 + H2O
SO3 + H2O
Cl2O7 + H2O
SiO2 + H2O ≠