Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Медь
Содержание
- 1. Медь
- 2. Положение в Периодической системеI группа, побочная подгруппа.6429Cud-элемент 1s22s22p63s23p63d104s1Степени окисления +1, +2
- 3. Физические свойства меди.Медь - металл розово-красного цвета,
- 4. Химические свойства меди.Медь - малоактивный металл, в
- 5. Химические свойства меди.5. В присутствии окислителей, прежде
- 6. Соединения медиОксид меди (I)Cu2O – красновато-коричневые
- 7. Соединения меди(+1)
- 8. Соединения меди(+2)Образование комплексовCu(OH)2 + 4NH3 = Cu(NH3)4 (OH)2Сг+2- окислительCu+2O + H2 = Cu0 + H2O
- 9. Область применения медиСплав меди, известный с древнейших
- 10. Домашнее задание - выучить изученную
- 11. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Положение в Периодической системе
I группа, побочная подгруппа.
6429Cu
d-элемент
1s22s22p63s23p63d104s1
Степени окисления +1,
Слайд 4Химические свойства меди.
Медь - малоактивный металл, в электрохимическом ряду напряжений
она стоит правее водорода.
1.Окисление во влажном воздухе
2Cu +
Н2О + O2 + CO2 = (CuOH)2CO32. Медь реагирует с галогенами при нагревании
Cu + Cl2 = CuCl2
3. При сплавлении меди с серой образуетcя нерастворимый
в воде сульфид
2Cu + S = Cu2S
4. Взаимодействие с кислородом
4Cu + O2 = 2Cu2O
2Cu + O2 = 2CuO
t = 800
t = 400
Слайд 5Химические свойства меди.
5. В присутствии окислителей, прежде всего кислорода, медь
реагирует с соляной и разбавленной серной кислотой, но водород при
этом не выделяется:2Cu + 4HCl + O2 = 2CuCl2 + 2H2O.
6. С азотной кислотой различных концентраций медь реагирует активно, при этом выделяются различные оксиды азота
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O.
7. С концентрированной серной кислотой медь реагирует при сильном нагревании:
Cu + 2H2SO4 = CuSO4 + SO2 + 2H2O.
8. Практическое значение имеет способность меди реагировать с растворами солей железа (III):
2FeCl3 + Cu = CuCl2 + 2FeCl2
Слайд 6 Соединения меди
Оксид меди (I)
Cu2O – красновато-коричневые кристаллы
1.В воде
не растворяется и не реагирует с ней. Имеет слабовыраженные амфотерные
свойства с преобладанием основных.2.Взаимодействует с растворами щелочей с образованием гидроксокомплексов:
Cu2O + 2NaOH + H2O = 2Na[Cu(OH)2].
3.В водных растворах аммиака образует гидроксид диамминмеди (I):
Cu2O + 4NH3 + H2O = 2[Cu(NH3)2]OH.
4.С соляной кислотой взаимодействует с образованием дихлорокупрата (I) водорода:
Cu2O + 4HCl = 2H[CuCl2] + H2O.
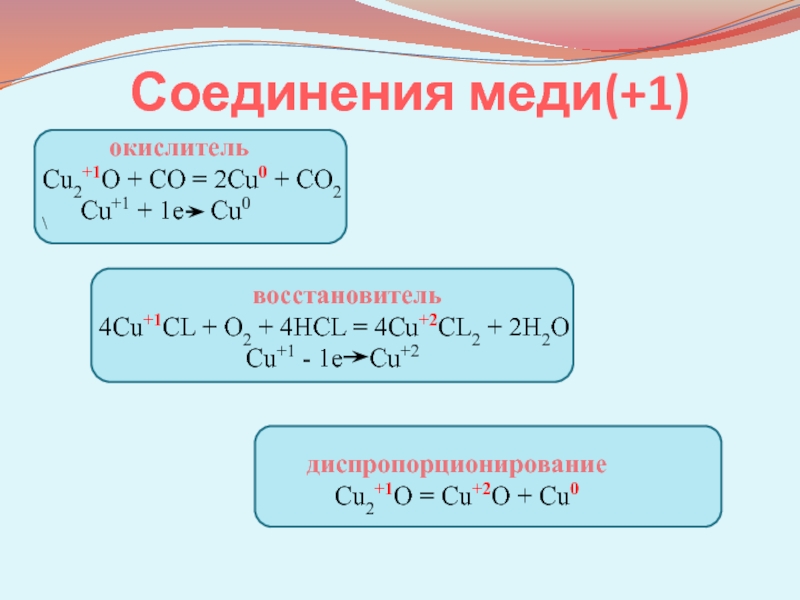
Слайд 7 Соединения меди(+1)
окислитель
Cu2+1O + CO = 2Cu0 + CO2
\ Cu+1
+ 1e Cu0 диспропорционирование
Cu2+1O = Cu+2O + Cu0
восстановитель
4Cu+1CL + O2 + 4HCL = 4Cu+2CL2 + 2H2O
Cu+1 - 1e Cu+2
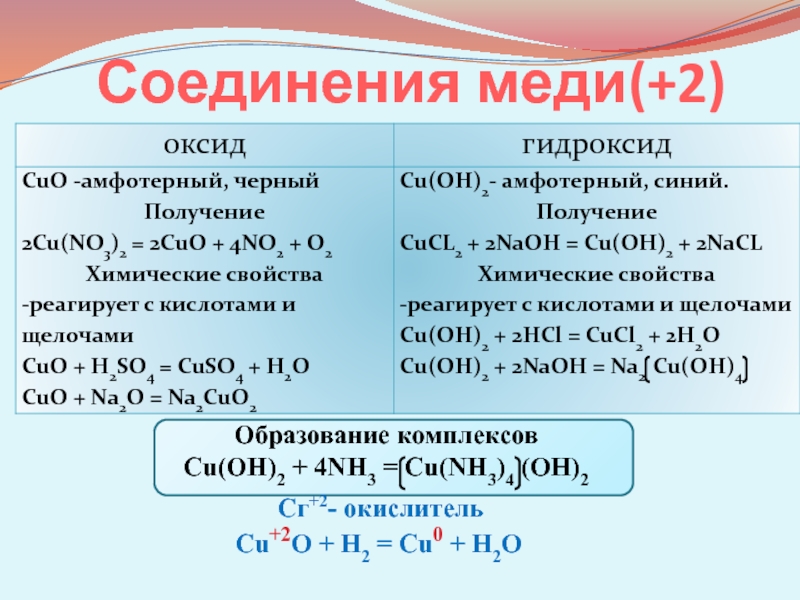
Слайд 8 Соединения меди(+2)
Образование комплексов
Cu(OH)2 + 4NH3 = Cu(NH3)4 (OH)2
Сг+2- окислитель
Cu+2O
+ H2 = Cu0 + H2O
Слайд 9Область применения меди
Сплав меди, известный с древнейших времен, — бронза
— содержит 4—30% олова (обычно 8—10%). Интересно, что бронза по
своей твердости превосходит отдельно взятые чистые медь и олово.Из бронзы отливали в средние века орудия и многие другие изделия. Знаменитые Царь-пушка и Царь-колокол в Московском Кремле также отлиты из сплава меди с оловом.