Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Производство аммиака цианамидным методом
Содержание
- 1. Производство аммиака цианамидным методом
- 2. Цель проектной работы.Создании альтернативного способа производства аммиака.
- 3. Термодинамические основы химического производства.Скорость химической реакции -
- 4. Химические равновесие – это состояние системы, при
- 5. Сырье. Сырье- это минералы, которые лежат в
- 6. Химизм. Химизм – это химические реакции, лежащие
- 7. Аппаратное оформление.Мельница для измельчения известняка.Печь для получения
- 8. Мельница для измельчения известняка.Известняк (CaCO3)CaCO3CaCO3CaCO3CaCO3
- 9. Печь для получения оксида кальция.Попутный газПопутный газПопутный газПопутный газCaOCO2CO2CaCO3
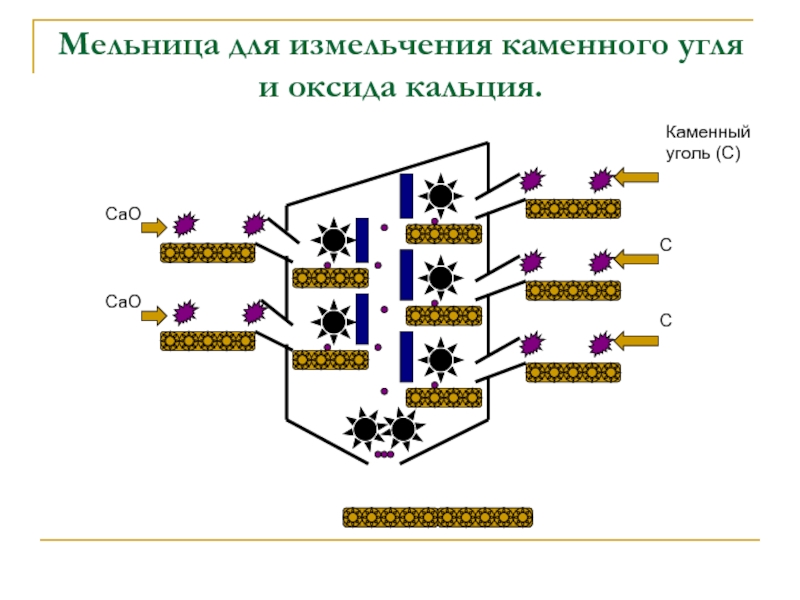
- 10. Мельница для измельчения каменного угля и оксида кальция.CaOCaOКаменный уголь (С)CC
- 11. Печь для получения карбида кальция.CaO и СПопутный газПопутный газCOCOO2CO2CаС2
- 12. Аппарат для получения цианамида кальция.КомпрессорКомпрессорВоздухN2гO2жN2N2N2N2СаС2СаСN2, СH2OH2OH2O
- 13. Аппарат для получения аммиака.компрессорКомпрессорCO2CO2NH3жC2Н2гСаСN2Са(ОН)2,С, СаСО3.СаСО3Н2ОН2О
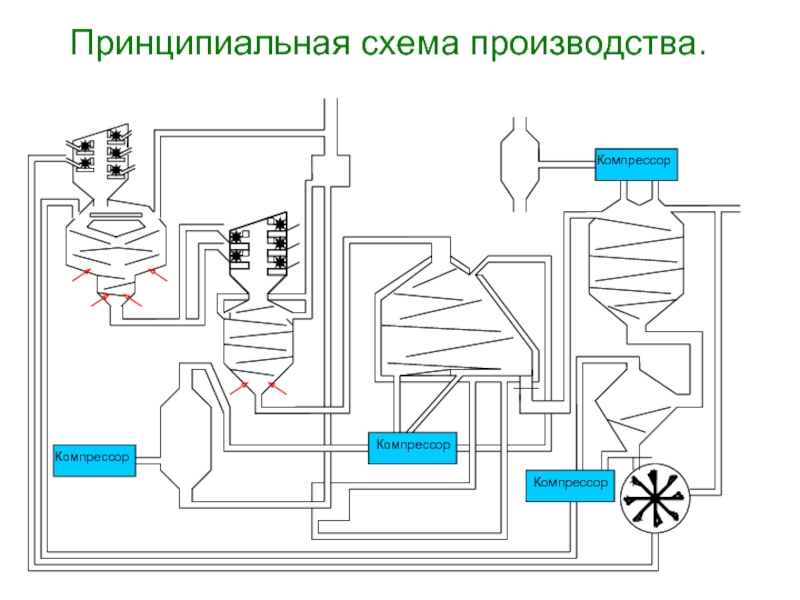
- 14. Принципиальная схема производства.КомпрессорКомпрессорКомпрессорКомпрессор
- 15. Вывод. Проект был создан
- 16. Скачать презентанцию
Цель проектной работы.Создании альтернативного способа производства аммиака. Обеспечить оптимальное протекание химических реакций.Создать производство, основанное на современных принципах.
Слайды и текст этой презентации
Слайд 2Цель проектной работы.
Создании альтернативного способа производства аммиака.
Обеспечить оптимальное протекание
химических реакций.
Слайд 3Термодинамические основы химического производства.
Скорость химической реакции - это быстрота изменения
количества вещества в единицу времени.
Скорость химической реакции зависит:
От природы реагирующих веществ
От поверхностей реагирующих веществ (для твердых веществ)
От концентрации реагирующих веществ (только для газов)
От температуры (при увеличении температуры на 10 градусов скорость реакции возрастает в 2-4 раза)
От присутствия некоторых веществ:
-катализаторы - вещества, ускоряющие скорость химические реакции.
-ингибиторы- вещества, замедляющие скорость химической реакции.
Слайд 4Химические равновесие – это состояние системы, при котором скорость прямой
реакции равна скорости обратной реакции.
Правила по принципу Ле-Шателье:
При увеличении давления
равновесие смещается в сторону меньшего числа газообразных молекул (только для газов).При увеличении температуры равновесие смещается в сторону эндотермической реакции.
При увеличении концентрации равновесие смещается в сторону его уменьшения (только для газов).
Термодинамические основы химического производства.
Слайд 5Сырье.
Сырье- это минералы, которые лежат в основе производства.
СаСО3- известняк
(карбоната кальция)
N2- азот
С - каменный уголь (углерод)
Н2О - вода
Природный или
попутный нефтяной газ.Слайд 6Химизм.
Химизм – это химические реакции, лежащие в основе производства.
CaCO3 тв CaOтв
+ CO2 г - QCaOтв +3Cтв CaC2тв + COг - Q
CaC2 тв + N2 г CaCN2 тв + Cтв + Q
CaCN2тв + 3H2Oж CaCO3тв + 2NH3г + Q
Слайд 7Аппаратное оформление.
Мельница для измельчения известняка.
Печь для получения оксида кальция.
Мельница для
измельчения каменного угля и оксида кальция.
Печь для получения карбида кальция.
Аппарат
для получения цианамида кальция.Аппарат для получения аммиака.
Принципиальная схема производства.
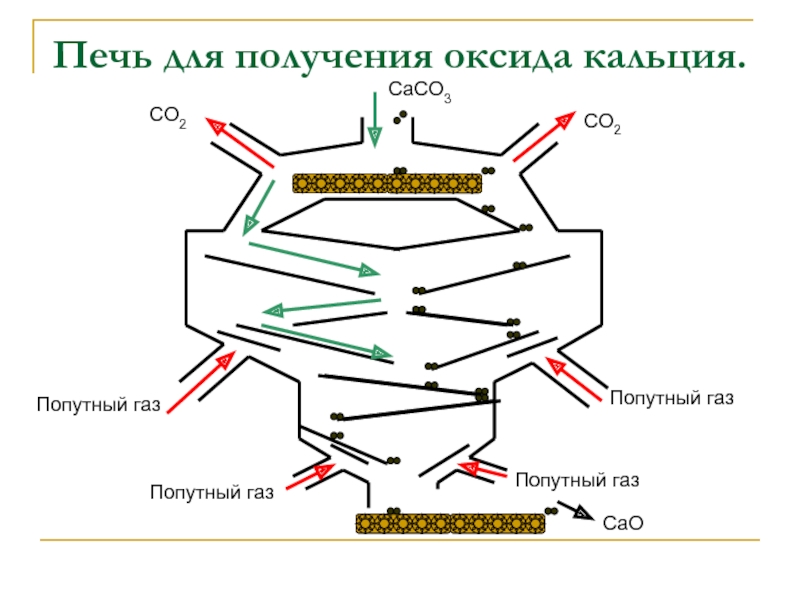
Слайд 9Печь для получения оксида кальция.
Попутный газ
Попутный газ
Попутный газ
Попутный газ
CaO
CO2
CO2
CaCO3
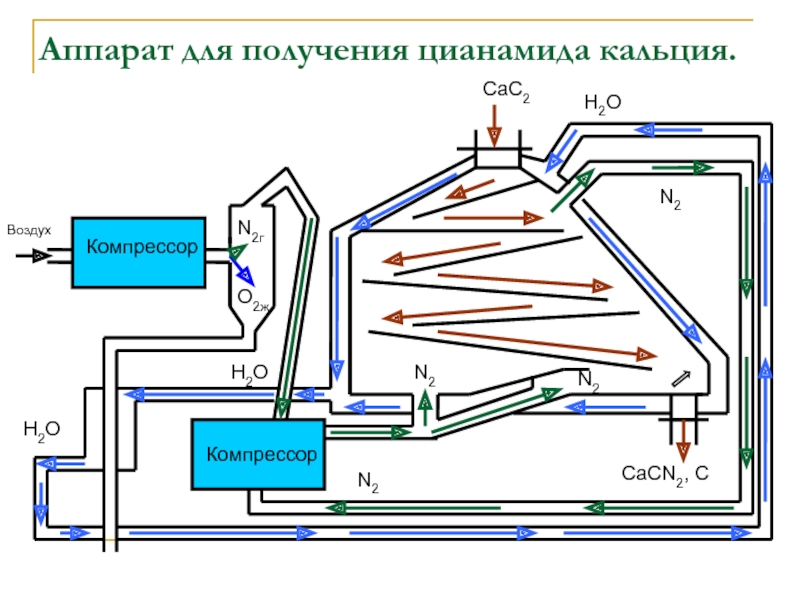
Слайд 12Аппарат для получения цианамида кальция.
Компрессор
Компрессор
Воздух
N2г
O2ж
N2
N2
N2
N2
СаС2
СаСN2, С
H2O
H2O
H2O
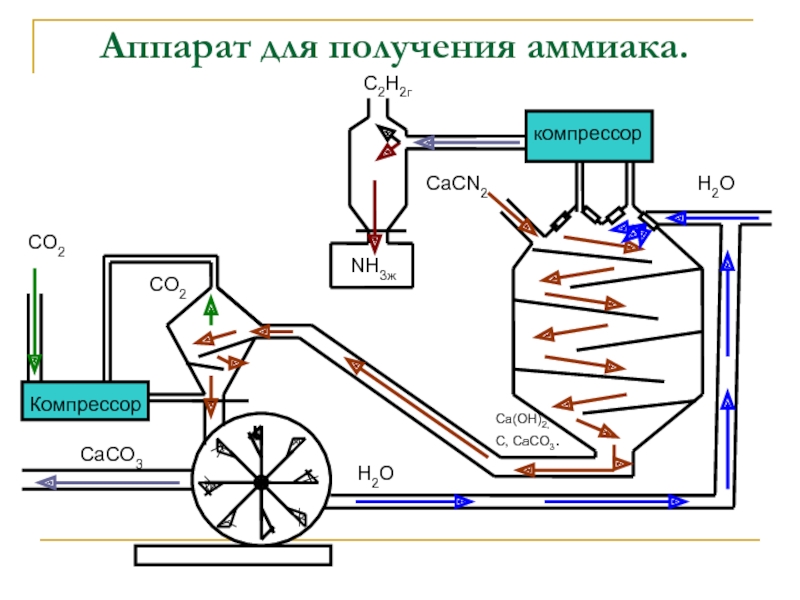
Слайд 13
Аппарат для получения аммиака.
компрессор
Компрессор
CO2
CO2
NH3ж
C2Н2г
СаСN2
Са(ОН)2,
С, СаСО3.
СаСО3
Н2О
Н2О
Слайд 15Вывод.
Проект был создан самостоятельно без использования
вспомогательной литературы, основываясь на знаниях полученных, на уроках химии. В
проекте созданы аппараты ранее нигде не использовавшиеся и неописанные. Соблюдены основные принципы химического производства: циркуляции, теплообмена, безотходности, экологичности.
Теги