Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Минеральные удобрения
Содержание
- 1. Минеральные удобрения
- 2. «Сами, трудясь, вы многое сделаете для себя
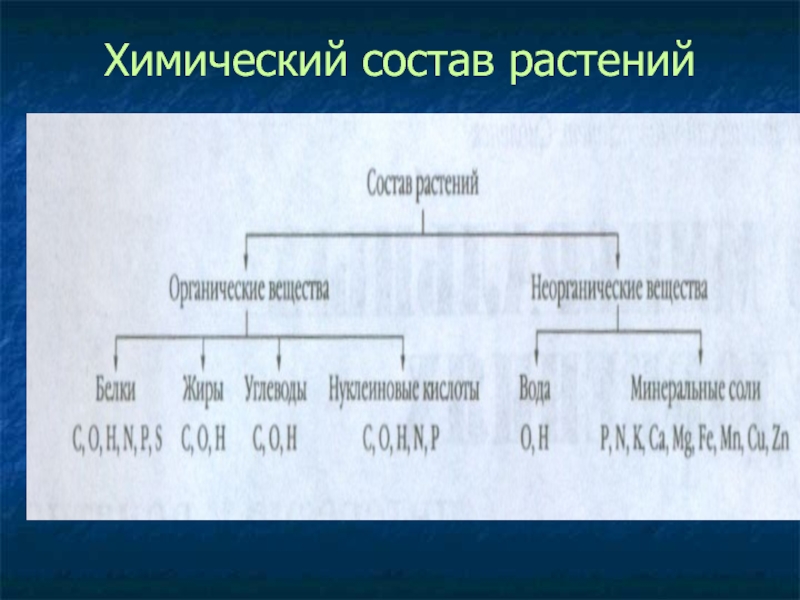
- 3. «Мозговой штурм»Какие вещества входят в состав растений?
- 4. Какие органические вещества вам известны?
- 5. Какие неорганические вещества содержатся в организме растений?
- 6. Из каких элементов состоят все упомянутые вещества? CN
- 7. Химический состав растений
- 8. Откуда растения получают необходимые им элементы? Откуда
- 9. Проблема: расход питательных веществ нужно восполнять, добавляя
- 10. Немецкий химик, академик. Один из основателей агрохимии.
- 11. Цель: получить знания о составе и классификации
- 12. Рабочая гипотеза:Получив данные о классификации минеральных удобрений,
- 13. Проверка гипотезы экспериментомЦель: отработка учебных приемов исследовательской деятельности«Деяние есть живое единство теории с практикой» Аристотель
- 14. Химический эксперимент(фронтальная работа)Исследование минеральных удобрений Вещество
- 15. Определение удобрения X Вывод Вещество X – сульфат аммония
- 16. Определение удобрения YВывод Вещество Y – суперфосфат
- 17. Задание для группы №1 «Незадачливый фермер»
- 18. Слайд 18
- 19. Задание для группы №2 «Опытный сосед»
- 20. Слайд 20
- 21. Задание для группы №3 «Молодой огородник» Молодому
- 22. Задание для группы №4 «Химическое производство»Сегодня химическая
- 23. Ответ :Ca3(PO4)2 → P → P2O5
- 24. Недостаток питательных элементов:Пожелтевшие нижние листья —признак недостатка
- 25. Воздействие повышенных количеств нитратов и их
- 26. Избыток минеральных веществ в почве:N Острое отравление
- 27. Удобрения
- 28. Слайд 28
- 29. РефлексияКитайская мудрость гласит «Даже если вы достигли вершины горы, продолжайте карабкаться дальше»
- 30. «Первое яблоко тому, кто рассказывал.Второе – тому,
- 31. Спасибо за сотрудничество! Урок окончен! До свидания! Всем добра и успехов!
- 32. Скачать презентанцию
«Сами, трудясь, вы многое сделаете для себя и близких.
Слайды и текст этой презентации
Слайд 2«Сами, трудясь, вы многое сделаете для себя и близких.
А если при труде успеха не будет, будет неудача, не беда – попробуйте еще, и тогда придет успех» Д.И.Менделеев
Слайд 8Откуда растения получают необходимые им элементы?
Откуда в растение поступает
углерод?
Откуда растение может брать кислород и водород?
Что является источником
азота для растений? Слайд 9Проблема: расход питательных веществ нужно восполнять, добавляя их в почву
путем внесения удобрений.
«Гораздо труднее увидеть проблему, чем найти ее
решение» С. Бернар
Слайд 10Немецкий химик, академик. Один из основателей агрохимии. В 1840 г. предложил
теорию минерального питания растений. На основе много численных анализов он
установил, что каждому растению необходимо для нормальной жизнедеятельности 10 элементов: C, H, O, N, Ca, K, P, S, Mg, и Fe. Он также установил, что важнейшим из этих элементов являются три – N, K,P.Ю.Либих
1803-1873)
Слайд 11Цель: получить знания о составе и классификации минеральных удобрений.
Добавляемые в
почву органические и минеральные вещества, содержащие питательные элементы, называют удобрениями.
Слайд 12Рабочая гипотеза:
Получив данные о классификации минеральных удобрений, необходимо исследовать их
состав и свойства,
научиться распознавать образцы важнейших удобрений;
выяснить, какое
влияние оказывают минеральные удобрения на питание растений.Слайд 13Проверка гипотезы экспериментом
Цель: отработка учебных приемов исследовательской деятельности
«Деяние есть живое
единство теории с практикой» Аристотель
Слайд 14
Химический эксперимент
(фронтальная работа)
Исследование минеральных удобрений
Вещество Х: белые гранулы,
легко сублимируются при нагревании, растворяются в воде, а при добавлении
к раствору нескольких капель раствора хлорида бария образуется белый осадок; при растворении гранул в щелочи и нагревании образуется газ с резким запахом, который изменяет цвет влажной лакмусовой бумажки из красного в синий.Вещество У: серые гранулы, нерастворимые в воде; при добавлении нескольких капель раствора нитрата серебра образуется желтый осадок; окрашивает пламя в кирпично-красный цвет. При добавлении карбоната калия выпадает белый осадок
Слайд 17Задание для группы №1 «Незадачливый фермер»
Поздней осенью, распахав землю,
фермер решил, что называется убить двух зайцев сразу: известковать участки
с кислой почвой и провести подкормку ее суперфосфатом (все-таки поверил, что без химии не обойтись). Однако весной оказалось, что желаемый эффект не был достигнут. Почему?Слайд 18
Помощь фермеру
Са(Н2РО4)2 + 2Са(ОН)2 = =Са3(РО4)2 + 4Н2О
осадокК какому типу относится реакция?
К каким классам соединений относятся данные вещества?
Назовите эти соединения.
Слайд 19Задание для группы №2
«Опытный сосед»
Опытный
сосед, пожалев молодого фермера, предложил ему исправить ошибку, внеся в
почву хорошо растворимое удобрение, содержащее фосфор.Он позабыл его название, но принес аккуратную запись результатов анализа (%):
Азота – 12,2,
Водорода – 5,5,
Фосфора – 27,0,
Кислорода – 55,6.
Что же это за вещество?
Слайд 20
Помощь фермеру
Дано:
Решение:W(N) = 12,2% Отношение элементов в веществе
W(Н) = 5,5% N : Н : Р : О =
W(Р) = 27,0% 12,2/14 : 5,5/1 : 27,0/31 : 55,6/16 =
W(О) = 55,6% 0,87 : 5,5 : 0,87 : 3,47 =
______________ 1 : 6 : 1 : 4
Формула ? NН6РО4 или NН4 Н2РО4
Ответ: NН4 Н2РО4 – дигидроортофосфат аммония
Слайд 21Задание для группы №3 «Молодой огородник»
Молодому огороднику необходимо внести в
почву минеральное удобрение, но на упаковке не сохранилось ни название,
ни его формула. К счастью сохранилась следующая запись: азота 12.2%, водорода – 5.5%, фосфора 27.0%, кислорода 55.6%. Сможет ли огородник по указанным данным определить это вещество?Слайд 22Задание для группы №4 «Химическое производство»
Сегодня химическая промышленность создает новые
рецептуры удобрений с улучшенными качествами. Это – суперфосфат, аммофос, сильвинит
и другие. Чтобы получить растворимый в почве суперфосфат, восстанавливают углем природный фосфат:Продукт реакции – двойной суперфосфат (Ca(H2PO4)2) так называется из-за процесса, который идет в две стадии, а также он содержит около 50% Р2О5, а простой содержит 20%.
Составьте цепочку превращений от природного фосфата до двойного суперфосфата. Запишите уравнения реакций.
Слайд 23Ответ :
Ca3(PO4)2 → P → P2O5 → H3PO4
→ Ca(H2PO4)2
1.Ca3(PO4)2 + 5C + 3 SiO2 = 2P
+ 5CO + 3 CaSiO32.4P + 5O2 = 2P2O5
3.P2O5 + 3H2O = 2H3PO4
4.Ca3(PO4)2 + 4H3PO4 = 3Ca(H2PO4)2
Слайд 24Недостаток питательных элементов:
Пожелтевшие нижние
листья —признак
недостатка азота.
Признаки недостатка
фосфора на листьях.
Пожелтение и отмирание
кончиков листьев — признаки
недостатка калия.
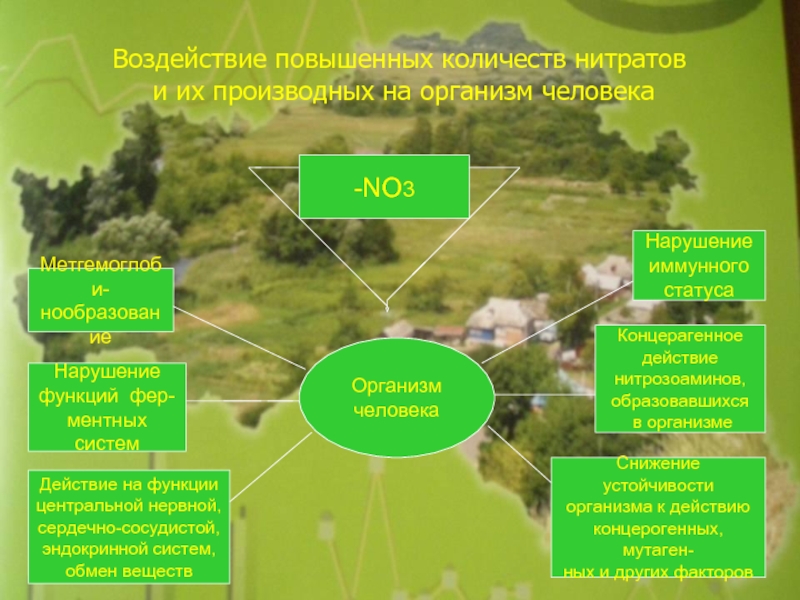
Слайд 25Воздействие повышенных количеств нитратов
и их производных на организм человека
-NO3
Организм
человека
Метгемоглоби-
нообразование
Нарушение
функций
фер-
ментных систем
Действие на функции
центральной нервной,
сердечно-сосудистой,
эндокринной систем,
обмен веществ
Нарушение
иммунного
статуса
Концерагенное
действие
нитрозоаминов,
образовавшихся
в организме
Снижение устойчивости
организма
к действиюконцерогенных, мутаген-
ных и других факторов
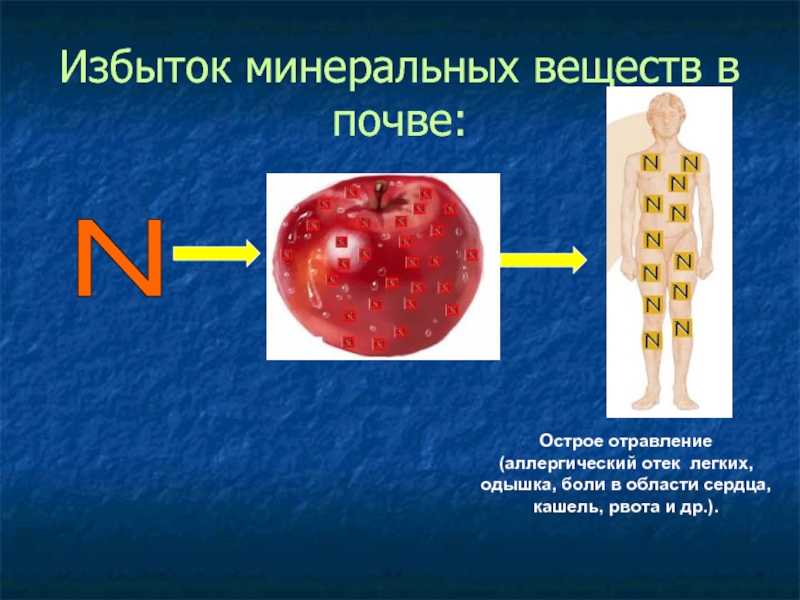
Слайд 26Избыток минеральных веществ в почве:
N
Острое отравление
(аллергический отек легких,
одышка, боли в области сердца,
кашель, рвота и др.).
Слайд 29Рефлексия
Китайская мудрость гласит «Даже если вы достигли вершины горы, продолжайте
карабкаться дальше»
Слайд 30«Первое яблоко тому, кто рассказывал.
Второе – тому, кто слушал.
А
третье-кому?
Тому – кто понял!»
Из армянской сказки
Теги