Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Неметаллы 11 класс
Содержание
- 1. Неметаллы 11 класс
- 2. Неметаллы - химические элементы с типично неметаллическими свойствамиНеметаллы
- 3. Неметаллы занимают правый верхний угол Периодической Системы Химических
- 4. Небольшой атомный радиусНа внешнем уровне 4-8 электроновРасполагаются
- 5. Агрегатное состояние
- 6. Типы кристаллических решеток
- 7. Преобладают окислительные свойства:В соответствии с численными значениями
- 8. Проявляют также восстановительные свойства:Восстановительные свойства постепенно возрастают
- 9. Аллотропия – это способность атомов одного химического элемента образовывать несколько простых веществАллотропия
- 10. Различный состав молекул простого вещества (аллотропия состава)Способ
- 11. Кислород (O2)Аллотропия составаОзон (O3)
- 12. Алмаз (С)Аллотропия формыГрафит (С)
- 13. Спасибо за внимание!
- 14. Скачать презентанцию
Неметаллы - химические элементы с типично неметаллическими свойствамиНеметаллы
Слайды и текст этой презентации
Слайд 3Неметаллы занимают правый верхний угол Периодической Системы Химических Элементов (ПСХЭ). Также
к неметаллам относят водород (Н) и гелий (Не)
таблице МенделееваСлайд 4Небольшой атомный радиус
На внешнем уровне 4-8 электронов
Располагаются только в главных
подгруппах
Характерно высокое значение ЭО (электроотрицательности)
Особенности атомного строения неметаллов
Слайд 7Преобладают окислительные свойства:
В соответствии с численными значениями относительной ЭО окислительные
способности неметаллов увеличиваются в следующем порядке:
Si B H2 P C S I2 N2 Cl2 O2 F2Химические свойства неметаллов
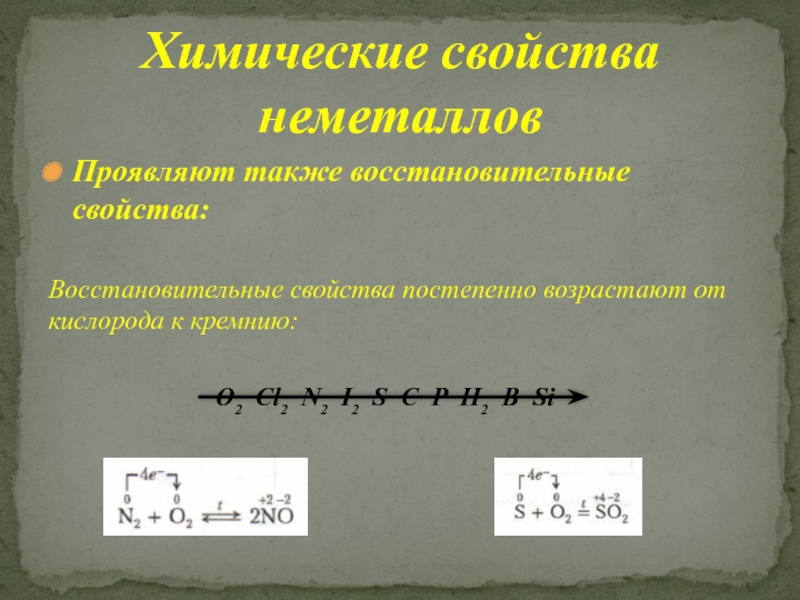
Слайд 8Проявляют также восстановительные свойства:
Восстановительные свойства постепенно возрастают от кислорода к
кремнию:
O2 Cl2 N2 I2 S C P H2 B SiХимические свойства неметаллов