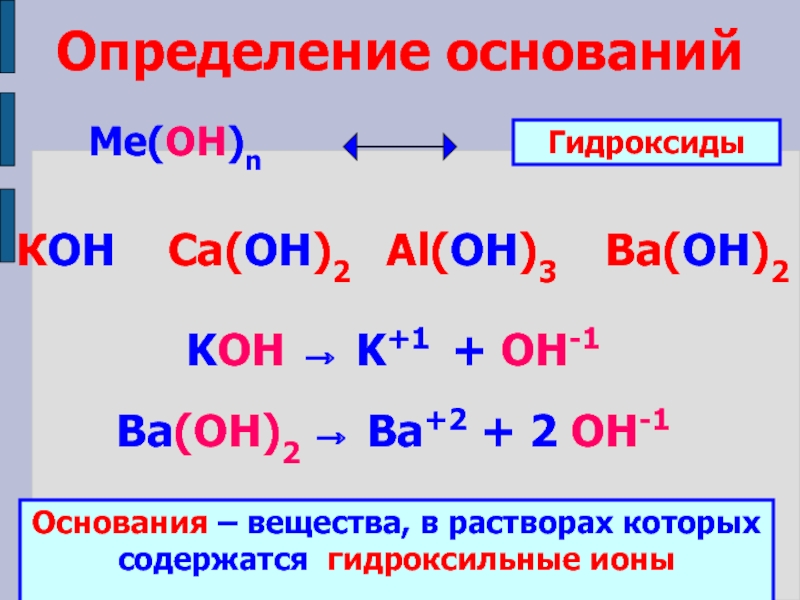
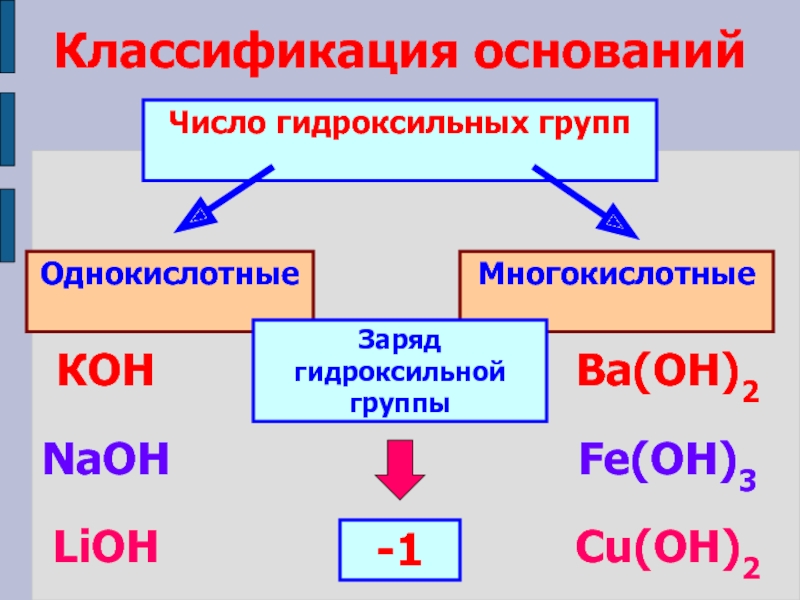
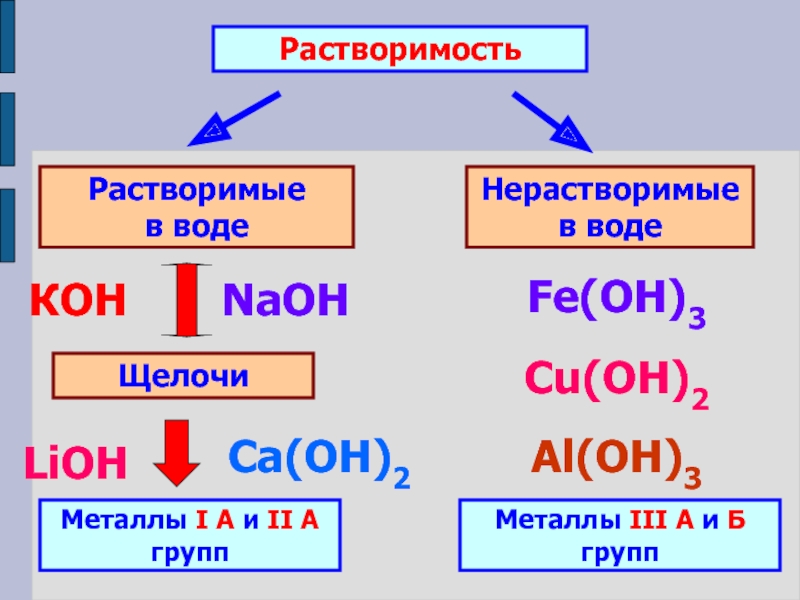
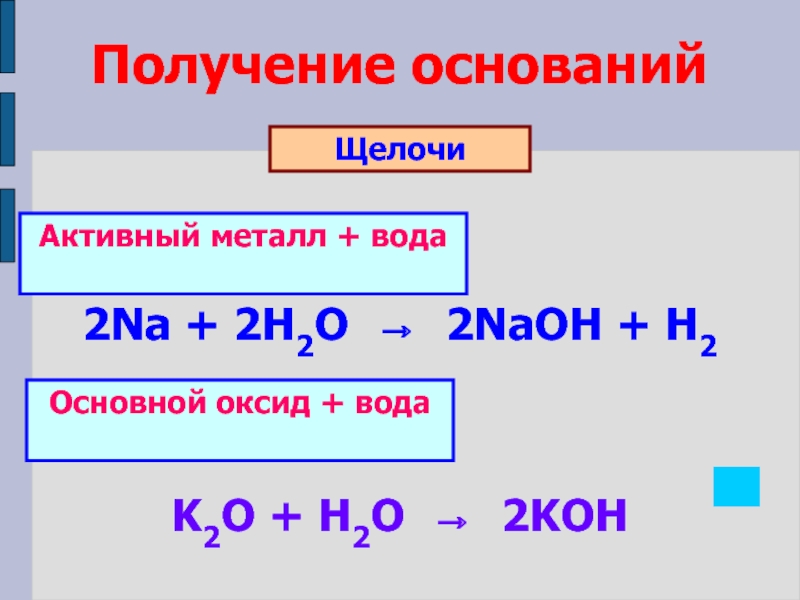
по различным признакам;
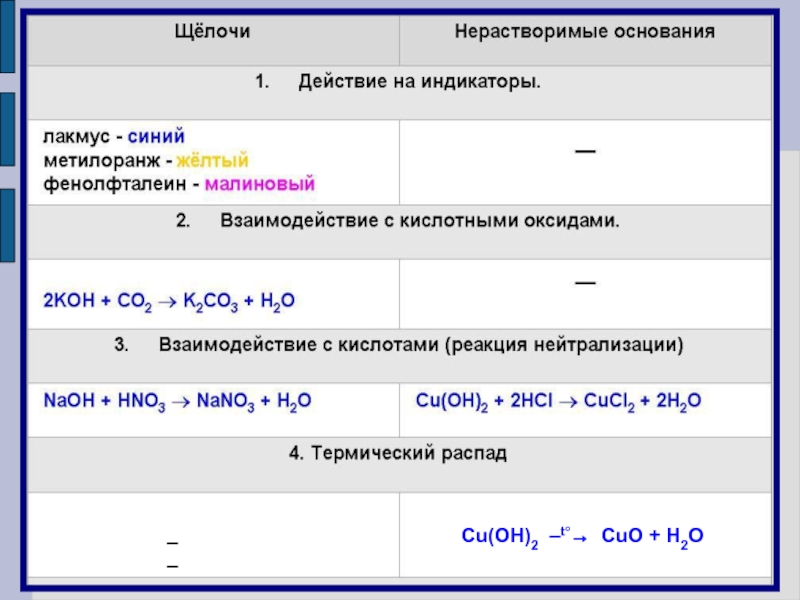
3) познакомить практически с химическими свойствами оснований в
свете теории электролитической диссоциации; 4) развивать умения и навыки работы с химическими реактивами и химическим оборудованием;
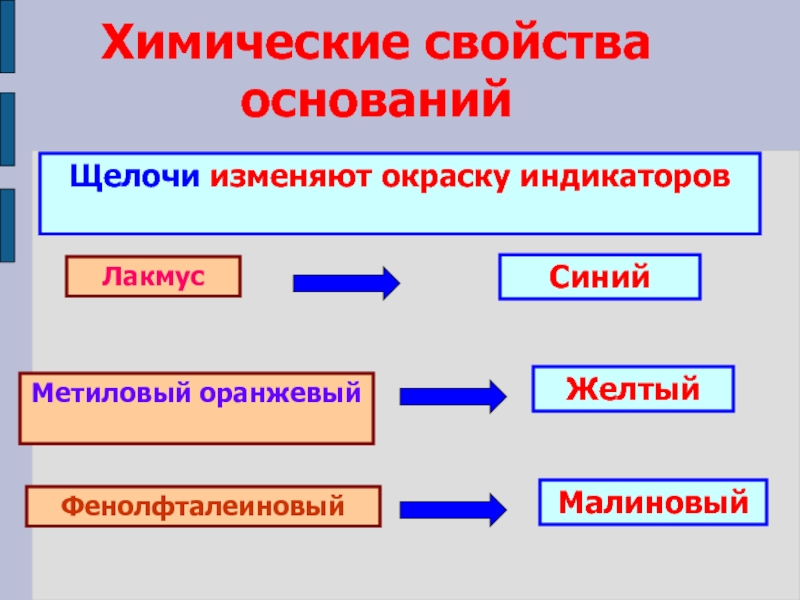
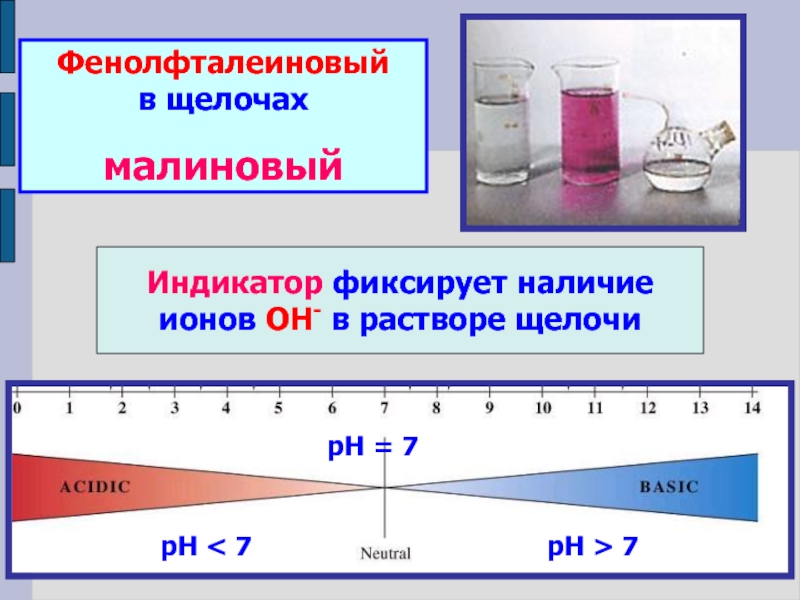
5) учить сравнивать, анализировать, делать выводы;
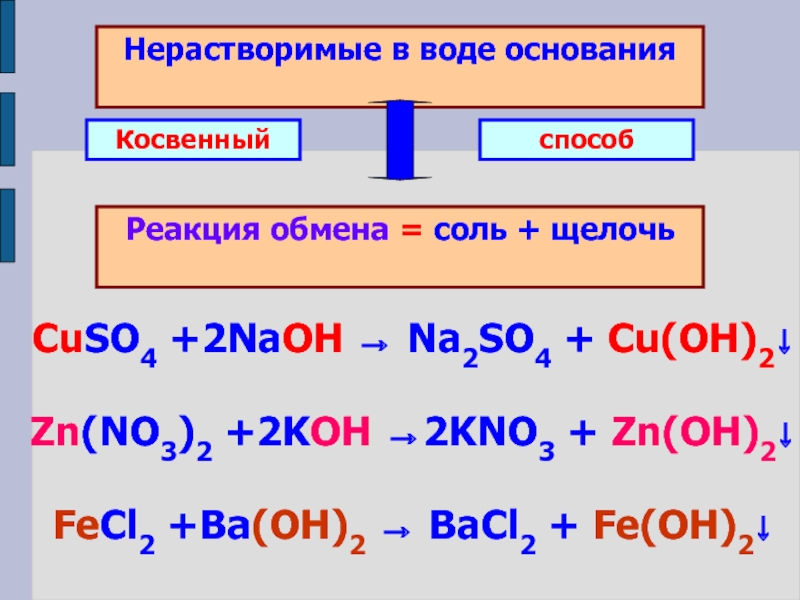
6) совершенствовать умения и навыки в написании формул веществ и уравнений химических реакций.
ЦЕЛИ УРОКА: