Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Положение металлов в Периодической системе Строение атомов
Содержание
- 1. Положение металлов в Периодической системе Строение атомов
- 2. Положение металлов в Периодической системеСтроение атомовКристаллические решёткиОбщие
- 3. Слайд 3
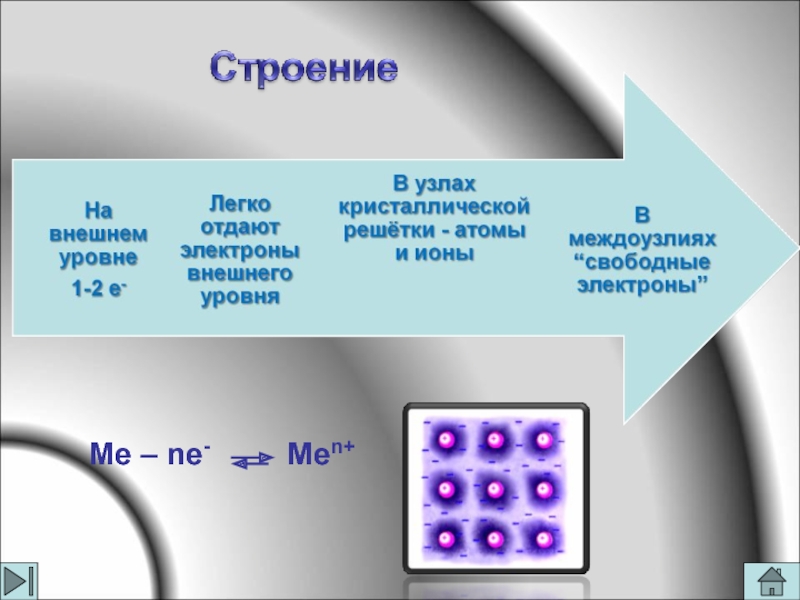
- 4. К металлам относятся простые вещества,которые образуют:
- 5. Ме – ne- Men+
- 6. Слайд 6
- 7. Все твердые, кроме ртути Металлический блеск Пластичность, ковкость Электропроводность Теплопроводность Высокие температурыплавления
- 8. Самый распространённый металл в природе - алюминий - более 8% от земной коры
- 9. Слайд 9
- 10. Слайд 10
- 11. Получение металлов из руд их восстановлением.
- 12. Получение металлов электролизом:
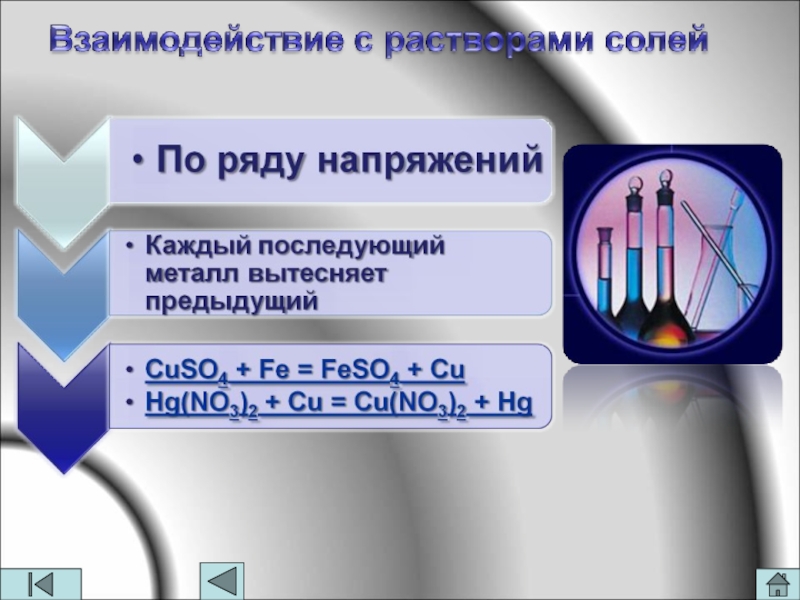
- 13. Получение металлов восстановлением из растворов солей:
- 14. Металлы - восстановители Ме0 – ne- =
- 15. Слайд 15
- 16. 2K + 2H2O = 2KOH + H2↑Zn
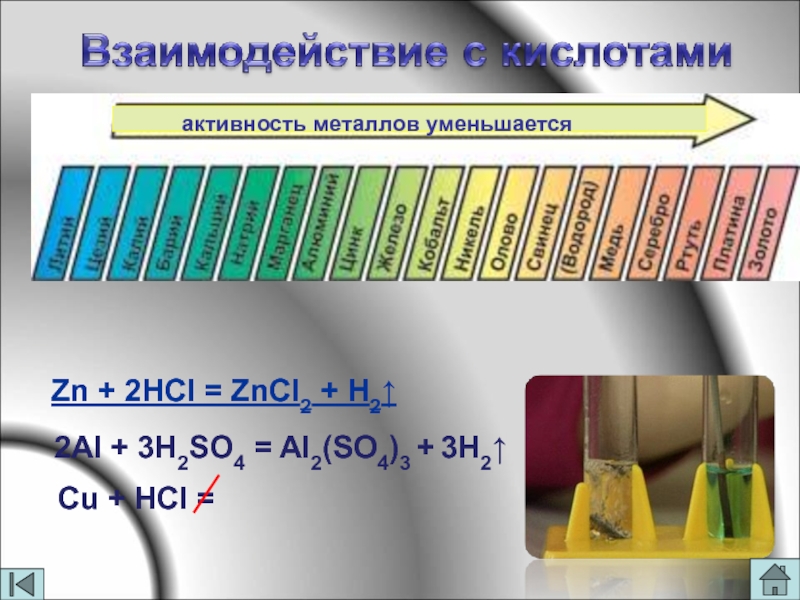
- 17. Zn + 2HCl = ZnCl2 + H2↑
- 18. Слайд 18
- 19. Продолжение следует…
- 20. Скачать презентанцию
Положение металлов в Периодической системеСтроение атомовКристаллические решёткиОбщие физические свойства Металлы в природе Способы получения металлов Химические свойства металлов