Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Получеение галогенов. Биалогические значение и их соединений
Содержание
- 1. Получеение галогенов. Биалогические значение и их соединений
- 2. К элементам VII группы, главной подгруппы относятся
- 3. Слайд 3
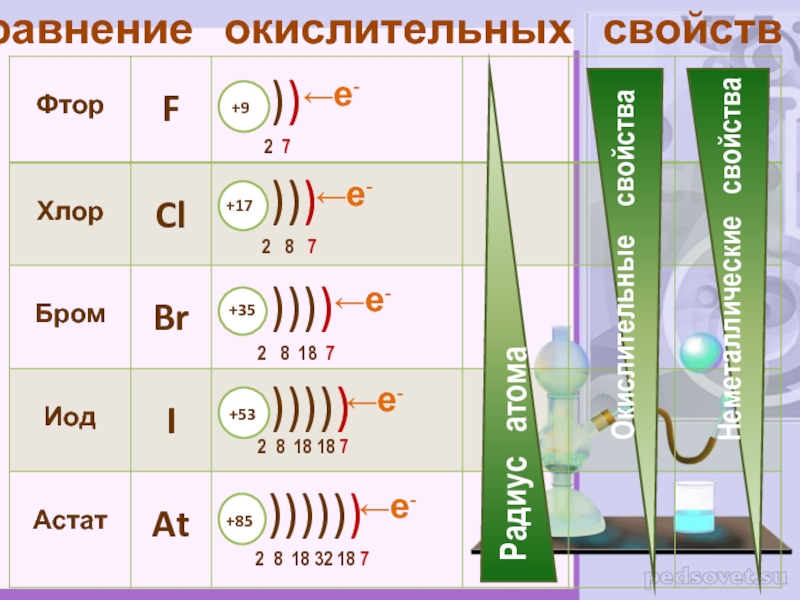
- 4. Сравнение окислительных свойств←е-←е-←е-←е-←е-
- 5. Степень окисления НCL
- 6. Молекулы галогенов состоят из двух атомовСвязь – ковалентная неполярная
- 7. В твердом состоянии фтор, хлор, бром, йод имеют молекулярные кристаллические решётки.
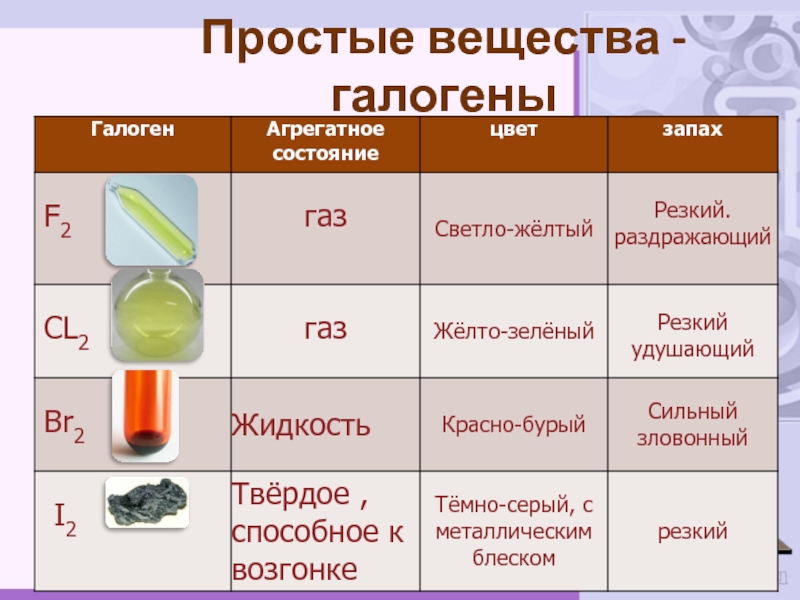
- 8. Простые вещества - галогены
- 9. 1. Взаимодействие с металлами Хлор
- 10. H2 + F2 = 2HF (со взрывом) H2
- 11. 3. Взаимодействие с водой с
- 12. Историческая справкаСлово «галогены» (“halogen”) ввел шведский химик Й.Я.Берцелиус галогены (греч. hals – соль, gen – рождаю)
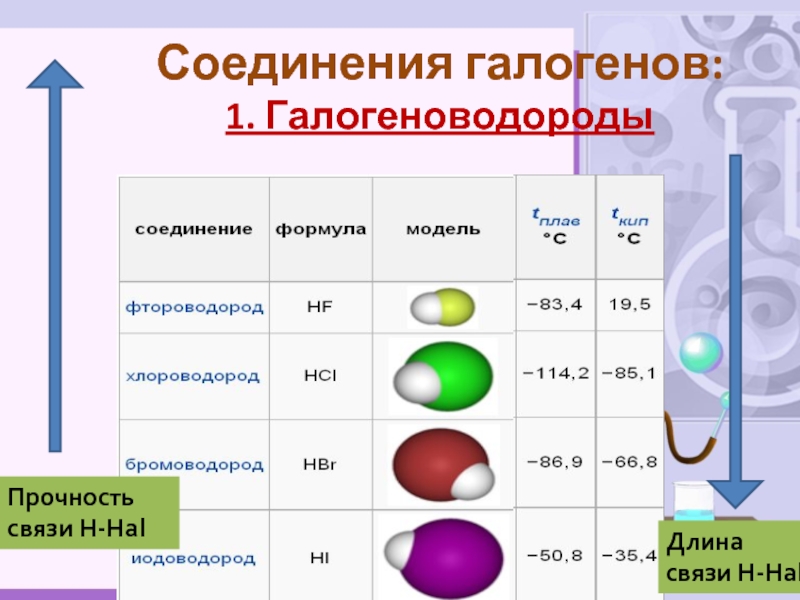
- 13. Соединения галогенов: 1. ГалогеноводородыДлина связи Н-HalПрочность связи Н-Hal
- 14. Бесцветные газы (HF при t
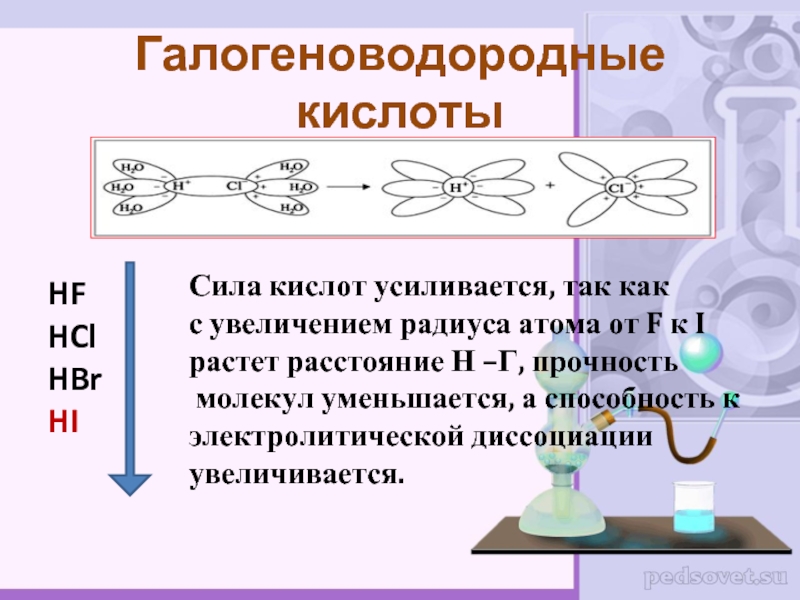
- 15. HFHClHBrHIГалогеноводородные кислотыСила кислот усиливается, так как с
- 16. В промышленности: синтезом из водорода и хлора: H2
- 17. Физические свойства: бесцветная, дымящая на воздухе
- 18. Используют для изготовления надписей и рисунков на
- 19. Вещество, при реакциис которым HCl даст осадок1.
- 20. Оксиды и гидроксидыКислотные свойства усиливаются, окислительные свойства ослабевают
- 21. Распространенность в природе галит NaClсильвин KClсильвинит KCl•NaClПлавиковый шпат - флюорит CaF2
- 22. Получение галогенов:F2 и Cl2 в промышленности получают
- 23. F Кости, зубы, обмен веществ в железах,
- 24. Применение фтораТефлон Фреон Na3AlF6 – производство алюминияОкислитель
- 25. Применение хлораОтбеливателиПроизводство HClПолучение
- 26. Применение бромаЛекарственные препаратыКрасители ФотографияВетеренарные препаратыИнгибиторыПрисадки
- 27. Применение йодаЛекарственные препаратыФотографияКрасителиДезинфекция одеждыЭлектролампы09.02.12
- 28. Домашнее задание: П.19, №3-4 П.20, №1-3
- 29. Спасибо за внимание!
- 30. Скачать презентанцию
Слайды и текст этой презентации
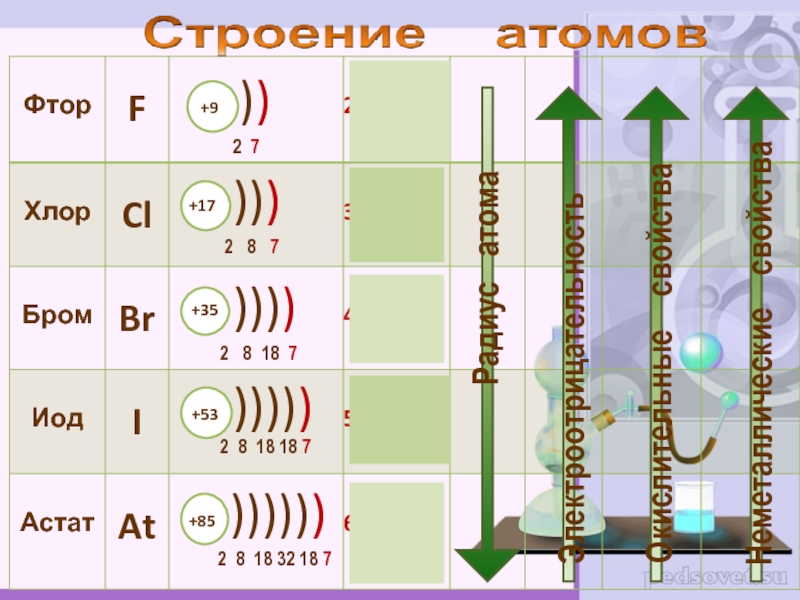
Слайд 2К элементам VII группы, главной подгруппы относятся
фтор F, хлор Cl, бром Br,
иод I, астат At Общее название - галогены (греч. «солеобразующие») - большинство их соединений с металлами представляют собой типичные соли (KCl, NaCl и т.д.).
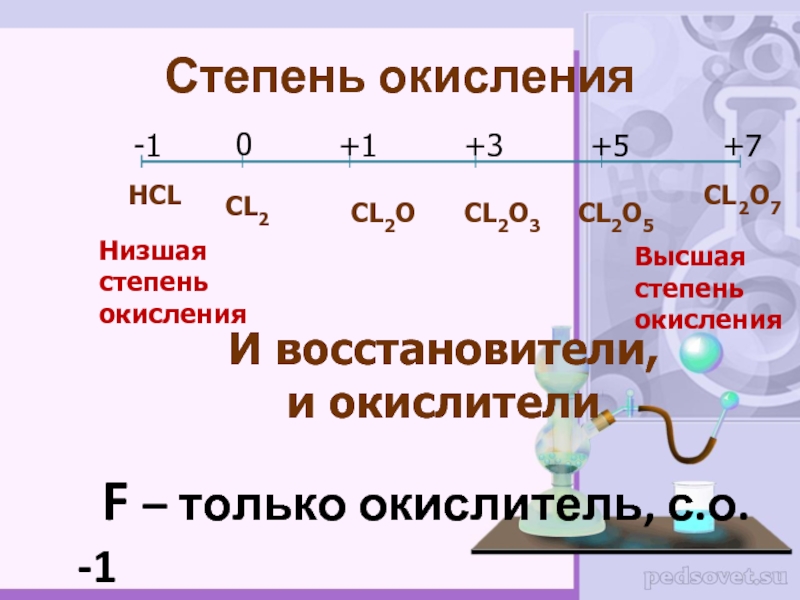
Слайд 5Степень окисления
НCL
CL2O7
F – только окислитель, с.о. -1
-1
0
+1
+3
+5
+7
CL2
CL2O
CL2O3
CL2O5
И восстановители,
и окислители
Низшая
степень
окисления
Высшая
степень
окисления
Слайд 91. Взаимодействие с металлами
Хлор непосредственно реагирует почти
со всеми металлами (с некоторыми только в присутствии
влаги или при нагревании):2. Взаимодействие с неметаллами
C неметаллами (кроме углерода, азота, кислорода и инертных газов), образует соответствующие хлориды.
F2 -наиболее реакционноспособен , реакции идут на холоду, при нагревании – даже с участием Au, Pt.
Слайд 10
H2 + F2 = 2HF (со взрывом)
H2 + Cl2 =
2HCl (на свету)
H2 + Br2 = 2HBr (при нагревании)
H2 +
I2 = 2HI (при нагревании, обратимая реакция)4. Взаимодействие с водородом
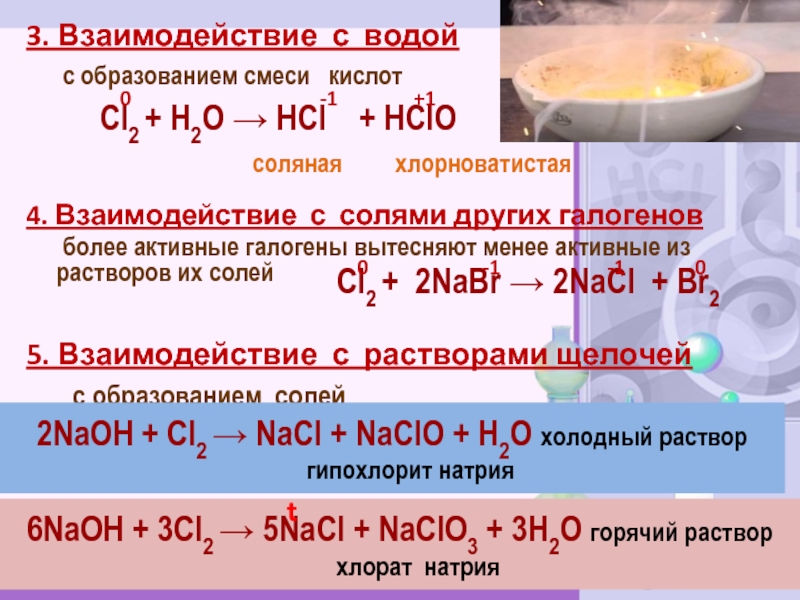
Слайд 113. Взаимодействие с водой
с образованием смеси
кислот
4. Взаимодействие с солями других галогенов
более активные
галогены вытесняют менее активные из растворов их солей5. Взаимодействие с растворами щелочей
с образованием солей
2NaOH + Cl2 → NaCl + NaClO + H2O холодный раствор
гипохлорит натрия
Слайд 12Историческая справка
Слово «галогены» (“halogen”) ввел шведский химик Й.Я.Берцелиус
галогены (греч. hals
– соль, gen – рождаю)
Слайд 14Бесцветные газы (HF при t
растворяются в воде
Дымят во влажном воздухе
Растворы галогеноводородов – кислоты
1V (H2O) растворяется 500V (HCl)Физические свойства галогеноводородов
Слайд 15
HF
HCl
HBr
HI
Галогеноводородные кислоты
Сила кислот усиливается, так как
с увеличением радиуса атома
от F к I
растет расстояние Н –Г, прочность
молекул
уменьшается, а способность к электролитической диссоциации
увеличивается.
Слайд 16В промышленности: синтезом из водорода и хлора:
H2 + Cl2 =
2HCl
2) В лаборатории:
NaCl (крист.) + H2SO4 (конц.)
= HCl↑ + NaHSO4Получение хлороводорода
t
Слайд 17Физические свойства: бесцветная,
дымящая на воздухе жидкость,
тяжелее воды
Химические свойства:
Типичная
кислота
Соляная кислота
С какими веществами взаимодействуют кислоты?
Слайд 18Используют для изготовления надписей и рисунков на стекле.
SiO2 + 2HF
= SiF4↑ + 2H2O
Плавиковая кислота
Травление или сатинирование
Эту технологию начали использовать
в 1771 г. с открытием плавиковой кислоты. Сама эта кислота делает стекло блестящим, а ее газы - матовым. Травить можно всю поверхность полностью (при этом она остается гладкой) или выборочно (только рисунок).
Слайд 19
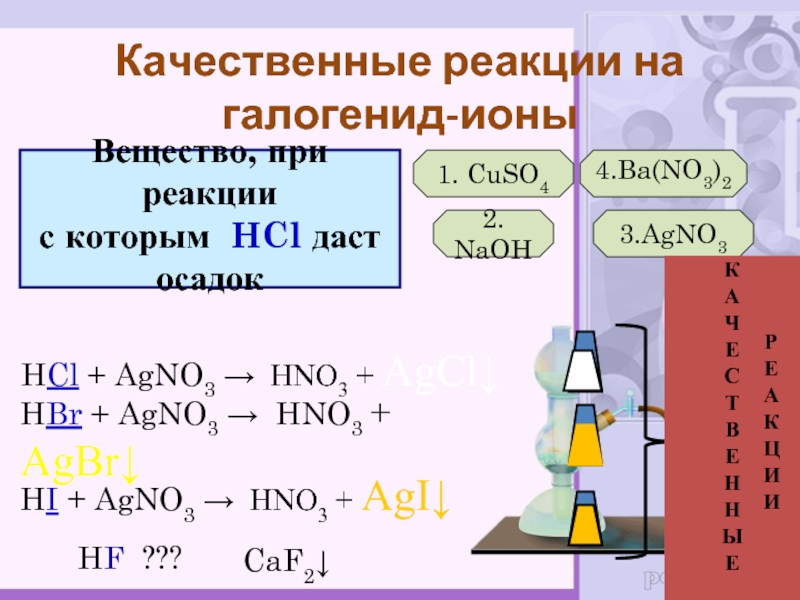
Вещество, при реакции
с которым HCl даст
осадок
1. CuSO4
2. NaOH
3.AgNO3
4.Ba(NO3)2
HCl +
AgNO3 → HNO3 + AgCl↓
HBr + AgNO3 → HNO3 +
AgBr↓ HI + AgNO3 → HNO3 + AgI↓
HF ???
CaF2↓
Качественные реакции на галогенид-ионы
Слайд 21Распространенность в природе
галит NaCl
сильвин KCl
сильвинит KCl•NaCl
Плавиковый шпат - флюорит
CaF2
Слайд 22Получение галогенов:
F2 и Cl2 в промышленности получают электролизом расплавов или
растворов их солей:
2NaCl
2Na + Cl22NaCl + 2H2O H2 + Cl2 + 2NaOH
раствор
Cl2 в лаборатории получают:
MnO2 + 4HCl = MnCl2 + Cl2 + H2O
расплав
Слайд 23
F
Кости, зубы, обмен веществ в железах, мышцах и нервных
клетках
Сl
Стимулирует обмен веществ, рост волос, придает бодрость и силу. Содержится
в плазме крови. НСl в желудочном сокеBr
Регуляция нервных процессов. Накапливается в морских водорослях
I
Выработка гормона щитовидной железы, который регулируетмускульное возбуждение, биение сердца, аппетит, пищеварение, работу мозга. Йодной настойкой обрабатывают раны.
09.02.12
Слайд 24
Применение фтора
Тефлон Фреон
Na3AlF6 – производство алюминия
Окислитель ракетного топлива
Заменитель крови
Фториды
в зубных
пастах09.02.12
Слайд 25
Применение хлора
Отбеливатели
Производство
HCl
Получение брома,
йода
Дезинфекция воды
Органические растворители
Лекарственные препараты
Хлорирование органических веществ
Получение
неорганических хлоридов09.02.12
Слайд 26
Применение брома
Лекарственные препараты
Красители
Фотография
Ветеренарные препараты
Ингибиторы
Присадки
к бензину
09.02.12