Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Предельные углеводороды. Алканы
Содержание
- 1. Предельные углеводороды. Алканы
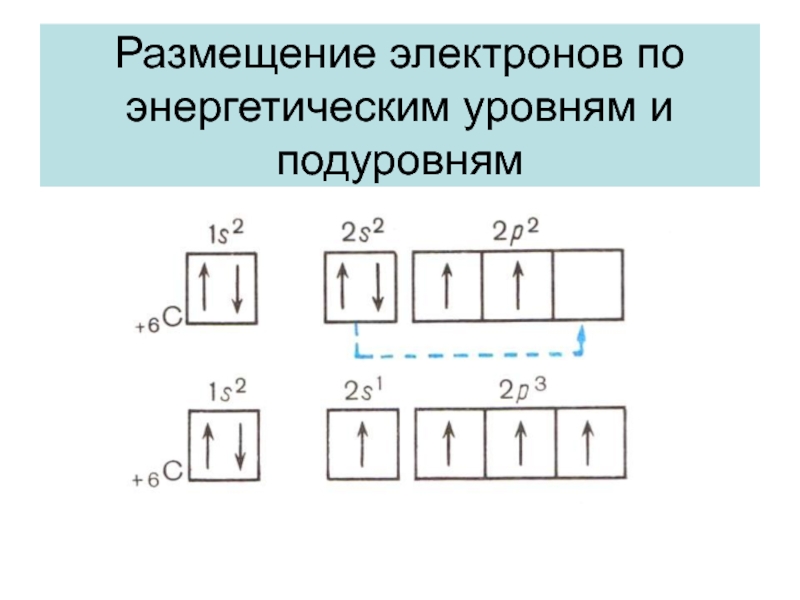
- 2. Размещение электронов по энергетическим уровням и подуровням
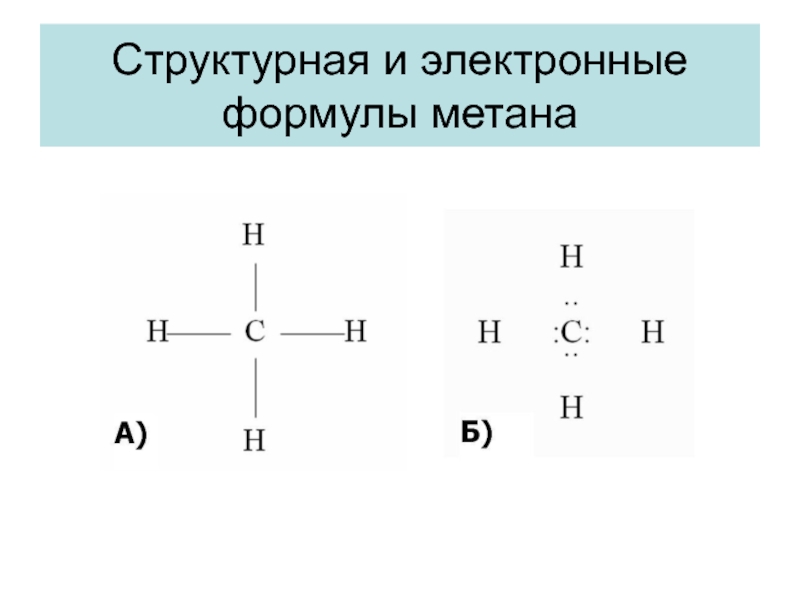
- 3. Структурная и электронные формулы метана
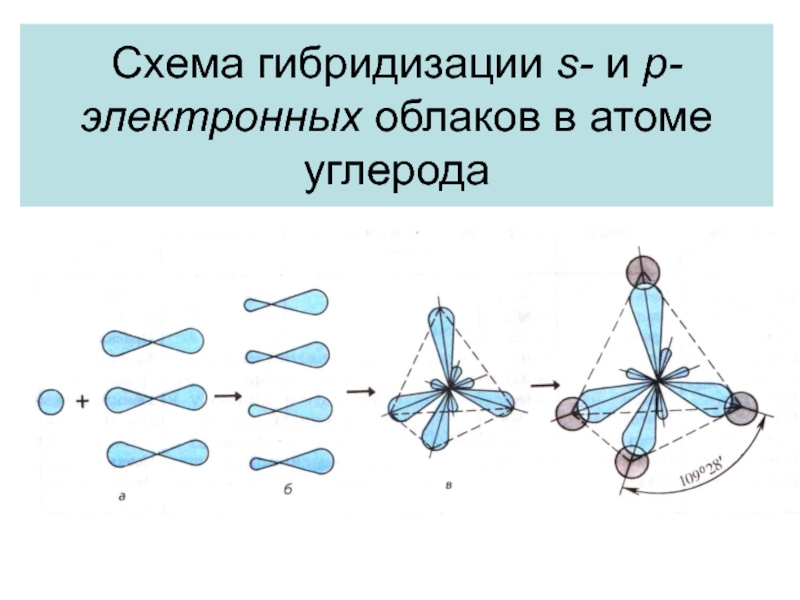
- 4. Схема гибридизации s- и p-электронных облаков в атоме углерода
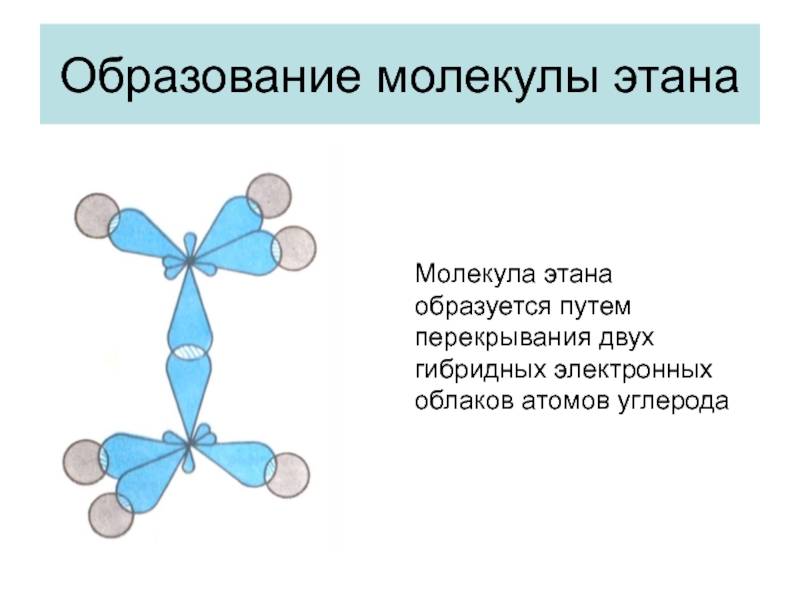
- 5. Образование молекулы этанаМолекула этана образуется путем перекрывания двух гибридных электронных облаков атомов углерода
- 6. Направление химических связей в молекуле пропанаТак как
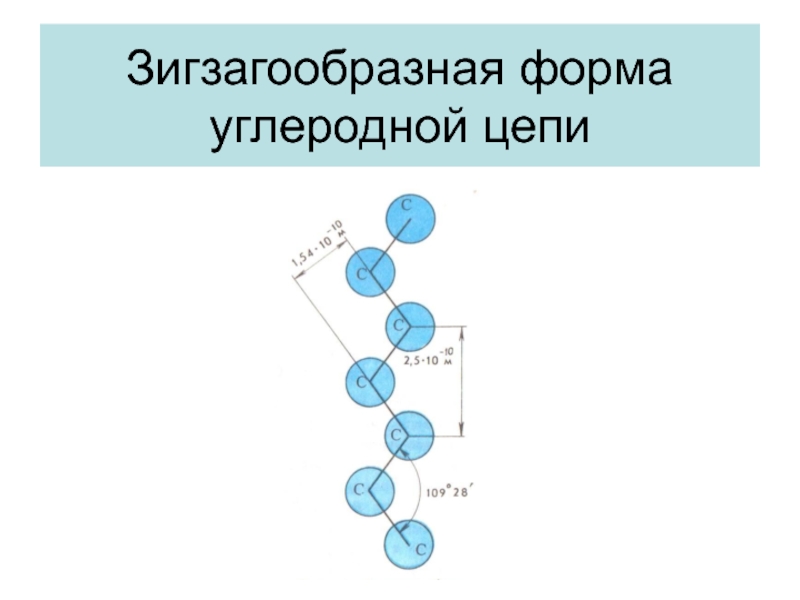
- 7. Зигзагообразная форма углеродной цепи
- 8. Изомерия и номенклатураТак как углеводородов очень много,
- 9. Алгоритм определения названий углеводородов1. Выбирают в формуле
- 10. Алгоритм определения названий углеводородов2. Называют радикалы (начиная
- 11. Алгоритм определения названий углеводородов3. Полное название данному
- 12. Получение алкановПрокаливание безводного ацетата натрия с натронной известью :CH3COONa + NaOH = CH4↑ + Na2CO3
- 13. Реакция ВюрцаЭтан и другие предельные углеводороды с
- 14. Гидролиз карбида алюминияAl4C3 + 12 H2O =
- 15. Использованные источники1. Габриелян О.С., Остроумов И.Г. Настольная
- 16. Скачать презентанцию
Размещение электронов по энергетическим уровням и подуровням
Слайды и текст этой презентации
Слайд 1Предельные углеводороды. Алканы
Учитель химии
МБОУ «Архангельская СОШ»
Губкинского района
Белгородской
области
Слайд 5Образование молекулы этана
Молекула этана образуется путем перекрывания двух гибридных электронных
облаков атомов углерода
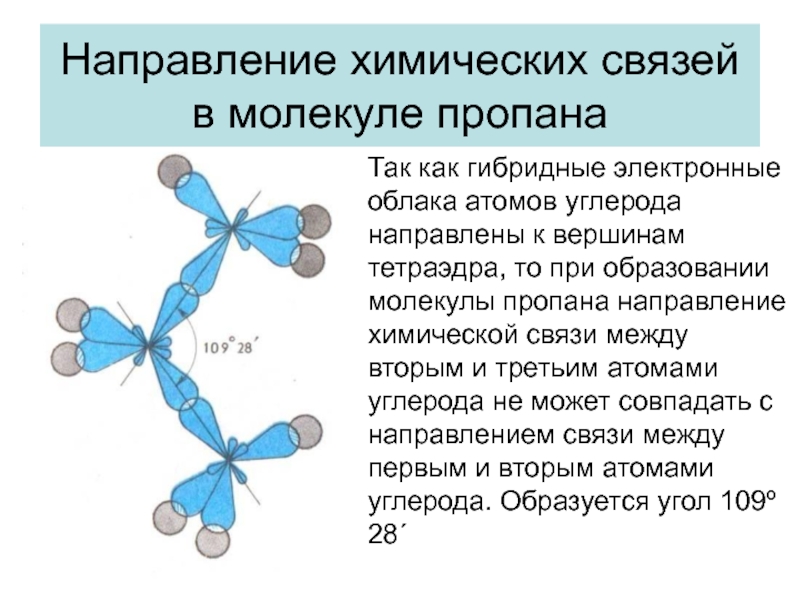
Слайд 6Направление химических связей в молекуле пропана
Так как гибридные электронные облака
атомов углерода направлены к вершинам тетраэдра, то при образовании молекулы
пропана направление химической связи между вторым и третьим атомами углерода не может совпадать с направлением связи между первым и вторым атомами углерода. Образуется угол 109º 28´Слайд 8Изомерия и номенклатура
Так как углеводородов очень много, то для них
международным союзом теоретической и прикладной химии принята специальная номенклатура –
International Union of Pure and Applied Chemistry, сокращенно IUPAC (ИЮПАК).Слайд 9Алгоритм определения названий углеводородов
1. Выбирают в формуле наиболее длинную углеродную
цепь и символы атомов углерода в ней нумеруют, начиная с
того конца цепи, к которому ближе разветвлениеСлайд 10Алгоритм определения названий углеводородов
2. Называют радикалы (начиная с простейшего) и
при помощи цифр указывают их место у нумерованных атомов углерода.
Слайд 11Алгоритм определения названий углеводородов
3. Полное название данному углеводороду дают по
числу атомов углерода в нумерованной цепи:
а) 2-метилпентан
б) 2,2-диметилбутан
в) 3-метилпентан
г) 2,3-диметилбутан
Слайд 12Получение алканов
Прокаливание безводного ацетата натрия с натронной известью :
CH3COONa +
NaOH = CH4↑ + Na2CO3
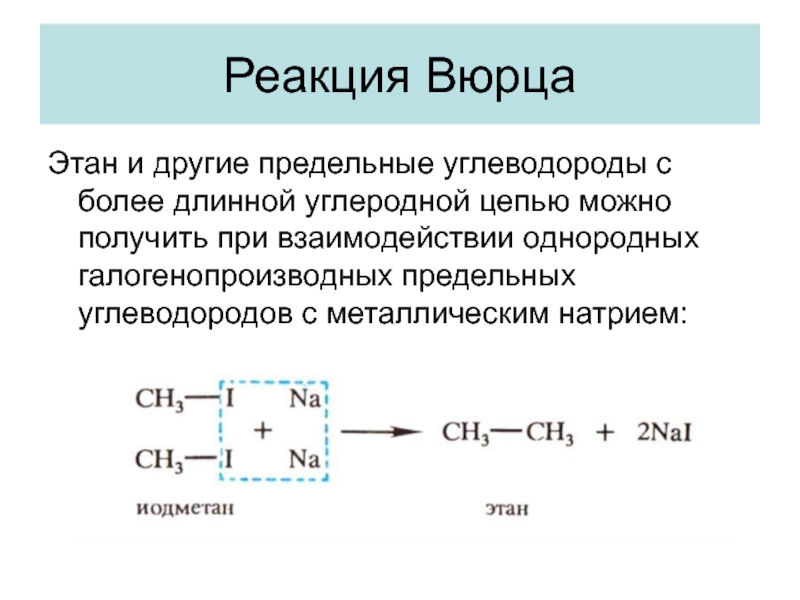
Слайд 13Реакция Вюрца
Этан и другие предельные углеводороды с более длинной углеродной
цепью можно получить при взаимодействии однородных галогенопроизводных предельных углеводородов с
металлическим натрием:Слайд 14Гидролиз карбида алюминия
Al4C3 + 12 H2O = 4Al(OH)3 + 3CH4↑
Примером
специфического способа получения алканов является гидролиз карбида алюминия. Этимология слова
гидролиз (от греч. слов hidor – вода и lisis - распад, разложение) позволяет определить такие реакции, как процесс разложения сложного соединения на два и более новых веществ под действием водыСлайд 15Использованные источники
1. Габриелян О.С., Остроумов И.Г. Настольная книга учителя химии.
10 класс. – М.: «Блик и Кº», 2001.
2. Рудзитис
Г.Е. Химия: Орган. химия: Учеб. для 10 кл. общеобразоват. учреждений. / Г.Е. Рудзитис, Ф.Г. Фельдман. – 8-е изд. – М.: Просвещение, 2001.3. http://www/school-collection.edu.ru (раздел «Химия. 10 класс. Органическая химия (видео опыты))