Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация к уроку по теме "Алюминий"
Содержание
- 1. Презентация к уроку по теме "Алюминий"
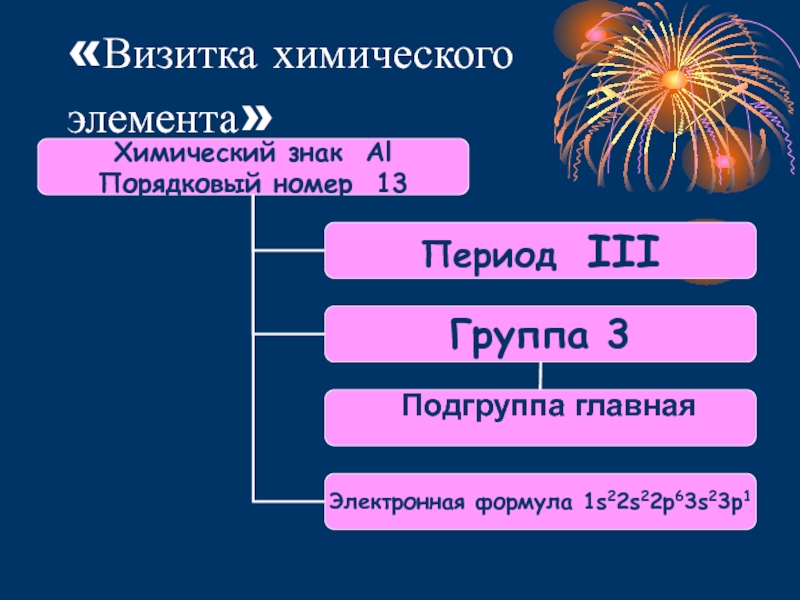
- 2. «Визитка химического элемента»Подгруппа главная
- 3. Алюминий с легкостью отдает 3 валентных электрона,
- 4. ПРОБЛЕМАЯвляется ли алюминий активным металлом?
- 5. ФИЗИЧЕСКИЕ СВОЙСТВА ВЕЩЕСТВА Al – серебристо-белый металл, пластичный,
- 6. Химические свойства
- 7. АЛЮМИНИЙ РЕАГИРУЕТ С ПРОСТЫМИ
- 8. АЛЮМИНИЙ РЕАГИРУЕТ СО СЛОЖНЫМИ ВЕЩЕСТВАМИ:1. Реагирует с
- 9. Реакции со сложными веществами3. Алюминотермия
- 10. ВЫВОД: АЛЮМИНИЙ ОБЛАДАЕТ ДОСТАТОЧНО ВЫСОКОЙ ХИМИЧЕСКОЙ
- 11. Алюминий - крылатый металл
- 12. В том числе и при изготовлении транспортных средств
- 13. Конструкционные сплавы используются также и в архитектуре городов
- 14. Алюминий и его сплавы широко применяют как конструкционный материал при строительстве мостов
- 15. Из алюминия делают линии электропередач, ёмкости, цистерны, «серебряную» краску.
- 16. Применяется в изготовлении посуды
- 17. Бенгальские огни и фейерверки
- 18. Урок понравился, всё было понятно.
- 19. Урок понравился, но не всё понятно или не всё интересно.
- 20. Урок не понравился, ничего не понятно.
- 21. сегодня я узнал… было интересно…было трудно…
- 22. Спасибо за работу!
- 23. Скачать презентанцию
«Визитка химического элемента»Подгруппа главная
Слайды и текст этой презентации
Слайд 1Урок химии в 9 классе по теме «АЛЮМИНИЙ»
Подготовила: учитель
химии Кивалкина Светлана Владимировна
Слайд 3
Алюминий с легкостью отдает 3 валентных электрона, проявляя при этом
постоянную степень окисления +3.
Алюминий – сильный восстановитель, легко окисляется.
В ряду
напряжений следует за магнием.Слайд 5ФИЗИЧЕСКИЕ СВОЙСТВА ВЕЩЕСТВА
Al – серебристо-белый металл, пластичный, легкий, хорошо проводит
тепло и электрический ток, обладает хорошей ковкостью, легко поддаётся обработке,
образует лёгкие и прочные сплавы.ρ=2,7 г/см3
tпл.=6600С
Слайд 7
АЛЮМИНИЙ РЕАГИРУЕТ С ПРОСТЫМИ ВЕЩЕСТВАМИ - НЕМЕТАЛЛАМИ:
1. 2Al+3O2
= 2Al2O3 – покрывается пленкой оксида, но в мелкораздробленном виде
горит с выделением большого количества теплоты.2. 2Al + 3Cl2 = 2 AlCl3 (Br2) – без нагревания
3. 2Al + 3S = Al2S3 - при нагревании
4. 4Al + 3С = Al4С3 - при нагревании
Слайд 8АЛЮМИНИЙ РЕАГИРУЕТ СО СЛОЖНЫМИ ВЕЩЕСТВАМИ:
1. Реагирует с разбавленными серной и
соляной кислотами (конц. H2SO4 и HNO3 пассивируют Al )
2Al
+ 6HCl = 2AlCl3 + 3H22. Реагирует с раствором щёлочи
2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2
Слайд 9Реакции со сложными веществами
3. Алюминотермия – получение металлов:
Fe, Cr, Mn, Ti, W и другие, например:
3Al + 3Fe3O4 = 4Al2O3 + 9Fe4. Реагирует с растворами солей менее активных металлов
2Al + 3CuCl2 = 2AlCl3 + 3Cu
Слайд 10ВЫВОД: АЛЮМИНИЙ ОБЛАДАЕТ ДОСТАТОЧНО ВЫСОКОЙ ХИМИЧЕСКОЙ АКТИВНОСТЬЮ: ОН РЕАГИРУЕТ СО МНОГИМИ
ПРОСТЫМИ И СЛОЖНЫМИ ВЕЩЕСТВАМИ ДАЖЕ ПРИ ОБЫЧНЫХ УСЛОВИЯХ. КАЖУЩАЯСЯ НЕАКТИВНОСТЬ ЭТОГО
МЕТАЛЛА ОБЪЯСНЯЕТСЯ ОБРАЗОВАНИЕМ НА ЕГО ПОВЕРХНОСТИ ОКСИДНОЙ ПЛЁНКИ, КОТОРАЯ И ЗАЩИЩАЕТ МЕТАЛЛ ОТ ХИМИЧЕСКИХ ПРОЦЕССОВ.Слайд 14Алюминий и его сплавы широко применяют как конструкционный материал при
строительстве мостов
Слайд 21
сегодня я узнал…
было интересно…
было трудно…
я выполнял задания…
я понял, что…
теперь я могу…
я почувствовал, что…
я приобрел…
я научился…
у
меня получилось …я смог…
я попробую…
меня удивило…
урок дал мне для жизни…
мне захотелось…